Компоненты таких сплавов неограниченно растворяются один в другом в жидком состоянии и не растворяются в твердом, например, свинец (Pb) + сурьма (Sb).
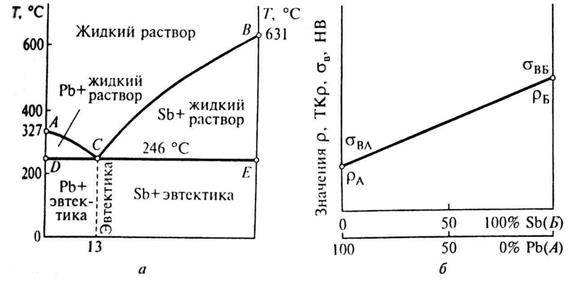
Рисунок 7.6 – Диаграмма состояния сплава I типа (а) и изменение физико-химических свойств в зависимости от состава сплава (б)
Кривая АСВ отвечает началу затвердения всех сплавов и называется температурой ликвидуса (от лат. liqiudus – жидкий). Прямая DCE соответствует концу затвердения сплавов и называется температурой солидуса (от лат. solidus – твердый). Выше линии ликвидуса все сплавы этой системы (Pb-Sb или в общем виде А+Б) находятся в жидком состоянии и образуют раствор. Ниже этой линии имеется жидкий раствор плюс кристаллы Pb (ниже линии АС) и кристаллы Sb (ниже линии СВ). Таким образом, по линии АС из жидкого раствора кристаллизуется компонент А (Pb), образуя α-фазу, а по линии СВ – компонент Б (Sb), образуя β-фазу. В чистом виде Pb начинает кристаллизоваться при температуре 327 °С, Sb – 631 °С; у сплавов температуры эти ниже. Твердый сплав, состав которого отвечает точке С, имеет гетерогенную структуры и представляет собой механическую смесь двух твердых фаз (α- и β-фазы) в определенных соотношениях друг с другом и одновременно кристаллизующихся из жидкого раствора. Для системы сплавов Pb-Sb соотношение компонентов в точке С составляет 87 % Pb и 13 % Sb. Такую структуру называют эвтектикой (от греч. eutektos – легко плавящаяся или хорошо плавящаяся), сплав – эвтектическим, температуру, при которой образуется этот сплав, - эвтектической температурой, а состав сплава – эвтектическим составом.
Сплавы, лежащие левее эвтектической точки С (на линии DC и ниже ее), называют доэвтектическими сплавами. После затвердевания они имеют структуру, состоящую из кристаллов Sb и эвтектики (87 % Pb + 13 % Sb). Структура доэвтектического, эвтектического и заэвтектического сплавов системы Pb-Sb представлена на рисунке 7.7.

а – доэвтектический сплав, 94 % Pb + 6 % Sb (темные кристаллы Pb + эвтектика);
б – эвтектический сплав, 87 % Pb +13 % Sb; в – заэвтектический сплав, 60 % Pb + 40 % Sb (светлые кристаллы Sb + эвтектика), х250
Рисунок 7.7 – Структура сплавов системы Pb-Sb
Свойства сплавов гетерогенных структур изменяются линейно от свойств компонента А к свойствам компонента Б (рисунок 7.7.б).
Диаграммы состояния II типа
Твердые растворы замещения могут быть с неограниченной и ограниченной растворимостью компонентов.
Если в сплавах (рисунок 7.8) образуется непрерывный ряд твердых растворов, то свойства изменяются по криволинейному закону, например, медь (Cu) + никель (Ni).
В интервале температур T1-T2 образуются кристаллы неоднородные по химическому составу. Неоднородность состава внутри кристалла называют внутрикристаллитной ликвацией. Концентрация компонентов по объему кристалла выравнивается в результате диффузии атомов при воздействии высокой температуры при максимальном искажении кристаллической решетки увеличивается твердость (HB), механическая прочность (σВ) и удельное электрическое сопротивление ρ, температурный же коэффициент удельного сопротивления (ТКр) становится минимальным.
а б
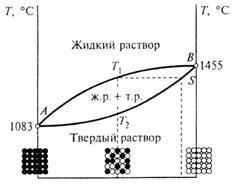
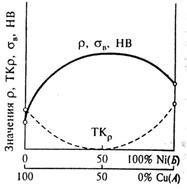
Рисунок 7.8 – Диаграмма состояния сплавов, образующих твердые растворы с неограниченной растворимостью компонентов, схема расположения атомов Cu (черные) и Ni (белые) в решетках сплавов (а) и изменение физико-химических свойств в зависимости от состава (б)
Диаграмма состояния сплавов, образующих твердые растворы с ограниченной растворимостью компонентов, представлена на рисунке 7.9.
Твердые растворы α- и β-фазы с максимальной концентрацией растворимого компонента образуются между линиями ликвидуса и солидуса.
В этих областях α- и β-фазы находятся вместе с жидким раствором. На линии DCE сплавы затвердевают и образуют механическую смесь кристаллов α-твердого раствора и β-твердого раствора. Двухкомпонентные сплавы, в которых происходит одновременная кристаллизация α- и β-фазы при постоянной и самой низкой для данной системы температуре, называются эвтектическими, а структура их – эвтектикой.
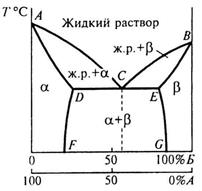
Рисунок 7.9 – Диаграмма состояния сплавов в упрощенном виде для твердых растворов с ограниченной растворимостью компонентов
Эвтектический сплав образуется в точке С. Сплавы, располагающиеся влево от эвтектического состава (левее точки С) и имеющие концентрацию компонентов в пределах точек D и C, называются доэвтектическими, а справа точки С – в пределах точек С и Е – заэвтектическими.
С понижением температуры растворимость компонента Б в α-фазе и компонента А в β-фазе все время снижается. В результате α- и β-твердые растворы становятся пересыщенными, и происходит вторичная кристаллизация: компонент Б выделяется из α-фазы, образуя отдельные кристаллы, называемые вторичными (βII), а компонент А – из β-фазы, образуя вторичные кристаллы (αII). Эти вторичные кристаллы αII и βII находятся не в структурно свободном состоянии, а в виде твердого раствора; αII – это твердый раствор А в Б, а βII – твердый раствор Б в А. Таким образом, при понижении температуры на линии DF выделяются вторичные кристаллы βII, а на линии EG – вторичные кристаллы αII. Следовательно, в левой области диаграммы состояния образуется гетерогенная структура, представляющая механическую смесь кристаллов твердого раствора α и вторичных кристаллов βII, а в правой – гетерогенная структура из смеси кристаллов β+αII.
В доэвтектических сплавах (ниже линии DC) при охлаждении из α-фазы выделяется β-фаза и образуется гетерогенная структура (конгломератного типа), состоящая из эвтектики плюс α- и β-фаза. В заэвтектических сплавах выделяется αII – фаза и образуется гетерогенная структура из эвтектики плюс β- и αII – фаза.
У этих типов сплавов в той части, где имеют место однофазные области твердых растворов (области α- и β-фазы), физико-химические свойства (твердость, механическая прочность, удельное электрическое сопротивление и др.) проявляют криволинейную концентрационную зависимость, как это наблюдалось у сплавов, образующих твердые растворы с неограниченной растворимостью компонентов в твердом состоянии. В двух фазных областях свойства изменяются аддитивно, как это наблюдалось у сплавов, образующих гетерогенные структуры.
Таким образом, в области, ограниченной линией FDEG, существует эвтектика (α + β) и избыточные кристаллы: слева α и (βII), справа β (и αII).
Диаграмма состояния сплавов III-го типа, компоненты которых образуют устойчивые, химические соединения представлена на рисунке 7.10.
Сплавы, образующие химические соединения одного металла с другим, называются интерметаллидами.
б
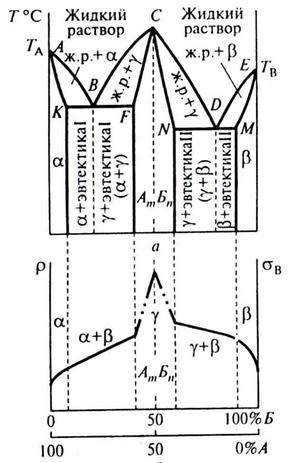
Рисунок 7.10 – Диаграмма состояния сплавов, образующих химические соединения (а) и изменение физико-химических свойств в зависимости от состава в общем виде (б)
Устойчивое химическое соединение AmБn, состоящее из химических элементов А и Б, является по существу самостоятельным веществом – компонентом, который может образовывать сплавы с каждым из входящим в него элементов (А и Б).
Диаграмму состояния сплавов, в которых присутствует устойчивое химическое соединение AmБn, можно разделить на две части, фактически на две самостоятельные диаграммы состояния (см. рисунок 7.10).
В месте соединения двух диаграмм можно выделить точку перелома или острие вершины – точку С, соответствующую концентрациям компонентов А и Б, при которых образуется устойчивое химическое соединение AmБn. Эту точку (С) называют сингулярной. Одна часть диаграммы (левая) характеризует сплавы, образуемые компонентом А и компонентом химического соединения AmБn (область А- AmБn). Правая часть диаграммы характеризует сплавы, образуемые Б и AmБn (область В- AmБn). При этом в левой области нет компонента Б, а в правой – А. Сплавы каждой части диаграммы представляют собой сплавы с ограниченной растворимостью в твердом состоянии и образуют соответствующие эвтектики (эвтектику I и эвтектику II).
γ-фаза – это сплавы, образующие твердые растворы, состоящие из вещества AmБn, в котором частично растворены химические элементы А и Б, образовавшие вещество AmБn. При этом слева от пунктирной перпендикулярной линии, опущенной из точки С, в AmБn растворен компонент А, а справа – компонент Б; α-фаза – это твердый раствор компонента Б в А, β-фаза – это твердый раствор компонента А в Б.
В точке В образуется эвтектика I – механическая смесь α- и γ-фазы. Слева от точки В и ниже линии КВ образуется механическая смесь, состоящая из α-фазы плюс эвтектика I (α + γ), справа от точки В и ниже линии BF – механическая смесь, состоящая из γ-фазы плюс эвтектика I (α + γ). В точке D (собственно по всей линии NDM) образуется эвтектика II (β + γ). Слева точки D образуется механическая смесь, состоящая из γ-фазы плюс эвтектика II (β + γ), а справа точки D – смесь из β-фазы плюс эвтектика II (β + γ).
Физико-химические свойства сплавов (твердость, удельное электрическое сопротивление и др.) в зависимости от концентрации элементов А и Б изменяются неравномерно (см. рисунок 4.10.б). Когда образуются сплавы твердые растворы, свойства проявляют криволинейную концентрационную зависимость, когда образуются сплавы гетерогенные структуры – аддитивную зависимость. Составу, образующему сплав химическое соединение AmБn, на концентрационной зависимости соответствует экстремум изменения физико-химических свойств.
Если компоненты А и Б при определенных соотношениях образуют друг с другом несколько явно выраженных устойчивых химических соединений, то на кривой зависимости удельного электрического сопротивления ρ, ТКр (и других физико-химических характеристик) от состава наблюдаются несколько сингулярных точек, каждая из которых соответствует новому химическому соединению. Между этими точками свойства сплавов изменяются линейно или криволинейно, в зависимости от типа образующихся сплавов. Химические соединения обладают свойствами, обычно резко отличающимися от свойств образующих компонентов. Например, химические соединения металлов с углеродом – карбиды и азотом – нитриды имеют очень высокую твердость, но хрупки.
Установлено, что чем больше интервал кристаллизации, тем больше склонность сплавов к образованию ликваций, рассеянной пористости и трещин в отливках. Лучшими литейными свойствами обладают эвтектические сплавы. Они лучше обрабатываются резанием, дают наилучшую чистоту обработки поверхности. Однофазные сплавы (твердые растворы) лучше деформируются как в горячем, так и в холодном состоянии.
Диаграмма состояния Fe - Fe 3 C
Диаграмма состояния железоуглеродистых сплавов (рисунок 7.11) описывает равновесное состояние сплава железо-углерод в зависимости от содержания углерода и температуры. По ней судят о структуре медленно охлажденных сплавов, а также о возможности изменения их микроструктуры в результате термической обработки, определяющей эксплуатационные свойства сплавов.
На диаграмме состояния железоуглеродистых сплавов, на оси ординат отложена температура, на оси абсцисс – содержание в сплавах углерода до 6,67 %, т.е. до такого количества, при котором образуется химическое соединение Fe3C-цементит. Пунктирными линиями нанесена диаграмма состояния системы железо – графит, так как возможен распад цементита.
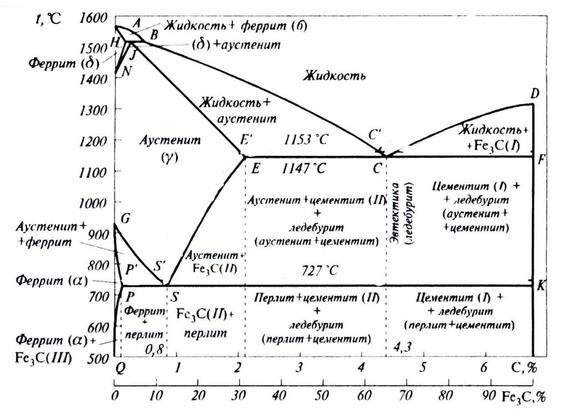
Рисунок 7.11 – Диаграмма состояния Fe-Fe3C
Рассматриваемую диаграмму правильнее считать не железоуглеродистой, а железоцементитной, так как свободного углерода в сплавах не содержится. Но так как содержание углерода пропорционально содержанию цементита, то практически удобнее все изменения структуры сплавов связывать с различным содержанием углерода.
Все линии на диаграмме соответствуют критическим точкам, т. е. тем температурам, при которых происходят структурные изменения в сплавах.
Точка А (1539 °С) соответствует температуре плавления чистого железа, точка D (1250 °С) – температуре плавления цементита Fe3C. Точки N (1392 °С) и G (910 °С) соответствует полиморфному превращению 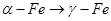 . Точка Е (1147 °С) характеризует предельную растворимость углерода (2,14 %) в
. Точка Е (1147 °С) характеризует предельную растворимость углерода (2,14 %) в 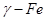 . Верхний левый угол диаграмма характеризует аллотропическое превращение
. Верхний левый угол диаграмма характеризует аллотропическое превращение 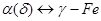 при высоких температурах. В интервале температур
при высоких температурах. В интервале температур 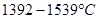
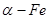 нередко обозначается, как
нередко обозначается, как 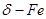 .
.
Линия ACD – линия начала кристаллизации сплава (линия ликвидуса), линия AECF – линия конца кристаллизации сплава (линия солидуса). Область AESG на диаграмме соответствует аустениту. Линия GS – начало выделения феррита, а линия SE – вторичного цементита. Линия PSK соответствует окончательному распаду аустенита и выделению перлита. В области ниже линии PSK никаких изменений структуры не происходит. Линия GSK и PSK имеют большое значение при термической обработке стали. Линию GSK называют линией верхних критических точек.
По мере охлаждения сплав железо-углерод проходит фазы жидкости и твердого тела.
Основными структурными составляющими железоуглеродистых сплавов являются:
- феррит;
- цементит;
- аустенит;
- перлит;
- ледебурит;
- графит.
При этом феррит и аустенит являются твердыми растворами, цементит – химическое соединение (Fe3C), перлит и ледебурит – механические смеси, а графит – разновидность углерода.
Феррит – твердый раствор углерода в 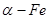 (рисунок 4.12). Атомы углерода располагаются в центре граней куба, в вакансиях, на дислокациях. Предельная растворимость углерода в феррите при 20
(рисунок 4.12). Атомы углерода располагаются в центре граней куба, в вакансиях, на дислокациях. Предельная растворимость углерода в феррите при 20 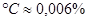 , 727
, 727 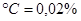 , в интервале 1392-1539
, в интервале 1392-1539 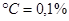 . В смеси с другими фазами феррит устойчив ниже линии GSK на диаграмме (рисунок 4.11) в доэвтектоидных сталях, серых и ковких чугунах. Чистый феррит пластичен, имеет небольшую прочность и твердость, магнитен.
. В смеси с другими фазами феррит устойчив ниже линии GSK на диаграмме (рисунок 4.11) в доэвтектоидных сталях, серых и ковких чугунах. Чистый феррит пластичен, имеет небольшую прочность и твердость, магнитен. 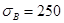 МПа,
МПа, 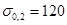 МПа,
МПа, 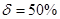 ,
, 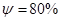 , HB 800-900 МПа.
, HB 800-900 МПа.
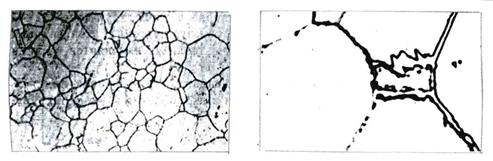
а - < 0,006 % С. ×300; б – 0,01 % С. ×600
Рисунок 7.12 – Микроструктура технически чистого железа
Аустенит – твердый раствор углерода в 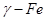 . Предельная растворимость углерода в аустените 2,14 % при 1147 °С. Атомы углерода располагаются в центре элементарной ячейки и дефектных областях кристалла. Повышенная растворимость углерода в аустените обусловлена большим объемом и числом пор в кристаллической решетке
. Предельная растворимость углерода в аустените 2,14 % при 1147 °С. Атомы углерода располагаются в центре элементарной ячейки и дефектных областях кристалла. Повышенная растворимость углерода в аустените обусловлена большим объемом и числом пор в кристаллической решетке 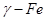 . Аустенит устойчив в железоуглеродистых сплавах при
. Аустенит устойчив в железоуглеродистых сплавах при 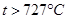 . Прочность и твердость (HB=1700-2000 МПа) аустенита в 2,5-3 раза больше феррита при той же пластичности и пределе текучести; он легко наклепывается, обладает большим температурным коэффициентом теплового расширения.
. Прочность и твердость (HB=1700-2000 МПа) аустенита в 2,5-3 раза больше феррита при той же пластичности и пределе текучести; он легко наклепывается, обладает большим температурным коэффициентом теплового расширения.
Перлит – эвтектоидная смесь феррита и цементита; образуется в процессе распада аустенита при 723 °С и содержании углерода 0,83 %. Примеси Si и Mn способствуют образованию перлита и при меньшем содержании углерода. Структура перлита может быть пластинчатой и глобулярной (зернистой). Механические свойства перлита зависят от формы и дисперсности частичек цементита. Прочность пластинчатого перлита несколько выше, чем зернистого.
Ледебурит – эвтектическая смесь аустенита и цементита, образующаяся при 1130 °С и содержании углерода 4,3 %. Структура неустойчивая: при охлаждении аустенит, входящий в состав ледебурита, распадается на вторичный цементит и перлит. Ледебурит очень тверд (HB = 700), хрупок.
Графит – мягкий и хрупкий компонент чугуна, состоящий из разновидностей углерода. Встречается в серых и ковких чугунах.
Цементит – химическое соединение железа с углеродом – карбид железа (Fe3C), содержащий 6,67 % С, имеет сложную ромбическую решетку с плотной упаковкой атомов. Цементит является метастабильной фазой, претерпевающей изменения при легировании и термической обработке сплавов. Различают первичный цементит, выделяющийся при кристаллизации из жидкого расплава и вторичный и третичный цементиты, выделяющиеся при распаде аустенита и феррита. Твердость цементита HB – 8000 МПа, он хрупок.
В зависимости от содержания углерода сплавы железа с углеродом подразделяют на стали (С < 2,14 %) и чугуны (С от 2,14 до 6,67 %).
Стали подразделяют в свою очередь на:
- технически чистое железо ( 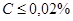 );
);
- доэвтектоидные стали ( 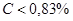 );
);
- эвтектоидные стали (С = 0,83 %);
- заэвтектоидные стали (0,83…2,14 % С).
Структура доэвтектоидных сталей состоит их феррита и перлита, эвтектоидной стали – из одного перлита, а заэвтектоидных сталей – из перлита и цементита, который выделяется по границам зерен перлита, уменьшая однородность структуры, характерную для эвтектоидной стали (рисунок 7.13).
а б в



г д

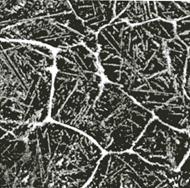
а – сталь с 0,15 % С: зерна феррита (светлые) и участки перлита (темные); б – сталь с 0,8 % С (пластинчатый перлит); в – сталь с 0,85 % С (пластины мартенсита и остаточный аустенит);
г – сталь с 0,91 % С (сфероидизированный цементит в феррите); д – сталь с 1,18 % С: сетка и пластины цементита (светлые) в перлите
Рисунок 7.13 – Структура сталей
При нормальных температурах в обычных углеродистых сталях аустенит не сохраняется. Он существует лишь при температурах выше 723 °С, распадаясь при охлаждении на эвтектоидную смесь феррита и цементита, называемую перлитом. Однако аустенит, обладая высокой пластичностью и вязкостью, играет очень важную роль в технологии стали, обусловливая возможность термической и механической обработки давлением (прокат, ковка, штамповка).
При введении большого количества (более 10 %) некоторых легирующих добавок (марганца, хрома, никеля и др.) аустенит может содержаться в структуре стали и при обычных температурах (например, в высокомарганцовистой стали, используемой для устройства крестовин железнодорожных стрелочных переводов).
Железоуглеродистые сплавы с содержанием углерода от 2,14 % до 6,67 % называются чугунами.
Чугуны делятся на три группы: доэвтектические (С = 2,14-4,3 %), эвтектический (С = 4,3 %) и заэвтектические (С > 4,3 %). Структура доэвтектических чугунов – прелит + цементит (II) + ледебурит, эвтектических – ледебурит (II) и заэвтектических – ледебурит (II) + цементит (I). Чугуны, в которых весь углерод связан и находится в форме цементита, называют белыми (рисунок 7.14).
а б в
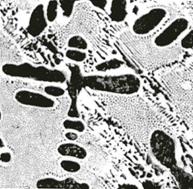
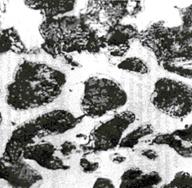
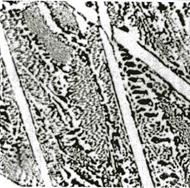
а – белый доэвтектический чугун: дендриты первичного аустенита (и ледебурит);
б – доэвтектический чугун (эвтектический монолитный цементит и перлит);
в – белый заэвтектический чугун (пластины первичного цементита и ледебурит)
Рисунок 7.14 – Структура белого чугуна
На диаграмме железоуглеродистых сплавов (рисунок 7.11) показаны белые чугуны, применяющиеся, как правило, не для изготовления чугунных изделий, а для получения стали. В белых чугунах углерод находится в химически связанном состоянии, т. е. в виде цементита. При медленном охлаждении и большом содержании кремния цементит распадается с выделением свободного углерода в виде графита; образуются серые чугуны, используемые для получения отливок, в том числе и для строительных деталей (опорных частей мостов, труб, тюбингов и т. д.).
С увеличением содержания углерода в железоуглеродистых сплавах меняется и структура, увеличивается содержание цементита и уменьшается количество феррита. Чем больше углерода в сплавах, тем выше их твердость и прочность, но ниже их пластические свойства. Механические свойства сплавов зависят также от формы и размера частиц структурных составляющих. Твердость и прочность стали тем выше, чем тоньше и мельче частицы феррита и цементита.
Дата: 2019-02-02, просмотров: 1204.