Обычно, считается, что извлечение проведено практически полностью (т.е. количественно), если R ≥ 99,9%. Если же R < 99,9%, то экстракционное извлечение повторяют.
Влияние объема экстрагента и числа экстракций на процессы экстракции.
Как уже отмечалось, экстракция веществ из одной жидкой фазы (обычно водной) в другую жидкую фазу (органическую) тем эффективнее, чем больше степень извлечения R. Выясним, как влияют на величину R объем экстрагента и число экстракций..Зависимость степени извлечения R от объема исходной водной фазы Vводн объема экстрагента Vорг и числа n последовательных экстракций одинаковым объемом Vорг описывается соотношением:
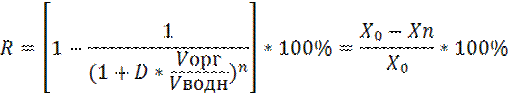
где D – коэффициент распределения.
Анализ формулы приводит к практически важным следствиям:
1. чем больше число экстракций n, тем выше степень извлечения экстрагируемого вещества.
2. чем больше объем органической фазы экстрагента, т.е. чем выше отношение Vорг/Vводн, тем больше степень извлечения экстрагируемого вещества (при неодинаковых объемах органической и водной фаз).
3. увеличение числа экстракций сильнее влияет на степень извлечения экстрагируемого вещества, чем увеличение объема экстрагента в то же число раз, поэтому одну и ту же степень извлечения можно получить, уменьшая объем экстрагента Vорг, но увеличивая число экстракций n. Обычно применяют 5-6 последовательных экстракций (делят экстрагент на 5-6 частей). Если коэффициент распределения достаточно велик (D > 100), то для практически количественного извлечения экстрагируемого вещества в органическую фазу бывает достаточно одной экстракции.
Органические растворители, используемые в процессе экстракции
Для экстракции органических веществ и координационных соединений элементов используют органические растворители различной природы:
1. углеводороды
а) гексан
б) циклогексан
в) бензол
г) толуол
2. хлороформные углеводороды
а) хлороформ
б) четыреххлористый углерод
в) хлорбензол
3. спирты
а) изоамиловый
б) бутиловый
в) изобутиловый
г) циклогексанол
4. простые и сложные эфиры
а) диэтиловый эфир
б) амилацетат
в) бутилацетат
5. кетоны
а) метилизобутилкетон
б) метилэтилкетон
в) циклогексанон
Природа органического растворителя в ряде случаев оказывает существенное влияние на экстракцию. Важны диэлектрическая проницаемость растворителя, его сольватирующая способность, способность участвовать в кислотно-основных взаимодействиях.
Экстракция типа твердое тело – жидкость
В фармации, кроме экстракции из жидкой фазы, широко применяется экстракция из твердой фазы, например для извлечения из растительного сырья различных масел и других физиологически активных веществ. Такой вид экстракции называется экстракцией типа твердое тело – жидкость.
Экстрагирование в системе твердое тело – жидкость – это извлечение одного или нескольких компонентов из сложного твердого тела путем избирательной растворимости.
В качестве растворителя применяется жидкость (экстрагент), в которой хорошо растворяется извлекаемый компонент и плохо – другие составляющие твердого тела.
Известны примеры, когда второй фазой (экстрагентом) может быть расплав какого-либо органического вещества (например, нафталин), содержащий органический реагент. После распределения вещества фазы охлаждают, расплав застывает, и его отделяют от водной фазы. В некоторых экстракционных системах органическая или водная фаза может расслаиваться с образованием трехфазной системы, причем одна из фаз – часто очень небольшая по объему – содержит практически все экстрагируемое соединение.
ЭТАЛОНЫ РЕШЕНИЯ ЗАДАЧ
Задача 1
Рассчитайте коэффициент распределения D фенола между водой и хлороформом при 25°С, если концентрация фенола в воде и хлороформе соответственно равны ΣСводн. = 0,0737; ΣСорг. = 0,254 моль/л.
Решение:
Аналитическая концентрация – это суммарная концентрация данного вещества в растворе. В соответствии с формулой можно записать:
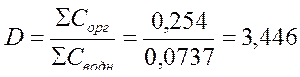
Задача 2
<Определите степень извлечения йода однократной экстракцией сероуглеродом из водной фазы при 25°С, если аналитическая концентрация йода в водной и органической фазах, находящихся в равновесии равна 25,71•10-5 и 0,1676 моль/л соответственно. Объёмы водной и органической фазы равны.
Решение:
Вначале вычислим коэффициент распределения йода:
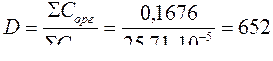
Теперь по формуле найдём степень извлечения йода с сероуглеродом из водного раствора:
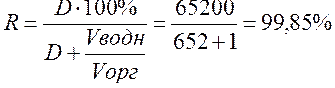
Задача 3
<При ><экстракции ><микроколичеств ><олова(I><V) ><диэтиловым ><эфиром ><из ><водных >< ><солянокислых >< ><(с(НС1) >< ><= >< ><6 >< >< ><моль/л) >< ><растворов >< >< ><коэффициент ><распределения ><олова(IV) ><D(Sn(IV)) ><= ><0,71. ><В ><присутствии ><в ><водном ><растворе ><железа(III) >< >< >< ><коэффициент >< >< ><распределения >< >< >< ><олова(IV) >< >< >< ><возрастает >< >< ><до ><D(Sn(IV)) ><= ><3,77 ><за ><счет ><соэкстракции.>
<Рассчитайте ><степень ><извлечения ><R ><олова(IV) ><при ><отсутствии ><и ><в ><присутствии ><железа (III) ><в ><водном ><растворе, ><если ><объем ><водного ><раствора ><равен ><объему ><экстрагента ><— ><органической ><фазы.>
<Решение:
><Согласно ><формуле, ><><степень ><извлечения>:
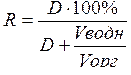
<><Поскольку ><по ><условию ><V><водн>< ><=V><opr><, ><то:>
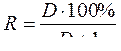
<><Следовательно, ><при ><отсутствии ><в ><растворе ><железа(III) >
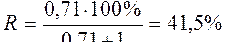
<><В ><присутствии ><в ><растворе ><железа(III)>
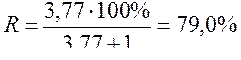
<Таким ><образом, ><железо(III) ><способствует ><увеличению ><степени ><извлечения ><микроколичеств ><олова(IV) ><из ><солянокислых ><водных ><растворов ><почти ><в ><два ><раза ><(соэкстракция).>
Задача 4
<Определите, ><как ><изменится ><степень ><извлечения ><олова(IV) ><диэтиловым ><эфиром, ><если ><в ><предыдущем ><примере ><объем ><экстрагента ><а) ><уменьшить ><в ><10 ><раз ><или ><б) ><увеличить ><в ><10 ><раз ><по ><сравнению ><с ><объемом ><водной ><фазы.>
<Решение:
><a) 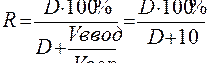 >
>
<><так ><как 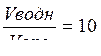 ><.>
><.>
<При ><отсутствии ><железа ><(III) ><степень ><извлечения ><олова(IV)>
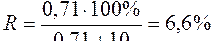
<><><><><><><><В ><присутствии ><железа ><(III) ><степень ><извлечения ><олова(IV)>
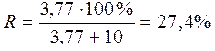
<Таким ><образом, ><степень ><извлечения ><олова(IV) ><из ><водных ><солянокислых ><растворов ><падает ><с ><уменьшением ><объема ><органической ><фазы ><(экстрагента).>
<б)  >
>
<><так ><как 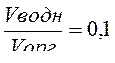 ><.>
><.>
<При ><отсутствии ><железа ><(III) ><степень ><извлечения ><олова(IV) ><равна>
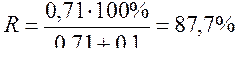
<><><><><><><>< ><В ><присутствии ><железа ><(III) ><степень ><извлечения ><олова(IV) >
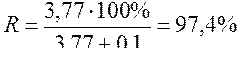
<следовательно, ><степень ><извлечения ><олова(IV) ><из ><водных ><солянокислых ><растворов ><возрастает ><с ><увеличением ><объема ><органической ><фазы ><(объема ><экстрагента).>
Задача 5
<<><Коэффициент ><распределения ><йода ><I><2>< ><между ><хлороформом ><и ><водой ><при ><25><°С ><составляет ><D(I><2><) ><=133. ><Определите ><отношение ><объемов ><органической ><и ><водной ><фаз ><( 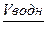 ><><), ><при ><котором ><степень ><извлечения ><иода ><из ><водного ><раствора ><в ><хлороформ ><составит <R(I><2>)>< ><= ><99,9%.>
><><), ><при ><котором ><степень ><извлечения ><иода ><из ><водного ><раствора ><в ><хлороформ ><составит <R(I><2>)>< ><= ><99,9%.>
<Решение :
><В ><соответствии ><с ><формулой>
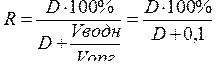
<><в ><данном ><случае:>
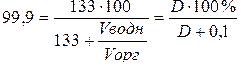
<><Решая ><это ><уравнение ><относительно 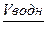 ><><, ><получаем: >
><><, ><получаем: >
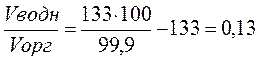
<Следовательно, ><чтобы ><добиться ><степени ><извлечения ><иода ><из ><водного ><раствора ><в ><хлороформ, ><равной ><99,9 ><%, ><при ><однократной ><экстракции ><необходимо, ><чтобы ><объем ><органической ><фазы ><был ><больше ><объема ><водной ><фазы ><в ><1/0,13 ><~ ><7,7 ><раза.>
Задача 6
Определите, сколько потребуется последовательных экстракций (n) для извлечения на 99,9% йода из водного раствора хлороформом, если объём органической фазы, используемой каждый раз для экстракционного извлечения, в 10 раз больше объёма водной фазы <( 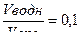 ><>).
><>).
<Степень ><извлечения ><йода, ><как ><и ><в ><предыдущем ><примере, ><равна ><99,9%, ><коэффициент ><распределения ><йода ><между ><хлороформом ><и ><водой ><равен>
<D(I><2><) ><=133.>
<Решение :>< ><
><><><Степень ><><извлечения>
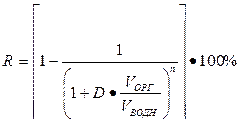
<><В ><><рассматриваемом ><><случае>
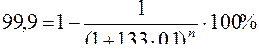
<><Решая ><это ><уравнение ><относительно ><n, ><получаем: ><n ><= ><2,6 ><~ ><3. ><Таким ><образом, ><требуются ><три ><последовательные ><экстракции.>
<Сравнивая ><полученные ><результаты ><с ><данными, ><приведенными ><в ><предыдущем ><примере, ><можно ><заключить, ><что ><при ><последовательной ><кратной ><экстракции ><расходуется ><намного ><меньше ><органического ><экстрагента ><(в ><данном ><случае ><— ><примерно ><в ><26 ><раз) ><для ><достижения ><одной ><и ><той ><же ><степени ><извлечения.>
Задачи для самостоятельного решения
< 1. Рассчитайте ><коэффициент ><распределения ><D ><муравьиной ><кислоты ><НСООН ><между ><бензолом ><и ><водой ><при ><25><°С ><и ><при ><двух ><ее ><суммарных ><концентрациях ><в ><водной ><фазе, ><равных ><2,5739 ><и ><9,0466 ><моль/л, ><если ><суммарные ><концентрации ><в ><органической ><фазе, ><находящейся ><в ><равновесии ><с ><водной ><фазой, ><соответственно ><равны ><0,00568 ><и ><0,0378 ><моль/л. >< Ответ: ><0,0022 ><и ><0,0042.>
< 2. Рассчитайте ><коэффициент ><распределения ><D ><уксусной ><кислоты ><СНЗСООН ><между ><хлороформом ><и ><водой ><при ><25><°С, ><находящимися ><в ><равновесии, ><если ><аналитическая ><концентрация ><уксусной ><кислоты ><в ><водной ><и ><органической ><фазе ><равна ><соответственно ><1,188 ><и ><0,1351 ><моль/л.> < Ответ: ><0,1137.>>
<< 3. Рассчитайте ><коэффициент ><распределения ><D ><йода ><между ><сероуглеродом ><и ><водой, ><находящимися ><в ><равновесии ><при ><25><°С, ><если ><аналитическая ><концентрация ><йода ><в ><органической ><и ><водной ><фазе ><равна ><соответственно ><0,03036 ><и ><5,18*10-><5><моль/л.> < Ответ: ><586.>
< 4. Определите ><степень ><извлечения ><бензойной ><кислоты ><С><6><Н><5><СООН ><диэтиловым ><эфиром ><из ><водного ><раствора ><при ><10><°С ><однократной ><экстракцией, ><если ><аналитическая ><концентрация ><бензойной ><кислоты ><в ><водной ><и ><органической ><фазе ><соответственно ><равна ><0,00249 ><и ><0,226 ><моль/л. ><Объемы ><водной ><и ><органической ><фазы ><одинаковы.> < Ответ: ><98,9%.>
< 5. При ><экстракции ><диэтиловым ><эфиром ><микроколичеств ><сурьмы(V) ><из ><водных ><солянокислых ><растворов ><(с(НС1) ><= ><6 ><моль/л) ><коэффициент ><распределения ><сурьмы(V) ><D(Sb><v><) ><= ><4,7. ><В ><присутствии ><в ><водном ><растворе ><железа(III) ><коэффициент ><распределения ><сурьмы(V) ><возрастает ><до ><D(Sb><v><) ><= ><22,1: ><наблюдается ><соэкстракция.> <Рассчитайте ><степень ><извлечения ><сурьмы(V) ><из ><водных ><растворов ><в ><органическую ><фазу ><при ><отсутствии ><и ><в ><присутствии ><железа(III), ><если ><объем ><водной ><и ><органической ><фаз ><одинаков: ><V><водн>< ><=V><opr><.> < Ответ: ><степень ><извлечения ><сурьмы(V) ><равна ><82,5 ><и ><95,5% ><при ><отсутствии ><и ><в ><присутствии ><железа(III) ><соответственно.>
< 6. Определите, ><как ><изменится ><степень ><извлечения ><сурьмы(V), ><если ><в ><предыдущей ><задаче: ><а) ><уменьшить ><объем ><органического ><экстрагента ><(диэтилового ><эфира) ><в ><5 ><раз ><или ><б) ><увеличить ><объем ><органического ><экстрагента ><в ><5 ><раз.> <Ответ: ><а) ><степень ><извлечения ><сурьмы(V) ><понизится ><до ><48,5 ><и ><80,4% ><соответственно ><при ><отсутствии ><и ><в ><присутствии ><железа(III); ><б) ><степень ><извлечения ><сурьмы(V) ><возрастет ><до ><95,9 ><и ><99,1% ><соответственно ><при ><отсутствии ><и ><в ><присутствии ><железа(III).>
< 7. При ><экстракции ><микроколичеств ><ионов ><цинка ><Zn ><диэтиловым ><эфиром ><из ><кислых ><водных ><растворов ><(с(III) ><=1,5 ><моль/л) ><степень ><извлечения ><цинка ><из ><водного ><раствора ><составляет ><R(Zn><2+><) ><= ><36,31%, ><а ><в ><присутствии ><ионов ><кадмия ><Cd><2+>< ><возрастает ><до ><R(Zn><2+><) ><= ><84,92% ><(наблюдается ><соэкстракция ><цинка ><и ><кадмия). ><Вычислите ><коэффициент ><распределения ><цинка ><между ><органической ><и ><водной ><фазами ><в ><обоих ><случаях, ><если ><объем ><водной ><и ><органической ><фаз ><одинаков.> < Ответ: ><0,57 ><и ><3 ><при ><отсутствии ><и ><в ><присутствии ><ионов ><кадмия ><соответственно.>
< 8. При ><экстракции ><анилином ><микроколичеств ><вольфрама(VI) ><из ><водных ><солянокислых ><растворов ><(с(НС1) ><=1,5 ><моль/л) ><в ><форме ><солей ><— ><поливольфраматов ><анилиния ><коэффициент ><распределения ><вольфрама ><между ><органической ><и ><водной ><рами ><составляет ><D(W><VI><) ><= ><9. ><В ><присутствии ><соединений ><молибдена(VI) ><он ><возрастает ><до ><D(W><VI><) ><= ><4450. ><Рассчитайте ><степень ><извлечения ><микроколичеств ><вольфрама(VI) ><в ><обоих ><случаях, ><если ><объемы ><водной ><и ><органической ><фаз ><одинаковы. >< Ответ: ><90 ><и ><99,98%;> <соэкстракция ><с ><молибденом(VI) ><приводит ><практически ><к ><полному ><переводу ><вольфрама(VI) ><из ><водной ><в ><органическую ><фазу.>>
<< 9. ><Коэффициент ><распределения ><бензойной ><кислоты ><между ><диэтиловым ><эфиром ><и ><водой ><при ><10><°С ><составляет ><D ><= ><90,91. ><Определите ><отношение ><объемов ><органической ><и ><водной ><фаз, ><при ><котором ><степень ><извлечения ><бензойной ><кислоты ><из ><водного ><раствора ><будет ><равна ><R ><= ><99%.> <Ответ: ><V><opr>< ></ ><У><водн>< ><~ ><1,1, ><т. ><е. ><объем ><органической ><фазы ><в ><1,1 ><раза ><превышает ><объем ><водной ><фазы.>
< 10. ><Определите ><число ><последовательных ><экстракций (><n) ><для ><извлечения ><на ><99% ><(как ><в ><предыдущей ><задаче) ><бензойной ><кислоты ><из ><водного ><раствора ><диэтиловым ><эфиром, ><если ><каждый ><раз ><для ><извлечения ><берется ><объем ><органической ><фазы, ><в ><10 ><раз ><меньший ><объема ><водной ><фазы. ><Коэффициент ><распределения ><D ><= ><90,91.> <Ответ: ><n ><= ><2, ><т. ><е. ><достаточно ><двух ><последовательных ><экстракций.>>
Контрольные вопросы и задания по теме занятия
1. Что называют простой перегонкой?
2. Что называют фракционной перегонкой? Что такое ректификация?
3. В чем заключаются особенности жидких смесей с взаимно нерастворимыми жидкостями? Что такое перегонка с водяным паром?
4. Каковы основные понятия жидкостной экстракции? Что такое экстрагент, экстракт?
5. В чем сущность закона распределения Нернста? Что называют константой распределения Р?
6.Что называют коэффициентом распределения D?
7. Что называют степенью извлечения (процентом экстракции) R?
8. В чем заключается взаимосвязь степени извлечения с коэффициентом распределения?
9. В чем заключается влияние на величину R объема экстрагента и числа экстракций? Каково применение экстракций в фармации?
Основная литература:
1. Аналитическая химия (аналитика). Общие теоретические основы. Качественный анализ. [Текст]: учеб. для вузов / Ю.Я. Харитонов [и др.]. - М.: Высш. шк., 2008. – 240 – 259 с.
Дополнительная литература:
1. Основы аналитической химии. Практическое руководство. Учеб. пособие для вузов [Текст] / Под ред. Ю.А. Золотова - М.: Высш. шк., 2001. – 142 – 154 с.
Тема 16 - 17
Дата: 2019-02-02, просмотров: 563.