Гель-хроматография
Метод основан на использовании в качестве НФ пористых веществ – так называемых молекулярных сит, размеры пор которых могут быть больше или меньше размеров частиц разделяемых компонентов. Частицы с размерами, меньшими размерам пор сорбента, проникают вместе с растворителем ПФ в эти поры и могут удерживаться в них, тогда как более крупные частицы не могут проникать в поры из-за своих размеров и уносятся с ПФ. Происходит разделение мелких и крупных частиц. Крупные частицы элюируются, таким образом, первыми. Более мелкие частицы, попавшие в поры НФ, элюируются после крупных частиц.
Методом ситовой хроматографии можно:
1) разделять высокомолекулярные и низкомолекулярные вещества
2) проводить обессоливание растворов
3) удалять примеси из газов, жидкостей т.д.
В качестве НФ применяют пористые стекла, уголь, продукты пиролиза пластмасс, силикаты натрия или кальция, различные гели. Ситовая хроматография, в которой в качестве НФ применяют гели, называется гель-хроматография (гель-проникающая хроматография).
Гели представляют собой вещества, способные к набуханию и имеющие поры разного размера. В зависимости от поставленных задач применяют гидрофильные и гидрофобные гели. К гидрофильным гелям относятся декстрановые (сефадексы, молселекты), полиакриламидные (биогели), оксиалкилметакрилатные (сфероны) и некоторые другие гели. К гидрофобным гелям относятся некоторые сефадексы, полистерольные (стирогель, порагель), поливинилацетатные гели, пористый силикагель, пористое стекло (порасил).
В независимости от способа решения поставленных задач иногда различают:
1) гель-фильтрование (гель-фильтрацию) – отделение очень больших по размеру молекул от небольших
2) собственно гель-хроматографию – разделение смеси частиц с неодинаковыми, но не экстремально различными размерами
При проведении процесса разделения часть жидкой ПФ проникает в поры геля, так что разделяемые частицы распределяются между НФ и ПФ одной и той же природы. Эффективность разделения компонентов зависит как от размеров частиц, так и от различий в скоростях их диффузии в жидкую фазу, находящуюся в порах геля. Сродство разделяемых веществ к самому пористому носителю должно быть минимальным.
Применяют различные гели: мягкие, полужесткие и жесткие.
Процессы разделения компонентов смеси в гель-хроматографии проводят либо в 1) хроматографических колонках, заполненных сорбентом – гелем, либо 2) на стеклянных пластинках, покрытых тонким закрепленным слоем геля (метод восходящей хроматографии), с использованием окрашенного стандарта, предварительно наносимого на линии старта и перемещающегося вместе с ПФ.
Гель-хроматография применяется:
1) при обессоливании растворов (малые по размеру ионы солей проникают в поры геля и удерживаются там)
2) для группового разделения высокомолекулярных и низкомолекулярных органических соединений (например, глицеридов жирных кислот с молекулярной массой около 200-500)
3) в анализе биологических объектов (часто с использованием буферных систем с целью предотвратить разрушение ферментов)
4) для определения молекулярной массы белков (в том числе содержащихся в сыворотке крови, в спинномозговой жидкости)
5) углеводов и других веществ
Для проведения более точных анализов применяют специальные физико-химические приборы – хроматографы (газовые или жидкостные). Хроматографы поддерживают все параметры хроматографического разделения на заданном уровне и преобразуют сигнал детектора в форму, удобную для количественного определения содержания веществ.
Основные узлы хроматографов – устройство для ввода пробы, хроматографическая колонка, детектор. В колонке с сорбентом анализируемая проба разделяется на составные компоненты. Детектор, расположенный на выходе из колонки, автоматически непрерывно определяет количество разделяемых веществ в потоке элюента.
Все вещества анализируемой пробы после ввода в колонку с потоком подвижной фазы расположены в начале хроматографической колонки. В потоке подвижной фазы компоненты смеси перемещаются вдоль колонки со скоростями, обратно пропорциональными коэффициентам распределения этих веществ. Вещества, значения констант распределения которых велики, передвигаются вдоль слоя сорбента по колонке медленнее, чем вещества с малыми константами распределения.
Величины сигнала детектора пропорциональны концентрации веществ в потоке элюента. Они автоматически регистрируются, например на диаграммной ленте в виде хроматограммы. Полученная хроматограмма отражает расположение зон на слое сорбента или в потоке подвижной фазы во времени.
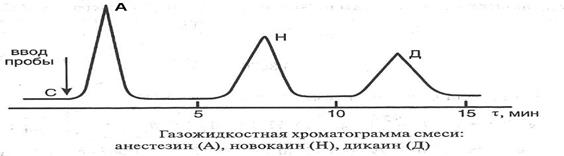
На рисунке представлена хроматограмма смеси лекарственных веществ (анестезин, новокаин, дикаин), полученная на хроматографе с использованием методики газожидкостной хроматографии. Идентификация лекарств проводится по времени удерживания τ – величине, измеряемой временем выхода данной зоны от момента ввода пробы в колонку. На сорбенте 3% полиэтиленгликольадипината на динохроме H при температуре Т = 573 K определены времена удерживания анестезина τ(A) = 102c, новокаина τ(Н) = 495с, дикаина (Д) = 765с. Площадь пика каждого вещества на хроматограмме при малых концентрациях пропорциональна содержанию этого вещества в пробе.
По технике выполнения выделяют хроматографические методы:
Колоночная хроматография.
В колонку (это обычно заполненная адсорбентом стеклянная трубка) вносят раствор смеси веществ. Затем колонку промывают растворителем. При продвижении растворителя происходит разделение смеси на отдельные вещества, которые располагаются зонами. Чем выше адсорбционная способность вещества, тем выше располагается в колонке соответствующая зона. В результате из колонки выходят фракции веществ в виде отдельной порции раствора. Этот раствор собирают и анализируют.
Тонкослойная хроматография.
Принцип и основные понятия метода ТСХ.
На чистую плоскую поверхность (пластинку из стекла, металла, пластмассы) наносят тонкий слой сорбента. На поверхности пластинки осторожно, чтобы не повредить слой сорбента, намечают (например, карандашом) линию старта (на расстоянии 2-3 см от нижнего края пластинки) и линию финиша растворителя.
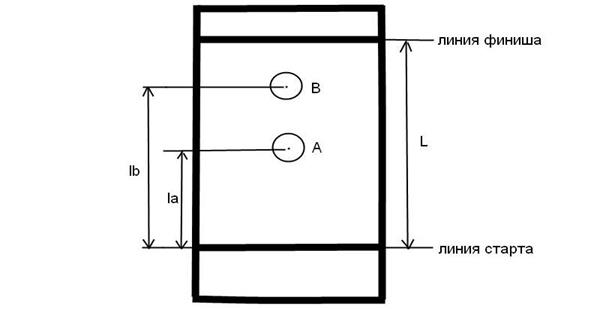
На линию старта пластинки наносят (микрошприцом, капилляром) пробу – небольшое количество жидкости, содержащей смесь разделяемых веществ, например, двух веществ А и В в подходящем растворителе. Дают возможность испариться растворителю, после чего пластинку погружают в хроматографической камере в жидкую фазу ПФ, представляющую собой специально подобранный для данного случая растворитель или смесь растворителей. Под действием капиллярных сил ПФ самопроизвольно перемещается вдоль НФ от стартовой линии до линии фронта растворителя, увлекая с собой компоненты условно А и В пробы, которые перемещаются с различной скоростью. Если сродство компонента А к НФ меньше сродства к той же фазе компонента В, то компонент А перемещается быстрее компонента В. После достижения за время t подвижной фазой (растворителем) линии финиша растворителя хроматографирование прерывают, пластинку извлекают из хроматографической камеры, высушивают на воздухе и определяют положение пятен веществ А и В на поверхности пластинки. Пятна (зоны) обычно имеют овальную или круглую форму. В рассматриваемом случае пятно компонента А переместилось от линии старта на расстояние lA, пятно компонента В – на расстояние lB , а растворитель прошел расстояние L.


 Для характеристики разделяемых компонентов используют коэффициент подвижности Rf (или Rf-фактор):
Для характеристики разделяемых компонентов используют коэффициент подвижности Rf (или Rf-фактор):
где Vi и VE – соответственно скорости перемещения i-ого компонента и растворителя Е; li и L – путь пройденный i-м компонентом и растворителем соответственно; t – время, необходимое для перемещения растворителя от линии старта до линии фронта растворителя. Расстояния li отсчитывают от линии старта до центра пятна, соответствующего компонента.
Обычно коэффициент подвижности лежит в пределах Rf = 0-1. Оптимальное значение составляет 0,3-0,7.
Коэффициент подвижности является важной характеристикой системы сорбент-сорбат. Для воспроизводимых и строго постоянных условий хроматографирование Rf = const.
Коэффициент подвижности Rf зависит от целого ряда факторов:
1) природы и качества растворителя, его чистоты
2) природы и качества сорбента (тонкого слоя), равномерности его зернения, толщины слоя
3) активности сорбента (содержания в нем влаги)
4) техники эксперимента (массы образца, длины L пробега растворителя)
навыка экспериментатора и т.д.
Для более надежной идентификации разделяемых компонентов используют «свидетели» - эталонные вещества, наличие которых предполагается в анализируемой пробе. Если Rf = Rf (свид), где Rf и Rf (свид) – соответственно коэффициенты подвижности данного компонента и свидетеля, то можно с большой вероятностью предположить, что вещество-свидетель присутствует в хроматографируемой смеси.
Для характеристики разделения двух компонентов А и В в данных условиях вводят степень (критерий) разделения R ( A / B ):
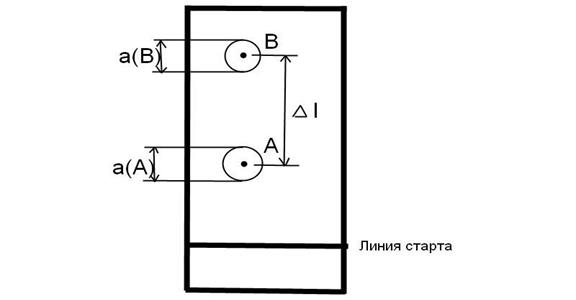
R(A/B) = Δl/[a(A)/2 + a(B)/2] = 2Δl/[a(A) + a(B)],
где Δl – расстояние между центрами пятен компонентов А и В; а(А) и а(В) – соответственно диаметры пятен А и В на хроматограмме.
Для оценки селективности разделения двух веществ А и В используют коэффициент разделения α:
α = lB/lA
где lB, lA – путь пройденный компонентами В и А.
Если α = 1, то компоненты А и В не разделяются.
Контрольные вопросы и задания по теме занятия
1. Кто изобрел хроматографию? Какой эксперимент был поведен?
2. Что называют хроматографией? Какие этапы включают все хроматографические методики?
3. Как классифицируют хроматографические методы?
4. Какие основные механизмы хроматографических методов анализа?
5. В чем заключается принцип действия хроматографа?
6. Какие техники эксперимента используют в хроматографии?
7. В чем принцип метода тонкослойной хроматографии?
8. Где применяют хроматографию в фармации и в медико-биологических исследованиях?
Основная литература:
1. Аналитическая химия (аналитика). Общие теоретические основы. Качественный анализ. [Текст]: учеб. для вузов / Ю.Я. Харитонов [и др.]. - М.: Высш. шк., 2008. – 264 – 285 с.
Дополнительная литература:
1. Основы аналитической химии. Практическое руководство. Учеб. пособие для вузов [Текст] / Под ред. Ю.А. Золотова - М.: Высш. шк., 2001. – 155 – 170 с.
Тема 19
Дата: 2019-02-02, просмотров: 558.