Основные формулы.
Количество вещества однородного газа (в молях):
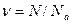 ;
; 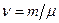
где N - число молекул газа; 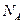 - постоянная Авогадро; m - масса газа;
- постоянная Авогадро; m - масса газа; 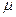 - молярная масса газа.
- молярная масса газа.
Если система представляет смесь нескольких газов, то количество вещества системы
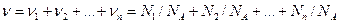 ,
,
или
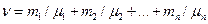 ,
,
где 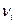 , N
, N 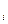 , m
, m 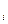 ,
, 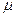
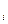 - соответственно количество вещества, число молекул, масса, молярная масса i-й компоненты смеси.
- соответственно количество вещества, число молекул, масса, молярная масса i-й компоненты смеси.
Уравнение Менделеева-Клапейрона (уравнение состояния идеального газа):
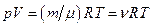 ,
,
где m - масса газа, 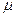 - молярная масса газа; R - универсальная газовая постоянная;
- молярная масса газа; R - универсальная газовая постоянная; 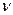 - количество вещества; T - термодинамическая температура.
- количество вещества; T - термодинамическая температура.
Опытные газовые законы, являющиеся частными случаями уравнения Менделеева-Клапейрона для изопроцессов:
- закон Бойля-Мариотта (изотермический процесс Т=const, m=const):
рV=const,
- закон Гей-Люcсака (изобарный процесс p=const, m=const):
V/T=const,
- закон Шарля (изохорный процесс V=const, m=const):
P/T=const,
- объединенный газовый закон (m=const):
PV/T=const
Закон Дальтона, определяющий давление смеси газов:
P= 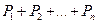
где 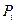 - парциальные давления компонентов смеси; n – число компонентов смеси.
- парциальные давления компонентов смеси; n – число компонентов смеси.
Парциальным давлением называется давление газа, которое производил бы этот газ, если бы только он один находился в сосуде, занятом смесью.
Молярная масса смеси газов:
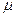 =(
=( 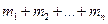 )/(
)/( 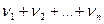 )
)
где 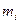 - масса i-го компонента смеси;
- масса i-го компонента смеси; 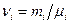 – количество вещества i-го компонента смеси; n - число компонентов смеси.
– количество вещества i-го компонента смеси; n - число компонентов смеси.
Массовая доля 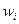 -го компонента смеси газа ( в долях единицы или процентах):
-го компонента смеси газа ( в долях единицы или процентах):
w 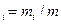
где m – масса смеси.
Концентрация молекул:
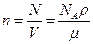
где N - число молекул, содержащихся в данной системе; 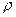 - плотность вещества, V - объём системы.
- плотность вещества, V - объём системы.
Основное уравнение кинетической теории газов:
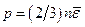
где 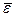 - средняя кинетическая энергия поступательного движения молекулы.
- средняя кинетическая энергия поступательного движения молекулы.
Средняя кинетическая энергия поступательного движения молекулы:
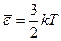
где k - постоянная Больцмана.
Средняя полная кинетическая энергия молекулы:
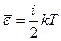
где i – число степеней свободы молекулы.
Зависимость давления газа от концентрации молекул и температуры:
р= nkT
Скорости молекул:
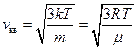 (средняя квадратичная);
(средняя квадратичная);
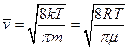 (средняя арифметическая);
(средняя арифметическая);
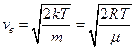 (наиболее вероятная),
(наиболее вероятная),
где m - масса одной молекулы.
Молярные теплоемкости газа при постоянном объеме ( 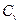 ) и при постоянном давлении (
) и при постоянном давлении ( 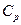 ):
):
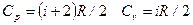
Связь между удельной c и молярной С теплоёмкостями:
с=С/ 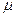
Уравнение Майера:
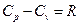
Внутренняя энергия идеального газа:
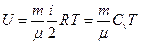
Первое начало термодинамики:
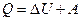
где 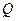 - теплота, сообщенная системе (газу);
- теплота, сообщенная системе (газу); 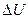 - изменение внутренней энергии системы; A - работа, совершенная системой против внешних сил.
- изменение внутренней энергии системы; A - работа, совершенная системой против внешних сил.
Работа расширения газа:
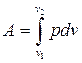 ( в общем случае);
( в общем случае);
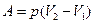 ( при изобарном процессе);
( при изобарном процессе);
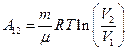 (при изотермическом процессе);
(при изотермическом процессе);

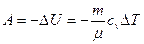 (при адиабатном процессе),
(при адиабатном процессе),
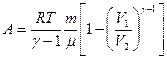
где 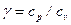 – показатель адиабаты.
– показатель адиабаты.
Уравнения Пуассона, связывающие параметры идеального газа при адиабатном процессе:
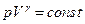
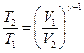
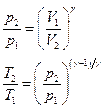
Термический к.п.д. цикла;
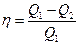
где 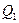 - теплота, полученная рабочим телом от теплоотдатчика,
- теплота, полученная рабочим телом от теплоотдатчика, 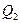 - теплота, переданная рабочим телом теплоприёмнику.
- теплота, переданная рабочим телом теплоприёмнику.
Термический к.п.д. цикла Карно:
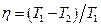
где 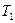 и
и 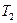 - термические температуры теплоотдатчика и теплоприёмника.
- термические температуры теплоотдатчика и теплоприёмника.
Коэффициент поверхностного натяжения:
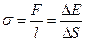
где F - сила поверхностного натяжения; действующая на контур l, ограничивающий поверхность жидкости; 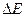 - изменение поверхностной энергии пленки жидкости, связанное с изменением площади
- изменение поверхностной энергии пленки жидкости, связанное с изменением площади 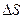 поверхности этой пленки.
поверхности этой пленки.
Формула Лапласа, выражающая давление p, создаваемое сферической поверхностью жидкости:
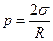
где R - радиус сферической поверхности.
Высота подъема жидкости в капиллярной трубке:
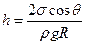
где 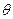 - краевой угол (
- краевой угол ( 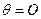 -при полном смачивании стенок трубки жидкостью;
-при полном смачивании стенок трубки жидкостью; 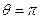 при полном несмачивании); R - радиус канала трубки; ρ - плотность жидкости; g - ускорение свободного падения.
при полном несмачивании); R - радиус канала трубки; ρ - плотность жидкости; g - ускорение свободного падения.
Высота подъёма жидкости между двумя близкими и параллельными друг другу плоскостями:
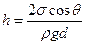
где 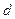 - расстояние между плоскостями.
- расстояние между плоскостями.
Средняя длина свободного пробега молекулы
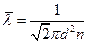
Распределение молекул в потенциальном поле сил (распределение Больцмана)
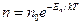
Барометрическая формула
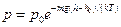
Уравнение диффузии (закон Фика)
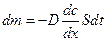
Сила внутреннего трения в жидкости и газе 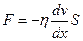
Уравнение теплопроводности 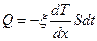
Коэффициент диффузии 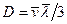
Коэффициент внутреннего трения (динамическая вязкость)
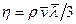
Коэффициент теплопроводности 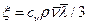
Изменение энтропии 
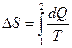
Задачи.
1. Определить количество молей вещества и количество молекул в 0.5 кг водорода.
2. Сколько атомов содержится в ртути: массой 1г; в 0.2 молях.
3. Определить массу одной молекулы углекислого газа.
4. Определить концентрацию молекул кислорода в сосуде емкостью 2 литра. Количество кислорода равно 0.2 моля.
5. В баллоне емкостью 3 литра содержится 10 г углекислого газа. Определить концентрацию молекул.
6. В цилиндр длиной 1.6 м, заполненным воздухом при атмосферном давлении, начали медленно вдвигать поршень площадью 200 см2 . Определить силу, действующую на поршень, если его остановили в 10 см от дна цилиндра.
7. В баллоне находится газ при температуре 400 К. До какой температуры его надо нагреть, чтобы давление возросло в 1.5 раза?
8. Баллон емкостью 20 л заполнен азотом при температуре 400 К. Когда часть газа израсходовали, давление понизилось на 200 кПа. Определить массу израсходованного газа. Процесс считать изотермическим.
9. В баллоне емкостью 15 л находится аргон под давлением 600 кПа и при температуре 300 К. Определить массу израсходованного газа, если давление понизилось до 400 кПа, а температура установилась в 260 К.
10. Два сосуда одинакового объема содержат кислород. В одном сосуде давление 2 МПа и температура 800 К, в другом – 2.5 МПа и 200 К. Сосуды соединили трубкой и охладили газ до 200 К. Определить установившееся в сосудах давление.
11. Определить внутреннюю энергию водорода, а также среднюю кинетическую энергию молекулы при температуре 300 К, если количество водорода равно 0.5 молей.
12. Определить суммарную кинетическую энергию поступательного движения молекул газа в сосуде емкостью 3 л под давлением 540 МПа.
13. Количество гелия 1.5 моля при температуре 120 К. Определить суммарную кинетическую энергию всех молекул газа.
14. Водород в количестве 0.5 моля находится при температуре 300 К. Найти среднюю кинетическую энергию вращательного движения молекулы и суммарную кинетическую энергию всех молекул.
15. В азоте взвешены мелкие пылинки, которые могут двигаться как крупные молекулы. Масса пылинки равна 6×10–10 г. Газ находится при температуре 400 К. Определить средние квадратичные скорости, а также средние кинетические энергии поступательного движения молекулы и пылинки.
16. Определить молярную массу двухатомного газа и его удельные теплоемкости, если известно, что разность удельных теплоемкостей этого газа равна 260 ДЖ/(кг×К).
17. Найти удельные, а также молярные теплоемкости углекислого газа.
18. Определить показатель адиабаты идеального газа, который при температуре 350 К и давлении 0.4 МПа занимает объем 300 л и имеет теплоемкость 857 Дж/К.
19. В сосуде емкостью 6 л находится при нормальных условиях двухатомный газ. Определить теплоемкость этого газа при постоянном объеме.
20. Вычислить удельные теплоемкости газа, зная, что его молярная масса равна 4*10–3 кг/моль и отношение теплоемкостей равно 1.67.
21. Определить среднюю длину свободного пробега молекулы азота в сосуде емкостью 5 литров. Масса газа равна 0.5 г.
22. Водород находится под давлением 20 мкПа и имеет температуру 300 К. Определить среднюю длину свободного пробега молекул газа.
23. Какова средняя арифметическая скорость молекул кислорода, если известно, что при нормальном давлении средняя длинна свободного пробега молекул равна 100 нм?
24. При каком давлении средняя длинна свободного пробега молекул азота равна 1 м, если температура газа равна 100С?
25. Средняя длинна свободного пробега молекулы водорода при некоторых условиях равна 2 мм. Найти плотность водорода при этих условиях.
26. Определить количество теплоты, которое надо сообщить кислороду объемом 50 л при изохорном нагревании, чтобы давление газа повысилось на 0.5 МПа.
27. При изотермическом расширении азота при температуре 280 К объем его увеличился в 2 раза. Определить:1) совершенную газом работу; 2) изменение внутренней энергии газа; 3) количество теплоты, полученной газом. Масса газа равна 0.2 кг.
28. При адиабатическом сжатии давление воздуха было увеличено с 50 кПа до 0.5 МПа. Затем при неизменном объеме температура воздуха была понижена до первоначальной. Определить давление газа в конце процесса.
29. Кислород массой 200 г занимает объем 100 л и находится под давлением в 200 кПа. При Нагревании газ изобарно расширился до объема 300 л, а затем его давление изохорно возросло до 500 кПа. Найти изменение внутренней энергии газа, совершенную им работу и полученную теплоту. Построить график процесса.
30. Азот массой 100 г изобарно нагрет от температуры 200 К до температуры 400 К. Определить работу газа, полученную теплоту и изменение внутренней энергии.
31. Идеальный газ совершает цикл Карно при температурах теплоприемника 290 К и теплоотдатчика 400 К. Во сколько раз увеличится к.п.д. цикла, если температура нагревателя возрастет до 600 К?
32. Идеальный газ совершает цикл Карно. Температура нагревателя в 4 раза больше температуры холодильника. Какую долю количества теплоты, полученного за один цикл от нагревателя, газ отдаст приемнику?
33. Газ, совершающий цикл Карно, отдал холодильнику теплоту в 14 кДж. Определить температуру нагревателя, если при температуре холодильника 280 К работа за цикл равна 6 кДж.
34. Определить работу изотермического сжатия газа, совершающего цикл Карно, к.п.д. которого равно 0.4, если работа изотермического расширения равна 8 Дж.
35. Идеальная тепловая машина работает при температурах нагревателя 500 К и холодильника 250 К. Определить к.п.д. машины, а также работу при изотермическом расширении, если работа при изотермическом сжатии равна 70 Дж.
36. Найти массу воды, вошедшей в стеклянную трубку диаметром 0.8 мм, опущенную в воду на малую глубину. Считать смачивание полным.
37. Какую работу надо совершить при выдувании мыльного пузыря, чтобы увеличить его объем от 8 см3 до 16 см3. Процесс считать изотермическим.
38. Какая энергия выделится при слиянии двух капель ртути диаметром 0.8 мм и 1.2 мм в одну каплю?
39. Определить давление внутри воздушного пузырька диаметром 4 мм, находящегося в воде у самой ее поверхности. Считать атмосферное давление нормальным.
40. Пространство между двумя стеклянными пластинами с поверхностью 100 см2 каждая, расположенными на расстоянии 20 мкм друг от друга, заполнено водой. Определить силу притяжения между пластинами. Мениск в зазоре считать вогнутым с диаметром, равным расстоянию между пластинами.
41. Во сколько раз изменится давление разреженного газа, если при его нагревании и сжатии абсолютная температура газа и концентрация молекул увеличатся в 2 раза?
42. В результате охлаждения одноатомного идеального газа его давление уменьшилось в 4 раза, а концентрация молекул газа не изменилась. Чему равно отношение конечной средней кинетической энергии теплового движения молекул газа к начальной?
43. При неизменном давлении одноатомного идеального газа среднеквадратичная скорость движения его атомов увеличилась в 2 раза. Чему равно отношение конечной плотности газа к начальной?
44. В закрытом сосуде объёмом 20 литров находится 5 моль кислорода. Температура газа равна 127 °С. Чему равно давление газа? Ответ выразите в кПа.
45. В закрытом сосуде объёмом 10 литров находится 5 моль азота. Температура газа равна 26 °С. Чему равно давление газа? Ответ выразите в килопаскалях и округлите до целого числа.
46. Идеальный одноатомный газ в количестве 0,05 моль подвергся адиабатическому сжатию. При этом его температура повысилась с +23 °C до +63 °C. Какая работа была совершена над газом? Ответ выразите в джоулях и округлите до целого числа.
47. Тепловая машина с КПД 40% за цикл работы отдаёт холодильнику количество теплоты, равное 60 Дж. Какое количество теплоты машина получает за цикл от нагревателя? (Ответ дайте в джоулях.)
48. Идеальный газ получил количество теплоты 300 Дж и при этом внутренняя энергия газа увеличилась на 100 Дж. Какова работа, совершенная газом? (Ответ дать в джоулях.)
49. В процессе эксперимента внутренняя энергия газа уменьшилась на 40 кДж, и он совершил работу 35 кДж. Какое количество теплоты (в кДж) газ отдал окружающей среде?
50. Тепловая машина с КПД 40% за цикл работы получает от нагревателя количество теплоты, равное 300 Дж. Какую работу машина совершает за цикл? Ответ приведите в джоулях.
51. Температура холодильника тепловой машины 400 К, температура нагревателя на 200 К больше, чем у холодильника. Каков максимально возможный КПД машины? (Ответ дайте в процентах, округлив до целых.)
52. В таблице приведена зависимость КПД идеальной тепловой машины от температуры ее нагревателя при неизменной температуре холодильника. Чему равна температура холодильника этой тепловой машины? (Ответ дайте в кельвинах.)
52. Некоторое число молей одноатомного идеального газа изохорически нагревается из состояния p1 = 105 Па и t1 = 27 °С до давления p2 = 2p1. Чему равна совершённая газом работа?
53. Алюминиевому и железному цилиндрам сообщили одинаковое количество теплоты, что привело к увеличению температуры цилиндров, причём увеличение температуры алюминиевого цилиндра оказалось в 2 раза больше, чем железного. Определите отношение масс этих цилиндров. Удельная теплоёмкость железа равна 460 Дж/(кг·К), алюминия — 900 Дж/(кг·К).
55. Относительная влажность воздуха в цилиндре под поршнем равна 70 %. Воздух изотермически сжали, уменьшив его объём в два раза. Какова стала относительная влажность воздуха? (Ответ дайте в процентах.)
56. Алюминиевому и железному цилиндрам одинаковой массы сообщили одинаковое количество теплоты. Определите примерное отношение изменения температур этих цилиндров . Удельная теплоёмкость железа равна 460 Дж/(кг·К), алюминия — 900 Дж/(кг·К).
57. Температура медного образца массой 100 г повысилась с 20 °С до 60 °С. Какое количество теплоты получил образец? Удельную теплоёмкость меди считать равной 1620Дж/кг*К
58. Какое количество теплоты необходимо для плавления 2,5 т стали, взятой при температуре плавления? Теплопотерями пренебречь. Ответ выразите в МДж.
59. В сосуде объёмом 1,5 л при температуре +50 °C находится смесь воздуха с водяными парами. Давление в сосуде равно 99,4 кПа, относительная влажность воздуха 50 %. Давление насыщенного водяного пара при данной температуре равно 12,5 кПа. Какое количество воздуха находится в сосуде?
60. Относительная влажность воздуха в закрытом сосуде 25 %. Какой будет относительная влажность, если объём сосуда при неизменной температуре уменьшить в 3 раза? (Ответ дать в %)
Дата: 2018-12-28, просмотров: 527.