Влияние температуры. Различные группы микроорганизмов развиваются при определенных диапазонах температур. Бактерии, растущие при низкой температуре, называют психрофилами, при средней (около 37 °С) — мезофилами, при высокой — термофилами.
К психрофильным микроорганизмам относится большая группа сапрофитов — обитателей почвы, морей, пресных водоемов и сточных вод (железобактерии, псевдомонады, светящиеся бактерии, бациллы). Некоторые из них могут вызывать порчу продуктов питания на холоде. Способностью расти при низких температурах обладают и некоторые патогенные бактерии (возбудитель псевдотуберкулеза размножается при температуре 4 °С). В зависимости от температуры культивирования свойства бактерий меняются. Интервал температур, при котором возможен рост психрофильных бактерий, колеблется от -10 до 40 °С, а температурный оптимум — от 15 до 40 °С, приближаясь к температурному оптимуму мезофильных бактерий.
Мезофилы включают основную группу патогенных и условно-патогенных бактерий. Они растут в диапазоне температур 10— 47 °С; оптимум роста для большинства из них 37 °С.
При более высоких температурах (от 40 до 90 °С) развиваются термофильные бактерии. На дне океана в горячих сульфидных водах живут бактерии, развивающиеся при температуре 250—300 °С и давлении 262 атм.
Термофилы обитают в горячих источниках, участвуют в процессах самонагревания навоза, зерна, сена. Наличие большого количества термофилов в почве свидетельствует о ее загрязненности навозом и компостом. Поскольку навоз наиболее богат термофилами, их рассматривают как показатель загрязненности почвы.
Хорошо выдерживают микроорганизмы действие низких температур. Поэтому их можно долго хранить в замороженном состоянии, в том числе при температуре жидкого газа (—173 °С).
Высушивание. Обезвоживание вызывает нарушение функций большинства микроорганизмов. Наиболее чувствительны к высушиванию патогенные микроорганизмы (возбудители гонореи, менингита, холеры, брюшного тифа, дизентерии и др.). Более устойчивыми являются микроорганизмы, защищенные слизью мокроты. Высушивание под вакуумом из замороженного состояния — лиофилизацию — используют для продления жизнеспособности, консервирования микроорганизмов. Лиофилизированные культуры микроорганизмов и иммунобиологические препараты длительно (в течение нескольких лет) сохраняются, не изменяя своих первоначальных свойств. Действие излучения. Неионизирующее излучение — ультрафиолетовые и инфракрасные лучи солнечного света, а также ионизирующее излучение — гамма-излучение радиоактивных веществ и электроны высоких энергий губительно действуют на микроорганизмы через короткий промежуток времени. УФ-лучи применяют для обеззараживания воздуха и различных предметов в больницах, родильных домах, микробиологических лабораториях. С этой целью используют бактерицидные лампы УФ-излучения с длиной волны 200—450 нм.
Ионизирующее излучение применяют для стерилизации одноразовой пластиковой микробиологической посуды, питательных сред, перевязочных материалов, лекарственных препаратов и др. Однако имеются бактерии, устойчивые к действию ионизирующих излучений, например Micrococcusradiodurans была выделена из ядерного реактора.
Методы, основанные на термической обработке стерилизуемых объектов
Губительное действие высокой температуры обусловливается повреждением коллоидного состояния плазмы, денатурацией белка с последующей коагуляцией его, а также нарушением ферментных систем микроорганизмов.
Различают влажные и сухие способы тепловой стерилизации.
Влажные способы используются, главным образом, для стерилизации питательных сред. К таким способам относятся стерилизация паром под давлением, стерилизация текучим паром (дробная стерилизация) и тиндализация.
Стерилизация паром под давлением – самый эффективный в бактериологической практике способ стерилизации питательных сред и посуды, так как с его помощью быстро достигается полное и надежное обеспложивание. Этот способ стерилизации основан на том, что образующийся при кипячении воды пар не выходит наружу, а, скапливаясь в замкнутом пространстве, повышает давление. При создании избыточного давления возрастает температура кипения воды и температура пара. Стерилизацию паром под давлением осуществляют в паровых стерилизаторах, принцип работы и устройство которого описаны в разделе 1.1.3.
Стерилизация текучим паром используется для сред, которые нельзя нагревать выше температуры 100 0С. Стерилизация проводится при 100 0С (температура парообразования) по 30…60 минут в течение 3 дней с промежутками в 18-20 часов, во время которых материал выдерживается в термостате или при комнатной температуре. Поэтому этот способ называют еще дробной стерилизацией. В основу способа дробной стерилизации положен следующий принцип: при нагревании до 100 0С в течение 30…60 минут погибают все вегетативные клетки, а споры остаются жизнеспособными. В промежутке между стерилизацией споры прорастают в вегетативные клетки. Через сутки проводят повторную стерилизацию. Обычно после третьей стерилизации достигается полное обеспложивание объекта. Стерилизацию текучим паром осуществляют в аппаратах Коха или текучепаровых аппаратах (кипятильниках Коха).
Тиндализация – это дробная стерилизация при низкой температуре – 56…58 0С. Применяют этот способ при стерилизации сред, которые нельзя нагревать до 100 0С. Такие среды подвергают нагреванию в течение 5…6 дней подряд по 1 часу ежедневно (в 1-й день – в течение 2 часов). В промежутках между прогреванием стерилизуемая жидкость хранится в термостате. При этом оставшиеся в живых споры прорастают в вегетативные клетки, которые погибают при последующем нагревании. Тиндализацию проводят в специальных приборах с терморегулятором или на водяных банях.
Сухие способы. При работе в микробиологической лаборатории из сухих способов термической стерилизации используются следующие:
Прокаливание на огне (фламбирование) очень быстрый и надежный способ стерилизации бактериологических петель, препаровальных игл перед посевами. Этим способом можно стерилизовать также мелкие металлические предметы (пинцеты, скальпели) и предметные стекла. Осуществляют прокаливание над пламенем горелки.
Стерилизация сухим жаром (сухим нагретым воздухом) используется для стерилизации микробиологической посуды (пипеток, чашек Петри), песка. Осуществляют стерилизацию сухим жаром при температуре 1650-180 0С в течение 1…1,5 часов в печах Пастера или в сушильных шкафах.
Методы холодной стерилизации
Механическая стерилизация (фильтрование). Этот способ применяется для стерилизации сред в тех случаях, когда их нельзя подвергать нагреванию. При механической стерилизации стерилизуемые жидкости фильтруют через специальные фильтровальные приборы, которые имеют настолько мелкие поры, что на своей поверхности задерживают взвешенные в жидкости частицы, в том числе и микробы. Для фильтрации в микробиологической практике применяют различные фильтровальные приборы (фильтры Зейтца, свечи Шамберлана, Мандлера, Беркефельда и др.).
Действие химических веществ . Химические вещества могут оказывать различное действие на микроорганизмы: служить источниками питания; не оказывать какого-либо влияния; стимулировать или подавлять рост. Химические вещества, уничтожающие микроорганизмы в окружающей среде, называются дезинфицирующими. Антимикробные химические вещества могут обладать бактерицидным, вирулицидным, фунгицидным действием и т.д.
Химические вещества, используемые для дезинфекции, относятся к различным группам, среди которых наиболее широко представлены вещества, относящиеся к хлор-, йод- и бромсодержащим соединениям и окислителям.
Антимикробным действием обладают также кислоты и их соли (оксолиновая, салициловая, борная); щелочи (аммиак и его соли).
Вопросы для контроля знаний:
- Что такое стерилизация?
- Что такое дезинфекция?
- Что такое асептика ?
- Что такое антисептика?
- Стерилизация посуды
- Стерилизация питательных сред; тиндализация, стрилизация текучим паром
- Обеспложивание (убивка м.о.)
- Механическая стерилизация
- Виды дезинфекции
Лекция 8
Антибиотики.
Антибио́тики (от др.-греч. ἀντί — против + βίος — жизнь) — вещества природного или полусинтетического происхождения, подавляющие рост живых клеток, чаще всего прокариотических или простейших.
По ГОСТ 21507-81 (СТ СЭВ 1740-79) Антибиотик — вещество микробного, животного или растительного происхождения, способное подавлять рост микроорганизмов или вызывать их гибель.
Исторический очерк.
В народной медицине для обработки ран и лечения туберкулеза издавна применяли экстракты лишайников. Позднее в состав мазей для обработки поверхностных ран стали включать экстракты бактерий Pseudomonas aeruginosa, хотя почему они помогают, никто не знал, и феномен антибиоза был неизвестен.
Однако некоторые из первых ученых-микробиологов сумели обнаружить и описать антибиоз (угнетение одними организмами роста других). Дело в том, что антагонистические отношения между разными микроорганизмами проявляются при их росте в смешанной культуре. До разработки методов чистого культивирования разные бактерии и плесени выращивались вместе, т.е. в оптимальных для проявления антибиоза условиях. Луи Пастер еще в 1877 описал антибиоз между бактериями почвы и патогенными бактериями – возбудителями сибирской язвы. Он даже предположил, что антибиоз может стать основой методов лечения.
Первые антибиотики были выделены еще до того, как стала известной их способность угнетать рост микроорганизмов. Так, в 1860 был получен в кристаллической форме синий пигмент пиоцианин, вырабатываемый небольшими подвижными палочковидными бактериями рода Pseudomonas, но его антибиотические свойства были обнаружены лишь через много лет. В 1896 Б. Гозио из жидкости, содержащей культуру грибка из рода Penicillium (Penicillium brevicompactum), выделил кристаллическое соединение — микофеноловую кислоту, подавляющую рост бактерий сибирской язвы.
В 1899 году Р. Эммерих и О. Лоу сообщили об антибиотическом соединении, образуемом бактериями Pseudomonas pyocyanea, и назвали его пиоцианазой; препарат использовался как местный антисептик.
Постепенно выяснилось, что антибиоз имеет химическую природу и обусловлен выработкой специфических химических соединений. В 1929 Александр Флеминг, наблюдая антагонизм Penicillium notatum и стафилококка в смешанной культуре, открыл пенициллин и предположил возможность его применения в лечебных целях. Антагонистические отношения между болезнетворными для растений микробами и непатогенными микроорганизмами почвы, выявленные в смешанных культурах, заинтересовали фитопатологов, и они попытались использовать этот феномен для борьбы с болезнями растений. Было известно, что в почве присутствует определенный грибок, который уменьшает выпревание ростков; в 1936 из культуры этого грибка был выделен антибиотик, получивший название глиотоксин. Это открытие подтвердило значение антибиотиков как средства профилактики заболеваний.
Годом ранее в 1935 –м Герхард Домагк опубликовал статью о терапевтическом действии пронтозила в Deutsche Medizinische Wochenschrift, данная статья была первым руководством по лечению антибиотиком, а в 1939-м году он получил Нобелевскую премию по физиологии и медицине за «за открытие антибактериального эффекта пронтозила».
В 1937-м М. Вельш описал первый антибиотик стрептомицетного происхождения — актиномицетин.
Среди первых исследователей, занявшихся целенаправленным поиском антибиотиков, был Р.Дюбо. Проведенные им и его сотрудниками эксперименты привели к открытию антибиотиков, вырабатываемых некоторыми почвенными бактериями, их выделению в чистом виде и использованию в клинической практике. В 1939 Дюбо получил тиротрицин – комплекс антибиотиков, состоящий из грамицидина и тироцидина; это явилось стимулом для других ученых, которые обнаружили еще более важные для клиники антибиотики. В этом же году Н. А. Красильников и А. И. Кореняко получили мицетин, а на химико-фармацевтическом заводе «АКРИХИН» начали производство стрептоцида.
В 1940 году — Э. Чейн выделил пенициллин в кристаллическом виде.
В 1942 год — Х.Флори со своими коллегами по Оксфордскому университету повторно исследовал пенициллин и доказал возможность его клинического использования в качестве нетоксичного средства лечения многих острых инфекций. Зельман Ваксман впервые ввел термин «антибиотик». З.Ваксман со своими студентами в Университете Ратджерса, США, занимался актиномицетами (такими, как Streptomyces) и в 1944 открыл стрептомицин, эффективное средство лечения туберкулеза и других заболеваний. После 1940 было получено множество клинически важных антибиотиков, в их числе бацитрацин, хлорамфеникол (левомицетин), хлортетрациклин, окситетрациклин, амфотерицин В, циклосерин, эритромицин, гризеофульвин, канамицин, неомицин, нистатин, полимиксин, ванкомицин, виомицин, цефалоспорины, ампициллин, карбенициллин, аминогликозиды, стрептомицин, гентамицин. В настоящее время открывают все новые и новые антибиотики. В середине 1980-х годов в США антибиотики прописывались чаще, чем любые другие лекарства, за исключением седативных средств и транквилизаторов.
Классификация антибиотиков.
Современная классификация антибиотиков разработана в Государственном центре по антибиотикам (С.М.Навашин, 1994), в соответствии с которой, они характеризуются по происхождению, способу получения, механизму действия, химической структуре, противомикробному спектру, типу действия на клетку.
Продуцентами большинства антибиотиков являются ( классификация по происхождению):
- актиномицеты (стрептомицин, тетрациклин),
- плесневые грибы (весь пенициллиновый ряд);
но их можно получить и из:
- бактерий (полимиксины),
- высших растений (фитонциды)
- тканей высших животных, человека и рыб (эритрин, эктерицид, лизоцим, интерферон).
По способу получения их делят на:
- природные (штаммы-продуценты антибиотиков выращивают на искусственных питательных средах, а за тем антибиотик извлекают из питательной среды химическими методами);
- синтетические (химические аналоги природных антибиотиков и синтезированные антибиотики, не имеющие природного аналога);
- полусинтетические (на начальном этапе получают естественным путем, затем синтез ведут искусственно, то есть изменяют химическую структуру природного антибиотика).
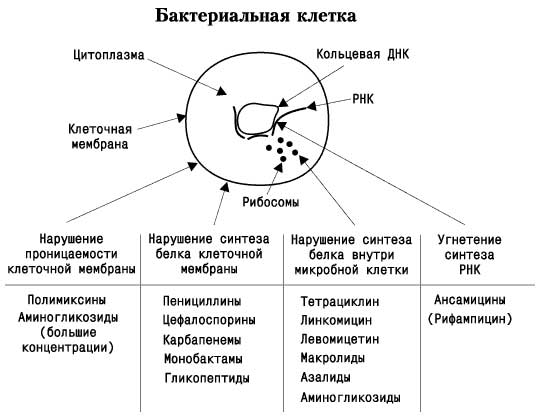
С учетом механизма действия антибиотики разделяют на три основные группы:
- ингибиторы синтеза клеточной стенки микроорганизма (пенициллины, цефалоспорины, ванкомицин, тейкопланин и др.);
- антибиотики, нарушающие молекулярную организацию, функции клеточных мембран (полимиксин, нистатин, леворин, амфотерицин и др.);
- антибиотики, подавляющие синтез белка и нуклеиновых кислот, в частности, ингибиторы синтеза белка на уровне рибосом (хлорамфеникол, тетрациклины, макролиды, линкомицин, аминогликозиды) и ингибиторы РНК-полимеразы (рифампицин) и др.
В зависимости от типа воздействия на микробную клетку антибиотики классифицируют на две группы:
- бактерицидные – вызывают гибель микробной клетки (пенициллины, цефалоспорины, аминогликозиды, рифампицин, полимиксины и др.);
- бактериостатические – задерживают рост микробной клетки (макролиды, тетрациклины, линкомицин, хлорамфеникол и др.).
По химическому строению антибиотики делятся на:
1. Бета-лактамные антибиотики - основу из молекулы составляет бета-лактамное кольцо. К ним относятся:
- пенициллины - это группа природных и полусинтетических антибиотиков, молекула которых содержит 6-аминопенициллановую кислоту, состоящую из двух колец - тиазолидонового и бета-лактамного. Среди них выделяют:
- биосинтетические (пенициллин G - бензилпенициллин),
- аминопенициллины (амоксициллин, ампициллин, бекампициллин),
- полусинтетические "антистафилококковые" пенициллины (оксациллин, метициллин, клоксациллин, диклоксациллин, флуклоксациллин), основное преимущество которых - устойчивость к микробным бета-лактамазам, в первую очередь, стафилококковым;
2. цефалоспорины - это природные и полусинтетические антибиотики, полученные на основе 7-аминоцефалоспориновой кислоты и содержащие цефемовое (также бета-лактамное) кольцо, т.е. по структуре они близки к пенициллинам. Они делятся на цефалоспорины:
- 1-го поколения: цепорин, цефалотин, цефалексин;
- 2-го поколения:- цефазолин (кефзол), цефамезин, цефамандол (мандол);
- 3-го поколения:- цефуроксим (кетоцеф), цефотаксим (клафоран), цефуроксим аксетил (зиннат), цефтриаксон (лонгацеф), цефтазидим (фортум);
- 4-го поколения:- цефепим, цефпиром (цефром, кейтен) и другие.
- монобактамы - азтреонам (азактам, небактам);
- карбопенемы - меропенем (меронем) и имипинем. Причем имипинем применяют только в комбинации со специфическим ингибитором почечной дегидропептидазы циластатином - имипинем/циластатин (тиенам);
3 Аминогликозиды - они содержат аминосахара, соединенные гликозидной связью с остальной частью (агликоновым фрагментом) молекулы. К ним относятся: стрептомицин, гентамицин (гарамицин), канамицин, неомицин, мономицин, сизомицин, тобрамицин (тобра) и полусинтетические аминогликозиды - спектиномицин, амикацин (амикин), нетилмицин (нетиллин);
4. Тетрациклины - основу молекулы составляет полифункциональное гидронафтаценовое соединение с родовым название тетрациклин. Среди них имеются природные тетрациклины - тетрациклин, окситетрациклин (клинимицин) и полусинтетические тетрациклины - метациклин, хлортетрин, доксициклин (вибрамицин), миноциклин, ролитетрациклин;
5. Макролиды - препараты этой группы содержат в своей молекуле макроциклическое лактоновое кольцо, связанное с одним или несколькими углеводными остатками. К ним относятся: эритромицин, олеандомицин, рокситромицин (рулид) азитромицин (сумамед), кларитромицин (клацид), спирамицин, диритромицин;
6. Линкозамиды - к ним относятся: линкомицин и клиндамицин. Фармакологические и биологические свойства этих антибиотиков очень близки к макролидам, и, хотя в химическом отношении это совершенно иные препараты, некоторые медицинские источники и фармацевтические фирмы - производители химиопрепаратов, например, делацина С, относят линкозамины к группе макролидов;
7. Гликопептиды - препараты этой группы в своей молекуле содержат замещенные пептидные соединения. К ним относятся: ванкомицин (ванкацин, диатрацин), тейкопланин (таргоцид), даптомицин;
8. Полипептиды - препараты этой группы в своей молекуле содержат остатки полипептидных соединений, к ним относятся: грамицидин, полимиксины М и В, бацитрацин, колистин;
9. Полиены - препараты этой группы в своей молекуле содержат несколько сопряженных двойных связей. К ним относятся: амфотерицин В, нистатин, леворин, натамицин;
10. Антрациклинновые антибиотики - к ним относятся противоопухолевые антибиотики - доксорубицин, карминомицин, рубомицин, акларубицин.
Есть еще несколько достаточно широко используемых в настоящее время в практике антибиотиков, не относящихся ни к одной из перечисленных групп - фосфомицин, фузидиевая кислота (фузидин) рифампицин.
По спектру противомикробного действия антибиотики разделяют на следующиие группы:
- антибиотики широкого спектра действия, активные в отношении грамположительных и грамотрицательных палочек: хлорамфеникол, тетрациклины, аминогликозиды, полусинтетические пенициллины широкого спектра действия (ампициллин, азлоциллин и др.) и цефалоспорины 2-го поколения.
- антибиотики узкого спектра действия - препараты, действующие преимущественно на грамположительные и грамотрицательные кокки (стафилококки, стрептококки, менингококки, гонококки), некоторые грамположительные микробы (коринебактерии, клостридии). К этим препаратам относятся бензилпенициллин, бициллины, феноксиметилпенициллин, пенициллиназоустойчивые пенициллины (оксациллин, метициллин), цефалоспорины 1-го поколения, макролиды, ванкомицин, линкомицин. Антибиотики с преимущественной активностью в отношении грамотрицательных палочек (полимиксины, цефалоспорины 3-го поколения). Противотуберкулезные антибиотики (стрептомицин, рифампицин, флоримицин). Противогрибковые антибиотики (нистатин, леворин, гризеофульвин, амфотерицин В, кетоконазол, анкотил, дифлюкан и др.).
По направленности действия :
- антибактериальные;
- противогрибковые;
- противоопухолевые;
- противовирусные.
Вышеперечисленные свойства в основном и диктуют выбор антибиотика для лечения инфекционного больного. При этом обязательно учитываются фармакодинамика и фармакокинетика препарата, индивидуальные особенности больного (возраст, состояние иммунитета, сопутствующие заболевания и др.).
Дата: 2018-12-28, просмотров: 425.