Перенос электрона от электрода (или к электроду) является гетерогенным процессом, то есть константа скорости такого процесса зависит от природы и предварительной обработки поверхности электрода, адсорбции исходных веществ и продуктов реакции на электроде и других факторов.
Когда окисленная и восстановленная форма сильно адсорбированы и электрохимическая реакция относится исключительно адсорбционная природа тока (3.4.1):.
i=nFAks { 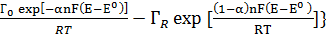 (3.4.1)
(3.4.1)
где ks – константа скорости электрохимической реакции (с-1 ), F0 и FR - поверхностные концентрации окисленной и восстановленной формы (моль/см2 ), А-площадь электрода (см2 )
Рассчитанное значение коэффициент переноса (α)(таблица№3.2.1) использовали для расчета константы скорости электронного переноса по формуле (3.4.1) [28]:
logks = αlog(1-α)+(1-α)logα-log 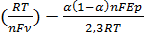 (3.4.2)
(3.4.2)
где : ks-константа скорости электронного переноса(с-1),α- коэффициент переноса, катодного процесса, (1-α)-коэффициент переноса, анодного процесса, ν - скорость развертки потенциала (В/с) , R-универсальная газовая постоянная (Дж·моль/K), Т - температура (K), n- число участвующих электронов, Ep-разность между анодным предельным потенциалом и катодным (В).
Для нахождения гетерогенной константы скорости электрохимической системы используют уравнение (3.4.3) [28]:
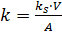 (3.4.3)
(3.4.3)
где: k- гетерогенная константа скорости электрохимической системы (с-1·см), ks- константа скорости электронного переноса(с-1), А-площадь электрода (см2 ), V- площадь графитовой пудры (см3).
1.5.2.Применение циклической вольтамперометрии для определения тяжелых металлов
Метод циклической вольтамперометрии может быть использован не только для обнаружения промежуточных частиц, возникающих в ходе электродных реакций, но и для выявления характера отдельных стадий и установления механизма процесса в целом. Метод позволяет исследовать процессы восстановления и окисления на одном и том же электроде в одном растворе. Прибор рисует циклическую вольтамперограмму, по которой оценивают потенциалы восстановления и окисления данного органического соединения.
Практическое использование различных модификаций вольтамперометрического метода в анализе объектов окружающей среды, пищевых продуктов. Среди удачных примеров аналитического применения можно назвать определение ионов тяжелых металлов (Hg, Pb, Cd, Zn, Cu, Ag), неметаллов (As, Se, I, Cl,Br), витаминов.
Присущие циклической вольтамперометрии ограничения, такие как невозможность получения информации о структуре вещества, устраняются при ее объединении с по структуре более богатым спектроскопическим методом. Например, одновременное применение циклической вольтамперометрии и различных типов спектроскопии, дифракционных методов, позволяет получить детальную структурную информацию о химических изменениях, которые сопровождают процесс электронного переноса.
Дата: 2018-12-21, просмотров: 893.