При анализах органические кислоты можно экстрагировать из свежих, замороженных или высушенных растительных тканей. Однако следует иметь в виду, что при высушивании в условиях повышенной температуры могут происходить изменения в содержании органических кислот (потери летучих кислот или их эфиров, взаимные превращения кислот, взаимодействие их с углеводами и т. д.), поэтому для определения органических кислот сушить материал лучше при комнатной температуре в вакууме или применять высушивание лиофилизацией.
Для экстракции кислот можно использовать воду или органические растворители, из которых чаще всего – эфир. Однако эфир растворяет свободные кислоты, но не соли органических кислот, поэтому для экстракции солей экстрагируемый материал надо предварительно подкислять минеральной кислотой.
При экстракции водой из растительного материала, кроме кислот, извлекается много сопутствующих веществ – сахаров, пектиновых веществ, аминокислот, белков, которые перед количественным определением необходимо тщательно удалять из раствора. Удаляют эти вещества или экстракцией и осаждением, или при помощи катионо- и анионообменных смол. Эфир не извлекает углеводов, аминокислот и белков, но растворяет жиры и липоиды.
Цель работы – определить кислотность плодов различных культур (яблоки, апельсины, помидоры).
Реактивы и материалы: дистиллированная вода, NaOH или KOH, фенолфталеин, фарфоровая ступка и пестик, кварцевый песок, колба Бунзена, конические колбы объемом 250 мл, мерные цилиндры, водяная баня.
Ход работы
Взвесить 10 –20 г свежих размельченных плодов. Перенести навеску в фарфоровую ступку и тщательно растереть с 1-2 г кварцевого песка до однородной массы. Растертую массу количественно перенести в коническую колбу на 250 мл, залить 100 мл горячей дистиллированной воды (80оС) и нагревать на водяной бане в течение 1 ч при 80оС. Затем содержимое колбы охладить и отфильтровать через воронку Шотта. Довести объем экстракта до 100 мл. Пипеткой взять 20 мл вытяжки и перенести в чистую коническую колбу, туда же добавить 2-3 капли фенолфталеина до розового окрашивания. Оттитровать вытяжку 0,1 н. раствором щелочи. Кислотность исследуемого объекта (Х, %) вычислить по формуле:
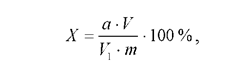
где а - количество 0,1 н. щелочи, пошедшей на титрование, в мл; V - общий объем вытяжки; V 1 - объем вытяжки, взятой для титрования; т- масса навески в граммах.
Если результат хотят выразить для какой-либо из главных органических кислот, то Х умножают на определенный расчетный коэффициент. Согласно А. И. Ермакову и др., 1 мл 0,1 н раствора щелочи пошедшей на титрование, соответствует 7,5 мг винной, 6,7 мг яблочной, 6,4 мг лимонной, 4,5 мг щавелевой кислот.
Результаты оформить в виде таблицы и сделать выводы.
| Объект | Количество щелочи, пошедшей на титрование, мл | Кислотность, % |
Определение общей кислотности
В плодах и овощах, а также в листьях многих растений часто накапливается значительное количество свободных кислот. Определение общего содержания кислот имеет большое значение при использовании плодов и овощей в пищу, при их консервировании, а также при изучении накопления и распада кислот в растениях. Величину общей кислотности можно определить алкалиметрическим, а также ацидиметрическим титрованием с использованием соответствующих индикаторов или потен-циометрически.
Принцип метода. Кислоты извлекаются из измельченного растительного материала в результате нагревания с содой при температуре 80-90° в течение 30 минут. Извлеченные кислоты оттитровывают раствором щелочи. Общее количество кислот обычно пересчитывают на яблочную кислоту.
Ход работы
1. Свежие плоды, овощи или листья растений тщательно измельчают на терке, в мясорубке или в ступке. Растительную массу перемешивают.
2. Берут навеску 20 г и переносят ее без потерь в широкогорлую колбу объемом 200 мл.
3. В колбу приливают около 150 мл дистиллированной воды и выдерживают в течение 30 минут в водяной бане при температуре 80-90°.
4. Затем колбу охлаждают водопроводной водой, доводят до метки и фильтруют в сухой стакан или колбу.
Полученный фильтрат служит для определения общей кислотности.
5. 50 мл фильтрата, содержащего кислоты, переносят в коническую колбу емкостью 200-250 мл и добавляют в нее 50 мл 1 н. NaOH.
6. Колбу нагревают на водяной бане при 80-90° в течение 10 минут.
При нагревании раствора с избытком щелочи ангидриды кислот расщепляются.
7. Затем в колбу добавляют 50 мл 1,2 н. НС1 и снова нагревают на бане в течение 10 минут.
При нагревании кислотного раствора из него удаляется углекислота. Затем раствор в колбе охлаждают.
Наряду с определением свободной кислотности в анализируемом образце проводят «холостое» определение. Для этого вместо раствора берут 50 мл дистиллированной воды, добавляют 50 мл 1,0 н. NaOH, нагревают на бане, затем вносят 1,2 н. НС1 и снова нагревают.
8. После охлаждения растворов приступают к титрованию. Для этого в обе колбы добавляют по нескольку капель спиртового раствора фенолфталеина и титруют 0,1 н. NaOH до ярко-розового оттенка раствора.
Если раствор сильно окрашен и переход окраски раствора при добавлении щелочи определить трудно, то при титровании можно использовать лакмусовую бумажку. Капли жидкости из колбы при титровании переносят на кусочек фильтровальной бумаги и наблюдают изменение окраски.
Вычисление результатов. При расчете необходимо учитывать количество миллилитров добавленных щелочи и кислоты. Разницу в титре 1 н. NaOH и 1,2 н. НС1 следует принимать во внимание при проведении «холос- того» определения (х) в таком же объеме жидкости.
Количество миллиэквивалентов кислот, содержащихся в 100 мл раствора (в 10 г образца), равняется:
100 X у – х
50 10
где у - число миллилитров 0,1 н. NaOH, затраченное на титрование исследуемого образца;
х - число миллилитров 0,1 н. NaOH, затраченное на титрование контроля.
Для вычисления процентного содержания кислот необходимо полученный результат умножить на 10, а для перечисления на яблочную кислоту умножить на коэффициент 0,0067 (1 м-экв. яблочной кислоты=134 : 2 = 67 мг).
Оборудование и реактивы: 1) водяные бани; 2) колбы мерные емкостью 200 мл; 3) колбы конические емкостью 200-300 мл; 4) воронки; 5) пипетки; 6) фильтры; 7) 1,0 н. и 0,1 н. NaOH; 8) 1,2 н. НС1; 9) фенолфталеин; 10) лакмусовая бумага.
Контрольные вопросы
1. Содержание в растениях органических кислот алифатического ряда.
2. Функции органических кислот в растении.
3. Характерные особенности основных органических кислот растений.
4. Обмен органических кислот у высших растений.
Дата: 2018-12-21, просмотров: 830.