Что такое металл? М. В. Ломоносов в своем труде «Первые основания металлургии или рудных дел» дал металлам такое определение: «Металлы суть ковкие блестящие тела». Позже, объясняя понятие «металлы», стали называть и другие металлические свойства. В энциклопедическом словаре Мейера о металлах говорится следующее: «Элементы, которые являются хорошими проводниками тепла и электричества, обладают характерным сильным блеском, непрозрачны (в не слишком тонком слое) и образуют с кислородом соединения преимущественно основного типа».
Металлы в твердом состоянии обладают рядом характерных свойств:
· высокой тепло- и электропроводностью;
· положительным температурным коэффициентом электросопротив- ления (с повышением температуры электросопротивление чистых метал- лов возрастает; большое число металлов обладает сверхпроводимостью – у этих металлов при температуре, близкой к абсолютному нулю, электро- сопротивление падает скачкообразно практически до нуля);
· термоэлектронной эмиссией, т. е. способностью испускать электроны при нагреве;
· хорошей отражательной способностью (металлы непрозрачны и об- ладают металлическим блеском);
· повышенной способностью к пластической деформации.
Эти свойства металлов обусловлены их электронным строением. Ме- таллическое состояние возникает в комплексе атомов, если при их сбли- жении внешние электроны теряют связь с отдельными атомами, становят- ся общими, т. е. коллективизируются и свободно перемещаются по опре- деленным энергетическим уровням между положительно заряженными и периодически расположенными в пространстве ионами. Устойчивость ме- талла, представляющего собой ионно-электронную систему, определяется электрическим взаимодействием между положительно заряженными ио- нами и коллективизированными электронами. Такое взаимодействие меж- ду ионным скелетом и электронным газом получило название металличе- ской связи.
Сила связи в металлах определяется соотношением между силами от- талкивания и силами притяжения между ионами и электронами. Атомы (ионы) располагаются на таком расстояния один от другого, чтобы энергия взаимодействия была минимальной. Этому положению соответствует рав- новесное расстояние d0 (рис. 1.1).
Сближение атомов (ионов) на расстояние меньшее d0 или удаление на расстояние больше d0, осуществимо лишь при совершении определенной работы против сил отталкивания или притяжения.
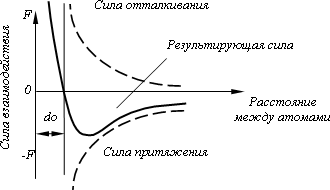
Рис. 1.1. Силы взаимодействия двух атомов
Каждый металл отличается от других строением и свойством, но по не- которым признакам их можно объединить в группы (рис. 1.2).
 Щелочноземельные металлы
Щелочноземельные металлы














































 Легкие
Легкие
Тугоплавкие металлы Железные


| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
металлы металлы
Рис.1.2. Классификация металлов периодической системы Д.И. Менделеева
Металлы делятся на две большие группы – черные и цветные. Черные металлы делятся на:
· железные – железо, кобальт, никель, марганец. Кобальт, никель и марганец часто применяют как добавки к сплавам железа, а также в каче- стве основы для соответствующих сплавов, похожих по своим свойствам на высоколегированные стали;
· тугоплавкие – титан, вольфрам, хром, молибден и др. – температура плавления выше, чем железа (выше 1539 °С). Применяют как добавки к легированным сталям, а также в качестве основы для соответствующих сплавов;
· урановые – актиний и актиноиды, имеющие преимущественное при- менение в сплавах для атомной энергетики;
· редкоземельные – лантан, церий, неодим и др., объединяемые под названием лантаноиды. Эти металлы обладают близкими химическими свойствами, но различными физическими (температура плавления и т. д.). Их применяют как присадки к сплавам др. элементов;
· щелочноземельные – литий, натрий, кальций и др., которые в сво- бодном металлическом состоянии не применяются.
Цветные металлы подразделяются на:
· легкие – бериллий, магний, алюминий, обладающие малой плотно- стью;
· благородные – серебро, золото, металлы платиновой группы. Обла- дают высокой устойчивостью против коррозии;
· легкоплавкие металлы – цинк, олово, свинец и др.
Дата: 2018-12-21, просмотров: 786.