Основная полимерная цепь алкидов состоит из регулярно повторяющихся фрагментов полиатомных спиртов и полиосновных кислот. Возможность введения в состав алкидов монофункциональных кислот-модификаторов достигается использованием полиатомных спиртов с функциональностью больше двух (глицерин и пентаэритрит), за счет которых удается сохранить среднюю функциональность системы, по крайней мере, близкую к двум, несмотря на значительную долю монофункциональных модификаторов.
Так, при взаимодействии глицерина с одним молем кислоты-модификатора (или пентаэритрита — с двумя молями) образуются бифункциональные спирты, участвующие в дальнейшем в поликонденсации, например с фталевым ангидридом, с образованием продуктов линейного строения.
Поэтому, при введении монофункциональных модификаторов не исключается возможность получения олигомерных продуктов с достаточной степенью поликонденсации.
При использовании в качестве модификаторов растительных масел, представляющих собой триглицериды монокарбоновых кислот, не имеющих свободных функциональных групп, их предварительно превращают в спиртовые компоненты, содержащие жирнокислотные остатки, путем переэтерификации (алкоголиза) многоатомными спиртами (глицерином или пен-таэритритом).
Различная химическая природа модификаторов (свободные монокарбоновые кислоты, растительные масла или их смеси) определяет выбор метода синтеза алкидного олигомера.
Существуют следующие методы синтеза алкидов: глицеридный, жирнокислотный и комбинированный.
Глицеридный метод используется при получении алкидов, модифицированных маслами. По этому методу процесс проводят в две стадии.
Первая стадия — алкоголиз растительных масел (переэтерификация), в результате которого образуются неполные эфиры полиатомных спиртов, состав которых в первую очередь определяется мольным соотношением масло: многоатомный спирт. Так, например, при мольном соотношении масло: глицерин 1: 1 переэтерификат содержит в основном смесь моно- и диглицеридов:
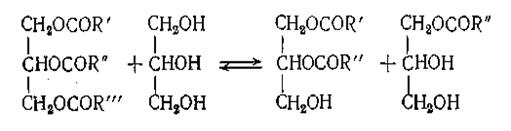
А при соотношении 1:2 — преимущественно моноглицериды:
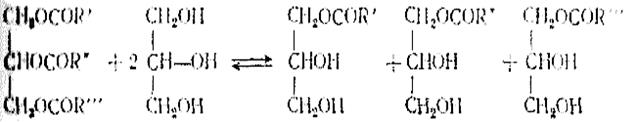
Аналогичным образом протекает и переэтерификация масла пентаэритритом:
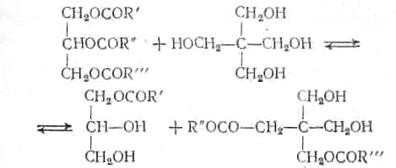
В состав пентафталей в этом случае будут входить фрагменты как четырех-, так и трехатомного спиртов.
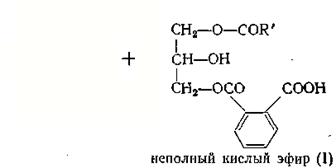
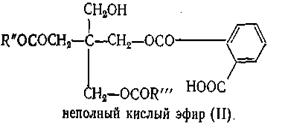
На второй стадии моно- и диглицериды взаимодействуют с фталевым ангидридом с образованием неполных кислых эфиров:
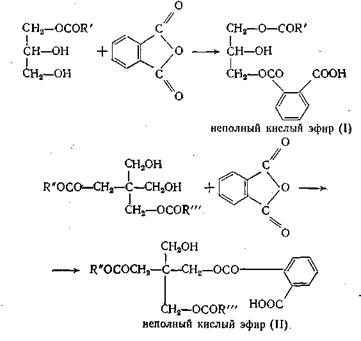
Эти неполные кислые эфиры (I) и (II) сразу же вступают в реакцию поликонденсации:
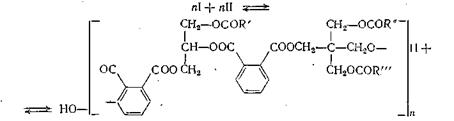
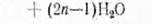 |
Переэтерификацию проводят при 210—240 °С в присутствии катализаторов РЬО, Nа2С03, СаО. Затем температуру понижают до 180 °С, вводят фталевый ангидрид и ведут процесс при постепенном повышении температуры до 240°С.
Иногда, например в полунепрерывном и непрерывном способах получения алкидов, оказывается целесообразным стадии получения неполных кислых эфиров и полиэтерификации разделять во времени и выполнять как отдельные операции. В этом случае на стадии образования неполных кислых эфиров температура реакционной массы не должна превышать 180 °С.
Для облегчения удаления низкомолекулярного побочного продукта (воды) из реакционной массы на завершающих стадиях реакции поликонденсации возможно применение вакуума. Воду можно также удалять в виде азеотропной смеси с толуолом или ксилолом.
Следует отметить, что приведенная схема образования алкида по глицеридному методу является упрощенной. Вследствие равновесного характера реакции переэтерификации переэтерификат имеет сложный состав: помимо моно- и диглицеридов в нем всегда содержится некоторое количество свободных полиатомных спиртов и триглицерида.
Вследствие этого в реакции поликонденсации помимо моно- и диглицеридов всегда принимают участие и другие компоненты, что значительно усложняет структуру образующегося алкидного олигомера. Существенное влияние на структуру олигомера и его молекулярно-массовое распределение оказывают также протекающие на второй стадии в условиях высокотемпературной равновесной полиэтерификации реакции межцепного обмена (эфиролиз, алкоголиз, ацидолиз).
Среди возможных побочных реакций при синтезе алкидов следует отметить также гомоконденсацию полиатомных спиртов, приводящую к образованию простых полиэфиров, например, полиглицеринов:
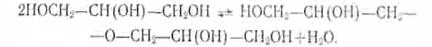
Эта реакция протекает при высоких (200°С) температурах, сопровождается выделением воды и катализируется теми же катализаторами, что и основной процесс полиэтерификации. Однако скорость ее на два порядка меньше скорости переэтерификации.
Синтез алкидов с использованием масел, содержащих в своем составе непредельные жирные кислоты, может также осложняться процессом окислительной полимеризации по двойным связям жирнокислотных остатков, что в свою очередь влияет на характеристики образующегося продукта. Относительную долю этого процесса можно уменьшить проведением синтеза в атмосфере инертного газа, не содержащего кислорода. Однако даже в отсутствие кислорода при температурах выше 200°С трудно избежать процессов термической полимеризации жирнокислотных остатков, протекающих в основном по реакциям диенового синтеза.
Жирнокислотный метод используется для получения алкидов, модифицированных свободными кислотами (кислоты растительных масел, СЖК и др.). Процесс проводят в одну или две стадии. При одностадийном способе все компоненты загружают одновременно и процесс ведут при постепенном подъеме температуры от 150 до 210°С.
В силу более высокой реакционной способности фталевого ангидрида в сравнении с кислотами вначале образуются неполные кислые эфиры фталевого ангидрида:
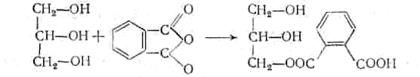
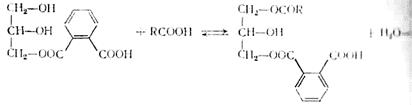 |
которые при дальнейшем подъеме температуры этерифицируются кислотой и подвергаются поликонденсации:
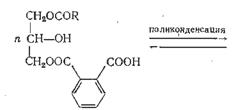 | 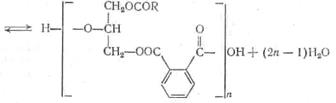 | ||
Двухстадийный процесс осуществляется по двум вариантам. По одному из них вначале в реакционную смесь вводят полиатомный спирт и фталевый ангидрид и после завершения реакции между ними — кислоту-модификатор.
По второму варианту на первой стадии при 200—210 °С проводят реакцию между полиатомным спиртом и монокарбоновыми кислотами, в результате которой получают неполные эфиры полиатомных спиртов:
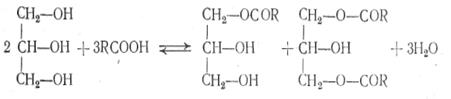
а на второй стадии при 180—240°С проводят реакцию неполных эфиров с фталевым ангидридом, приводящую в конечном счете к образованию алкидных олигомеров. Процесс на этой стадии идет по той же схеме, что и в случае глицеридного метода.
Следует отметить, что жирнокислотный метод дает возможность получать алкиды более регулярной структуры с хорошо воспроизводимыми характеристиками. Этот метод позволяет также осуществлять синтез алкидов, не содержащих в цепи глицеридных фрагментов.
Комбинированный метод включает элементы и глицеридного и жирнокислотного методов. Он используется в том случае, если для модификации алкида применяются растительные масла в сочетании со свободными кислотами (СЖК, канифоль, бензойные кислоты). По этому методу процесс ведут в две стадии, причем на первой стадии проводят одновременно реакции алкоголиза растительного масла многоатомным спиртом и частичную этерификацию гидроксильных групп свободными кислотами; на второй — осуществляют взаимодействие полученных продуктов с фталевым ангидридом и поликонденсацию:
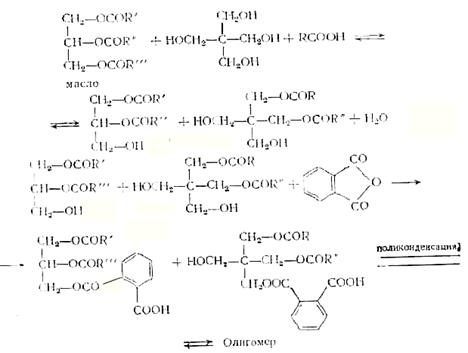
Для контроля реакции алкоголиза растительных масел, при которой концентрация функциональных групп не изменяется, -используют растворимость неполных эфиров полиатомных спиртов в этаноле. Иногда эту реакцию контролируют по электропроводности.
Процессы этерификации и полиэтерификации контролируются по изменению концентрации свободных карбоксильных групп в реакционной массе, которая оценивается кислотным числом. Полиэтерификация помимо кислотного числа контролируется также по изменению вязкости реакционной массы, так как именно этот показатель наиболее полно отражает увеличение молекулярной массы олигомера в процессе синтеза [6].
Дата: 2019-12-22, просмотров: 536.