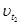 =
= 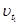 γ
γ 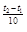
Температура увеличивается на 50°С, а γ = 3. Подставляя эти значения, получим 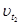 = 3
= 3 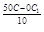 = 243
= 243
Ответ: скорость увеличится в 234 раза.
2. Для реакции первого порядка А→2В определите время за которое прореагировало на 90% вещества А. Константа скорости реакции 1*10-4 с-1.
Решение:
А → 2В
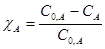 ;
; 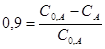 ;
;
C 0, A - CA =0,9 C 0, A
CA = 0,1 C0,A
k1t = lnC0,A- lnCA
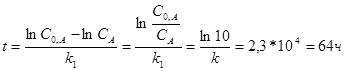 Ответ: 64 ч.
Ответ: 64 ч.
3. Как изменится скорость реакции 2А+В2 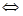 2АВ, протекающей и закрытом сосуде, если увеличить давление в 4 раза?
2АВ, протекающей и закрытом сосуде, если увеличить давление в 4 раза?
Решение:
По закону действия масс скорость химической реакции прямо пропорциональна произведению молярных концентраций реагирующих веществ: w= 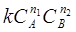 . Увеличивая в сосуде давление, мы тем самым увеличиваем концентрацию реагирующих веществ. Пусть начальные концентрации А и В равнялись [А] =а,
. Увеличивая в сосуде давление, мы тем самым увеличиваем концентрацию реагирующих веществ. Пусть начальные концентрации А и В равнялись [А] =а,
[В]=b. Тогда w=ka2b. Вследствие увеличения давления в 4 раза увеличились концентрации каждого из реагентов тоже в 4 раза и стали [A]=4a, [B]=4b.
При этих концентрациях w 1 =k(4а)2 *4b = k64а2b. Значение k и обоих случаях одно и то же. Константа скорости для данной реакции есть величина постоянная, численно равная скорости реакции при молярных концентрациях реагирующих веществ, равных 1. Сравнивая w и w 1, видим, что скорость реакции возросла в 64 раза. Ответ: скорость реакции возросла в 64 раза.
4. Энергия активации некоторой реакции в отсутствие катализатора равна
76 кДж/моль и при температуре 27°С протекает с некоторой скоростью k1. В присутствии катализатора при этой же температуре скорость реакции увеличивается в 3,38 • 104 раз. Определите энергию активации реакции в присутствии катализатора.
Решение:
Константа скорости реакции в отсутствие катализатора запишется в виде
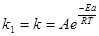 = Ае
= Ае 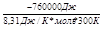 = Ae-30,485.
= Ae-30,485.
Константа скорости реакции в присутствии катализатора равна
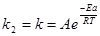 = Ае
= Ае 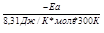 = Ае
= Ае 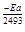 .
.
По условию задачи
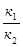 =e – (- 30,485-
=e – (- 30,485- 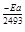 )=3,38 * 104.
)=3,38 * 104.
Логарифмируем последнее уравнение и получаем
30,485 - 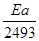 = 1n(3,38*104) = 10,43.
= 1n(3,38*104) = 10,43.
Отсюда Еа = 2493 • 20,057 = 50 кДж/моль.
Ответ: энергия активации реакции в присутствии катализатора равна 50 кДж/моль.
Задачи для самостоятельного решения
1. За какое время пройдет реакция при 60◦С, если при 20◦С она заканчивается за
40 с, а энергия активации 125,5 кДж/моль?
2. В загрязненном воздухе содержится примесь монооксида углерода, который образуется при неполном сгорании твердого топлива и работе двигателей внутреннего сгорания. Монооксид углерода медленно окисляется кислородом воздуха до диоксида углерода. Допустим, что при определенных условиях скорость такой реакции составляет 0,05 моль/л*с, а концентрация диоксида углерода равна 0,2 моль/л*с. Рассчитайте концентрацию диоксида углерода через 10 с после указанного момента.
3. Один из важных видов сырья для органического синтеза — так называемый водяной газ, представляющий собой смесь водорода и монооксида углерода. Эту смесь получают при пропускании водяного пара через башни, наполненные раскаленным углем. Из водяного газа получают метанол, формальдегид и другие вещества. Рассчитайте значение константы скорости реакции получения водяного газа, если при концентрации водяного пара, равной 0,03 моль/л скорость реакции составляет 6,1 • 10 -5 моль/л*с.
4. В реакции А + В → С с общим порядок равным 1, k1 = 5*10-5 c-1 Определите концентрации веществ А и В и скорость через 1 час и через 5 ч, если начальная концентрации А составляет 0,2 моль/л.
5. Причиной появления опасного для здоровья тумана (смога) считают образование большого количества выхлопных газов автомобилей при высокой влажности воздуха. В смоге присутствует ядовитый диоксид азота, который получается при реакции монооксида азота с атомарным кислородом. Рассчитайте скорость этой реакции, если через 5 мин после начала наблюдений концентрация диоксида азота была равна 0,05 моль/л, а через 20 мин - 0,08 моль/л.
6. Уравнение реакции омыления уксусноэтилового эфира:
СН2СООС2Н5 + NаОН = СН3СООNa+ С2Н5ОН
Исходные концентрации реагирующих веществ до начала реакции были: [СН3СООС2Н5] =0,50 моль/л, [NаОН] = 0,25 моль/л. Определить, как и во сколько раз изменится скорость реакции в момент, когда концентрация [СН3СООС2Н5] стала равной 0,30 моль/л.
7. Атмосферные загрязнения, например фторированные и хлорированные углеводороды — фреоны (СС13F, СС12F2, СС1F3), разрушают защитный озоновый слой Земли. Фреоны химически стабильны в нижних слоях атмосферы, но в стратосфере под действием ультрафиолетового излучения Солнца разлагаются, выделяя атомарный хлор, который и взаимодействует с озоном. Рассчитайте скорость такой реакции с образованием кислорода и монооксида хлора, если через 15 с после начала реакции молярная концентрация озона была 0,30 моль/л, а через 35с (от начала реакции) стала равна 0,15 моль/л.
8. За реакцией дегидрирования бутана, протекающей по уравнению
С4Н10 → С4Н8 + Н2 при температуре 800 К, следили по объему реагирующих газов, занимаемому ими при давлении 101 кПа и 293 К. Объем реактора 0,2 л, скорость протекания реакции равна 1,33 • 10-2 кПа/с. Рассчитайте, через какое время после начала реакции изменение объема достигнет 0,01 л.
9. Рассчитайте изменения константы скорости реакции, имеющей энергию активации 191 кДж/моль, при увеличении температуры от 330 до 400 К.
10. Вычислите порядок реакции и константу скорости, если при изменении начальной концентрации с 0,502 моль/л до 1,007 моль/л время полупревращения уменьшится с 51 с до 26 с.
11. Для реакции омыления уксусно-этилового эфира при большом избытке воды константа скорости при 20ºС равна 0,00099 мин-1, а при 40С ее величина составляет 0,00439 мин-1. Определите энергию активации и константу скорости реакции при 30ºС.
3.2 Технико-экономические показатели химических производств
Значение химии становится особенно ясным, когда изучаемый материал связывается с практическими вопросами. Один из способов его связи с жизнью — решение задач на темы с производственны содержанием. Для химической промышленности, как отрасли материального производства имеет значение технический и экономический аспекты, от которых зависит нормальное функционирование производства. Технико-экономические показатели (ТЭП) отражают возможности предприятия выпускать продукцию заданной номенклатуры и качества, удовлетворяющий требованиям заказчика, и в заданном количестве. Они являются критериями, позволяющий установить экономическую целесообразность организации данного производства и его рентабельность.
Рентабельность процесса производства характеризуется следующими ТЭП: степень превращения, выход продукта, селективность, производительность, мощность и интенсивность аппаратуры, практический и теоретический расходный коэффициент.
В этом разделе рассматриваются задачи следующих типов:
1. Задачи, в которых обращается внимание на получение вещества или на применение его в производственных условиях.
2. Задачи на определение выхода получаемого вещества по отношению к теоретическому.
3. Задачи, вскрывающие химическую сторону технологии производства и требующие составления уравнения реакции по которой оно протекает.
4. Задачи, в которых обращается внимание на масштабы производства или размеры аппаратуры (башен, камер, колонок) и т. п.
Степень превращения ( 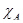 ) – это отношение количества вещества, вступившего в реакцию, к его исходному количеству вещества. Допустим, протекает простая необратимая реакция типа А → В. Если обозначить через
) – это отношение количества вещества, вступившего в реакцию, к его исходному количеству вещества. Допустим, протекает простая необратимая реакция типа А → В. Если обозначить через 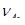 исходное количество вещества А, а через
исходное количество вещества А, а через 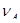 - количество вещества А в данный момент, то степень превращения реагента А составит
- количество вещества А в данный момент, то степень превращения реагента А составит
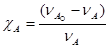 (2.1)
(2.1)
Чем выше степень превращения, тем большая часть исходного сырья вступила в реакцию и полнее прошел процесс химического превращения.
Выход продукта (η) является показателем совершенства процесса и показывает отношение количества фактически полученного количества того или иного продукта к его теоретическому количеству.
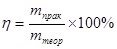 ;
; 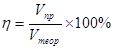 (2.2), (2.3)
(2.2), (2.3)
Производительность аппарата (П) определяет количество готового продукта m фактически вырабатываемый в единицу времени t при заданных условиях процесса производства. Измеряется т/сут, тыс.т/год, кг/ч, нм3/сут.
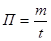 (2.4)
(2.4)
Интенсивность аппарата – производительность, отнесенная к единице полезного объема или к единице полезной площади. Измеряется кг/м3 и кг/м2
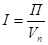 или
или 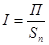 (2.5), (2.6)
(2.5), (2.6)
Максимально возможная производительность аппарата при оптимальных условиях процесса производства называется его мощностью W
W =П max (2.7)
Селективность – отношение массы целевого продукта к общей массе продуктов, полученных в данном процессе, или к массе превращенного сырья за время t.
Если А → В, А → С, где В – целевой продукт, С – побочный продукт, то уравнение имеет следующий вид:
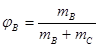 (2.8)
(2.8)
Это отношение скорости превращения вещества А в целевой продукт к общей скорости расхода вещества А.
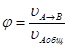
Расходный коэффициент Кр определяет расходы сырья, воды, топлива, электроэнергии пара на единицу произведенной продукции
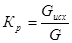 (2.9)
(2.9)
Gисх – затраты сырья, топлива, энергии при производстве продукта в количестве G. Измеряется в т/т, нм3/т, нм3/ нм3, кВт*ч/т.
Примеры решения задач
1. Сколько теоретически можно получить чугуна, содержащего 3% углерода и 3% других элементов, из 1 т железной руды, содержащей 80% железа?
Из каждой тонны железной руды, содержащей в среднем 80% магнитного железняка, выплавляют 570 кг чугуна, содержащего 95% железа. Каков был выход железа от теоретического?
Решение:
М(Fе3О4) = 232 г/моль
М(Fе) = 56 г/моль
Записываем формулу определения η(Fе):
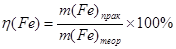
Обеих величин в условии нет. Но m(Fе)пр можно рассчитать по массе чугуна и массовой доле железа в нем:
m(Fе)пр = 570 кг • 0,95 = 541,5 кг.
Сразу теоретическую массу железа по условию не вычислить. Можно найти массу магнитного железняка по массе руды и содержанию в ней массовой доли железняка:
m(Fе3О4) = 1000 кг • 0,8 = 800 кг.
По вычисленной массе магнитного железняка и его формуле найдем массу железа в нем:
800 > 232 в 3,45 раза => m(Fе) будет > 168 (56 • 3) тоже в 3,45 раза, т. е.
M(Fе) = 168 • 3,45 = 579,6 (кг).
Подставляя полученные значения практической и теоретической массы железа в первоначальную формулу, получим выход железа:
η(Fе) = 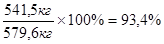
Ответ: η(Fе) =93,4%.
2. Для получения формальдегида метиловый спирт необходимо окислить на серебряном катализаторе: СН3ОН + 0,5О2 = СН2О + Н2О. Кроме основных реакций протекают и побочные. Предположим, что на окисление подается 3,2 кмоль метилового спирта. Их них образовалось 1,8 кмоль формальдегида, 0,8 моль – побочных продуктов (суммарно) и остались неокисленными 0,6 кмоль метилового спирта. Необходимо найти степень превращения метилового спирта, выход формальдегида и селективность.
Решение:
Определим степень превращения. Для этого количество непрореагировавшего спирта, оставшегося после реакции, 0,6 кмоль необходимо вычесть из его начального количества 3,2 кмоль. Подставив данные значения в формулу (2.1) получим:
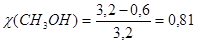
Рассчитаем селективность по формальдегиду. Общее количество полученных продуктов равно сумме количества формальдегида 1,8 кмоль и количества продуктов 0,8 кмоль.
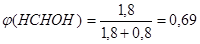
Найдем выход продукта формальдегида.
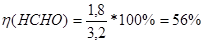
Ответ: 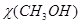 = 0,81, φ(НСНО)= 0,69, η(НСНО)= 56%
= 0,81, φ(НСНО)= 0,69, η(НСНО)= 56%
Задачи для самостоятельного решения
1. Рассчитать основные технико-экономические показатели получения синтетического аммиака:
а) расходный коэффициент сырья по Н2 и N2 (в м3) на 1т аммиака.
Б) выход аммиака
в) производительность завода.
Г) интенсивность процесса синтеза аммиака в т/м3 полезного объема колонки в сутки. На 1т аммиака практически расходуется 3000 нм3 азотоводородной смеси, теоретически 2635 нм3. 5 колонок с высотой 0,36 м.
2. Вычислить расходный коэффициент на 1т СН3СООН для СаС2, содержит 65% СаС2, если выход С2Н2 97%, уксусного альдегида 95% и СН3СООН 96%.
3. Вычислить количество аммиака и СО2 (в кг) израсходованных на производство мочевины. Потери мочевины 5% избыток аммиака 100%, степень превращения карбомата аммония мочевину 75%
4. При окислительном дегидрировании метилового спирта протекают одновременно две реакции: дегидрирование и окисление метанола. Выход формальдегида 90% при степени конверсии метанола 65%. Вычислите расход метанола на 1т формальдегида.
5. Производительность мечи для обжига серного колчедана составляет 30т в сутки. Выход SО2- 97,4% от теоретического. Сколько тонн SО2 производит печь в сутки, если содержание серы в колчедане 42,4%?
6. Печь для варки стекла, производящая в сутки 300т стекломассы имеет ванну длиной 60м, шириной 10м и глубиной 1,5 м. Определить:
а) годовую производительность, если 15 суток печь находится на ремонте
б) интенсивность печи за сутки работы.
В) количество листов оконного стекла за из свариваемой стекломассы (стандарт. Лист 1250 * 700 * 2 мм и плотность 2500 г/м3)
7. При прямой гидратации этилена наряду с основной реакцией присоединения Н2О протекают побочные реакции. Так 2% (от массы) этилена расходуется на образование простого диэтилового эфира, 1% ацетальдегида, 2% низкомолекулярного жидкого полимера. Общий выход спирта при многократной циркуляции сост. 95%. Напишите уравнению химической реакции образовавшихся выше перечисленных соединений и подсчитайте расход этилена на 1т этилового спирта, и сколько диэтилового эфира может при этом получится.
8. Шахтная печь для получения оксида кальция имеет в среднем высоту
14 м и диаметр 4 м; выход оксида кальция составляет 600- 800 кг на 1 м3 печи в сутки. Определите суточный выход оксида кальция.
9. Производительность печи для обжига колчедана составляет 30 т колчедана в сутки. Колчедан содержит 42,2% серы. Воздух расходуется на 60% больше теоретического. Выход сернистого газа составляет 97,4%.
Вычислить а) содержание колчедана FеS2 (в%); б) объем и состав газовой смеси, выходящей из смеси за 1 час; в) массу оставшегося в печи огарка; г) массу оставшегося в печи не прореагировавшего FeS2.
10. Протекают две параллельные реакции 2А → С и А → 3В. Определите выход продукта С, степень превращения реагента А и селективность по продукту В, если на выходе из реактора известно количество веществ ν(А) = 2 моль, ν(С)=ν(В)=3 моль.
3.3 Задачи с экологическим содержанием
Охрана воздушного и водного бассейнов, защиты почв, сохранение и воспроизводство флоты и фауны – важные проблемы современности. В нашей стране разработано несколько общих направлений защиты биосферы от промышленных выбросов: создание безотходных технологий, замкнутых систем производств, основанный на полном комплексном использовании сырья; уменьшение объема промышленных стоков путем создания бессточных производств; проведение мероприятий по уменьшению загрязнения биосферы газообразными выбросами сжигания топлива; разработка методов утилизации; и обезвреживания производственных отходов и выбросов на действующих предприятиях.
Экологическая химия – наука, изучающая основы экологических явлений и химических процессов, происходящих в природе. В данном разделе применяются основные законы и формулы, применяемые для расчета массы, количества вещества, объема, концентрации, в том числе и для определения предельно-допустимых концентраций.
Предельно-допустимая концентрация (ПДК) – это такая концентрация, которая не оказывает на живые организмы прямого или косвенного влияния, не снижает его работоспособность, самочувствие. Основной задачей газоочистки и очистки сточных вод служит доведение содержания токсичных примесей в газах и сливных водах до ПДК установленных санитарными нормами. При невозможности достигнуть ПДК путем очистки иногда применяют многократное разбавление токсичных веществ или выброс газов через высокие дымовые трубы для рассеивания примесей в верхних слоях атмосферы. Для санитарной оценки среды используют несколько видов ПДК.
- ПДК воздушной среды;
- ПДК водной среды;
- ПДК почвы.
Для определения предельно-допустимой концентрации применяют следующую формулу:
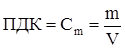 ,
,
где С m – предельно-допустимая концентрация, m – масса токсичного соединения,
V – объем, в котором присутствует соединение данной массы.
Теоретическое определение концентрации примесей в нижних слоях атмосферы в зависит от высоты трубы. Высота трубы, от которой зависит содержание примесей в приземном слое воздуха, рассчитывается по эмпирической формуле:
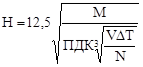

где М – количество вредных веществ, выбрасываемых в атмосферу, г/с; V – объем выбрасываемых газов, м3 /с; ∆Т – разность между температурами выходящих газов и окружающего воздуха, ◦С; N – число труб, через которые выводятся отходные газы.
Предельно допустимый выброс (ПВД) вредных примесей в атмосферу, обеспечивающий концентрацию этих веществ в приземном слое воздуха не выше ПДК, рассчитывается по формуле
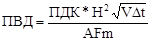
где А – коэффициент, определяющий условия вертикального и горизонтального рассеивания вредных веществ в воздухе; F- коэффициент, учитывающий скорость седиментации вредных веществ в атмосфере; m- коэффициент, учитывающий условия выхода газа из устья трубы. Коэффициент m может быть вычислен по формуле
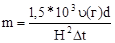
где v –средняя скорость газа на выходе из трубы, м/с; d - диаметр трубы, м.
Примеры решения задач.
1. В настоящее время муравьиную кислоту получают из природного газа путем каталитического окисления содержащегося в нем метана. Вычислите объем природного газа (и. у.), необходимого для получения муравьиной кислоты массой 69 т, если объемная доля метана в нем равна 0,95. Определите преимущества данной технологии по сравнению с методом получения муравьиной кислоты путем разложения формиата натрия серной кислотой при охлаждении раствора.
Решение:
СН4 + 3[О] →НСООН+Н2О
ν(НСООН) = 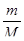 =
= 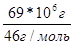 =1,5*106 моль;
=1,5*106 моль;
V(СН4) =ν*Vm= 1,5*106 моль*22,4 л/моль=33,6*105 л.
V(природного газа)=33,6* 106 л: 0,95=35,37*106 л=35,37*103 м3
Ответ: объем природного газа равен 35,37*103 м3.
Современный способ получения муравьиной кислоты дает экономическую выгоду, так как его использование уменьшает расход ценного сырья. Экологическая выгода заключается в том, что если природный газ используют без предварительной переработки, то это вызывает попадание в атмосферу большого количества продуктов его сгорания: оксидов серы, азота, углерода, которые загрязняют окружающую среду. Данная технология получения муравьиной кислоты имеет также преимущества в сравнении с синтезом кислоты из формиата натрия, который осуществляется в несколько стадий и дает в качестве побочных продуктов производства соли серной кислоты, кислотные и щелочные сточные воды.
Природный газ данного объема почти полностью расходуется на получение муравьиной кислоты. Следовательно, выброс отходов производства в окружающую среду уменьшается по сравнению с методом получения ее разложением формиата натрия, так как используется малоотходная технология.
2. В сточных водах химико-фармацевтического комбината был обнаружен хлорид ртути HgCl2, концентрация которого составила 5 мг/л. Для его очистки решили применить метод осаждения. В качестве осадителя использовали сульфид натрия (Na2S) массой 420 г. Будут ли достаточно очищены сточные воды, чтобы допустить их сброс в соседний водоем, содержащий 10 000 м3 воды?
ПДК (HgCl2) = 0,0001 мг/л. Объем сточных вод 300 м3
Решение:
HgCl2 + Na2S = HgS + 2NaCI
C(HgCI2)= 5 мг/л = 5 * 10-3г/л; V=300 м3 = 300*10 3л;
m(HgCl2)=1500г
ν(HgCl2)= 5,52 моль
m(Na2S) =420 г; ν(Na2S) = 5,38 моль. Согласно уравнения реакции в недостатке содержится сульфид натрия, в избытке - хлорид ртути. Останется хлорида ртути количеством 0,14 моль, m =0,14 моль*271,58 г/моль= 38 г.
m (HgCl2) = 38 г;
Находим ПДК
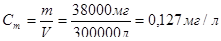
Это число значительно превышает ПДК. Однако при сбросе сточных вод в природный водоем концентрация хлорида ртути понизится и будет равна: 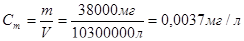 . Полученное число также больше ПДК. Таким образом, сброс воды недопустим.
. Полученное число также больше ПДК. Таким образом, сброс воды недопустим.
Ответ: Сm (HgCl) = 0,127 мг/л в сточных водах и 0,0037 мг/л в открытом водоеме, что значительно больше ПДК.
3. Как можно утилизировать доменный газ?
Решение:
Доменный газ имеет высокую температуру, поэтому на первой стадий его
переработки осуществляют утилизацию тепла, на второй - от газа отделяют
колошниковую пыль (оксиды меди) с помощью циклонов и электрофильтров. В дальнейшем доменный газ используют в качестве топлива. Кроме того, его
можно очистить от оксидов серы по реакции Клауса:
SO2 + 2H2S = 3S + 2Н2О.
Следует отметить, что в настоящее время доменный процесс считается бесперспективным. Его заменяют прямым восстановлением железа из руды.
Задачи для самостоятельной работы
1. В радиусе 2 км вокруг химического завода ощущается легкий запах сероводорода. Анализ проб воздуха, отобранных с вертолета, показал, что газ находится в атмосфере на высоте до 2,0 км. Средняя концентрация сероводорода в воздухе составляет 1/20 промышленно допустимой концентрации (ПДК), равной 0,01 мл/л. Сколько тонн серной кислоты (считая на безводную) можно было бы получить, если бы удалось уловить весь сероводород в этом пространстве?
2. Картофель, выращенный вблизи шоссе, всегда содержит весьма ядовитые соединения свинца. В пересчете на металл в 1кг такого картофеля было обнаружено 0,001 моль свинца. Определите, во сколько раз превышено предельно допустимое содержание свинца в овощах, значение которого равно 0,5 кг?
3. Природный газ содержит главным образом метан СН4, но в нем присутствуют и примеси, например ядовитый сероводород Н2S — до 50 г на 1 кг метана. Чтобы удалить примесь сероводорода, можно окислить его перманганатом калия КМnО4 в кислой среде до серы. Рассчитайте массу серы, которую можно таким образом выделить из 1 т природного газа. Определите также массу серной кислоты, которая может быть получена из этой серы.
4. Диоксид серы образуется в основном при сжигании твердого топлива на тепловых электростанциях. Это бесцветный газ с резким запахом, он сильно раздражает слизистые оболочки глаз и дыхательных путей. Наличие диоксида серы в атмосфере — причина кислотных дождей, поскольку под действием кислорода воздуха и воды диоксид серы превращается в серную кислоту. Однако далеко не все производства, в выбросах которых содержится диоксид серы, имеют современные сооружения для газоочистки. Чаще применяется разбавление выбросов чистым воздухом или рассеивание их в воздушной среде путем устройства дымовых труб большой высоты. Установлено, что при высоте трубы 100 м на расстоянии 2 км от предприятия содержание диоксида серы в воздухе равно 2,75 мг/м3. Во сколько раз этот показатель превышает значение предельно допустимой концентрации, равное 7,8*10-6 моль/м3.
5. Формальдегид НСНО применяется при изготовлении древесностружечных плит, красок, искусственного волокна, лекарственных средств, оргстекла и т.п. Он обладает сильным и резким запахом и угнетающе действует на сердечнососудистую и нервную системы. Запах формальдегида чувствуется при его содержании в воздухе, равном 0,2 мг/м3, а санитарные нормы требуют, чтобы примесь формальдегида в воздухе не превышала 0,003 мг/м3. Рассчитайте молярную концентрацию формальдегида: а) при полном соответствии воздуха санитарным нормам; б) при появлении запаха формальдегида.
6. Рассчитайте, какой высоты должна быть труба, чтобы концентрация оксида серы (IV) в приземистом слое воздуха не превышала ПДК (0,5 мг/г3). Отходящий топливный газ с объемной долей оксида серы (IV) 0,05% поступает в дымовую трубу со скоростью 300 м3/ч при температуре 130◦С. Температура воздуха 20◦С.
7. Незаконное захоронение ртути привело к тому, что ее содержание в 1кг почвы на некотором участке лесопарковой зоны составило 0,005 моль. ПДК ртути в почве равно 21 мг/кг. Во сколько раз превышено значение ПДК ртути в почве?
8. Водный раствор 0,001 моль йода в избытке йодида калия полностью обесцветился после пропускания через него 1м3 воздуха. Рассчитайте содержание диоксида серы (мг/м3) в исследуемом воздухе и сравните полученный результат с ПДК (SO2), равной 0,05мг/м3. Превышено ли значение ПДК диоксида серы?
9. Историки полагают, что случаи отравления соединениями свинца в Древнем Риме были обусловлены использованием свинцовых водопроводных труб. Свинец в присутствии диоксида углерода взаимодействует с водой. При этом образуется растворимый гидрокарбонат свинца:
Рb+СО2+Н2О=РbСО3+Н2↑
РbСО3+СО2+Н2О=Рb(НСО3)2
Катионы свинца не приносят вреда здоровью, если их содержание в воде не превышает 0,03 мг/л. Во сколько раз оно было превышено, если считать, что 1 литр водопроводной воды содержал 0,0000145 моль Рb2+?
10. При производстве серы автоклавным методом неизбежно выделяется около
3 кг сероводорода на каждую тонну получаемой серы. Сероводород — чрезвычайно ядовитый газ, вызывающий головокружение, тошноту и рвоту, а при вдыхании в большом количестве - поражение мышцы сердца и судороги, вплоть до смертельного исхода. Какой объем сероводорода (при н. у.) необходимо поглотить в системах газоочистки при получении 125 т серы на химзаводе?
11. На нефтеперерабатывающем заводе из-за поломки произошел аварийный выброс нефтепродуктов в ближайшее озеро. Масса сброшенных продуктов составила 500 кг. Выживут ли рыбы, обитающие в озере, если известно, что примерная масса воды в озере 10000 т. Токсичная концентрация нефтепродуктов для рыб составляет 0,05 мг/л.
12. Определите ПВД фтороводорода (в г в сек), обеспечивающий концентрацию его в приземном слое атмосферы в районе суперфосфатного завода не выше ПДК 0,05 мг/м3, при высоте дымовой трубы 100 м и ее диаметре 0,7 м. Объем газового выброса равен 160, а коэффициент седиментации – 1. Средняя скорость газа на выходе из трубы – 0,4 м/с. Температура выходящего газа 40С, а атмосферы – 23С.
3.4 Производство неорганических соединений
Металлургия
Металлургия – это наука о промышленных способах получения металлов из природного сырья. Металлургией также называю металлургическую промышленность. Сырьем в производстве металлов является металлические руды. За исключением небольшого числа металлов находящихся в природе в виде химических соединений входящих в состав металлических руд. Основной задачей металлургической промышленности является получение металлов из руд. Для этого руду подготавливают, подвергают вторичной обработке и процессу восстановления.
Задачи, которые приводятся в этом разделе являются расчетными задачами по уравнениям химических реакций. При решении задач используют основные законы и формулы химии, а также формулы которые рассматривались в предыдущих разделах (выход продукта, интенсивность, производительность и тд.)
Одной из важнейших задач химической технологии является обогащение сырья. Для этого применяют метод флотации, который основан на различной смачиваемости водой минералов.
Выход концентрата (Вк) называется процентное отношение веса полученного концентрата к весу взятой руды.
Степень извлечения (Си) называется процентное отношение веса извлеченного элемента в концентрате к его весу в руде.
Степенью обогащения (Со) называется отношение процентного содержания элемента в концентрате к содержанию его в исходной руде.
В этом разделе при решение задач используют следующие понятия: выход продукта, расчет состава руды, возможность самопроизвольного протекания реакции получения металла, которые подробно описываются в других разделах.
Примеры решения задач
1. Рассчитать минимальный расход магния для удаления сурьмы из 10 т чернового свинца, в котором сурьма составляет 0,5% массы. Сурьма выделяется из сплава в составе соединения Мg3Sb2
Решение:
Составим первое уравнение масса магния, добавленного в черновой сплав, равна массе магния в выделившемся из сплава соединении Mg3Sb2. Запишем второе уравнение, полагая, что масса сурьмы, содержащейся в 10 т чернового сплава, равна массе сурьмы и образовавшемся соединении Мg3Sb2.
 m(Mg) =
m(Mg) =  m(Mg3Sb2)*(3*M(Mg)/M(Mg3Sb2)
m(Mg3Sb2)*(3*M(Mg)/M(Mg3Sb2)
10*0,005 = m(Mg3Sb2)*(2*M(Sb)/M(Mg3Sb2)
Или
 m(Mg) = m(Mg3Sb2)*(3*24)/316
m(Mg) = m(Mg3Sb2)*(3*24)/316
0,05 = m(Mg3Sb2)*(2*122/316)
Для решения системы уравнении разделим правую и левую части первого уравнения на соответствующие части второго и обозначая (Мg) через х, получим:
x/0,05=24*3/122*2, x=0,0148
Ответ. Минимальный расход магния— 14,8 кг.
2. На обогатительной фабрике флотации подвергается руда, содержащая 1,3% меди. При флотации 1т исходной руды получится 110,5 кг концентрата, содержащего 9,6% меди. Определите выход концентрата, степень извлечения и степень обогащения.
Решение
1.Вк= 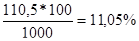
2. Для вычисления Си рассуждаем так
а) в 100 кг исходной руды содержится 1,3 кг меди
в 1000 кг ---------------------------------- х кг меди
х= 13 кг меди
б) в 100 кг концентрата содержится 9,6 кг меди
в 110,5 кг ---------------------------------- х кг меди
х= 10,6 кг меди.
Следовательно, степень извлечения будет равна
Си= 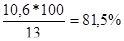
3. Со= 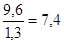 раза.
раза.
Ответ Вк=11,05%, Си=81,5%, Со=7,4 раза.
Примеры решения задач
1. Имеется титановая руда, состоящая из минералов рутила, перовскита и пустой породы. Массовая доля ТiО2 в этих минералах составляет соответственно 97% и 59%. Вычислить массовые доли названных выше минералов в руде, если известно, что содержание титана равно 27% от массы руды, а пустой породы – 38%.
2. Для легирования стали, требуется внести в расплав титан, чтобы его массовая доля составила 0,12%. Какую массу сплава ферротитана надо добавить к расплаву стали массой 500 кг, если массовые доли металлов в ферротитане составляют: титана – 30%, железа – 70%
3. Некоторая порода состоит из минералов сильвинита (KCl), каинита (MgSO4*KCl*3H2О) и карналлита (MgCl2*KCl*6H2О). Массовая доля калия в породе составляет 18%, а примесей (не содержащих калия и магния) – 12%. Вычислите возможную массу магния в 100 кг породы.
4. При обогащение 10 т медной сульфидной руды, содержащей 1,5% меди, получено 400 кг концентрата, содержащего 30% меди. Определить степень извлечения и степень концентрации.
5. При флотации 5т цинковой руды, содержащего 3% цинка, получено 340 кг концентрата, содержащего 22% цинка. Определите выход концентрата, степень извлечения и степень концентрации. 
6. Восстанавливая углем соединение Fe(CrO2)2 (хромистый железняк), получают сплав феррохром, используемый в металлургии. Определите массовую долю хрома в этом сплаве, считая, что других компонентов, кроме железа и хрома, он не содержит.
7. Железная руда имеет состав: магнетит Fе3О4 (массовая доля 55%), ильменит FеТiО3 (массовая доля 15%) и другие вещества, не содержащие железо и титан. Какую массу железа и титана можно получить из такой руды массой 300 кг?
8. Из медной руды массой 16т, содержащей халькозин Cu2S и вещества, не содержащие медь, получили черновой металл массой 650 кг. Определите массовые доли меди и халькозина в руде, если массовая доля меди в черновом металле составляет 98,46%.
9. Для удаления висмута из черного свинца к расплавленному металлу добавляют сплав Pb – Ca, массовая доля кальция в котором составляет 0,03. Рассчитать теоретический расход сплава Pb – Ca для удаления висмута из 100 т чернового свинца, массовая доля висмута в котором равна 0,001. Висмут выделятся из сплава в составе соединения Ca3Bi2.
10. Медная руда содержит CuCO3*Cu(OH)2 и азурит 2CuCO3*Cu(OH)2 Какую массу меди можно получить из руды массой 5т, если массовая доля малахита 8%, азурита 3,6%. Определите массовую долю меди в руде.
3.4.2 Электрохимические производства
Электролизом называется окислительно-восстановительная реакция, протекающая при пропускании постоянного электрического тока через расплав или раствор электролита.
Сущность электролиза заключается в следующем: при пропускании электрического тока через расплав или раствор электролита положительные ионы электролита (ионы металлов или водорода) притягиваются катодом, а отрицательные ионы (кислотные остатки или гидроксильные группы) — анодом. Приносимые к катоду от источника тока электроны присоединяются к положительным ионам электролита, восстанавливая их. Одновременно отрицательные ионы электролита отдают свои электроны аноду, от которого они двигаются к источнику тока. Теряя свои электроны, они окисляются в нейтральные атомы или группы атомов. Таким образом, у катода протекает процесс восстановления, а у анода — процесс окисления.
А (+): nAn- - ne- → nAp-
K (-): nBn+ + ne- → nBp+
Оба процесса образуют единую окислительно-восстановительную реакцию. Но в отличие от обычных окислительно-восстановительных реакций электроны от восстановителя к окислителю переходят не прямо, а посредством электрического тока. Катод, приносящий электроны, является восстановителем, а анод, уносящий их,— окислителем.
Основными показателями электрохимических производств являются выход по току, степень использования энергии. Расходный коэффициент по энергии, напряжение, приложенное к электролизеру, и др. Большинство вычислений основано на законе Фарадея, согласно которому масса вещества, выделившегося при электролизе пропорционально силе тока I, времени электролиза t и электрохимическому эквиваленту этого вещества ЭЭ
Масса вещества вычисляется по формуле
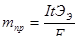 (1.3.1)
(1.3.1)
где, I - сила тока, F – постоянная Фарадея (96500 Кл)
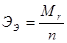 (г-экв) (1.3.2)
(г-экв) (1.3.2)
Mr – относительная молекулярная масса вещества,
n – заряд иона (абсолютное значение) в виде которого вещество находится в растворе или в расплаве (т.е. количество отданных или принятых электронов).
Выход по току определяется отношением массы вещества, выделившегося при электролизе, к массе вещества, которое теоретически должно выделится согласно закону Фарадея, и выражается в процентах:
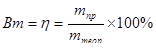 (1.3.3)
(1.3.3)
Масса mтеор находится по формуле
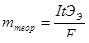
 (1.3.4)
(1.3.4)
Выход по энергии определяется по уравнению
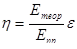 (1.3.5)
(1.3.5)
где, Етеор и Епр – теоретическое и практическое напряжение разложения при электролизе соответственно, В; η - выход по энергии,%.
Выход по энергии может быть вычислен и по количеству затраченной энергии:
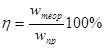 (1.3.6)
(1.3.6)
где w теор и w пр – количество энергии, теоретически необходимое и практически затраченное на получение единицы продукта.
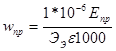 (1.3.7)
(1.3.7)
где 1000 – коэффициент перевода Вт*ч в кВт*ч;
1*10-6 – число, используемое для перевода граммов в тонны.
Теоретический расход электроэнергии находится по отношению
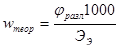 (1.3.8)
(1.3.8)
где φразл – напряжение разложения.
Примеры решения задач
1. Какие процессы происходят при электролизе расплава гидроокиси натрия?
Решение:
В расплаве едкого натра содержатся ионы Nа+ и ОН  . Окисляющиеся у анода ионы ОН
. Окисляющиеся у анода ионы ОН  в следующей стадии разлагаются с образованием воды и кислорода. Процесс можно изобразить следующим образом:
в следующей стадии разлагаются с образованием воды и кислорода. Процесс можно изобразить следующим образом:
К(-): 2Na+ + 2е- = 2Na;
А(+): 2ОН  - 2e- = Н2О + О2
- 2e- = Н2О + О2
Два атома кислорода, соединяясь друг с другом, образуют молекулу кислорода О2. Таким образом, суммарное уравнение
4NаОН = 4Na + 2Н2О + О2
При электролизе расплавов солей кислородных кислот окисляющиеся ионы кислотных остатков тут же разлагаются на кислород и соответствующие оксиды.
Своеобразно протекает электролиз в водном растворе. Дело в том, что сама вода — электролит, хотя и очень слабый. Таким образом, в водном растворе фактически содержатся два электролита — растворитель и растворенное вещество и соответственно по два вида как положительных, так и отрицательных ионов. Какие из них будут разряжаться, зависит от ряда условий. Как правило, можно руководствоваться следующим. Если положительные ионы электролита являются ионами очень активных металлов, как например Na+ или К-, то при электролизе разряжаются не ионы этих металлов, а ионы водорода из воды с выделением свободного водорода и освобождением гидроксильных ионов, что может быть выражено следующим электронно-ионным уравнением:
2H+OH  + 2е- = Н2↑ + 2ОН
+ 2е- = Н2↑ + 2ОН 
Если отрицательными ионами электролита являются кислотные остатки кислородных кислот, то при электролизе разряжаются не кислотные остатки этих кислот, а ионы ОН  из воды с выделением кислорода, что можно выразить уравнением:
из воды с выделением кислорода, что можно выразить уравнением:
4Н2О — 4е- = 4Н+ + 4ОН 
4ОН- 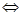 2Н2О+О2
2Н2О+О2
Складывая оба уравнения, получаем:
2Н2О — 4е- = 4H+ + O2
2. Определить выход по току (в%), если в течение 24 ч в электролизере раствора поваренной соли при силе тока 15500А было получено 4200 л электролитической щелочи с концентрацией NaOH 125 кг/м3.
Решение:
По уравнению (1.3.4) масса гидроксида натрия теоретически должна была составить
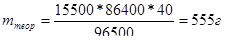
практически было получено
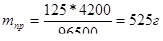
Следовательно, выход по току по формуле (1.3.3) будет равен
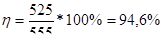
Ответ: выход по току 94,6%.
3. Определите фактический расход электроэнергии (в киловатт-часах) на получение хлора массой 1 т и выход по энергии (в%), если среднее напряжение на электролизере 3,35В, выход по току 96%, а электрохимический эквивалент хлора равен 1,323 г/А*ч.
Решение:
Использовав формулу (1.3.7), определим фактический расход энергии
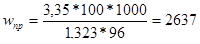
Если принять выход по току за 100%, то при теоретическом напряжении разложения NaCl, равном 2,17В, теоретический расход энергии на 1т хлора составит
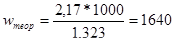
В этом случае выход по энергии
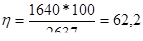
Ответ: выход по энергии 62,2%; 2637 кВ/ч
Задачи для самостоятельного решения
1. Один из способов промышленного получения кальция – электролиз расплавленного хлорида кальция. Какая масса металла будет получена, если известно, что в результате электролиза выделился хлор объемом 896 л (н.у.)?
2. При электролизе раствора хлорида натрия в электролизе, работавшем в течении 24ч при силе тока 30000 А, было получено 8,5 м3 электролитической щелочи с концентрацией NaOH 120 кг/м3. рассчитать выход по току (для щелочи)
3. Определить силу тока, необходимые для выработки 100% -ного гидроксида натрия массой 1720 кг в сутки в электролизере с железным катом при его непрерывной работе, если выход по току составляет 96%
4. Вычислить массу хлора, вырабатываемого за год заводом, на котором установлено 5 серий по 150 электролизеров с железными катодами при непрерывной работе в течении 350 дней, силе тока 34000 А и выходе по току 95%. Определить мощность генератора переменного тока электростанции, обеспечивающий потребности завода в электрической энергии при напряжении донной серии 550 В, если КПД выпрямителя тока составляет 95%.
5. Вычислить теоретический и практический расход электроэнергии на 1т 100% NаОН для электролиза раствора хлорида натрия с ртутным катодом. Теоретическое напряжение разложения равно 3,168 В. Определить выход по энергии, если практическое напряжение разложения 4,4 В, а выход по току 92,5%.
6. Какие вещества, и в каком количестве выделяются на угольных электродах, если состав раствора 0,1 моль HgCl2 и 0,2 моль CuCl2 и через него пропускается ток силой 10 А в течение 1 ч?
7. При прохождении электрического тока через разбавленный раствор серной кислоты в течении 10 мин выделилось 100 мл водорода при 18С и давлении
755 мм рт. ст. Вычислите силу тока.
8. При электролитическом получении магния в качестве электролита может служит расплавленных хлорид магния. Вычислите выход по току, если в ванне, работающем при силе тока 40000 А, в течении 5 ч, выделилось 72,6 кг магния.
9. Определить количество электричества, необходимое для выделения 1 м3 водорода и 0,5 м3 кислорода, получаемое при электролизе воды. Теоретическое напряжение воды равно 1,23 В, а фактическое превышает его в 1,5 – 2 раза. Рассчитать фактический расход электрической энергии.
10. При электролизе раствора содержащего 2,895 г смеси FeCl2 и FeCl3, на катоде выделилось 1,12 г металла. Вычислите массовую долю каждого из компонентов исходной смеси, если электролиз проводили до полного осаждения железа.
Дата: 2019-07-30, просмотров: 461.