ΔG0T=ΔH0T – TΔS0T
При стандартной температуре
ΔG0298=ΔH 0298– TΔS0298
ΔG0298 – стандартная энергия Гиббса, изменение энергии Гиббса при образовании 1 моль вещества из простых веществ в стандартных условиях, (кДж/моль).
Стандартную энергию Гиббса реакции рассчитывают по первому следствию из закона Гесса.
∆rG 0298= ∑(n j ΔfG0298) прод. -∑ (n i ΔfG0298)исход.
ΔS0298 - стандартная энтропия 1 моль вещества в стандартном условиях, (Дж/К*моль). Энтропию можно характеризовать как меру беспорядка (неупорядоченности) системы. Эта величина характеризует изменение температуры в системе.
Поскольку энтропия – функция состояния системы, ее изменение (ΔS) в процессе химической реакции можно подсчитать, используя следствие из закона Гесса.
ΔrS0298 =∑ (n j ΔfS0298) прод. –∑(n i ΔfS0298)исход
где, n j и n i – количество вещества продуктов реакции и исходных веществ соответственно (численно равно коэффициенту в уравнении реакции), (моль).
ΔrS0298 =∑ (n i ΔfS0298) исход –∑(n j ΔfS0298)прод
где, n i и n j - количество вещества исходных веществ и продуктов реакции соответственно (численно равно коэффициенту в уравнении реакции), (моль).
ΔrS0298 – стандартная энтропия реакции, (Дж/К).
ΔfS0298 – стандартная энтропия образования химического вещества, (Дж/К*моль).
Знак « - » перед членом TΔS0298 (энтропийным членом) ставится, для того чтобы при ΔH=0 сделать ∆G отрицательной величиной ΔG<0 – условие самопроизвольного протекания реакции.
Если пренебречь изменением ΔS0 и ΔН0 с увеличением температуры, то можно определить Травн, т.е. температуру, при которой устанавливается химическое равновесие химической реакции для стандартного состояния реагентов, т.е. из условия равновесия реакции ΔG=0 имеем 0=ΔrH 0298– TΔrS 0298, отсюда


Следует знать:
Если ΔS=0 (ΔS>0), ΔH<0(ΔH=0) то ΔG <0 – реакция протекает самопроизвольно, процесс протекает в прямом направлении (энергетически выгоден).
Если ΔS=0(ΔS<0), ΔH>0 (ΔH=0) то ΔG>0 – протекание реакции невозможна, возможна только в обратном направлении (энергетически невыгоден).
Если ΔS=0, ΔH=0 ΔG=0 – система находится в состоянии равновесия.
Примеры решения задач
1. Вычислить тепловой эффект реакции получения гидроксида кальция
СаО(т) + Н2О(ж) = Са(ОН)2(т), если теплота образование СаО(т) равна +635701,5Дж/моль, теплота образования Н2О(ж) +285835,5 Дж/моль и теплота образования Са(ОН)2 +986823 Дж/моль.
Решение:
Тепловой эффект реакции
СаО (т) + Н2О (ж) = Са(ОН)2(т) по первому следствию закона Гесса, будет равен теплоте образования Са(ОН)2(т) минус теплота образования Н2О(ж) и теплота образования (СаО(т)):
ΔrН0298 =∑(nj •ΔfН0298)прод - ∑(ni• ΔfН0298)исх.
ΔrН0298=1 моль•ΔfН0298(Са(ОН)2(т)) - (1 моль ΔfН0298(СаО(т)) +
+1 моль• ΔfН0298(Н2О (ж)))=1 моль*986823 Дж/моль - (1 моль* 635701,5 Дж/моль +
+ 1 моль*285835,5 Дж/моль)= 65 286 Дж.
Ответ: 65286 Дж.
2. Вычислите изменения энергии Гиббса в реакции димеризации диоксида азота при стандартной температуре, при 0 и 100ºС. Сделать вывод о направлении процесса.
Решение:
При стандартной температуре 298 К изменение энтальпии в реакции
2NO2 (г) 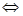 N2O4(г) равно (первое следствие закона Гесса)
N2O4(г) равно (первое следствие закона Гесса)
ΔrН0298 =∑(nj •ΔfН0298)прод - ∑(ni• ΔfН0298)исх.
Δ rН0298 =1 моль* 9660 Дж/моль – 2 моль*33800 Дж/ моль = - 57940 Дж
Изменение температуры равно
ΔrS0298 =∑ (nΔfS0298) прод. –∑(nΔfS0298)исход = 1 моль*304 Дж/моль*К -
–2 моль*234 Дж/моль*К = - 164 Дж/К
Зависимость энергии Гиббса реакции от температуры описывается уравнением
ΔG0T =ΔH0T – TΔS0T
При стандартной температуре
ΔrG0298=ΔH 0298– TΔS0298 = - 57940 Дж – (298 К*(-164 Дж/К)) = -9068 Дж/моль
Отрицательное значение энергии Гиббса реакции говорит о том, что смещении равновесия вправо (самопроизвольный процесс), т.е. в сторону образования диоксида азота.
При 0ºС (273К)
ΔrG0273 = -57940 Дж + 273К* 164 Дж/К = -13168 Дж/моль
Более высокое отрицательное значение ΔG273 по сравнению с ΔG0298 свидетельствует о том, что при 273 К равновесие еще больше смещено в сторону прямой реакции.
При 100ºС (373 К)
ΔrG373 = -57940 Дж + 373К*164 Дж/К = 3232 Дж/моль.
Положительная величина ΔG373 указывает на изменение направления реакции: равновесие смещено влево, т.е. в сторону распада димера N2O4 (реакция невозможна). Ответ: при 0ºС (273 К) ΔrG273= -13168 Дж/моль, реакция протекает самопроизвольно; при 100ºС (373 К) ΔrG373= 3232 Дж/моль, реакция невозможна.
3. Составьте термохимическое уравнение горения метана СН4 и рассчитайте объем воздуха, необходимый для сжигания 1моль метана, если известно, что при сгорании 5,6 л метана выделяется 220 кДж теплоты, содержание кислорода в воздухе равно 20%.
Решение:
СН4 + 2О2 = СО2 + 2Н2О, ∆Н<0
Находим количество вещества метана объемом 5,6 л
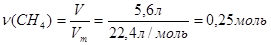
Если при сгорании СН4 количеством вещества 0,25 моль выделяется 220 кДж теплоты, то при сгорании СН4 количеством вещества 1 моль выделяется 880 кДж теплоты.
Термохимическое уравнение:
СН4 +2О2 = СО2+ 2Н2О+ 880 кДж
Из уравнения реакции видно, что на сгорание СН4 количеством вещества 1моль расходуется О2 количеством вещества 2 моль, на сгорание СН4 количеством вещества 0,25 моль расходуется х моль О2, откуда х = 0,5 моль.
Кислород количеством вещества 0,5 моль занимает объем 11,2 л.
В воздухе 20% кислорода, следовательно, объем воздуха будет равен
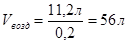
Ответ: 880 кДж, 56 л.
Задачи для самостоятельного решения
1. Рассчитайте, какая из ниже перечисленных реакций при стандартных условиях может идти самопроизвольно:
а) Fe(к) + Al2O3(к) = Al(к) + Fe2O3(к)
б) Al(к) + Fe2O3 (к)= Fe(к) + Al2O3(к)
в) CuSO4(к) + 2NH4OH(ж) = Cu(OH)2(к) + (NH4)2SO4(к)
г) Al2O3(корунд) + 3SO3 = Al2(SO4)2(к)
2. При сварке трамвайных рельсов используют термитную смесь, которую готовят, смешивая порошки алюминия и оксида железа (III) в количественном отношении 2:1. Термохимическое уравнение горения термитной смеси следующее: 2Al + Fe2O3= Al2O3 + 2Fe + 829,62 кДж. Сколько теплоты выделится при образовании: 1) 4 моль железа; 2) 1 моль железа?
3. Рассчитайте, достаточно ли теплоты, выделяющейся при сгорании 200 кг каменного угля, содержащего 82% углерода, для полного разложения 162 кг карбоната кальция, если для разложения 1 моль СаСО3 необходимо 180 кДж теплоты, а при сгорании 1 моль углерода, входящего в состав каменного угля, выделяется 402 кДж теплоты.
4. Процесс алюминотермии выражается химическим уравнением
8Al + 3 Fe3O4 = 4Al2O3 + 9Fe ΔH<0. Рассчитайте, сколько теплоты выделится при сгорании 1 кг термита.
5. Возможен ли обжиг колчедана массой 1т по следующему уравнению химической реакции 4FeS2 + 11O2 →2 Fe2O3 + 8SO2 ∆H<0
6. Вычислите тепловой эффект образования NH3 из простых веществ, при стандартном условии по тепловым эффектам реакции:
2H2 + O2 = 2H2O(ж) ΔН01 = -571, 68 кДж,
NH3 + 3O2 = 6H2O(ж) + 2N2 ΔН02 = -1530,28 кДж.
7. Стандартный тепловой эффект реакции сгорания этана равен -1560 кДж. Рассчитайте стандартную теплоту образования этана, если известно, что
ΔfН0298 (H2O)= -285,84 кДж/моль и ΔfН0298(СО2) = -396,3 кДж/моль.
8. Вычислите тепловой эффект реакции восстановления оксида железа водородом, пользуясь следующими данными.
FeO + CO = Fe + CO2 ΔН = -13,19 кДж
CO + 1/2O2 = CO2 ΔН = -283,2 кДж
2H2 + 1/2O2 = 2H2O(г) ΔН = -242 кДж
9. Протекание, какой из приведенных реакций восстановления оксида железа (III) наиболее вероятно при 298 К.
Fe2O3(k) + 3H2(г) = 2Fe(к) + 3H2O(к)
Fe2O3(k) + 3С(графит) = 2Fe(к) + 3СO(к)
Fe2O3(k) + 3СО(г) = 2Fe(к) + 3СО2(к)
10. В какой их перечисленных ниже реакций тепловой эффект ΔН0298 будет стандартной теплотой SO3(г)
а) S(г) + 3/2 O2 = SO3(г)
а) S(г) + 1/2 O2 = SO3(г)
а) S(к) + 3/2 O2 = SO3(г)
3.1.2 Химическое равновесие
При протекании химической реакции через некоторое время устанавливается равновесное состояние (химическое равновесие). Слово «равновесие» означает состояние, в котором сбалансированы все противоположно направленные на систему воздействия. Тело, находящееся в состоянии устойчивого равновесия, обнаруживает способность возвращаться в это состояние после какого-либо возмущающего воздействия.
Примером тела, находящегося в состоянии устойчивого равновесия, может служить шарик, лежащий на дне ямки. Если его толкнуть в одну или другую сторону, он вскоре снова возвращается в состояние устойчивого равновесия. В отличие от этого шарик, лежащий на краю ямки, находится в состоянии неустойчивого равновесия — достаточно ничтожного толчка, чтобы он необратимо скатился в ямку.
Оба этих примера являются примерами статического равновесия. В химии, однако, приходится сталкиваться не столько со статическими равновесиями, столько с динамическими («подвижными»). Динамическое равновесие устанавливается, когда оказываются сбалансированными два обратимых или противоположных процесса. Динамические равновесия подразделяют на физические и химические. Наиболее важными типами физических равновесий являются фазовые равновесия. Система находится в состоянии химического равновесия, если скорость прямой реакции равна скорости обратной реакции.
Например, если скорость протекания реакции (константа скорости к1)
k1
А(г) + В(пар) 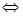 АВ(г)
АВ(г)
равна скорости обратной реакции (константа скорости k2)
k2
АВ(г) 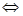 А(г) + В(пар)
А(г) + В(пар)
то система находится в динамическом равновесии. Подобные реакции называются обратимыми, а их уравнения записывают с помощью двойной стрелки:
k1
А(г) + В(пар) 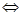 АВ(г)
АВ(г)
k2
Реакции, протекающие слева направо, называются прямой, справа налево – обратной.
Нужно подчеркнуть, что реакционная система остается в состоянии динамического равновесия лишь до тех пор, пока система остается изолированной. Изолированной называют такую систему, которая не обменивается с окружающей средой ни веществом, ни энергией.
Состояние химического равновесия обратимых процессов количественно характеризуется константой равновесия. Так, для обратимой реакции общего вида
k1
аA +bB 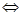 сC + dD (1.2.1)
сC + dD (1.2.1)
k2
константа равновесия К, представляющая собой отношение констант скорости прямой и обратной реакций, запишется
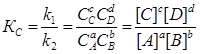 (1.2.2)
(1.2.2)
где, Кс – константа скорости реакции, зависящая от концентрации реагирующих компонентов; С i или [ i ]- равновесная молярная концентрация i -того компонента;
a , b , c , d – стехиометрические коэффициенты веществ.
В правой части уравнения (1.2.2) стоят концентрации взаимодействующих частиц, которые устанавливают при равновесии, - равновесные концентрации.
Уравнение (1.2.2) представляет собой математическое выражение закона действующих масс при химическом равновесии. Для реакции с участием газов константа равновесия выражается через парциальные давления, а не через их равновесные концентрации. В этом случае константу равновесия обозначают символом Кр.
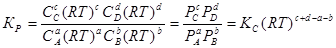
Р i - равновесные парциальные давления i-того компонента.
С i - равновесная молярная концентрация компонентов.
a , b , c , d – стехиометрические коэффициенты веществ.
Состояние химического равновесия при неименных внешних условиях теоретически может сохраняться бесконечно долго. В реальной действительности, т.е. при изменении температуры, давления или концентрации реагентов, равновесии может «сместиться» в ту или иную сторону протекания процесса.
Изменения, происходящие в системе в результате внешних воздействий, определяется принципом подвижного равновесия – принципом Ле Шателье – Брауна. При воздействие на равновесную систему, любого внешнего фактора, равновесие в системе смещается в таком направлении, чтобы уменьшить воздействие этого фактора.
1. Влияние давления на равновесие химической реакции (для реакции, проходящей в газовой фазе).
aA + bB 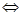 cC + dD
cC + dD
- если реакция идет с увеличением количества компонентов a + b < c + d, то повышение давления смещает равновесие химической реакции справа налево.
- если реакция идет с уменьшением количества компонентов a + b > c + d, при увеличении давления сдвиг равновесия произойдет слева направо.
- если количество компонентов одинаково a + b = c + d, то изменение давления не повлияет на положении равновесия.
2. Влияние инертного газа. Введение инертного газа подобно эффекту уменьшения давления (Ar, N2, водяной пар). Инертный газ не участвует в реакции.
3. Влияние изменения концентрации реагирующих веществ. При введение дополнительного количества вещества равновесие химической реакции сместиться в ту сторону где концентрация вещества уменьшается.
4. Влияние температуры на химическое равновесие реакции.
Если к равновесной системе подводится теплота, то в системе происходят изменения, чтобы ослабить это воздействие, т.е. процессы с поглощением теплоты. При экзотермических реакциях снижение температуру сместит равновесие слева направо, а при эндотермических реакциях повышение температуры сместит равновесие справа налево.
Зависимость Кр от температуры – уравнение Вант – Гоффа.
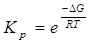 ;
; 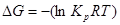 ;
;
( 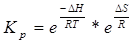 ); lnkT 1 – lnkT 2 =
); lnkT 1 – lnkT 2 = 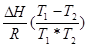
Примеры решения задач
1. Реакция соединения азота и водорода обратима и протекает по уравнению
N2 + 3Н2 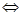 2NН3. При состоянии равновесия концентрации участвующих в ней веществ были: [N2] = 0,01 моль/л, [Н2] = 2,0 моль/л, [NH3] = 0,40 моль/л. Вычислить константу равновесия и исходные концентрации азота и водорода.
2NН3. При состоянии равновесия концентрации участвующих в ней веществ были: [N2] = 0,01 моль/л, [Н2] = 2,0 моль/л, [NH3] = 0,40 моль/л. Вычислить константу равновесия и исходные концентрации азота и водорода.
Решение:
Для приведенной реакции
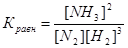
Подставляя значение равновесных концентраций, получим
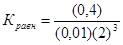 = 2
= 2
Согласно уравнению реакции из 1 моль азота и 3 моль водорода получаем
2 моль аммиака, следовательно, на образование 0,4 моль аммиака пошло
0,2 моль азота и 0,6 моль водорода. Таким образом, исходные концентрации будут [N2] = 0,01 моль/л + 0,2 моль/л = 0,21 (моль/л),
[H2] = 2,0 моль/л + 0,6 моль/л = 2,6 (моль/л).
Ответ: Кравн = 2; С0 (N2) = 0,21 моль/л и С0 (Н2) = 2,6 моль/л.
2. Один моль смеси пропена с водородом, имеющей плотность по водороду 15, нагрели в замкнутом сосуде с платиновым катализатором при 320°С, при этом давление в сосуде уменьшилось на 25%. Рассчитайте выход реакции в процентах от теоретического. На сколько процентов уменьшится давление в сосуде, если для проведения эксперимента в тех же условиях использовать 1 моль смеси тех же газов, имеющей плотность по водороду 16?
Решение:
С3Н6 + Н2 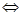 С3Н8
С3Н8
1) Пусть ν(C3H6) = х, ν(H2) =1-x, тогда масса смеси равна
42х + 2(1 - х) = 2 • 15 = 30,
откуда х = 0,7 моль, т. е. ν(C3H6) = 0,7 моль, ν(H2) = 0,3 моль.
Давление уменьшилось на 25% при неизменных температуре и объеме за счет уменьшения на 25% числа молей в результате реакции. Пусть у моль Н2 вступило в реакцию, тогда после реакции осталось:
ν(C3H6) = 0,7 - у, ν(H2) = 0,3 – у, ν(C3H8) = у,
νо6щ = 0.75 =(0,7 - у) + (0,3 - у) + у, откуда y = 0,25 моль.
Теоретически могло образоваться 0,3 моль С3Н8 (H2 — в недостатке), поэтому выход равен 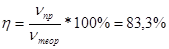 . Константа равновесия при данных условиях равна
. Константа равновесия при данных условиях равна
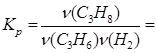
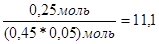
2) Пусть во втором случае ν(C3H6) = a моль, ν(H2) = (1 – а) моль, тогда масса смеси равна 42а + 2(1 - а) = 2 • 16 = 32, откуда, а= 0,75, т. е. ν(C3H6) = 0,75, ν(H2) = 0,25. Пусть в реакцию вступило b моль Н2. Это число можно найти из условия неизменности константы равновесия
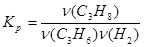 =
= 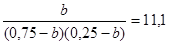
Из двух корней данного квадратного уравнения выбираем корень, удовлетворяющий условию 0 < b < 0,25, т. е. b = 0,214 моль
Общее число молей после реакции равно
νoбщ =((0,75 - 0,214) + (0,25 - 0,214) + 0,214 - 0,786) моль, т. е. оно уменьшилось на 21,4% по сравнению с исходным количеством (1 моль). Давление пропорционально числу молей, поэтому оно также уменьшилось на 21,4%.
Ответ: выход С3Н8 — 83,3%; давление уменьшится на 21,4%.
Задачи для самостоятельного решения
1. В реакции между раскаленным железом и паром
3Fe(тв) + 4Н2О(г) 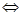 Fe3O4(тв)+4Н2(г), при достижении равновесия парциальные давления водорода и пара равны 3,2 и 2,4 кПа соответственно. Рассчитайте константу равновесия.
Fe3O4(тв)+4Н2(г), при достижении равновесия парциальные давления водорода и пара равны 3,2 и 2,4 кПа соответственно. Рассчитайте константу равновесия.
2. Вычислите константы равновесия Кр КС газовой реакции
СО + Cl2 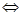 СОCl2, состав газовой смеси при равновесии был следующим (% по объему): СО=2,4, Cl2 =12,6, СОCl2 =85,0, а общее давление смеси при 20С составляло 1,033*105 Па. Вычислите ΔG реакции.
СОCl2, состав газовой смеси при равновесии был следующим (% по объему): СО=2,4, Cl2 =12,6, СОCl2 =85,0, а общее давление смеси при 20С составляло 1,033*105 Па. Вычислите ΔG реакции.
3. Рассчитайте константу равновесия при некоторой заданной данной температуре для обратимой реакции СО + Н2О 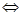 СО2 + Н2, учитывая, что в состоянии равновесия концентрации участвующих в реакции веществ были равны [СО] = 0,16 моль/л, [Н2О] = 0,32 моль/л, [СО2] = 0,32 моль/л, [Н2] = 0,32 моль/л.
СО2 + Н2, учитывая, что в состоянии равновесия концентрации участвующих в реакции веществ были равны [СО] = 0,16 моль/л, [Н2О] = 0,32 моль/л, [СО2] = 0,32 моль/л, [Н2] = 0,32 моль/л.
4. В стальном резервуаре находятся карбонат кальция и воздух под давлением 1 атм. при температуре 27°С. Резервуар нагревают до 800°С и дожидаются установления равновесия. Вычислите константу равновесия Кр реакции CaCO3 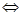 СаО + СО2 при 800°С, если известно, что равновесное давление газа в резервуаре при этой температуре равно 3,82 атм., а при 27°С СаСО3 не разлагается.
СаО + СО2 при 800°С, если известно, что равновесное давление газа в резервуаре при этой температуре равно 3,82 атм., а при 27°С СаСО3 не разлагается.
5. При постоянной температуре в гомогенной системе А + В = 2С установилось равновесие с равновесными концентрациями [А]=0,8 моль/ль, [В]=0,6 моль/л, [С]=1,2 моль/л. определите новые равновесные концентрации, если в систему дополнительно ввели 0,6 моль/л вещества В.
6. Как можно обосновать оптимальные условия промышленного синтеза аммиака с высоким выходом на основе термохимического уравнения реакции
N2 + ЗН2 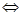 2NH3 + 491,8 кДж и с учетом того, что при низких температурах скорость прямой реакции очень мала?
2NH3 + 491,8 кДж и с учетом того, что при низких температурах скорость прямой реакции очень мала?
7. Вычислите константу равновесия ниже приведенных реакции, протекающей при стандартных условиях и при 400К.
а) Na2O(к) + CO2(г) → Na2CO3(к)
б) N2O4(г) = 2NO2(г)
8. Уравнение реакции окисления хлорида водорода
4НСl (г) + O2(г) = 2H2O(г) + 2Cl2(г) Вычислите константу равновесия этой реакции при Т=500К. Предположите способы увеличения концентрации хлора в равновесной смеси.
9. При смешении 2 моль уксусной кислоты и 2 моль этилового спирта в результате реакции СН3СООН + С2Н5ОН = СН3СООС2Н5 + Н2О к моменту наступления равновесия осталось 0,5 моль СН3СООН и С2Н5ОН, а также некоторое количество эфира и воды. Определите состав равновесной смеси, если смешивают по 3 моль СН3СООН и С2Н5ОН при той же температуре.
10. Вычислить начальные концентрации веществ в обратимой реакции
2СO +О2 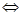 2СО2 и константу равновесия, если равновесные концентрации составляют [СО]=0,44 моль/л, [О2]=0,12 моль/л, [СО2] =0,18 моль/л.
2СО2 и константу равновесия, если равновесные концентрации составляют [СО]=0,44 моль/л, [О2]=0,12 моль/л, [СО2] =0,18 моль/л.
Химическая кинетика
Это раздел физической химии, изучающей скорость химических реакций, а в более широком смысле – закономерности их протекания.
Термин скорость реакции означает скорость, с которой образуются продукты, либо скорость, с которой расходуются агенты при протекании химической реакции. Химические реакции происходят с самыми разными скоростями. Со скоростью химических реакций связаны представления о превращении веществ, а также экономическая эффективность их получения в промышленных масштабах. Основным понятием в химической кинетике является понятие о скорости реакции, которая определяется изменением количества вещества реагентов (или продуктов реакции) в единицу времени в единице объема. Если при неизменном объеме и температуре концентрация одного из реагирующих веществ уменьшилась (или увеличилась) от значения с1 до значения с2 за промежуток времени от t1 до t2, то средняя скорость реакции составит
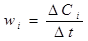 (1.3.1)
(1.3.1)
где D С i – изменения концентрации i-того компонента, моль/м3 или моль/л,
wi - скорость реакции, (моль/(л • с) или моль/м3 *с). Уравнение (1.3.1) подходит для реакций протекающих в гомогенном реакционном пространстве.
Если реакция протекает в гетерогенном пространстве, то выражение для скорости реакции по данному веществу i имеет вид (моль/м3 *с).
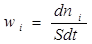 (1.3.2)
(1.3.2)
dni – изменение количества i-того компонента, моль; S- площадь, м2;
dt – изменение времени, с.
I . Продукты реакции или промежуточные соединения образуются при взаимодействии частиц в элементарном химическом акте. Число частиц в элементарном химическом акте называется молекулярностью реакции. Элементарные реакции бывают трех типов:
- мономолекулярные А ® Р1+ Р2 + …
- бимолекулярные А + В ® Р1+ Р2 +...
- тримолекулярные 2А + В ® Р1+ Р2 + … 3А ® Р1+ Р2 + …,
А + В + С ® Р1+ Р2 + …
Четырехмолекулярных реакций не бывает, т.к. вероятность одновременного столкновения четырех молекул ничтожно мала.
Скорость реакции можно измерить, определяя количество реагента или продукта во времени. Скорость реакции зависит от природы реагирующих веществ и от условий, в которых реакция протекает. Важнейшими из них являются концентрация, температура и присутствие катализатора.
Рассмотрим реакцию между веществами А и В, протекающую по схеме
аА + вВ + …. → сС + dD + …
Скорость реакции зависит от концентраций А и В, однако заранее нельзя утверждать, что она прямо пропорциональна концентрации того или другого. Зависимость скорости химической реакции от концентрации реагирующих веществ выражается основным законом химической кинетики — законом действующих масс: скорость элементарной химической реакции прямо пропорциональна произведению концентрации реагирующих веществ в степенях, равных стехиометрическим коэффициентам в уравнении реакции.
Для элементарной реакции
n1А + n2В ® n3С + n4Е + …
w= 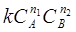 или w = k [A]nA [B]n В. (1.3.3)
или w = k [A]nA [B]n В. (1.3.3)
Выражение такого типа называют кинетическим уравнением, где k - константа скорости (не зависит от концентрации реагирующих реагентов и времени); CA , CB – текущие концентрации реагирующих веществ; n 1, n 2 - некоторые числа, которые называются порядком реакции по веществам А и В соответственно. Порядок реакции совпадает со стехиометрическими показателями элементарной реакции. Порядок реакции n – сумма показателей кинетических степеней в химическом уравнении реакции. Сумма показателей степеней n 1 + n2 = n называется общим порядком реакции. Для элементарной реакции общий порядок равен молекулярности, а порядок по веществам равны коэффициентам в уравнении реакции. Порядок реакции по i-тому компоненту не равен его стехиометрическому коэффициенту в химическом уравнении сложной реакции.
1. Реакции нулевого порядка. Скорость этих реакций не зависит от концентрации реагирующего вещества n=0. Из уравнений 1.3.1 и 1.3.3 получим следующее
w = k или 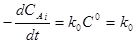 . (1.3.4)
. (1.3.4)
Интегрируя выражение (1.3.4) получаем:
CA,t=CA,0 – k0t, k0t = CA,0 – CA,t (1.3.5)
Введем понятие время полупревращения t 1/2 – это время, в течение которого превращается половина исходного вещества.
Для реакции нулевого порядка в уравнение 1.3.5 подставим 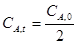
t 1/2 = 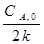
2. Реакции первого порядка. Для реакции первого порядка n=1 типа
А ® Р1+ Р2 + …, скорость прямо пропорциональна концентрации вещества А:
w = 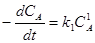 ;
; 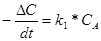
lnCA , t = lnCA ,0 – kt
С=СА, t = CA ,0 e - kt
t 1/2= 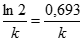
3. Реакции второго порядка. Для реакции второго порядка n=2 типа
А + В ® Р1+ Р2 +..., если СА,0=СВ,0 кинетическое уравнение имеет вид
w= 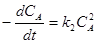 ;
; 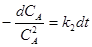
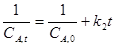
t1/2 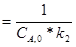

Для реакции второго порядка типа А + В ® Р + … если СА,0 ¹ СВ,0 кинетическое уравнение имеет вид
w = 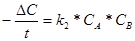
Периоды полураспада вещества А и В, если СА,0 ¹ СВ,0, различны,
т.е. t 1|2 ( A ) ¹ t 1|2 ( B ).
4. Реакции третьего порядка. Кинетика реакции третьего порядка n=3 типа
2А + В ® Р1+ Р2 + … 3А ® Р1+ Р2 + …, А + В + С ® Р1+ Р2 + …
при равных начальных концентрациях описывается уравнением
w = 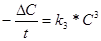
t 1|2 = 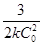
Для реакции А + В + С ® Р + …,если СА,0 ¹ СВ,0¹СС,0 кинетическое уравнение примет вид
w= 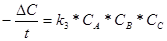
II . Выражение (1.3.1) записано для фиксированной температуры. Для приближенной оценки изменения скорости широко используется эмпирическое правило Вант-Гоффа, в соответствии с которым скорость химической реакции становится в 2-4 раза больше при повышении температуры на каждые 10°C. В математической форме зависимость изменения скорости реакции от температуры выражается уравнением
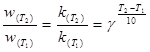 (1.3.4)
(1.3.4)
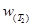 — скорость реакции при повышенной температуре Т2,
— скорость реакции при повышенной температуре Т2,
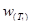 - скорость реакции при начальной температуре Т1; γ —температурный коэффициент скорости, показывающий, во сколько раз увеличится скорость реакции при повышении температуры на 10°С (2-4). Это позволяет предположить, что между скоростью реакции и температурой должна существовать экспоненциальная зависимость. Точное соотношение между скоростью реакции и температурой установил шведский химик Аррениус в 1899 г. Это соотношение, получившее название уравнение Аррениуса, имеет вид
- скорость реакции при начальной температуре Т1; γ —температурный коэффициент скорости, показывающий, во сколько раз увеличится скорость реакции при повышении температуры на 10°С (2-4). Это позволяет предположить, что между скоростью реакции и температурой должна существовать экспоненциальная зависимость. Точное соотношение между скоростью реакции и температурой установил шведский химик Аррениус в 1899 г. Это соотношение, получившее название уравнение Аррениуса, имеет вид
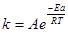 (1.3.5)
(1.3.5)
где k – константа скорости реакции; А — постоянная, характеризующая каждую конкретную реакцию (константа Аррениуса, или «предэкспонента»);
Еa — постоянная, характерная для каждой реакции и называемая энергией активации, Дж; R — универсальная газовая постоянная Дж/(К*моль);
Т — температура, К.
Подчеркнем, что это уравнение связывает температуру не со скоростью реакции, а с константой скорости. Приведем уравнение Аррениуса для двух температур
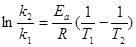
III . Одно из наиболее сильных средств влияния на скорость реакции — присутствие в реагирующей системе катализатора - вещества, которое усиливают (а иногда и понижают - тогда его называют ингибитором) скорость химической реакции, но само не расходуется в этом процессе.
Примеры решения задач
1. Во сколько раз увеличится скорость химической реакции при повышении температуры с 0 до 50°С, принимая температурный коэффициент скорости равным трем?
Решение:
Дата: 2019-07-30, просмотров: 575.