Одна из главных задач химической науки и промышленности - получение необходимых человеку веществ (продуктов, материалов). Поэтому большинство учебных химических задач снизано с расчетами по уравнению химической реакции, которую в общем виде можно представить так:
аА+ вВ 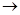 cC+dD
cC+dD
где A, В, С, D - условные обозначения формул различных веществ;
а, в, с, d — стехиометрические коэффициенты.
Расчет по уравнению реакции наиболее прост лишь в идеальном случае, когда реагенты абсолютно чистые, взяты в строго стехиометрических отношениях, потерь при реакции нет, т.е. выход продукта составляет 100%. Практически эти условия не выполняются. Как правило, исходные вещества содержат примеси или взяты в виде растворов; обычно одно из веществ, вступающих в реакцию (наиболее доступное, дешевое, берут в избытке и, наконец, реальный выход продуктов всегда меньше 100%.)
Итак, химические задачи делят на:
1) Расчетные
2) Качественные
Расчетные задачи условно делятся на две группы:
1) Задачи, решаемые с использованием химической формулы вещества или на вывод формулы.
2) Задачи, для решения которых используют уравнения химических реакций.
3) Задачи, для решения которых используют только математические формулы.
Первая группа задач включает расчеты по определению массы чистого вещества в смеси (растворе) по известной массовой доле его (или процентному содержанию); вычисление массовой доли (или процента) элементов по формулам веществ (прямая и обратная задачи).
Ко второй группе задач относятся вычисления по химическим уравнениям массы, объема и количества продуктов реакции или взаимодействующих веществ в различных единицах измерения. При этом учитывают произвольное соотношение компонентов, т. е. наличие избытка одного из реагирующих веществ; практический выход продукта реакции; наличие примесей в исходных веществах или продуктах реакции.
На уроках обобщения знаний о химических производствах составляются задачи с производственным содержанием. Совместно с учащимися определяем, какие особенности таких задач следует при этом учитывать:
1) условия процесса (концентрация, давление, температура);
2) возможность протекания процесса;
3) кинетику и равновесие реакций;
4) состав сырья (наличие примесей, необходимость очистки);
5) выход продукта (потери в процессе очистки; обратимость процесса; побочные реакции; циркуляция);
6) использование энергии экзотермических процессов;
7) утилизация побочных продуктов и отходов производства.
8) экологический аспект;
9) технико-экономические показатели химических производств;
10) использование электрической энергии. [54]
При составлении методического пособия для решения задач по химической технологии мы условно выделили несколько разделов задач по их химической тематике:
I. Общие вопросы химической технологии.
1. термохимия.
2. химическая кинетика.
3. химическое равновесие.
II. Технико-экономические показатели химических производств.
III. Задачи с экологическим содержанием.
IV. Производство неорганических соединений.
1. металлургия.
2. электрохимические производства.
V. Производство органических соединений.
VI.Творческие и изобретательские задачи.
Каждый раздел задач сопровождается методической частью, где приводятся основные теоретические аспекты темы, законы и формулы для математических расчетов. Далее рассматриваются методические рекомендации по решению задач, конкретные примеры решения типичных и наиболее сложных задач, а также задачи для самостоятельного решения. Эти задачи могут быть использованы на практических занятиях, для проведения коллоквиумов, индивидуального собеседования при защите лабораторных работ, а также в средней общеобразовательной школе при изучении факультативного курса по химии.
3.1 Общие вопросы химической технологии
Термохимия
Термохимия — учение о тепловых эффектах химических реакций. Для решения задач по термохимии необходимо знать такие понятия, как тепловой эффект реакции, стандартная тепловой эффект образования вещества, стандартная тепловой эффект сгорания химического соединения, закон Гесса и следствия из него, возможность самопроизвольного протекания реакции, зависимость энергии Гиббса от температуры. Наиболее важным понятием химической энергетики является тепловой эффект химической реакции. Данные о тепловых эффектах применяются для определения строения и реакционной способности соединений, энергии межатомных и межмолекулярных связей, используются в технологических и технических расчетах. В основе термохимических расчетов по уравнениям реакций лежит закон сохранения и превращения энергии, или первое начало термодинамики. Сущность его состоит в том, что при всех превращениях энергия не возникает и не исчезает, а одни ее виды переходят в эквивалентные количества других видов. Количество выделившейся (поглощенной) теплоты в результате химической реакции называется тепловым эффектом реакции Q (при p-const QP или V-const QV) (измеряется в кДж). По тепловому эффекту химические реакции подразделяются на экзотермические (с выделением теплоты (+Q)) и эндотермические (с поглощением теплоты (-Q)). Существует величина обратная тепловому эффекту (записывается с противоположным знаком). Она характеризует внутреннюю энергию вещества и называется энтальпией (∆Н). Изменение энтальпии измеряют в кДж/моль, т.е. это то количество теплоты, которое выделяется или поглощается при образовании 1 моль вещества из простых веществ. С термодинамической точки зрения принимают, что тепловой эффект при постоянном давлении и температуре равен изменению энтальпии ΔН. Передачу энергии при этом рассматривают как бы со стороны самой реакционной системы. Если система отдала энергию во внешнюю среду, величина ΔН считается отрицательной ΔН<0, если реакционная система получила энергию за счет внешней среды — величину ΔН считают положительной ΔН>0. Вычисление теплоты реакции по теплотам образования участвующих в ней веществ, производится на основании закона Гесса.
Закон Гесса: Тепловой эффект химической реакции при постоянном давлении и объеме не зависит от пути реакции (т.е. от промежуточных стадий), а определяется начальным и конечным состоянием системы (т.е. состоянием исходных веществ и продуктов реакции (газ, жид., тв.)).
ΔrН0298 – стандартная энтальпия реакции (reaction), тепловой эффект реакции.
ΔfН0298 – стандартная энтальпия образования (formation) 1 моль вещества из простых веществ в стандартных условиях (Т=298К или 25С, Р=1 атм.), на которые указывает знак «0», (кДж/моль).
ΔсН0298 – стандартная энтальпия сгорания (combustion) 1 моль вещества (до образования СО2, Н2О, и др. продуктов), (кДж/моль).
Следствие 1 из закона Гесса:
Тепловой эффект химической реакции равен разности между алгебраической суммой теплот образования продуктов реакции и алгебраической суммой теплот образования исходных веществ
ΔrН0298 =∑(n j •ΔfН0298)прод - ∑(n i • ΔfН0298)исх.
где, n j и n i – количество вещества продуктов реакции и исходных веществ соответственно (численно равно коэффициенту в уравнении реакции), (моль).
Следствие 2 из закона Гесса:
Тепловой эффект химической реакции равен сумме теплот сгорания исходных веществ минус сумма теплот сгорания продуктов реакции
ΔrН0298 =∑(n i • ΔсН0298) - ∑(n j • ΔсН0298)
где, n i и n j - количество вещества исходных веществ и продуктов реакции соответственно (численно равно коэффициенту в уравнении реакции), (моль).
В химических реакциях может одновременно изменяется и энергия системы и ее энтропия, поэтому реакция протекает в том направлении, в котором общая суммарная движущая сила реакции уменьшается. Если реакция происходит при постоянном температуре и давлении, то общая движущая сила реакции называется энергией Гиббса (ΔG0) и направление реакции определяется ее изменением.
Дата: 2019-07-30, просмотров: 320.