Жесткость воды (Ж) выражается суммой миллиэквивалентов ионов кальция и магния, содержащихся в одном литре воды (ммоль/л). Один миллимоль жесткости отвечает содержанию 20,04 мг/л Ca2+ или 12,16 мг/л Mg2+.
 Ж =
Ж = 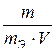 , (1)
, (1)
 где m - масса вещества, обусловливающего жесткость воды или
где m - масса вещества, обусловливающего жесткость воды или
применяемого для устранения жесткости, мг;
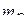 - молярная масса эквивалента этого вещества, г/моль;
- молярная масса эквивалента этого вещества, г/моль;
V – объем воды, л.
Различают карбонатную (временную) и некарбонатную (постоянную) жесткость. Карбонатная жесткость (Жк) обусловлена содержанием в воде гидрокарбонатов кальция и магния. Постоянная жесткость (Жп) представляет собой разность между общей (Ж о) и карбонатной жесткостью. Постоянная жесткость вызывается присутствием в воде хлоридов, сульфатов и других растворимых солей кальция и магния.
Соли жесткости образуют плотные осадки (накипь) на стенках котлов, трубопроводов и другого оборудования, существенно снижая эффективность его работы. Поэтому используемая в производстве вода предварительно умягчается. Умягчением называют процесс уменьшения жесткости, т.е. удаление из воды ионов кальция и магния.
Карбонатная жесткость уменьшается при простом кипячении воды (поэтому ее называют временной):
Ca(HCO3)2 ® ¯CaCO3 + H2O + CO2;
Mg(HCO3)2 ® ¯Mg(OH)2 + 2 CO2.
На практике этот метод применяют редко. Обычно для осаждения ионов кальция и магния используют соответствующие химические реагенты: гашеную известь – Ca(OH)2 и соду – Na2CO3.
Ca(HCO3)2 + Ca(OH)2 ® 2 ¯CaCO3 + 2 H2O;
Mg(HCO3)2 + 2 Ca(OH)2® ¯Mg(OH)2 + 2 ¯CaCO3 + 2 H2O.
При введении гашеной извести устраняется только карбонатная жесткость. Количество извести должно точно соответствовать содержанию гидрокарбонатов, так как избыток Ca(OH)2 приведет к увеличению содержания ионов кальция, т.е. к возрастанию жесткости.
Для уменьшения всех видов жесткости применяют смесь соды и извести:
CaCl2 + Na2CO3 ® ¯CaCO3 = 2 NaCl;
MgSO4 + Ca(OH)2 ® ¯Mg(OH)2 + CaSO4;
Ca(HCO3)2 + Ca(OH)2 ® 2 ¯CaCO3 + 2 H2O;
Для устранения общей жесткости можно применять одну только соду. Но преимущественно используют смесь соды с известью, что является более экономичным, так как сода значительно дороже извести.
Наиболее эффективным способом устранения жесткости воды является метод ионного обмена. Воду пропускают через колонки, заполненные слоем ионита. Иониты представляют собой твердые синтетические высокомолекулярные соединения, у которых ионы одного знака закреплены на полимерной матрице, а ионы противоположного знака способны переходить в раствор и замещаться на другие ионы того же знака. В зависимости от заряда ионов, переходящих в раствор, различают катиониты и аниониты. Для устранения жесткости, т. е. для удаления из воды ионов Ca2+ и Mg2+, используют катиониты (Na+-kt или H+-kt). Ионы кальция и магния обмениваются на ионы натрия или водорода. При использовании Н+-катионита снижается не только жесткость. но и солесодержание. Однако может повыситься коррозионная агрессивность воды за счет понижения рН. Поэтому для обессоливания применяют метод последовательного пропускания воды через Н+-катионит и ОН—анионит.
Отработанный катионит легко подвергается регенерации растворами солей натрия (Na+-kt) или кислот(Н+-kt).
Пример 1. Вычислить жесткость воды, если известно, что в 500 л содержится 202,5 г Ca(HCO3)2.
Решение. Найдем молярную массу эквивалента соли Ca(HCO3)2:
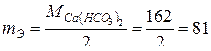 г/моль.
г/моль.
Вычисляем жесткость воды по формуле (1):
Ж =  ммоль/л.
ммоль/л.
Пример 2. Сколько граммов CaSO4 содержится в 1 м3 воды, если жесткость, обусловленная присутствием этой соли, равна 4 ммоль?
Решение. Молярная масса CaSO4 равна 136,14 г/моль; молярная масса эквивалента составляет 136,14/2 = 68,07 г/моль. Применяем формулу (1):
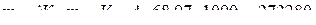 мг = 272,280г.
мг = 272,280г.
В 1 м3 воды жесткостью 4 ммоль содержится 272,280 г CaSO4.
Пример 3. Какую массу соды надо добавить к 500 л воды, чтобы устранить ее жесткость, равную 5 ммоль?
Решение. В 500 л воды содержится 500 ´ 5 = 2500 моль солей, обусловливающих жесткость воды. Для устранения жесткости следует прибавить 2500 ´53 = 132500 мг = 132,5 г соды (53 г/моль – молярная масса эквивалента Na2CO3).
Или по формуле (1): 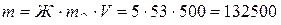 мг = 132,5 г.
мг = 132,5 г.
Пример 4. Вычислите карбонатную жесткость воды, зная, что на титрование 100см3 этой воды, содержащей гидрокарбонат кальция, потребовалось 6,25 см3 0,08 н. Раствора HCl.
Решение. В соответствии с законом эквивалентов:
VHCl∙NHCl = VH  O∙NH
O∙NH  O.
O.
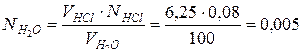 н.
н.
Таким образом, в 1 л исследуемой воды содержится 0,005 моль эквивалентов гидрокарбоната кальция или 5 ммоль Ca2+-ионов. Карбонатная жесткость воды Жк = 5 ммоль/л.
КОНТРОЛЬНЫЕ ВОПРОСЫ
301. Какую массу Na3PO4 надо прибавить к 500 л воды, чтобы устранить жесткость, равную 5 ммоль/л?
Ответ: 136,6 г.
302. Какие соли обусловливают жесткость природной воды? Какую жесткость называют карбонатной, некарбонатной? Как можно устранить карбонатную, некарбонатную жесткость? Напишите уравнения соответствующих реакций. Чему равна жесткость воды, в 100 л которой содержится 14, 632 г гидрокарбоната магния?
Ответ: 2 ммоль/л.
303. Вычислите карбонатную жесткость воды, зная, что для реакции с гидрокарбонатом кальция, содержащимся в 200 см3 воды, требуется 15 см3 0,08 н. раствора HCl.
Ответ: 6 ммоль/л.
304. В 1 л воды содержится 36,47 мг ионов магния и 50,1 мг ионов кальция. Чему равна жесткость этой воды?
Ответ: 5,5 ммоль/л.
305. Какую массу карбоната натрия надо прибавить к 400 л воды, чтобы устранить жесткость, равную 3 ммоль/л?
Ответ: 63,6 г.
306. Вода, содержащая только сульфат магния, имеет жесткость, равную 7 ммоль/л. Какая масса сульфата магния содержится в 300 л этой воды?
Ответ: 126,3 г.
307. Вычислите жесткость воды, зная, что в 600 л ее содержится 65,7 г гидрокарбоната магния и 61.2 г сульфата кальция.
Ответ: 3 ммоль/л.
308. В 220 л воды содержится 11 г сульфата магния. Чему равна жесткость этой воды?
Ответ: 0,83 ммоль/л.
309. Жесткость воды, в которой растворен только гидрокарбонат кальция, равна 4 ммоль/л. Какой объем 0,1 н. Раствора HCl потребуется для реакции с гидрокарбонатом кальция, содержащимся в 75 см3 этой воды?
Ответ: 3 см3.
310. В 1 м3 воды содержится 140 г сульфата магния. Вычислите жесткость этой воды.
Ответ: 2,33 ммоль/л.
311. Вода, содержащая только гидрокарбонат магния, имеет жесткость 3,5 ммоль/л. Какая масса гидрокарбоната магния содержится в 200 л этой воды?
Ответ: 51,1 г.
312. К 1 м3 жесткой воды прибавили 132,5 г карбоната натрия. На сколько понизилась жесткость?
Ответ: на 2, 5 ммоль/л.
313. Чему равна жесткость воды, если для ее устранения к 50 л воды потребовалось прибавить 21, 2 г карбоната натрия?
Ответ: 8 ммоль/л.
314. Какая масса CaSO4 содержится в 200 л воды, если жесткость, обусловливаемая этой солью, равна 8 ммоль/л.
Ответ:108, 9г.
315. Вода, содержащая только гидрокарбонат кальция, имеет жесткость 9 ммоль/л. Какая масса гидрокарбоната кальция содержится в 500 л воды?
Ответ:364,5 г.
316. Какие ионы надо удалить из природной воды, чтобы сделать ее мягкой? Введением каких ионов можно умягчить воду? Составьте уравнения соответствующих реакций. Какую массу Ca(OH)2 надо прибавить к 2,5 л воды, чтобы устранить ее жесткость, равную 4,43ммоль/л?
Ответ: 0,406 г.
317. Какую массу карбоната натрия надо прибавить к 0,1 м3 воды, чтобы устранить жесткость, равную 4 ммоль/л?
Ответ: 21,2 г.
318. К 100 л жесткой воды прибавили 12,95 г гидроксида кальция. На сколько понизилась карбонатная жесткость?
Ответ: на 3,5 ммоль/л.
319. Чему равна карбонатная жесткость воды, если в 1 л ее содержится 0,292 г гидрокарбоната магния и 0,2025 г гидрокарбоната кальция?
Ответ: 6,5 ммоль/л.
320. Какую массу гидроксида кальция надо прибавить к 275 л воды, чтобы устранить ее карбонатную жесткость, равную 5,5 ммоль/л?
Ответ: 55,96 г.
ВАРИАНТЫ КОНТРОЛЬНЫХ ЗАДАНИЙ
| № вари- анта | Номера задач, относящихся к данному варианту | |||||||||||||||
| 1 | 1 | 21 | 41 | 61 | 81 | 101 | 121 | 141 | 161 | 181 | 201 | 221 | 241 | 261 | 281 | 301 |
| 2 | 2 | 22 | 42 | 62 | 82 | 102 | 122 | 142 | 162 | 182 | 202 | 222 | 242 | 262 | 282 | 302 |
| 3 | 3 | 23 | 43 | 63 | 83 | 103 | 123 | 143 | 163 | 183 | 203 | 223 | 243 | 263 | 283 | 303 |
| 4 | 4 | 24 | 44 | 64 | 84 | 104 | 124 | 144 | 164 | 184 | 204 | 224 | 244 | 264 | 284 | 304 |
| 5 | 5 | 25 | 45 | 65 | 85 | 105 | 125 | 145 | 165 | 185 | 205 | 225 | 245 | 265 | 285 | 305 |
| 6 | 6 | 26 | 46 | 66 | 86 | 106 | 126 | 146 | 166 | 186 | 206 | 226 | 246 | 266 | 286 | 306 |
| 7 | 7 | 27 | 47 | 67 | 87 | 107 | 127 | 147 | 167 | 187 | 207 | 227 | 247 | 267 | 287 | 307 |
| 8 | 8 | 28 | 48 | 68 | 88 | 108 | 128 | 148 | 168 | 188 | 208 | 228 | 248 | 268 | 288 | 308 |
| 9 | 9 | 29 | 49 | 69 | 89 | 109 | 129 | 149 | 169 | 189 | 209 | 229 | 249 | 269 | 289 | 309 |
| 10 | 10 | 30 | 50 | 70 | 90 | 110 | 130 | 150 | 170 | 190 | 210 | 230 | 250 | 270 | 290 | 310 |
| 11 | 11 | 31 | 51 | 71 | 91 | 111 | 131 | 151 | 171 | 191 | 211 | 231 | 251 | 271 | 291 | 311 |
| 12 | 12 | 32 | 52 | 72 | 92 | 112 | 132 | 152 | 172 | 192 | 212 | 232 | 252 | 272 | 292 | 312 |
| 13 | 13 | 33 | 53 | 73 | 93 | 113 | 133 | 153 | 173 | 193 | 213 | 233 | 253 | 273 | 293 | 313 |
| 14 | 14 | 34 | 54 | 74 | 94 | 114 | 134 | 154 | 174 | 194 | 214 | 234 | 254 | 274 | 294 | 314 |
| 15 | 15 | 35 | 55 | 75 | 95 | 115 | 135 | 155 | 175 | 195 | 215 | 235 | 255 | 275 | 295 | 315 |
| 16 | 16 | 36 | 56 | 76 | 96 | 116 | 136 | 156 | 176 | 196 | 216 | 236 | 256 | 276 | 296 | 316 |
| 17 | 17 | 37 | 57 | 77 | 97 | 117 | 137 | 157 | 177 | 197 | 217 | 237 | 257 | 277 | 297 | 317 |
| 18 | 18 | 38 | 58 | 78 | 98 | 118 | 138 | 158 | 178 | 198 | 218 | 238 | 258 | 278 | 298 | 318 |
| 19 | 19 | 39 | 59 | 79 | 99 | 119 | 139 | 159 | 179 | 199 | 219 | 239 | 259 | 279 | 299 | 319 |
| 20 | 20 | 40 | 60 | 80 | 100 | 120 | 140 | 160 | 180 | 200 | 220 | 240 | 260 | 280 | 300 | 320 |
| 21 | 1 | 22 | 43 | 64 | 85 | 106 | 127 | 148 | 169 | 190 | 211 | 222 | 243 | 264 | 285 | 306 |
| 22 | 2 | 23 | 44 | 65 | 86 | 107 | 128 | 149 | 170 | 191 | 212 | 223 | 244 | 265 | 286 | 307 |
| 23 | 3 | 24 | 45 | 66 | 87 | 108 | 129 | 150 | 171 | 192 | 213 | 224 | 245 | 266 | 287 | 308 |
| 24 | 4 | 25 | 46 | 67 | 88 | 109 | 130 | 151 | 172 | 193 | 214 | 225 | 246 | 267 | 288 | 309 |
| 25 | 5 | 26 | 47 | 68 | 89 | 110 | 131 | 152 | 173 | 194 | 215 | 226 | 247 | 268 | 289 | 310 |
| 26 | 6 | 27 | 48 | 69 | 90 | 111 | 132 | 153 | 174 | 195 | 216 | 227 | 248 | 269 | 290 | 311 |
| 27 | 7 | 28 | 49 | 70 | 91 | 112 | 133 | 154 | 175 | 196 | 217 | 228 | 249 | 270 | 291 | 312 |
| 28 | 8 | 29 | 50 | 71 | 92 | 113 | 134 | 155 | 176 | 197 | 218 | 229 | 250 | 271 | 292 | 313 |
| 29 | 9 | 30 | 51 | 72 | 93 | 114 | 135 | 156 | 177 | 198 | 219 | 230 | 251 | 272 | 293 | 314 |
| 30 | 10 | 31 | 52 | 73 | 94 | 115 | 136 | 157 | 178 | 199 | 220 | 231 | 252 | 273 | 294 | 315 |
| 31 | 11 | 32 | 53 | 74 | 95 | 116 | 137 | 158 | 179 | 200 | 201 | 232 | 253 | 274 | 295 | 316 |
| 32 | 12 | 33 | 54 | 75 | 96 | 117 | 138 | 159 | 180 | 181 | 202 | 233 | 254 | 275 | 296 | 317 |
| 33 | 13 | 34 | 55 | 76 | 97 | 118 | 139 | 160 | 161 | 182 | 203 | 234 | 255 | 276 | 297 | 318 |
| 34 | 14 | 35 | 56 | 77 | 98 | 119 | 140 | 141 | 162 | 183 | 204 | 235 | 256 | 277 | 298 | 319 |
| 35 | 15 | 36 | 57 | 78 | 99 | 120 | 121 | 142 | 163 | 184 | 205 | 236 | 257 | 278 | 299 | 320 |
| 36 | 16 | 37 | 58 | 79 | 100 | 101 | 122 | 143 | 164 | 185 | 206 | 237 | 258 | 279 | 300 | 301 |
| 37 | 17 | 38 | 59 | 80 | 81 | 102 | 123 | 144 | 165 | 186 | 207 | 238 | 259 | 280 | 281 | 302 |
| 38 | 18 | 39 | 60 | 65 | 86 | 107 | 128 | 145 | 166 | 187 | 208 | 239 | 260 | 261 | 282 | 303 |
| 39 | 19 | 40 | 44 | 66 | 87 | 108 | 129 | 146 | 167 | 188 | 209 | 240 | 241 | 262 | 283 | 304 |
| 40 | 20 | 23 | 45 | 67 | 88 | 109 | 130 | 147 | 168 | 189 | 210 | 221 | 242 | 263 | 284 | 305 |
| 41 | 2 | 24 | 46 | 68 | 89 | 110 | 131 | 148 | 169 | 190 | 201 | 223 | 241 | 265 | 281 | 306 |
| 42 | 3 | 25 | 47 | 69 | 90 | 111 | 132 | 149 | 170 | 191 | 202 | 224 | 242 | 266 | 282 | 307 |
| 43 | 4 | 26 | 48 | 70 | 91 | 112 | 133 | 150 | 171 | 192 | 203 | 225 | 243 | 267 | 283 | 308 |
| 44 | 5 | 27 | 49 | 71 | 92 | 113 | 134 | 151 | 172 | 193 | 204 | 226 | 244 | 268 | 284 | 309 |
| 45 | 6 | 28 | 50 | 72 | 93 | 114 | 135 | 152 | 173 | 194 | 205 | 227 | 245 | 269 | 285 | 310 |
| 46 | 7 | 29 | 51 | 73 | 94 | 115 | 136 | 153 | 174 | 195 | 206 | 228 | 246 | 270 | 286 | 311 |
| 47 | 8 | 30 | 52 | 74 | 95 | 116 | 137 | 154 | 175 | 196 | 207 | 229 | 247 | 271 | 287 | 312 |
| 48 | 9 | 31 | 53 | 75 | 96 | 117 | 138 | 155 | 176 | 197 | 208 | 230 | 248 | 272 | 288 | 313 |
| 49 | 10 | 32 | 54 | 76 | 97 | 118 | 139 | 156 | 177 | 198 | 209 | 231 | 249 | 273 | 289 | 314 |
| 50 | 11 | 33 | 55 | 77 | 98 | 119 | 140 | 157 | 178 | 199 | 210 | 232 | 250 | 274 | 290 | 315 |
| 51 | 12 | 34 | 56 | 78 | 99 | 120 | 122 | 158 | 179 | 200 | 211 | 233 | 251 | 275 | 291 | 316 |
| 52 | 13 | 35 | 57 | 79 | 100 | 103 | 121 | 159 | 180 | 182 | 212 | 234 | 252 | 276 | 292 | 317 |
| 53 | 14 | 36 | 58 | 80 | 85 | 104 | 123 | 160 | 161 | 183 | 213 | 235 | 253 | 277 | 293 | 318 |
| 54 | 15 | 37 | 59 | 61 | 84 | 105 | 124 | 141 | 162 | 184 | 214 | 236 | 254 | 278 | 294 | 319 |
| 55 | 16 | 38 | 60 | 62 | 83 | 106 | 125 | 143 | 163 | 185 | 215 | 237 | 255 | 279 | 295 | 320 |
| 56 | 17 | 33 | 41 | 63 | 82 | 101 | 126 | 142 | 164 | 186 | 216 | 238 | 256 | 280 | 296 | 301 |
| 57 | 18 | 40 | 42 | 61 | 81 | 102 | 127 | 144 | 165 | 187 | 217 | 239 | 257 | 271 | 297 | 302 |
| 58 | 19 | 21 | 43 | 62 | 87 | 103 | 128 | 145 | 166 | 188 | 218 | 240 | 258 | 272 | 298 | 303 |
| 59 | 20 | 22 | 41 | 63 | 88 | 104 | 129 | 146 | 167 | 189 | 219 | 223 | 259 | 273 | 299 | 304 |
| 60 | 1 | 24 | 42 | 64 | 89 | 105 | 130 | 147 | 168 | 190 | 220 | 222 | 260 | 274 | 300 | 305 |
| 61 | 3 | 25 | 43 | 65 | 90 | 106 | 131 | 148 | 169 | 191 | 201 | 221 | 250 | 275 | 281 | 301 |
| 62 | 4 | 26 | 44 | 66 | 91 | 107 | 132 | 149 | 170 | 192 | 202 | 222 | 251 | 276 | 282 | 302 |
| 63 | 5 | 27 | 45 | 67 | 92 | 108 | 133 | 150 | 171 | 193 | 203 | 223 | 252 | 277 | 283 | 303 |
| 64 | 6 | 28 | 46 | 68 | 93 | 109 | 134 | 151 | 172 | 194 | 204 | 224 | 253 | 278 | 284 | 304 |
| 65 | 7 | 29 | 47 | 69 | 94 | 110 | 135 | 152 | 173 | 195 | 205 | 225 | 254 | 279 | 285 | 305 |
| 66 | 8 | 30 | 48 | 70 | 95 | 111 | 136 | 153 | 174 | 196 | 206 | 226 | 255 | 280 | 286 | 306 |
| 67 | 9 | 31 | 49 | 71 | 96 | 112 | 137 | 154 | 175 | 197 | 207 | 227 | 256 | 261 | 287 | 307 |
| 68 | 10 | 32 | 50 | 72 | 97 | 113 | 138 | 155 | 176 | 198 | 208 | 228 | 257 | 262 | 288 | 308 |
| 69 | 11 | 33 | 51 | 73 | 98 | 114 | 139 | 156 | 177 | 199 | 209 | 229 | 258 | 263 | 289 | 309 |
| 70 | 12 | 34 | 52 | 74 | 99 | 115 | 140 | 157 | 178 | 200 | 210 | 230 | 259 | 264 | 290 | 310 |
| 71 | 13 | 35 | 53 | 75 | 100 | 116 | 121 | 158 | 179 | 181 | 211 | 231 | 260 | 265 | 291 | 311 |
| 72 | 14 | 36 | 54 | 76 | 86 | 117 | 122 | 159 | 180 | 182 | 212 | 232 | 241 | 266 | 292 | 312 |
| 73 | 15 | 37 | 55 | 77 | 85 | 118 | 123 | 160 | 162 | 183 | 213 | 233 | 242 | 267 | 293 | 313 |
| 74 | 16 | 38 | 56 | 78 | 84 | 119 | 124 | 142 | 161 | 184 | 214 | 234 | 243 | 268 | 294 | 314 |
| 75 | 17 | 39 | 57 | 79 | 83 | 120 | 125 | 141 | 163 | 185 | 215 | 235 | 244 | 269 | 295 | 315 |
| 76 | 18 | 40 | 58 | 80 | 82 | 101 | 126 | 143 | 164 | 186 | 216 | 236 | 245 | 270 | 296 | 316 |
| 77 | 19 | 23 | 59 | 61 | 81 | 102 | 127 | 144 | 165 | 187 | 217 | 237 | 246 | 271 | 297 | 317 |
| 78 | 20 | 21 | 60 | 62 | 100 | 103 | 128 | 145 | 166 | 188 | 218 | 238 | 247 | 272 | 298 | 318 |
| 79 | 4 | 22 | 51 | 63 | 99 | 104 | 129 | 146 | 167 | 189 | 219 | 239 | 248 | 273 | 300 | 319 |
| 80 | 5 | 23 | 52 | 64 | 98 | 105 | 130 | 147 | 168 | 190 | 200 | 240 | 249 | 274 | 281 | 320 |
| 81 | 6 | 24 | 53 | 65 | 97 | 106 | 131 | 148 | 169 | 191 | 201 | 231 | 250 | 275 | 282 | 301 |
| 82 | 7 | 25 | 54 | 66 | 96 | 107 | 132 | 149 | 170 | 192 | 202 | 232 | 251 | 276 | 283 | 302 |
| 83 | 8 | 26 | 55 | 67 | 95 | 108 | 133 | 150 | 171 | 193 | 203 | 233 | 252 | 277 | 284 | 303 |
| 84 | 9 | 27 | 56 | 68 | 94 | 109 | 134 | 151 | 172 | 194 | 204 | 234 | 253 | 278 | 285 | 304 |
| 85 | 10 | 28 | 57 | 69 | 93 | 110 | 135 | 152 | 173 | 195 | 205 | 235 | 254 | 279 | 286 | 305 |
| 86 | 11 | 29 | 58 | 70 | 92 | 111 | 136 | 153 | 174 | 196 | 206 | 236 | 255 | 280 | 287 | 306 |
| 87 | 12 | 30 | 59 | 71 | 91 | 112 | 137 | 154 | 175 | 197 | 207 | 237 | 256 | 264 | 288 | 307 |
| 88 | 13 | 31 | 60 | 72 | 90 | 113 | 138 | 155 | 176 | 198 | 208 | 238 | 257 | 265 | 289 | 308 |
| 89 | 14 | 32 | 41 | 73 | 89 | 114 | 139 | 156 | 177 | 199 | 209 | 239 | 258 | 266 | 290 | 309 |
| 90 | 15 | 33 | 42 | 74 | 88 | 115 | 140 | 157 | 178 | 200 | 210 | 240 | 259 | 267 | 291 | 310 |
| 91 | 16 | 34 | 43 | 75 | 87 | 116 | 131 | 158 | 179 | 181 | 201 | 221 | 260 | 268 | 292 | 311 |
| 92 | 17 | 35 | 44 | 76 | 86 | 117 | 132 | 159 | 180 | 182 | 202 | 222 | 241 | 269 | 293 | 312 |
| 93 | 18 | 36 | 45 | 77 | 85 | 118 | 133 | 160 | 161 | 183 | 203 | 223 | 242 | 270 | 294 | 313 |
| 94 | 19 | 37 | 46 | 78 | 84 | 119 | 134 | 141 | 162 | 184 | 204 | 224 | 243 | 261 | 295 | 314 |
| 95 | 20 | 38 | 47 | 79 | 83 | 120 | 135 | 142 | 163 | 185 | 205 | 225 | 244 | 262 | 296 | 315 |
| 96 | 1 | 39 | 48 | 80 | 82 | 110 | 136 | 143 | 164 | 186 | 206 | 226 | 245 | 263 | 297 | 316 |
| 97 | 2 | 40 | 49 | 61 | 81 | 111 | 137 | 144 | 165 | 187 | 207 | 227 | 246 | 271 | 298 | 317 |
| 98 | 3 | 24 | 50 | 62 | 100 | 112 | 138 | 145 | 166 | 188 | 208 | 228 | 247 | 272 | 299 | 318 |
| 99 | 4 | 25 | 51 | 63 | 99 | 113 | 139 | 146 | 167 | 189 | 209 | 229 | 248 | 273 | 300 | 319 |
| 00 | 5 | 26 | 52 | 64 | 98 | 114 | 140 | 147 | 168 | 190 | 210 | 230 | 249 | 274 | 281 | 320 |
Дата: 2019-04-23, просмотров: 396.