При решении задач этого раздела см. табл. 9 и табл. III приложения.
Ионно-молекулярные, или ионные, уравнения реакций обмена отражают состояние электролита в растворе. В этих уравнениях сильные растворимые электролиты, поскольку они полностью диссоциированы, записывают в виде ионов, а слабые электролиты, малорастворимые и газообразные вещества, записывают в молекулярной форме.
В ионно-молекулярном уравнении одинаковые ионы из обеих его частей исключаются. При составлении ионно-молекулярных уравнений следует помнить, что сумма электрических зарядов в левой части уравнения должна быть равна сумме электрических зарядов в правой части уравнения.
Пример 1. Напишите ионно-молекулярные уравнения реакций взаимодействия между водными растворами следующих веществ:
а) НС1 и NaOH; б) Рb(NO3)2 и Na2S; в) NaCIO и НNО3; г) К2СОз и H2SО4;
д) СНзСООН и NaOH.
Решение. Запишем уравнения взаимодействия указанных веществ в молекулярном виде:
а) НС1 + NaOH = NaCI + H2O
б) Pb(NО3)2 + Na2S = PbS + 2 NaNО3
в) NaCIO + HNО3 = NaNО3 + HC1О
г) К2СОз + Н2S04 = К2SО4 + СО2 + Н2О
д) СН3СООН + NaOH = CH3COONa + Н2О
Отметим, что взаимодействие этих веществ возможно, ибо в результате происходит связывание ионов с образованием слабых электролитов (Н2О, HC10), осадка (PbS), газа (СО2).
В реакции (д) два слабых электролита, но так как реакции идут в сторону большего связывания ионов и вода — более слабый электролит, чем уксусная кислота, то равновесие реакции смещено в сторону образования воды. Исключив одинаковые ионы из обеих частей равенства:
а) Na+ и Сl-; б) Na+ и NO 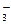 ; в) Na+ и NO
; в) Na+ и NO 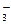 3 ; г) К+ и SO
3 ; г) К+ и SO 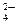 ; д) Na+,
; д) Na+,
получим ионно-молекулярные уравнения этих реакций:
а) H+ + ОН 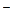 = Н2О
= Н2О
в) Pb2+ + S 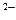 = PbS
= PbS
б) С1О 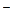 + H+ = HC1О
+ H+ = HC1О
г) СО 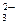 +2 H+ = CО2+H2О
+2 H+ = CО2+H2О
д) СНзСООН + ОН 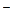 = СНзСОО
= СНзСОО 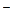 + Н2О
+ Н2О
Пример 2. Составьте молекулярные уравнения реакций, которым соответствуют следующие ионно-молекулярные уравнения:
а) SO 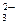 +2 H+ = S02 + H2О
+2 H+ = S02 + H2О
б) Pb2+ + CrО 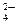 = PbCr04
= PbCr04
в) НСО 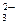 + ОН
+ ОН 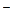 = СО
= СО 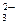 + Н2О
+ Н2О
г) ZnOH+ + H+ = Zn2+ + H2O
Решение. В левой части данных ионно-молекулярных уравнений указаны свободные ионы, которые образуются при диссоциации растворимых сильных электролитов. Cледовательно, при составлении молекулярных уравнений следует исходить из соответствующих растворимых сильных электролитов. Например:
а) Na2SО3 + 2 НС1 = 2 NaCl + SO2 + Н2О
б) Pb(NO3)2 + K2CrO4 = PbCrO4 + 2 KNO3
в) КНСО3 + КОН = К2СО3 + H2O
г) ZnOHCl + НС1 = ZnCl2 + H2O
КОНТРОЛЬНЫЕ ВОПРОСЫ
161. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) NаНСОз и NaOH;
б) K2SiO3 и НС1; в) BaCl2 и Na2SO4.
162. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: a) K2S и НС1;
б) FeSО4 и (NH4)2S; в) Сг(ОН)3 и КОН.
163. Составьте по три молекулярных уравнения реакций, которые выражаются ионно-молекулярными уравнениями:
а) Mg2+ + CO 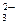 = MgCО3; б) H+ + ОН
= MgCО3; б) H+ + ОН 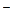 = H2O.
= H2O.
164. Какие из веществ — А1(ОН)3; H2SО4; Ва(ОН)2 — взаимодействуют с гидроксидом калия? Выразите эти реакции молекулярными и ионно-молекулярными уравнениями.
165. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) КНСО3 и H2SО4;
б) Zn(OH)2 и NaOH; в) СаСl2 и AgNО3.
166. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: a) CuSО4 и H2S;
б) ВаСО3 и HNO3; в) FеС13 и КОН.
167. Составьте по три молекулярных уравнения реакций, которые выражаются следующими ионно-молекулярными уравнениями:
а) Си2+ + S 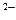 = CuS
= CuS
6) SiO 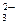 + 2 H+ = H2SiO3.
+ 2 H+ = H2SiO3.
168. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: a) Sn(OH)2 и НС1;
б) BeSО4 и КОН; в) NH4Cl и Ва(ОН)2.
169. Какие из веществ — КНСО3, СН3СООН, NiS04, Na2S — взаимодействуют с раствором серной кислоты? Напишите молекулярные и ионно-молекулярные уравнения этих реакций.
170. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) AgNО3 и К2СrO4;
б) Pb(NО3)2 и KI; в) CdSО4 и Na2S.
171. Составьте молекулярные уравнения реакций, которые выражаются ионно-молекулярными уравнениями:
а) СаСО3 + 2 Н+ = Са2+ + H2O + CO2;
б) А1(ОН)3 + ОН 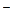 = А1O
= А1O 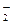 + 2 Н2О;
+ 2 Н2О;
в) РЬ2+ + 2 I 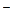 = PbI2
= PbI2
172. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) Ве(ОН)2 и NaOH; б) Си(ОН)2; и HNО3; в) ZnOHNО3 и HNО3.
173. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: a) Na3PО4 и CaCl2;
б) К2СО3 и ВаСl2; в) Zn(OH)2 и КОН.
174. Составьте молекулярные и ионно-молекулярные уравнения реакций, которые выражаются ионно-молекулярными уравнениями:
Fе(ОН)3 + З H+ = Fe3+ + З Н2О;
Cd2+ + 2 OН 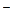 = Cd(OH)2;
= Cd(OH)2;
H+ + NO 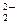 = HNO2.
= HNO2.
175. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: a) CdS и НС1;
б) Сг(ОН)3 и NaOH; в) Ba(OH)2 и CoCl2.
176. Составьте молекулярные и ионно-молекулярные уравнения реакций, которые выражаются ионно-молекулярными уравнениями:
а) Zn2+ + H2S = ZnS + 2 H+;
б) НСО 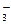 + Н+ = H2O + СО2;
+ Н+ = H2O + СО2;
в) Ag+ + С1 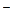 = AgCl.
= AgCl.
177. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: a) H2S04 и Ва(ОН)2;
б) FеС13 и NH40H; в) CH3COONa и НС1.
178. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) FеС13 и КОН;
6) NiSO4 и (NH4)2S; в) MgCO3 и HNO3.
179. Составьте молекулярные уравнения реакций, которые выражаются ионно-молекулярными уравнениями:
а) Ве(ОН)2 + 2 OН 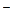 = ВеО
= ВеО 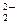 + 2 Н2O
+ 2 Н2O
б) СНзСОО 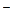 + Н+ = СНзСООН
+ Н+ = СНзСООН
в)Ba2+ + SO 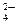 = BaSO4
= BaSO4
180. Какие из веществ — NaCl, NiS04, Ве(ОН)2, КНСОз — взаимодействуют с раствором гидроксида натрия. Запишите молекулярные и ионно-молекулярные уравнения этих реакций.
Дата: 2019-04-23, просмотров: 423.