Биосинтез витаминов. Витамины синтезируются при обработке молочной сыворотки дрожжами и бактериями.
Молочная сыворотка при производстве концентрата на линии Le Francua (Франция) обогащается витаминами, содержание которых (в мг/кг) в сухом продукте следующее: B1 - 7,2; В2 – 42 - 49; РР - 123-193; В12 - 0,22; пантотеновая кислота - 84-99; фолиевая кислота - 0,94; биотин - 0,11; пиридоксин - 8,2.
Сущность направленного синтеза витаминов бактериями с использованием молочной сыворотки, разработанного под руководством проф. В. М. Богданова, заключается в следующем. В одной части сыворотки, обогащенной 0,5 % дрожжевого автолизата и 5 % гидролизованного молока, культивировали пропионовокис-лые бактерии при 30 °С в течение трех суток. За это время в 1 мл среды накапливалось до 500 млн клеток бактерий. В другой части сыворотки культивировали дрожжи с доведением количества клеток до 50 млн в 1 мл. На стерильном обезжиренном молоке выращивали в течение 16 ч при 37 °С ацидофильную палочку (2 млн клеток в 1 мл). По 10 л каждого препарата смешивали и сушили распылением. Готовый продукт содержал следующее количество витаминов: B12 - 13,5 -55 мг/кг; B1 – 1,541 мг % ; В2 - 1080 мг/кг; фолиевой кислоты - 1027 мг/кг.
Молочная сыворотка является самой благоприятной средой для синтеза витамина В2. Наибольший выход витамина достигается при использовании в качестве питательной среды подсырной сыворотки.
Для обогащения сыворотки витамином В2 рекомендуется использовать культуры Е. ashbyii и Cl. acetobutilicum. Для приготовления питательной среды при использовании Е. ashbyii в сыворотку добавляют 1% сахарозы, микроэлементы (марганец, цинк, медь, кобальт, бор), а также инозид и тиамин. Ферментацию ведут при 24—28 °С и рН 5,5. Накопление рибофлавина показано в табл. 2.28.
Таблица 2.28.
| Питательная среда | Содержание рибофлавина, мкг/мл | |
| Через 4 дня брожения | Через 6 дней брожения | |
| Обезжиренное молоко | 1250 | 1375 |
| Молочная сыворотка | 457 | 677 |
| Смесь обезжиренного молока и молочной сыворотки (47,9 : 52,1) | 1562 | 1962 |
Эффективность накопления витамина В2 (в мкг/мл) при использовании Cl. acetobutilicum нa различных питательных средах показана ниже.
| Патока | 1-2 |
| Зерно кукурузы | 25- 30 |
| Обезжиренное молоко | 20-50 |
| Молочная сыворотка с ксилозой | 70 - 97 |
Витамин В1 синтезируется культурой Cl. acetobutilicum. Оптимальная температура ферментации соответствует 38 °С, количество закваски — 5 %. Сыворотку также обогащают микроэлементами и ростовыми веществами.
Молочную сыворотку и ее концентраты можно использовать для получения провитамина А (каротина и каротиноидов).
Сравнительные испытания 6 штаммов дрожжей Rh. lactis показали, что в оптимальных условиях культивирования из 1 т сыворотки можно получить до 50 кг белково-каротиноидного препарата с достаточно высоким содержанием β-каротина и витаминов группы В.
Методы обогащения сыворотки комплексом витаминов разработаны в ТСХА.
Биосинтез жира. Возможность синтеза жира микроорганизмами на молочной сыворотке изучена с использованием плесневых грибов Asp. niger и R. nigrigens. В целях интенсификации процесса в сыворотку добавляют 1 % раствора сернокислого аммония, 1 % аспарагиновой кислоты и 3 % глюкозы.
Способностью синтезировать жир обладает также плесень О. lactis. При ее культивировании на молочной сыворотке в анаэробных условиях концентрацию жира можно довести до 22 - 23 У. Активно синтезирует жир культура О. wallroth, которая накапливает до 50% его в сухом веществе. Гриб A. ustus в условиях глубинного культивирования с обогащением сыворотки нитратом аммония накапливает в 1 л сыворотки 17 г биомассы, в том числе 28 % жира и 13 % белка.
Дрожжи С. humicola при переработке 1 т сыворотки дают до 9 кг жира (45—48 кг сухого вещества) . При этом основной фракцией жира являются триглицериды (более 80 7с). Жир содержит 42,4 % насыщенных и-57,6% ненасыщенных жирных кислот, по свойствам напоминает растительное масло. Накопившийся жир можно извлечь эфиром или хлороформом, а также обработкой соляной кислотой по специальной технологии.
Сравнительные испытания по синтезу жира на натуральной и концентрированной молочной сыворотке показали следующее. Дрожжи Candida Curvata D. на натуральной сыворотке, обогащенной комплексом ростовых факторов, в условиях активного культивирования через 30 ч дают выход сухих веществ из1 дм3 субстрата 26,71 г. в том числе 8,74 г жира при степени использования лактозы 83,13%. Для выделения жира из клеток дрожжей используют дезинтеграторы. В оттоках наблюдалось 9-кратное снижение ХПК (химического потребления кислорода).
Культивирование этого же штамма дрожжей на концентратах очищенной от белка сыворотки в течение 64 ч со снижением лактозы с 8,22 до 0,2 % позволило получить от 27,28 до 51,39 г жира из 100 г лактозы, что близко к теоретически возможному. В результате ХПК снижалось на 76,19%. Биомасса дрожжей имела следующий состав (в %) жира 38,43; общего белка 32,92.
По количественному и качественному составу жирных кислот полученный в результате биосинтеза жир близок к обычным жирам, что позволяет использовать продукт для кормления телят и птицы.
Биосинтез ферментов. Разработаны способы получения фермента лактазьГ (β-галактозидазы, β-D-галактозидгалактогидролазы) и пектолитических ферментов на основе молочной сыворотки. Влияние различных источников углерода на рост и образование 3-галактозидазы в условиях глубинного культивирования (в течение 24ч) культурой S. fragilis показано в табл. 2.29.
Таблица 2.29.
| Источник углерода в среде | Количество сухих дрожжей, г на 100 мл среды. | Содержание β-галактозидазы, ед. | |
| В 100 мл среды | В 1 г сухих дрожжей | ||
| Сахароза | 0,65 | 1,9 | 2,8 |
| Лактоза | 0,6 | 165 | 175 |
| Глюкоза | 0,48 | 2,1 | 4,4 |
| Галактоза | 0,65 | 315 | 484 |
| Мальтоза | 0,05 | - | - |
Как видно из табл. 2.29, активный синтез фермента наблюдается лишь при введении в питательную среду лактозы либо ее производной галактозы. Глюкоза является ингибитором биосинтеза β-галактозидазы. Скорость биосинтеза фермента на лактозе является функцией двух противоположных факторов — индукции и репрессии и определяется отношением концентраций индуктора (лактоза и галактоза) и ингибитора (глюкоза). Питательная среда для синтеза лактозы включает творожную сыворотку; 0,4% (NH4)2 НРО4; 0.016% MnSO4 и 1 % дрожжевого автолизата.
Динамика образования лактазы (в ед/ч) на указанной среде в зависимости от продолжительности культивирования составляет: 24 ч - 60; 48 ч - 78; 72 ч - 80; 96 ч - 102; 120 ч - 117; 144 ч - 122.
Технологическая схема получения β-галактозидазы на сыворотке включает следующие операции: выращивание дрожжей глубинным методом в течение 26 ч при 26-28 °С и начальном рН 5,5-6; инактивация дрожжевых клеток при 60 °С в течение 2,5 ч; экстракция фермента из дрожжевых клеток толуолом и фосфатным буфером при рН 6,9; концентрация экстракта в 4—5 раз при 25— 26 °С; лиофильная сушка концентрата.
Полученный фермент активно гидролизует лактозу в молочной сыворотке. При концентрации его 0,1%, рН 6,9 и температуре 30 °С в течение 1 ч гидролизуется до 40% лактозы, при увеличении концентрации фермента до 0,4 % и продолжительности культивирования до 4 ч гидролизуется 95 % лактозы.
Молочная сыворотка может быть средой для развития плесеней Тr. koningii и S. sclerotiorum, которые синтезируют некоторые гидролитические ферменты.
Изучение закономерностей биосинтеза пектолитических ферментов и β-галактозидазы грибами S. sclerotiorum [штамм ВКМ (ƒ) = 879] и A. awamori (штамм 16) на обогащенной творожной сыворотке показало, что оба продуцента синтезируют ферменты. При этом не наблюдается репрессии, что бывает при использовании традиционного сырья (свекловичный жом).
В качестве продуцента используют Т. lignorum, который, усваивая глюкозу, одновременно обеспечивает гидролиз лактозы до моноз. При этом скорость утилизации продуктов расщепления несколько выше скорости их образования, что обеспечивает активное течение процесса.
Биосинтез антибиотиков. Лактоза является одним из основных компонентов субстрата при ферментации ряда антибиотиков. Из молочной сыворотки, очищенной от белка, готовят концентрат (кристаллизат), который ранее использовался при изготовлении пенициллина. В настоящее время вместо него используется сухой молочный сахар-сырец.
Из творожной сыворотки путем вымораживания выделен антибиотик низин, который на специальном тесте проявлял такие же свойства, как и биомицин. Вероятно, большинство микроорганизмов при их культивировании на сыворотке обеспечивают накопление биологически активных веществ, антибиотиков и органических кислот. С учетом невысокой стоимости молочной сыворотки представляется целесообразным более широкое изучение и использование этого свойства.
Обработка пектином
Использование яблочного пектина в качестве полимера-осадителя позволило разработать технологию переработки молочной сыворотки с получением белково-полисахаридного концентрата, обладающего высокими функциональными свойствами. При этом в концентрат переходят полностью белки молочной сыворотки в неденатулированном состоянии и могут быть полностью использованы на пищевые цели. Исходная молочная сыворотка сепарируется, пастеризуется, подвергается частичной деминерализации на электродиализной установке. В подготовленную таким образом молочную сыворотку вносится пектин.
Сывороточно-пектиновая смесь подвергается центрифугированию. В результате получается белково-полисахаридный концентрат и безбелковый концентрат. Белково-полисахаридный концентрат может быть высушен на распылительных сушильных установках. Оставшийся равновесная жидкость (безбелковый раствор) может быть использован в производстве молочного сахара.
Компонентный состав полученных полуфабрикатов приведен в табл. 2.30.
Таблица 2.30.
| Наименование показателя | Белково-полисахаридный концентрат | Равновесная жидкость | |
| жидкий | сухой | ||
| Массовая доля сухих веществ, % | 7±2 | 94, ±2 | 2,3±0,5 |
| Массовая доля белка, % | 2,5±0,5 | 34±2 | 0,05±0,02 |
| Массовая доля пектина, % | 2,5±0,5 | 34±2 | 0,05±0,02 |
| Массовая доля лактозы, % | 2,0±0,5 | 26±3 | 2,0±0,3 |
Исследование пенообразующих свойств белково-полисахаридного концентрата показано, что полученные пены по своим физико-химическим характеристикам (плотность, стабильность) почти не уступают пенам, полученным с использованием яичного белка (табл. 2.31.).
Таблица 2.31.
| Показатели | Белково-полисахаридный концентрат | Яичный белок | Пектин |
| Плотность пены, г/см3 | 0,44±0,01 | 0,28±0,01 | - |
| Стойкость пены в % отслоившейся фазы через 2 часа | 1,7±0,1 | 14,0±0,1 | - |
| 24 часа | 41,7±1,8 | 61,1±1,8 | - |
| Прочность студня в г по Валенту | 425±25 | - | 325±25 |
В течение первых двух часов стабильность таких пен почти в 20 раз выше стабильности пен из яичного белка, что имеет определённое значение при производстве ряда взбивных изделий в кондитерской промышленности.
Мембранные методы обработки
Мембранные методы обработки можно разделить на два основных: гиперфильтрация (микрофильтрация, ультрафильтрация, обратный осмос) и электродиализ. В эту группу методов обработки условно относят ионный обмен, гельфильтрацию, сорбцию – десорбцию.
Сущность мембранных технологий основана на свойствах молочной сыворотки (как и другого молочного сырья) как гетерогенной системы с четко выраженной селективностью компонентов по молекулярной, размерам и ионной силе.
Академик ВАСХНИЛ Н.Н. Липатов еще в 1973 году на основе обобщения имеющихся к тому времени материалов ввел в классификационную схему понятие о мембранных методах разделения молочного сырья и четко определил перспективу их развития. Необходимость разработки и внедрения новых нетрадиционных способов переработки молока, в том числе и мембранных методов, была подчеркнута и на XXI Международном молочном конгрессе.
В настоящее время наибольший интерес, по нашему мнению, представляют процессы гиперфильтрации, электродиализа и сорбции – десорбции. Ионный обмен и гельфильтрация, хотя и привлекают внимание исследователей, широкого практического применения пока не нашли.
Гиперфильтрация является физическим способом разделения растворов (без превращения фаз) через полупроницаемую перегородку – мембрану с определенным размером пор от 1 до 1000 нм (0,001 – 1 мкм).
Основной деталью мембранных установок являются специальные полупроницаемые мембраны с различным диаметром пор, соизмеримых с молекулами находящихся в растворе компонентов. В зависимости от диаметра пор мембраны происходит разделение находящихся в растворе компонентов:
компоненты с размерами менее диаметра пор проходят через мембрану, а компоненты с большими размерами задерживаются. Получаются два раствора с различными компонентами (рис. 2.41.).
Рисунок - 2.41.
Рисунок 2.41. – Принцип разделения молекул при ультрафильтрации: 1 — мембрана; 2 — макромолекулы; 3—вода; 4—минеральные вещества
Процесс гиперфильтрации основан на принципе обратного осмоса. Часть компонентов раствора, и прежде всего растворитель, за счет давления, создаваемого на раствор, переходит через мембрану, а другая, например белки, задерживается. Происходит концентрация раствора.
Проницаемость всех видов мембран во время работы снижается, что обусловлено концентрационной поляризацией (образованием на поверхности фильтра слоя раствора с повышенной концентрацией), вследствие чего осмотическое давление и гидродинамическое сопротивление увеличиваются. Для уменьшения этого раствора энергично перемешивают или резко увеличивают его скорость.
Применительно к молочной сыворотке главными достоинствами мембранных способов разделения являются:
возможность направленного регулирования ее состава и свойств при сравнительно небольших энергетических затратах;
создание на этой основе новых молочных продуктов с редуцированной калорийностью и высокой биологической ценностью;
рациональное использование молочной сыворотки на основе малоотходных и безотходных технологических процессов.
В настоящее время выполнено большое количество исследования по гиперфильтрации молочной сыворотки, созданы и внедрены высокопроизводительные установки.
Основные критерии процесса гиперфильтрации определяются избирательностью, проницаемостью, устойчивостью к механическому, химическому и микробиологическому загрязнению мембран.
Гиперфильтрацию в зависимости от пористости (проницаемости) применяемой мембраны и эффективности процесса разделения гетерогенных растворов условно делят на микрофильтрацию, ультрафильтрацию и обратный осмос (рис. 2.42.)
Рисунок - 2.42.
Рисунок 2.42. – Схема разделения гетерогенных растворов молекулярно-ситовой фильтрацией.
Микрофильтрация
При микрофильтрации происходит разделение суспензии и коллоидных растворов. Отличительной особенностью микрофильтрации является использование мембран с диаметром пор 0,1-1 мкм (100-1000 нм). Она может быть использована для холодной стерилизации молочной сыворотки. При этом считается, что отсутствие мицелл казеина обеспечивает относительно легкое проведение процесса удаления бактерий, которые остаются на мембране. Одновременно из сыворотки извлекается остаточный молочный жир в количестве 05-1,18 г на 1л.
Ультрафильтрация
В тех случаях, когда осмотическое давление пренебрежимо мало по сравнению с рабочим давлением, что, например, характерно для водных растворов высокомолекулярных веществ, процесс разделения растворов с помощью полупроницаемых мембран называют ультрафильтрацией. Для проведения ультрафильтрации используют полупроницаемые мембраны диаметром пор от 10 до 100 нм, способные задерживать компоненты с молекулярной массой от 104 ед. и выше.
При ультрафильтрации мембрана задерживает только высокомолекулярные соединения и пропускает с фильтратом вещества, образующие «истинный» раствор. Так, при ультрафильтрации молочной сыворотки задерживается (концентрируется) белок, а в фильтрат уходят соли и лактоза. В фильтрат переходит около 30% кальция, 90—калия и натрия, 70—магния, 80—хлора и 50% фосфора, содержащихся в исходной сыворотке. Содержание витаминов в концентрате такое же, как и в исходной сыворотке. Белки сохраняют свои нативные свойства. Необходимое давление для осуществления процесса ультрафильтрации (по принципу обратного осмоса) находится на уровне 0,1—1 МПа (1—10 атм).
В результате ультрафильтрации получается белковый концентрат (ретентант), содержащий высокомолекулярные соединения молочной сыворотки (и соответственно его концентрации компоненты), и фильтрат (пермеат) — раствор лактозы, минеральных солей и других низкомолекулярных соединений, аналогичный по составу молочной сыворотке.
Основной задачей управления процессом ультрафильтрации является поддержание заданных технологических режимов с получением белкового концентрата необходимой концентрации, состав которого приведен в табл. 2.32.
Таблица 2.32.
| Продукт | Содержание, % | |||||
| Сухих веществ | Белка | Лактозы | Минеральных солей | Молочной кислоты | Воды | |
| Исходная сыворотка | 6,5 | 0,7 | 4,5 | 0,6 | 0,6 | 93,5 |
| Концентрат | 18 | 12,5 | 4,5 | 0,6 | 0,6 | 82 |
Состав фильтрата (табл. 2.33.) зависит от вида исходной сыворотки.
Таблица 2.33.
| Показатель | Фильтрат | |
| Подсырной сыворотки | Творожной сыворотки | |
| Сухие вещества, % | 5,1 – 5,4 | 5,2 – 5,6 |
| Лактоза | 4,2 – 4,8 | 4,2 – 4,8 |
| Белок | 0,2 – 0,24 | 0,20 – 0,24 |
| Зола | 0,5 – 0,75 | 0,6 – 0,9 |
| Макроэлементы, мг % | ||
| Кальций | 55 – 70 | 85 – 120 |
| Фосфор | 40 – 65 | 65 – 80 |
| Калий | 120 – 180 | 150 – 280 |
| Натрий | 61 – 90 | 45 – 75 |
| Микроэлементы, мг на 100 г | ||
| Медь | 2,7 – 4 | – |
| Цинк | 11,5 – 20,5 | – |
| Железо | 63 – 80 | – |
| Марганец | 5,2 – 5,5 | 4,6 – 4,8 |
| рН | 5,2 – 5,8 | 4,7 – 5,1 |
| Титруемая кислотность, ˚Т | 8 – 18 | 80 – 100 |
| Плотность, кг/м3 | 1012 – 1018 | 1016 – 1018 |
| Вязкость, Па∙с | 1,135 – 1,15 | 1,130 – 1,155 |
Технологическая схема обработки 5000 кг подсырной сыворотки с помощью ультрафильтрации (с указанием промежуточных продуктов и их состава) приведена ниже [ в % и кг (в скобках) ].
Опыт эксплуатации ультрафильтрационных установок показал, что важным вопросом стабилизации процесса является подготовка воды для санитарной обработки оборудования.
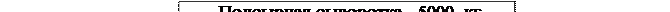
Машиностроительными заводами освоено производство комплексной линии А1-ОБС производительностью 5000 л/ч исходного сырья для выделения из подсырной сыворотки жира и белков. В комплект линии входят оборудование для предварительной обработки сыворотки (сепарирования, пастеризации, охлаждения).
Техническая характеристика линии А1-ОБС
| Производительность техническая, л/ч по подсырной сыворотке – не менее по жидкому концентрату (с массовой до лей сухих веществ не менее 24%) | 5000 160 – 170 |
| Расход пара, кг/ч, не более | 740 |
| Расход холода, Вт, не более | 45000 |
| Расход воды (средний за цикл мойки), м3, не более | 25 |
| Установленная мощность электродвигателей, кВт | 169 |
| Потребляемая мощность, кВт∙ч, не более | 167 |
| Занимаемая площадь, м2, не более | 250 |
| Масса, кг | 46000 |
Линия предназначена для получения сухих концентратов сывороточных белков с массовой долей белка в сухом веществе не менее 50%. Ее рекомендуется устанавливать на сыродельных заводах, перерабатывающих в смену 50 т и более молока имеющих цехи по производству молочного сахара (для переработки фильтрата, образующегося пр, ультрафильтрации сыворотки) В комплект линии не включено оборудование для пастеризации жидкого белкового концентрата, поэтому для получения готового продукта, отвечающего требованиям технических условий по микробиологическим показателям, необходимо создать участок его тепловой обработки после ультрафильтрации согласно схеме представленной на рисунке 2.43.
Рисунок 2.43
Рисунок 2.43. — Схема участка тепловой обработки белкового концентрата после ультрафильтрации:
I — концентрат после ультрафильтрации; II — концентрат пастеризованный на дальнейшую обработку; 1— охладитель; 2 — резервуар для концентрата; 3 — насос; 4 — пастеризационно-охладительная установка; 5 — резервуар пастеризованного и охлажденного концентрата.
Концентрат пастеризуют при температуре 72±2 °С с выдержкой 16—20 с, после чего его охлаждают до 8—10 °С и только непосредственно перед распылительной сушкой подогревают до 50±2 °С.
Благодаря уникальным биологическим и функциональным свойствам концентрат сывороточных белков, вырабатываемый на линии А1-ОСБ, рекомендуется использовать в качестве белкового обогатителя при производстве продуктов детского питания, а также продуктов повышенной биологической питательной ценности.
Частным случаем ультрафильтрации является диафильтрация, используемая для получения высокобелковых молочных концентратов. При диафильтрации концентраты, получаемые ультрафильтрацией, разбавляют водой (лучше деминерализованной) и подвергают повторной ультрафильтрации с целью «вымывания» низкомолекулярных компонентов, в частности лактозы и минеральных веществ.
Обратный осмос
Разграничить высоко- и низкомолекулярные соединений трудно, деление это зачастую условно, поэтому нельзя четко разграничить процесс ультрафильтрации и обратного осмоса. В обоих случаях требуется преодолевать осмотическое давление фильтруемого раствора, так как растворитель переносится в направлении, противоположном возрастанию концентрации растворенного вещества, задерживаемого фильтром. Способом обратного осмоса производят концентрированно практически всех веществ, находящихся в растворе, и выделение чистого растворителя из раствора за исключением некоторого количества одновалентных ионов Na, K, Cl. Практически обратный осмос сводится к сгущению раствора (рис. 2.44.)
Рисунок 2.44.
Рисунок 2.44. – Принцип разделения при обратном осмосе: 1 — мембрана; 2 — макромолекулы; 3 — минеральные вещества; 4 — вода
В этом случае приходится преодолевать более высокое осмотическое давление раствора, которое резко возрастает для низкомолекулярных соединений. Например, 3%-ный раствор поваренной соли имеет осмотическое давление в 500 раз больше, чем 3%-ный раствор казеина. Поэтому, если при ультрафильтрации применяют рабочее давление 0,3—1 МПа, обратный осмос проводят при более высоких рабочих давлениях (10 МПа и более). Фильтры, применяемые для ультрафильтрации и обратного осмоса, принципиально различаются лишь размерами пор, они мельче и обеспечивают перенос только растворителя. При обратном осмосе применяют полупроницаемые мембраны диаметром пор от 1 до 10 нм, способные задерживать компоненты раствора с молекулярной массой от 50 ед. и выше. Преимуществом обратного осмоса перед существующими способами концентрации растворов (например, сгущения в вакуум-выпарных установках) является возможность проведения процесса при любых температурах. Кроме того, расчеты показывают, что затраты энергии при обратном осмосе меньше, чем при использовании других традиционных способов концентрации, а расход тепловой энергии может быть исключен совсем. В связи с этим применение обратного осмоса особенно целесообразно при выработке пищевых продуктов, где выпаривание при повышенных температурах приводит к нежелательным последствиям.
За рубежом для обработки молочного сырья выпускают специализированные обратноосмотические установки.
Установка фирмы DDS (Дания), смонтированная на одном из заводов во Франции, обрабатывает 80 т сыворотки в сутки с получением 20 т концентрата и 60 т воды.
Хорошие результаты дает совмещение процессов ультрафильтрации и обратного осмоса. Одна из фирм США выпускает установки для ультрафильтрации и обратного осмоса (две ступени) молочной сыворотки. В результате получается 20%-ный раствор сывороточного белка и 20%-ный раствор лактозы.
Оптимальным считается концентрирование методом обратного осмоса до массовой доли сухих веществ 20—30%.
В первую очередь обратный осмос должен найти применение для концентрирования сыворотки, что снизит потери и расширит пути ее рационального использования. Кроме того, одним из перспективных направлений использования обратного осмоса является обработка соленой сыворотки в целях исключения нежелательных явлений, связанных с наличием хлористого натрия, а также обработка конденсата вакуум-выпарных установок, что позволит рационально использовать оборотную воду и уловить отходящие с пеной и вторичными парами компоненты молочного сырья.
Техническая характеристика промышленной установки для сгущения молочной сыворотки обратным осмосом
| Производительность, м/ч: | |
| по сыворотке | 5,0 |
| по концентрату | 1,25 |
| Количество модулей: | |
| Рабочих | 4 |
| Резервных | 1 |
| Тип мембраны | МГА-95 |
| Площадь активной зоны мембран, м2: | |
| одного модуля | 113 |
| всей установки | 450 |
| Проницаемость, л/м2 в сутки | 200 |
| Скорость прохождения сыворотки в канале, м/с | 2,0 |
| Рабочее давление, МПа | 4,9 |
| Режим работы | Непрерывный |
Производственные испытания по оптимальному режиму обратного осмоса ультрафильтратов творожной сыворотки позволили получить следующие результаты (табл. 2.34.).
Таблица 2.34.
| Показатель | Творожная сыворотка | Концентрат | фильтрат |
| Массовая доля сухих веществ, % | 5,69 | 22,7 | 0,2 – 0,3 |
| В том числе | |||
| Белка | 0,89 | 0,8 | Нет |
| Лактозы | 17,2 | – | 0,13 – 0,2 |
| Золы | 0,4 – 0,5 | 1,2 | 0,1 |
| Жира | 0,1 | Нет | Нет |
Наряду с концентрированием сухих веществ до 20 – 25% в фильтрат отходит незначительное количество лактозы и минеральных солей.
За рубежом для обработки молочного сырья рядом фирм выпускаются специализированные обратноосмотические установки.
Считается, что наиболее сложной проблемой при концентрировании сыворотки с помощью обратного осмоса заключается в осаждении высокомолекулярных веществ с низкой скоростью диффузии, например сывороточных белков, а также в существовании пограничного слоя из низкомолекулярных соединений, например лактозы и солей.
Пограничный слой можно удалить с помощью кратковременного промывания водой, в то время как удаление осадка требует специальных операций по очистке. Удаление белково-жировых отложений связано с трудностями. Эти отложения уменьшают проток жидкости, но через определенное время наступает состояние равновесия. Достичь усиления протока путем повышения давления удается лишь на короткое время. Количество отложений вновь возрастает, проток жидкости уменьшается, пока опять не наступает равновесие. При снижении давления замедляется поток фильтрата. Уменьшаются прохождение химических веществ через мембраны и количество отложений. Удаление осадка из мембран происходит медленно, особенно если они не удалялись в течение длительного времени и между молекулами образовались стабильные полимерные связи.
Если рабочее давление опускается ниже осмотического, происходит обратное всасывание фильтрата через мембраны. В результате органические отложения разрыхляются и удаляются.
Предварительная обработка сыворотки, аналогичная производимой перед ультрафильтрацией, имеет все же существенный недостаток, если сыворотка в дальнейшем подвергается концентрированию с помощью обратного осмоса. Это связано с тем, что состав и форма минеральных веществ играют более важную роль в процессе обратного осмоса, чем белок. Наиболее эффективной предварительной обработкой для казеиновой сыворотки является деминерализация с помощью ионообменника или электродиализа.
При очистке установок для обратного осмоса используют неспецифические высокоактивные протеазы. Для дезинфекции применяется раствор С1; в дозах 5—10 мг/кг при рН 3,5.
После окончания процесса концентрирования оборудование для обратного осмоса в течение 5 мин тщательно промывают водой, а затем ферментным раствором из бактериальных протеаз при температуре 30°С. Ферментный раствор медленно пропускается через аппарат. Примерно через час или в тот момент, когда скорость прохождения фильтрата достигает желательных значений либо становится постоянной, промывку прекращают, установку ополаскивают водой и дезинфицируют, медленно пропуская раствор Сl (5—10 мг/кг) при рН 3,5. Заключительной операцией по очистке является промывка водой в течение 2—3 ч.
Электродиализ
Одним из эффективных способов деминерализации молочной сыворотки является электродиализ. Суть процесса электродиализа заключается в том, что селективная ионитовая мембрана (перегородка), находясь в контакте с раствором, под влиянием электрического поля пропускает ионы одного заряда и служит барьером для ионов противоположного заряда*.
Схема обессоливания — концентрирования в двухкамерных электродиализных ячейках—показана на рисунке 2.45.
Рисунок 2.45.
Рисунок 2.45. – Схема обессоливания-концентрирования растворов в двухкамерных электродиализных ячейках с мембранами: а — катионитовыми (к) и анионитовыми (а); б — с катионитовыми (к) и нейтральными (н); М—молочная сыворотка; Р — рабочий раствор; К1, К2—катионы; А1, А2—анионы; Э — электродные камеры
Допустим, что в молочной сыворотке содержатся катионы К1 и анионы А1 солей, в рабочем растворе — соответственно К2 и А2.
При пропускании постоянного (или выпрямленного) электрического тока катионы солей, содержащихся в молочной сыворотке и рабочем растворе, перемещаются по направлению к катоду, а анионы солей—к аноду.
Перемещаясь к катоду, катионы солей молочной сыворотки через катионитовую мембрану переходят в рабочий раствор соседних камер. Анионы, перемещаясь к аноду, через анионитовую мембрану также переходят в рабочий раствор. Дальнейший путь из рабочего раствора к катоду катионам преграждает анионитовая мембрана, а анионам к аноду — катионитовая, поэтому катионы и анионы солей, удаляемых из молочной сыворотки, накапливаются в рабочем растворе. В результате описанной миграции ионов молочная сыворотка обессоливается, а рабочий раствор концентрируется. Процессы электродиализного обессоливания и концентрирования протекают одновременно и тесно взаимосвязаны. При изменении направления электрического тока на противоположное процесс будет протекать в обратном направлении. То же произойдет, если поменять местами катионитовые и анионитовые мембраны.
Электронейтральные молекулы других веществ, входящих в состав молочной сыворотки, в электродиализном процессе не участвуют, поэтому при электродиализном обессоливании молочной сыворотки (или молока) в рабочий раствор переходят только ионы солей, а содержание белков и лактозы не меняется.
Конструкция большинства электродиализаторов многокамерная — из большого числа чередующихся анионо-катионообменных мембран, заключенных между двумя электродами (рис. 2.46.)
По данным японских ученых, удаление различных ионов при электродиализе происходит неодинаково. В начальный период обессоливания сыворотки удаляются практически лишь одновалентные ионы — натрий, калий, хлор, которые наиболее сильно влияют на вкусовые качества сыворотки. Затем, по мере обессоливания, одновременно удаляются анионы фосфорной и лимонной кислот, что приводит к частичной диссоциации комплексов, связывающих ионы кальция и магния. С повышением степени обессоливания скорость удаления из сыворотки двухвалентных катионов возрастает, что показано на рис. 2.47. Молочная кислота удаляется со скоростью, занимающей промежуточное положение между одно- и двухвалентными неорганическими анионами. Однако микроэлементы (железо, цинк, медь, марганец) остаются в сыворотке. Данные о содержании микроэлементов в молочной сыворотке при различном уровне ее деминерализации приведены в табл. 2.35.
Изучение деминерализации творожной сыворотки показало возможность удаления до 90% минеральных веществ (табл. 2.36.) при незначительных потерях сывороточных белков (3 — 4%) и лактозы (4—5%). Величина рН практически не меняется, титруемая кислотность снизилась на 70%, удельная электропроводность — на 80%. Степень выделения отдельных ионов при уровне деминерализации 90% составила, %: хлора—97, калия — 90, натрия — 86, кальция — 75 и магния — 56.
Рисунок 2.46.
Рисунок 2.46. – Схема процесса электродиализа молочной сыворотки:
А — анионитовая мембрана; К — катионитовая мембрана
Электродиализ молочной сыворотки не оказывает существенного влияния на качество и содержание сывороточных белков, лактозы и витаминов. Потери белка составляют 2—3%, причем количество небелкового азота уменьшается на 25%, а потери лактозы при уровне деминерализации 90% составляют 6%. Одновременно с уменьшением содержания солей, по данным фирмы SRTI (Франция), происходит снижение титруемой кислотности. Для подсырной сыворотки при уровне деминерализации 58 и 90% степень раскисления составляет соответственно 29 и 60%, для творожной—при уровне деминерализации 50%—33%. Величина рН в процессе обработки практически не меняется. В результате электродиализной обработки органолептические показатели молочной сыворотки значительно улучшаются.
Рисунок 2.47.
Рисунок 2.47. – Содержание ионов минеральных веществ в зависимости от уровня деминерализации сыворотки
Таблица 2.35. Содержание микроэлементов в сухом веществе молочной сыворотки при различных уровнях деминерализации, мг %
| Уровень деминерализации сыворотки, % | микроэлементы | |||
| железо | медь | цинк | марганец | |
| 0 | 1,69 | 0,24 | 0,51 | 0,09 |
| 51 | 0,91 | 0,3 | 1,73 | 0,1 |
| 74 | 2,01 | 0,33 | 1,72 | 0,1 |
| 90 | 0,81 | 0,26 | 1,74 | 0,06 |
Таблица 2.36. Состав творожной сыворотки при различных уровнях деминерализации
| Уровень деминерализации, % | Массовая доля веществ, % | Кислотность, ˚Т | Степень раскисления | рН | Удельная электропроводимость,Ом/м | |
| сухих | минеральных | |||||
| 0 | 5,70±0,38 | 0,65±0,06 | 58±5 | 0 | 4,44±0,13 | 0,74±0,06 |
| 30 | 5,36±0,36 | 0,45±0,05 | 50±5 | 14 | 4,49±0,13 | 0,55±0,05 |
| 50 | 5,16±0,34 | 0,32±0,04 | 42±4 | 27 | 4,50±0,13 | 0,42±0,04 |
| 70 | 4,13±0,34 | 0,20±0,03 | 31±3 | 46 | 4,45±0,13 | 0,24±0,02 |
| 90 | 4,73±0,34 | 0,07±0,01 | 18±2 | 69 | 4,39±0,13 | 0,17±0,01 |
Процесс производства деминерализованной сыворотки начинают с предварительной очистки от молочного жира и казеиновой пыли традиционными способами. Затем сыворотку целесообразно подсгустить. Установлено, что при обессоливании натуральной сыворотки капитальные и производственные затраты выше, чем при обессоливании сгущенной сыворотки, на 15% при 59%-ном и на 30%—при 90%-ном уровне деминерализации. Сгущение сыворотки приводит к снижению энергозатрат на процесс ее обессоливания и на перекачивание насосами, а также к повышению рабочей плотности тока и, следовательно, скорости обессоливания.
Подсгущение сыворотки проводят до разной степени концентрации сухих веществ: 15—24, 50% и более. При сгущении до 50% и более из сыворотки необходимо удалять образующиеся кристаллы лактозы.
С помощью электродиализа можно деминерализовать молочную сыворотку до 90%-ного уровня. Однако с экономической точки зрения электродиализ оправдывает себя только при уровне деминерализации 70%. По данным фирмы SRTI, расход сыворотки при 90%-ном уровне обессоливания в 3,5 раза выше, чем при 50%-ном. При уровне деминерализации 90% и более обессоливание эффективнее осуществлять другими способами, например с помощью ионообменных смол.
Полученные методом электродиализа продукты часто, используются в качестве основы для заменителей женского молока. Для того чтобы приготовить молоко с необходимым соотношением сывороточного белка, казеина, лактозы, жира и минеральных солей, молочную сыворотку после электродиализа нужно смешать с переработанным этим же методом молоком, а также с лактозой и молочным жиром. Предлагается использование получаемого методом электродиализа продукта «Нутритек 250» (степень деминерализации 25%) при изготовлении мороженого и кондитерских изделий. «Нутритек 900» (степень деминерализации 90%) рекомендован для применения в производстве диетических, продуктов, парфюмерной промышленности и т. д. Химический состав этих двух продуктов, получаемых с помощью электродиализа, приводится в таблице 2.37.
Таблица 2.37. Химический состав продуктов, получаемых из молочной сыворотки методом электролиза
| Показатель | «Нутритек 250» | «Нутритек 900» |
| Белок, % | 11,5—14,0 | 13,0—15,5 |
| Лактозогидрат, % | 73—78 | 80 – 85 |
| Молочный жир, % | 0,6—0,9 | 0,6—0,9 |
| Вода, % | 4,2—4,8 | 4,5—5,0 |
| Зола, % | 5,0—5,5 | 0,7 – 1,0 |
| Натрий, % | 0,6 | 0,01 |
| Калий, % | 1,0 | 0,25 |
| Кальций, % | 0,7 | 0,15 |
| Магний, % | 0,09 | 0,003 |
| Фосфор, % | 0.5 | 0,14 |
| Хлорид, % | 0,4 | 0,05 |
| Цитрат, % | 1,9 | 0,2 |
| рН (10%-ного раствора) | 6,2—6,6 | 6,2—6,6 |
| Индекс растворимости, мл | <0,1 | <0,1 |
| Степень деминерализации, % | 25 | 90 |
В последнее время разрабатывается комбинированная технология, предусматривающая объединение методов электродиализа и ультрафильтрации. При этом получают сухой белковый препарат с максимальной концентрацией белка 35% и содержащий лактозу деминерализованный ультрафильтрат. В зависимости от используемого оборудования производственные потери в процессе электродиализа могут составить 10%. Поэтому с недавнего времени применяется также комбинирование электродиализа с ионообменной хроматографией. При этом содержание минеральных солей в молочной сыворотке путем электродиализа снижается только на 50%. Считается, что расход энергии на 1 кг деминерализованной молочной сыворотки составляет 10—28 кВт∙ч.
Мембраны
Наиболее специфическим и важным компонентом мембранного оборудования являются мембраны. От их свойств в большой степени зависят качественные показатели получаемых продуктов, надежность и долговечность мембранного оборудования, а также экономическая целесообразность его применения.
Мембранные процессы основаны на использовании полупроницаемых мембран, обладающих способностью селективно (избирательно) пропускать или задерживать компоненты разделяемой жидкой смеси.
Мембраны, которые можно применять в молочной промышленности, должны отвечать определенным требованиям: высокой удельной производительностью (проницаемостью); хорошей задерживающей способностью (селективностью) по отношению к высокомолекулярным веществам молока и молочной сыворотки (белок, жир); низкой селективностью по отношению к низкомолекулярным компонентам (лактозе); достаточной механической прочностью, отвечающей условиям монтажа, транспортировки и хранения; устойчивостью к действию среды разделяемой системы и ее компонентов; стабильностью основных характеристик в процессе эксплуатации; возможностью регенерации их свойств с помощью различных моющих средств; возможно низкой стоимостью. Электродиализные мембраны, кроме того, должны обладать высокой проницаемостью для ионов (катионов или анионов в зависимости от полярности мембраны) и в то же время высокой сопротивляемостью свободной диффузии электролита; минимальным омическим сопротивлением во избежание высоких затрат электроэнергии на его преодоление при прохождении электрического тока через мембрану.
Полупроницаемые мембраны для ультрафильтрации изготавливают из полимерных материалов. Они имеют тонкий (около 0,25 мкм) поверхностный слой (так называемый «активный слой») и микропористую подложку (матрицу) из того же полимера толщиной примерно 50 мкм. Для придания повышенной механической прочности мембрану дополнительно армируют нетканой подложкой из пористого полимера (рис. 2.48.)
Для ультрафильтрации молочного сырья созданы два типа полупроницаемых мембран: ацетатцеллюлозные (первое поколение) и полисульфонамидные на подложке из электроизоляционной бумаги (второе поколение).
Техническая характеристика мембран
|
| Мембраны | |
| Ацетатцеллюлозного типа УАМ | Полисульфонамидные на подложке типа УМП-II | |
| рН среды | 3 – 8 | 1 – 13 |
| Температура среды, ˚С | 0 – 55 | 0 – 90 |
| Давление, МПа | До 0,7 | До 0,7 |
| Средняя проницаемость при обработке молочного сырья (Р=0,3 МПа), л/м2/ч: | ||
| Т=50 ˚С | 35 – 40 | 40 – 45 |
| Т=10 ˚С | 8 – 10 | 8 – 10 |
| Селективность, %: | ||
| По белку | 90 – 92 | 92 – 95 |
| По лактозе | 8 – 10 | 6 – 8 |
| Гарантийный срок, месяцев: | ||
| До эксплуатации | 6 | 12 |
| При эксплуатации | 6 | 12 |
| Оптовая цена, руб/м2 | 8,5 | 15 |
Ацетатцеллюлозные мембраны имеют низкую механическую прочность, так как изготавливаются без армирующей подложки, и недостаточную термохимическую стойкость. При их мойке предусмотрено использовать дорогостоящий ферментный препарат панкреатин, поэтому при переработке молочного сырья предпочтение отдают полисульфонамидным мембранам на подложке. Мембраны поставляют потребителям в виде рулона, помещенного в герметично запаянный полиэтиленовый пакет, внутрь которого залит консервант, в ящике из гофрированного картона. Длина намотки ленты составляет 50 м, ширина — 400 — 420 мм.
Рисунок 2.48.
Рисунок 2.48. — Анизотропная мембрана: а — без армирующей подложки; б — с подложкой; 1 — активный слой (полупроницаемый); 2 — матрица (поддерживающий дренажный слой); 3 — армирующая подложка
Мембраны третьего поколения, изготовленные на основе окиси циркония и других металлосодержащих веществ с подложкой из графита и выдерживающие температуру до 400 °С и воздействие различных моющих химических веществ.
Следует отметить, что как мембраны, так и конструкции мембранных установок постоянно совершенствуются.
Для осуществления процессов гиперфильтрации используются аппараты типа «фильтр – пресс», трубчатые, спиральные. В аппаратах типа «фильтр – пресс» используются мембраны в виде пластин с набором в модули. Трубчатые и спиральные аппараты создаются на основе рулонных или волокнистых мембран.
По конструкции установки отечественного производства относятся к установкам фильтр – прессового типа непрерывного действия. Налажен выпуск ультрафильтрационных установок А1-ОУС производительностью 5000 л/ч для обработки подсырной сыворотки, А1-ОУВ производительностью 2000 л/ч—для обработки обезжиренного молока, А1-ОУП производительностью 2000 л/ч—для обработки молочной сыворотки.
Мембранный модуль — это основной элемент ультрафильтрационного аппарата. В установке А1-ОУС используют модули двух типоразмеров с рабочей поверхностью 7,7 и 3,6 м2. Первый из них содержит 53 фильтрующих элемента и 54 эластичные прокладки, второй — соответственно 25 и 26. В аппарате первые четыре секции компонуют из модулей .первого типоразмера, две последние— из второго (рис. 2.49.).
Рисунок 2.49.
Рисунок 2.49. – Принцип конструкции модуля ультрафильтрационных установок А1-ОУС и А1-ОУП: а — модуль; б — фильтрующий элемент; 1 — прижимная плита; 2 — прокладка; 3 — опорная пластина; 4 — дренаж; 5 — мембрана; 6 — уплотнительная вставка
Фильтрующие элементы включают опорные пластины, изготавливаемые из ударопрочного полистирола методом литья, дренажный материал из лавсанового нетканого материала, уплотнительные вставки, отливаемые из пищевой резины, и полупроницаемые мембраны. Эластичные прокладки также делают из пищевой резины. Другие ультрафильтрационные установки имеют аналогичное устройство.
Перед гиперфильтрацией, так же как и перед гель-фильтрацией, сыворотку осветляют центрифугированием или фильтрованием. Для получение микробиологически чистых продуктов сыворотку подвергают пастеризации при температуре 60 – 65 ˚С.
Производительность мембран зависит, помимо размеров пор, также от давления фильтрации и температуры продукта (рис. 2.50. и 2.51.).
Рисунок 2.50.
Рисунок 2.50. – Зависимость проницаемости мембран по творожной сыворотке при температуре 20 ˚С от давления: 1, 2, 3, 4, 5, 6 – зависимость соответственно для мембран «Альбопор-200», УМП-50, «Альбопор-100», УАМ-500, УАМ-250, УАМ-200.
Рисунок 2.51.
Рисунок 2.51. – Зависимость проницаемости мембран по творожной сыворотке при давлении 0,4 МПа от температуры: 1, 2, 3, 4 – зависимость соответственно для мембран УМП-500, «Альбопор-200», УАМ-500, «Альбопор-100».
Из приведенных рисунков видно, что с повышением рабочего давления производительность мембран возрастает но по достижении определенного уровня (максимально допустимого давления фильтрации) рост ее прекращается. Производительность мембран типа УАМ при дальнейшем повышении давления до некоторой величины (критической величины давления фильтрации) резко снижается. Многими исследователями отмечено, кроме того, что даже при давлении в пределах максимального (0,3—0,4 МПа) мембраны типа УАМ снижают производительность до 50% в течение 2 ч работы. За это время, происходит их усадка, и только по истечении его эти мембраны приобретают свои стабильные характеристики (производительность и селективность). Мембраны типа УПМ не имеют критических давлений фильтрации. Это свидетельствует о том, что они отличаются более жесткой крупнозернистой структурой. Однако и эти мембраны на первоначальной стадии работы дают усадку (коэффициент усадки — 0,35 — 0,40).
Повышение температуры фильтрации от 20 до 50 °С способствует увеличению производительности мембран на 80—90 % (за счет уменьшения вязкости раствора и интенсификации броуновской диффузии молекул раствора), поэтому эффективнее вести процесс ультрафильтрации при более высоких температурах.
С точки зрения сохранности нативных свойств молочного сырья, а также получения концентратов и фильтратов с хорошими микробиологическими показателями температуру 50—55 °С можно рекомендовать как наиболее оптимальную при ультрафильтрации молока, пахты, молочной сыворотки.
Большое значение для надежной работы мембранной техники, имеет эффект очистки мембран от загрязнений, образующихся в процессе концентрации молочного сырья. Моющие средства и режимы мойки подбирают с учетом физико-химических свойств используемых мембран, а также свойств других конструкционных материалов установок. Осадок, образующийся на ультрафильтрационных мембранах, состоит из белковых веществ молока или сыворотки.
Возможные способы очистки оборудования для гиперфильтрации (обратного осмоса) включают следующие основные процессы:
промывка водой;
промывка раствором детергента;
удаление протеина раствором, содержащим протеолитические ферменты;
повторная промывка водой;
периодическая промывка кислотой для удаления осадка нерастворимых фосфатов;
дезинфекция растворами гипохлорита (содержание активного хлора 5—200 мг/л), четвертичными соединениями аммония (20 г/л) и иодофора (100 мг/л активного иода). Тщательная очистка необходима потому, что хотя полупроницаемые мембраны не пропускают микробов, последние могут развиваться на обращенной к фильтрату стороне мембраны. При этом отдельные микроорганизмы используют для своего питания ацетилцеллюлозу и тем самым повреждают мембраны. В ГДР разработан и запатентован метод очистки и дезинфекции оборудования для ультрафильтрации и обратного осмоса. Мембраны не из целлюлозы (в частности, мембраны из полиамидов, полиимидов, полисульфона, полиакрилнитрила и поливинилхлорида) очищают также 0,5%-ным раствором NaOH при 75 °С в течение 45 мин.
Спиральные трубчатые мембраны НFМ-100 из резистентных , полимеров фирмы «Аbcor» (рис. 2.52.) весьма эффективно очищают и дезинфицируют щелочным раствором (рН 10,0—10,5; 200— 1000 мг/л активного хлора) с последующей промывкой раствором Н3РО4 (рН 2,0). Затем мембраны дезинфицируют раствором NaOCl.
Рисунок 2.52.
Рисунок 2.52. – Спирально-трубчатые мембраны фирмы «Аbcor»: 1 — молочная сыворотка; 2 — перфорированная трубка; 3 — устройство для фиксации мембран; 4 — концентрат; 5 — ультрафильтрат; 6 — мембраны; 7 — полость для сбора ультрафильтрата; в - сетчатая пленка; 9 – кожух; 10 — поток ультрафильтрата; 11— поток сыворотки через разделительный слой.
ВНИКМИ совместно со Всероссийским научно-исследовательским институтом поверхностно-активных веществ (ВНИИПАВ) разработаны моющие средства и композиции для мойки и дезинфекции мембран, а также инструкции по их применению. По окончании работы установку промывают водой от остатков продукта, 0,8—1%-ным раствором щелочного моющего средства РОМ-САФ-1 температурой 55—57°С в течение 60 мин, водой от остатков щелочного раствора. Затем ее дезинфицируют 0,005— 0,01%-ным раствором гипохлорита натрия температурой 20—30 °С в течение 10 мин и вновь ополаскивают водой в течение 5 мин. Непосредственно перед пуском установки после длительного (свыше 6 ч) перерыва вновь дезинфицируют мембраны. Один раз в 3 дня после щелочной мойки и ополаскивания водой промывают мембраны 0,3%-ным раствором азотной или фосфорной кислоты температурой 55—57 °С в течение 30 мин, затем дезинфицируют, как указано ранее.
При длительной эксплуатации установок и концентрировании сыворотки до содержания сухих веществ 24—26% необходимы более жесткие условия мойки. Кроме того, следует иметь в виду, что при концентрации сухих веществ происходит и концентрация микробных клеток, а температура окружающего воздуха способствует их быстрому росту. С целью поддержания необходимого санитарно-гигиенического уровня ультрафильтрационного оборудования ежедневно после мойки рекомендуется проводить его дезинфекцию. В качестве дезинфицирующих средств предпочтение следует отдавать дихлоризоцианурату натрия. Этот дезинфектант не влияет на свойства мембран, их производительность. Активного хлора в нем содержится до 65%, поэтому на приготовление 1 т раствора требуемой концентрации (0,005%) достаточно 50 г вещества. Дезинфектант обладает бактерицидностью не только к вегетативным формам бактерий, но и к споровым, а также к плесеням и дрожжам. Данный препарат является сильно концентрированным веществом, поэтому при работе с ним необходимо предусматривать соответствующие меры предосторожности.
Раствор гипохлорита натрия с концентрацией 0,02—0,03% — также довольно эффективное вещество. Применение растворов хлорной извести запрещается, так как соединения кальция обладают способностью к осаждению на мембранах.
Несмотря на то, что мембраны второго поколения (типа УПМ) можно эксплуатировать при повышенных температурах (до 90— 100 °С), температуру моющих растворов следует поддерживать в пределах 55—58 °С в связи с низкой термостойкостью опорных пластин установок, изготовленных из полимерного материала— полистирола.
Одним из факторов стабильной работы ультрафильтрационных установок является предотвращение образования на поверхности мембран малорастворимых солей кальция (сульфатов, карбонатов), гидроокисей железа и марганца, выпадающих в осадок из воды повышенной жесткости. Отложения солей на поверхности мембран резко ухудшают показатели их работы, уменьшают эффективную фильтрующую поверхность, снижая тем самым их проницаемость. Чаще всего на мембранах встречаются отложения соединений железа.
Разработчики мембран в нашей стране предъявляют определенные требования к показателю карбонатной жесткости воды (не более 0,02 мг∙экв/л). ВНИКМИ разработаны временные рекомендации по водоподготовке в процессах ультрафильтрации молочного сырья. Выбор методов обезжелезивания воды, расчетных параметров и доз реагентов производят на основе результатов технологических исследований. Воду обезжелезивают по специальной технологии фильтрованием в сочетании с одним из способов ее предварительной обработки: упрощенной аэрацией или аэрацией. Для устранения карбонатной и некарбонатной жесткости проводят натрий-катионитовое умягчение обезжелезенной воды. С этой целью используют серийно выпускаемую водоподготовительную установку ВПУ-5. В качестве загрузки применяют сильнокислотный катионит КУ-2-8. Для очистки воды от механических примесей, в том числе и катионитовой пыли, целесообразно в схему водоподготовки вводить фильтр для очистки воды 11 4ВМ-2,5-001 или 11 4ВМ-2,5-002.
Тщательное выполнение перечисленных требований обеспечивает длительную эксплуатацию ультрафильтрационных мембран при хорошей их работе, что гарантирует получение продуктов высокого качества.
Для электродиализной обработки молочного сырья используют два типа ионоселективных мембран, изготовляемых Щекинским химическим комбинатом. Их техническая характеристика представлена в табл. 2.38.
Таблица 2.38. – Техническая характеристика ионоселективных мембран
| Показатель | I тип | II тип | ||
| Катионитовая МК-40к | Анионитовая МА-40к | Катионитовая МК-40л | Анионитовая МА-41л | |
| Удельное поверхностное сопротивление, Ом/см2 | 6 | 6 | 10 | 10 |
| Сопротивление продавливанию, нс/м | 11,4 | 11,4 | 15,6 | 15,6 |
| Селективность по NaCl, % | 93 | 93 | 98 | 98 |
| рН обрабатываемой среды, ед. | 1 – 14 | 1 – 14 | 1 – 14 | 1 – 14 |
| Температура среды, ˚С | 0 – 55 | 0 – 55 | 0 – 55 | 0 – 55 |
| Срок службы, месяцев | 18 | 18 | 18 | 18 |
Гельфильтрация
Гельфильтрацию применяют для фракционирования сложных биологических систем на молекулярном уровне в целях получения отдельных компонентов в нативном состоянии.
В качестве молекулярного сита используют гидрофильные гели — сефадексы: модифицированные декстраны микробиологического происхождения, полиакриламид, агарозу и др. Благодаря множеству гидро-ксильных групп в сетеподобной полисахаридной структуре сефадексы сильно набухают в воде и водных растворах. Гели представляют собой неионные материалы, поэтому их можно применять для разделения заряженных и электронейтральных веществ.
В настоящее время известно несколько видов порошкообразных гелей, состоящих из микроскопических гранул. Структура каждого вида геля характеризуется степенью плотности поперечных связей частиц. Наиболее широкое применение получили декстрановые гели "Сефадекс" (Швеция). На "Сефадекс" разделяют глобулярные белки с молекулярной массой 700—800 тыс. ед. Гели "Молселект" (Венгрия) по свойствам близки к декстрановым "Сефадекс". На основе полиакрила-мида выпускают гели "Акрилекс" (Венгрия) и "Биогель" (США), которые по свойствам близки "Сефадекс". Гели на основе агарозы, например "Сефароза" (Швеция), используют для разделения веществ с молекулярной массой более 800 тыс. ед. Синтезирован новый вид гелей — ксерогели (пористые стекла), представляющие собой малонабухающие полимеры. В нашей стране создаются отечественные гели и осваивается их промышленное производство.
Процесс гелевой фильтрации осуществляется за счет вымывания частиц разделяемого раствора через слой набухшего геля растворителем (водой). Большие молекулы, не проникая в поры геля, свободно проходят с потоком растворителя. Более мелкие молекулы распределяются в жидкой среде снаружи и внутри гелевых частиц. Молекулы, находящиеся внутри геля, элюируются медленнее. Молекулы среднего размера элюируются позднее крупных, но раньше мелких молекул. Следовательно, компоненты раствора выходят из колонки соответственно убыванию их молекулярной массы (рис. 2.53.)
Рисунок 2.53.
Рисунок 2.53. – Принцип разделения при гель-фильтрации; три стадии одного процесса: 1 — декстрановый гель (зерна шарообразной формы, полимеризированный); 2 — сывороточные белки (макромолекулы); 3 — вода, минеральные соли, лактоза и низкомолекулярные азотсодержащие вещества (НБА)
Теоретически молочная сыворотка является идеальной средой для гелевой фильтрации, так как относится к гетерогенным растворам сложного состава. Исходя из состава сыворотки и свойств геля, при осуществлении процесса следует ожидать выход белков, затем лактозы и минеральных солей.
Экспериментальные исследования, проведенные во ВНИИМС, подтвердили, что гелевая фильтрация — эффективный, метод разделения компонентов молочной сыворотки. Крупномолекулярная белковая фракция выделяется при этом практически в чистом виде. Удовлетворительно разделяются средне- и низкомолекулярные азотистые соединения — полипептиды, пептиды и небелковые азотистые компоненты.
Лактоза и минеральные вещества хотя и выделяются последовательно, но с наложением зон друг на друга. Поэтому для их разделения необходимо использование дополнительных методов разделения — ультрафильтрации и электродиализа.
Максимальная производительность, достигнутая при использовании декстрановых гелей, составляет 500 кг/ч через 1 м2 поперечного сечения колонки. Степень очистки белка от лактозы составляет 99%, степень разбавления белковой фракции - не более чем в 1,5 раза. При этом длина колонки должна составлять около 4 м.
Известно, что для разделения сыворотки с препаративными целями и в индустриальном масштабе в мировой практике применяется, однако, исключительно сефадекс Ж-25 грубого зернения.
В отличие от других методов гель-фильтрация на колонках позволяет добиться полного разделения ингредиентов низкомолекулярной фракции в ходе одного рабочего цикла. В апробированных до настоящего времени пилотных и промышленных установках, которые управляются автоматически с помощью фотометрического измерения экстинкции элюата, получают сывороточный концентрат с содержанием белка 40—80%.
В настоящее время выпускают белковые продукты: Енр-Ро (добавка к хлебобулочным изделиям), Енр-Екс (заменитель сухого обезжиренного молока), Енр-Про (высокобелковый продукт общего назначения) и 99%-ная чистая лактоза Енр-Лак.
Стандартный состав белковых концентратов, полученных с помощью гель-фильтрации, представлен в таблице 2.39.
Для сравнения ниже приводятся данные о химическом составе двух продуктов шведского производства, полученных при использовании техники колоночного разделения и содержащих соответственно белка 54,1 и 71,2%; лактозы 32,7 и 14,1, золы 4,2 и 2,0, жира 3,5 и 5,0, воды 5,0 и 7,0%.
Сам процесс выделения белка относительно прост, но для проведения гель-фильтрации необходим ряд вспомогательных операций, что удорожает метод.
Предварительное и заключительное концентрирование путем сгущения под вакуумом — наиболее трудоемкие этапы, поэтому гель-фильтрацию комбинируют с ультрафильтрацией и обратным осмосом.
Таблиц 2.39 .- Химический состав трех белковых концентратов, полученных в промышленных условиях из молочной сыворотки с помощью гель-фильтрации
| Химический состав | Енр-Про 50 | Енр-Экс | Енр-Ро |
| Белок (N×6,38), % | 54,2 | 18,0 | 15,8 |
| Лактоза, % | 24,6 | 40,6 | 36,5 |
| Зола, % | 14,0 | 25,6 | 33,9 |
| Вода, % | 3,1 | 2,2 | 2,5 |
| Жир, % | 2,0 | 0,1 | 1,3 |
| Лактат, % | 3,3 | 7,7 | 4,0 |
| Цитрат, % | 1,7 | 4,5 | 3,0 |
| рН (3%-ный раствор) | 7,2 | 7,3 | 6,9 |
| Энергетическая ценность, кДж/100 г | 1478,0 | 1214,0 | 1084,0 |
| PER* (скорректированное) | 3,2 | 2,4 | 2,5 |
Как показывают исследования по изучению влияния состава наносимых на гелевую колонку проб, при проведении гель-фильтрации как в лабораторных, так и в промышленных условиях перед нанесением проб на колонку из них требуется удалять молочный жир, преципитированный казеин и фосфат кальция (после нейтрализации его Са(ОН)2). Сыворотка перед гель-фильтрацией должна быть сконцентрирована до вязкости 2,3— 2,5 мПа-с. При большей вязкости проб зоны разделения получаются нестабильными, пики различных веществ перекрываются, значительно снижается скорость прохождения жидкости через колонку. По этой же причине перед гель-фильтрацией требуется частично удалять из сыворотки молочный сахар.
Очистка и дезинфекция оборудования для гель-фильтрации не представляет затруднений. Гель устойчив в широком диапазоне рН и температур, его можно автоклавировать при 120°С в течение 30 мин. Ежедневная очистка осуществляется с применением 0,1-и 1%-ного раствора NаОН при 60°С (в зависимости от типа геля), примерно через 200 ч работы геля он обрабатывается 0,8—1,0%-ным раствором НNОз. При обработке кислотой удаляются соли кальция, в результате чего содержание Са в геле снижается с 3,5 до 0,01%. При этом структура геля остается стабильной и он сохраняет свои разделительные свойства. Срок службы геля значительно выше срока использования мембран. Тем не менее, как об этом можно судить на основании литературных данных, гель-фильтрация не нашла еще широкого применения в мировой практике. Продолжительность использования геля может составлять до 5000 ч рабочего времени. Затраты на получение 75%-ного белкового концентрата примерно в четыре раза выше, чем при получении порошка с 40%-ным содержанием белка. Производство значительно удорожается из-за необходимости предварительной концентрации сыворотки, отделения лактозы и высушивания. Кроме того, стоимость конечного продукта зависит от дальнейшего использования низкомолекулярных фракций элюата, хотя имеются различные возможности повышения экономической эффективности, в частности использование конечного продукта для откорма сельскохозяйственных животных.
Промышленная установка в Швеции позволяет перерабатывать 3,7 т сыворотки в час с получением белкового продукта, содержащего 75 % белка.
Молочная сыворотка очищается от взвешенных частиц казеина и жира, сгущается до 18-20% сухих веществ, еще раз сепарируется и охлаждается до 8 ˚С. Полученный концентрат может храниться до 15 ч. Перед гельфильтрацией концентрат многократно обрабатывается на специальных фильтровальных блоках для удаления мельчайших частиц взвесей и нагревается до 75 °С. В процессе гелевой фильтрации сыворотка разделяется на две фракции: с высокой молекулярной массой (белки) и низкой (лактоза и соли). Высокомолекулярную фракцию сгущают и сушат распылением. Производительность установки по готовому продукту составляет 28 кг/ч. Продукт имеет хорошую растворимость (86-95%) и используется в производстве детских и диетических продуктов для улучшения взбиваемости и желирования, а также безалкогольных напитков.
Для исключения недостатков технологии всех гелей (использование небольшого объема насадки разделяемого раствора, длительность цикла и разбавление водой) разработан усовершенствованный метод (С. Морр, США), суть которого заключается в том, что сефадексы вносят в разделяемый раствор, тщательно перемешивают, центрифугируют или фильтруют. Каждый грамм сухого сефадекса поглощает 2,5 г раствора. Однократное проведение операции позволяет сконцентрировать раствор примерно в три раза. При необходимости цикл повторяют.
В настоящее время из-за довольно высокой стоимости гелей, их относительно низкой стойкости и периодичности процесса разделения гельфильтрация не нашла широкого промышленного применения.
Сорбция – десорбция
Извлечение из молочной сыворотки белковых веществ, небелковых азотосодержащих и красящих соединений возможно осуществлять, исходя из принципов сорбционных процессов. В качестве сорбентов используются активированные угли, синтетические смолы и природные сорбенты.
Процесс сорбции включает адсорбцию, абсорбцию и хемосорбцию. При обработке молочной сыворотки, когда хотят извлечь определенные компоненты, необходимо осуществлять процесс адсорбции и последующей десорбции с поверхности сорбента.
Адсорбционные процессы используются в молочной промышленности для очистки воды, при производстве рафинированного молочного сахара и проведении некоторых химических анализов молочных продуктов.
В последние годы появились сообщения о реализации сорбционных процессов для получения чистых сывороточных белков, некоторые из них более подробно рассматриваются ниже.
Процесс "Вистек". Этот процесс разработан английской фирмой "Koch-Light. Lab. Limited". Для осуществления процесса используется специальная ионообменная целлюлоза, известная под названием "среда Вистек".- Процесс осуществляется в динамике (рис. 2.54.) и включает следующие операции:
поступление молочной сыворотки в реактор и перемешивание со средой при низких рН;
отделение депротеинизированной сыворотки (элюата) через фильтрующую сетку;
промывка сорбента с белком водой;
заполнение реактора раствором с высоким рН и перемешивание;
отделение белкового раствора от сорбента с последующим его извлечением.
Полученный раствор нативных белков молочной сыворотки концентрируется методом ультрафильтрации и высушивается распылительным способом.
Полученный продукт отличается большой степенью чистоты (97 % белка) и состоит в основном из а-лактоальбумина и ß-лактоглобулина. В продукте присутствует около 2 % лактозы и только 0,2 % молочного жира. Минеральный состав продукта включает (в %): Nа — 1,05, К – 0,009, Са – 0,12, Мg – 0,012, С1 – 0,24, РО4 – 0,09.
Аминокислотный состав (относительное распределение) продукта "Вистек" (в %) следующий:
| Аланин | 5,6 | Валин | 5,3 |
| Аргинин | 3,2 | Изолейцин | 5,3 |
| Аспарагин | 11,8 | Лейцин | 11,5 |
| Цистин | 2,6 | Лизин | 10,2 |
| Глутаминовая кислота | 16,5 | Метионин | 2,6 |
| Глицин | 2,4 | Фенилаланин | 2,1 |
| Гистидин | 2,4 | Пролин | 6,1 |
| Тирозин | 2,3 | Серин | 4,7 |
| Треонин | 5,5 |
Рисунок 2.54.
Рисунок 2.54. – Схема производства из молочной сыворотки белкового продукта "Вистек": 1 – резервуар для исходной сыворотки; 2 – реактор; 3 – промежуточный резервуар; 4,5 – резервуары для кислоты и щелочи; 6 — резервуар для продукта
Обращает на себя внимание высокое содержание лизина, лейцина и аспарагина. Продукт полностью растворяется в воде, дает прозрачный раствор, хорошо сбивается, образуя пену наподобие яичной, и при температуре 60 °С образует устойчивый гель. Рекомендуется в качестве наполнителя и обогатителя для макарон, тортов и колбас.
Отмечая принципиальную возможность извлечения белков из молочной сыворотки сорбцией — десорбцией, следует обратить внимание на сложность процесса, необходимость решения проблемы использования элюата и значительный расход воды.
Процесс "Сферосил". Этот процесс разработан французской фирмой "Rhone-Pouienc". Для осуществления процесса используют специальные сорбенты ионогенного характера на основе "кремнезема в виде мельчайших шариков. Процесс совмещает гель- и аффинную хроматографию. Сорбенты получают путем фиксации на сферосиле ХОВ 015 различных ионообменных групп.
Известны четыре группы ионообменных сорбентов: сферосил DEA – слабый щелочной ионообменник; сферосил QMA — сильный щелочной анионообменник; сферосил С - слабый кислотный катионообменник; сферосил S — сильный кислотный катионообменник. Объем пор у этих ионообменных сорбентов составляет 0,8-1 см3/г; удельная поверхность 25 м2/г; средний диаметр пор до 125 нм (1250Å). Следовательно, пористость такова, что молекулы сывороточных белков легко проникают внутрь сорбента и сорбируются на функциональных группах. В то же время мицеллы казеина, микроорганизмы, молочный жир не могут проникнуть в структуру сферосила и остаются в элюате молочной сыворотки.
Жесткий каркас сферосила (кремнезем) исключает набухание частиц, их пористость не зависит от ионной силы и рН молочной сыворотки. К тому же сферическая форма не создает значительных гидродинамических сопротивлений.
Применение сферосила позволяет получать неденатурированные белки молочной сыворотки с чистотой на уровне 90%, а также селективно разделять их по фракциям.
Принципиальная схема извлечения белков из молочной сыворотки включает следующие основные операции. Молочную сыворотку пропускают через реактор (ионообменную колонку), содержащий сферосил. Белки сорбируются сферосилом. Реактор промывают водой для удаления остатков молочной сыворотки. Затем из сферосила вымывают белок, причем из анионообменных колонок его вымывают кислым раствором, а из катионообменных – щелочным. После этого реактор промывают водой для удаления вымывающего раствора и рабочий цикл повторяется. Если необходимо извлечь фракции белков, процесс проводят в двух или более последовательно соединенных колонках: одна – с анионообменным сферосилом, другая — с катионообменным.
Технологическая схема извлечения белков из подсырной сыворотки с помощью сферосил приведена на рис. 2.55.
Осветленная (менее 0,2 г/л казеиновой пыли) и обезжиренная (менее 0,2 г/л молочного жира) сыворотка с рН на уровне 6,6 (белки находятся в анионной форме) пропускается через колонку с сильным анионообменником – сферосилом QМА. Расход сыворотки должен в 10 раз превышать объем колонки. На анионообменнике сорбируется 87 - 90 % белков молочной сыворотки (основное количество). Затем эту же сыворотку, лишенную большей части белков, пропускают через вторую колонку, соединенную последовательно с первой, которая заполнена слабым катионообменником – сферосилом ХОВ 015. Во второй колонке сорбируется 7 - 10 % остаточных белков молока, в основном иммуноглобулнна.
Из первой колонки белки вымывают разбавленной соляной кислотой, из второй колонки - аммиачным раствором.
За сутки можно провести 10-12 циклов обработки молочной сыворотки.
Установка, содержащая 600 кг сферосила QМА, позволяет обрабатывать за один цикл до 10 т подсырной сыворотки, содержащей 6 г/л белка. После вымывания белка из колонки со сферосилом QМА получают 700 л концентрата (элюата), содержащего в 1 л 60 г белков, а из колонки со сферосилом ХОВ 015 - 95 л концентрата (элюата), содержащего в 1 л 40 г белка.
Рисунок 2.55.
Рисунок 2.55. – Схема производства белков с использованием сферосила из подсырной (сладкой) сыворотки: 1 - резервуар для исходной подсырной сыворотки; 2 - колонка со сферосилом QМА; 3 - колонка со сферосилом ХОВ 015; 4 - резервуар очищенной от белков молочной сыворотки; 5 - емкость для раствора NН4ОН; 6 - емкость для раствора НCl; 7 - емкость для циркулируемого раствора реагентов; 8 - резервуары для сбора концентрата белков
Получаемые из обеих колонок концентраты содержат указанное количество нативных сывороточных белков и по 0,5 % лактозы и жира.
Изучение процесса показало, что по истечении двух лет ухудшения свойств сферосила не наблюдается.
Технологическая схема извлечения белков из творожной сыворотки показана на рис. 2.56.
Кислая очищенная от взвесей и жира молочная сыворотка с рН на уровне 4,5 пропускается через колонку со сферосилом 5. Белки, находящиеся в катаонной форме, полностью сорбируются. За сутки осуществляется 10-12 циклов. При наличии в колонке 450 кг сферосила 8 обрабатывается до 10 тыс. л творожной сыворотки, содержащей в 1 л до 62 г белка. Из колонки получается 1200 л концентрата (элюата), содержащего в 1 л 45 г белка. Концентрат, кроме белков, содержит 0,5 % лактозы и 0,5 % молочного жира.
Рисунок 2.56.
Рисунок 2.56. – Схема производства белков с использованием сферосила из творожной (кислой) сыворотки: 1 – резервуар для исходной творожной сыворотки; 2 – колонка со сферосилом; 3 – резервуар очищенной сыворотки; 4 – резервуар для концентрата белков; 5 – емкость для раствора NН4OН
Состав получаемых продуктов приведен в табл. 2.40
Таблица 2.40.
| Массовая доля, % | Содержание | ||
| В подсырной сыворотке | В творожной сыворотке белка сферосила | ||
| Белок сферосила МА | Белок сферосила ХОВ 015 | ||
| Сухие вещества | |||
| Белковый азот | 2,3 | 12,7 | 13,8 |
| Зола | 2,5 | 3,7 | 2,2 |
| Лактоза | 0,5 | 0,5 | 0,5 |
| Жир | 0,5 | 0,5 | 0,5 |
| Вода | 9 | 9 | 6 |
| Минеральные вещества | |||
| Кальций | 0,7 | 1,1 | 0,8 |
| Фосфор | 0,5 | 0,8 | 0,6 |
| Натрий | 0,08 | 0,02 | 0,04 |
| Калий | 0,06 | 0,07 | 0,03 |
| Магний | 0,04 | 0,05 | 0,03 |
Коэффициент набухаемости продукта составляет 550 – 650, время набухания 4 мин при 80 °С.
Считается, что получаемый продукт полностью заменяет белок яиц и стоит в 2 раза дешевле его. Предназначен для продуктов детского и диетического питания, а также безалкогольных напитков.
Технологические схемы с использованием сферосила позволяют обрабатывать другие виды молочной сыворотки, в том числе после деми-нерализации и сгущения. При этом количество сорбируемых сферосилом сывороточных белков увеличивается.
Оценивая использование сферосил, следует отметить, что хотя получаемый фильтрат может быть использован для получения лактозы, однако не исключено его загрязнение реагентами. Кроме того, для осуществления процесса необходимо значительное количество промывных вод.
Ионный обмен
Одним из способов регулирования солевого и кислотного составов молочной сыворотки является ионный обмен. При этом сохраняется ценность, улучшаются функциональные свойства сыворотки и вкусовые характеристики.
Сущность ионного обмена заключается в том, что при определенных условиях между твердым телом (ионообменная смола) и раствором, содержащим нежелательные примеси, происходит обмен ионов в результате которого твердое тело сорбирует ион из раствора, отдавая в него также ион, менее вредный для основного производства (рис. 2.57.).
Рисунок 2.57.
Рисунок 2.57. – Схема ионообменной установки для переработки молочной сыворотки: 1— поступление молочной сыворотки (10 ˚С); 2 — деминерализованная (95%) молочная сыворотка; 3 — устройство для измерения рН или электропроводности; 4 — деминерализованная молочная сыворотка; 5 — катионит; 6— анионит
Молочную сыворотку пропускают вначале через катионит, а затем через анионит. Катионит связывает катионы присутствующих в молочной сыворотке минеральных солей, при этом выделяются соответствующие кислоты, анионы которых связываются анионитом.
Гетерогенный обмен на ионите R с исходным зарядом ZR и переходным ZX противоиона А с зарядом ZA на ион В с зарядом ZB можно записать в виде следующего уравнения:

 ZBAZRRZA + (ZAZR/ZX)BZXXZB = ZABZRRZB + (ZBZR/ZX)AZXXZA
ZBAZRRZA + (ZAZR/ZX)BZXXZB = ZABZRRZB + (ZBZR/ZX)AZXXZA
Черта над формулой означает ионит, отсутствие черты - раствор, Если обмен в системе ионит — раствор протекает с участием нескольких, например п ионов, для его описания достаточно n — 1 независимых стехиохимических уравнений.
Иониты — это природные или синтетические многовалентные электролиты, структурно они состоят из жесткого каркаса (матрицы) и функциональных групп, достаточно прочно связанных с матрицей химическими связями.
В зависимости от заряда иониты классифицируют на катиониты (отрицательный заряд), аниониты – положительный заряд и амфолиты, содержащие в составе катионы (Н+) и анионы (ОН-).
После прохождения через обе колонки с ионообменниками эффективность деминерализации молочной сыворотки в зависимости от ее вида составляет 90 — 99%. Для производства некоторых продуктов желательна меньшая (50 — 60%) степень деминерализации. В этих случаях деминерализованная сыворотка автоматически смешивается в соответствующих пропорциях (регуляция по величине рН) с необработанной. Для организации непрерывного производства необходимо иметь в эксплуатации две установки для деминерализации, чтобы при работе одной иметь возможность регенерировать другую. Ионообменники должны автоматически регенерироваться после каждого рабочего цикла. Катионит регенерируют НС1 по принципу противотока. Деиони-зированную воду для последующей промывки берут из сборника конденсата выпарной установки. Для регенерации анионита используют растворы Na2CO3 или NH4OH.
В настоящее время в Европе работает более 20 установок этого типа для деминерализации подсырной и творожной сыворотки (во Франции, Бельгии, Швейцарии и Великобритании).
Обессоливание предварительно очищенной от белков молочной сыворотки с использованием ионного обмена достаточно полно изучено применительно к производству молочного сахара.
Деминерализация натуральной молочной сыворотки применяется пока недостаточно.
Испытан анионит нового типа АМЦ-1, синтезируемый на основе целлюлозы совместно с сильнокислотным катионитом КУ-2-8. АМЦ-1 – это полифункциональный слабоосновной анионит, представляет собой аминированную древесную целлюлозу, содержащую первичную, вторичную и третичную алифатические аминогруппы. Полная обменная емкость анионита достигает 4,2 мг экв/г, удельный объем набухшей целлюлозы 5 мг/л. В результате испытаний на токсичность и гигиеничность анионита было получено разрешение на использование АМЦ-1 для обработки пищевого сырья, в том числе в сахарной промышленности. Эффективность процесса можно сравнить с сильноосновным анионитом АВ-17-8ч.
Схема обработки, сыворотки включала: обезжиривание, осаждение белков путем нагрева до 95 °С с подкислением до рН 4,6 и отделением осадка фильтрованием. Сыворотка после обработки имела следующий состав (в %) и свойства:
| Сухих веществ | 5,71 |
| В том числе | |
| лактозы | 4,8 |
| золы | 0,64 |
| рН | 4,6 |
| Чистота фильтрата* | 84,2 ед. |
Осветленную сыворотку пропускали последовательно через катионит в Н+-форме и анионит в ОН--форме. Иониты загружали в колонки диаметром 30 мм. Скорость фильтрации сыворотки составляла 0,4 ± 0,05 мл/ (г ∙ мин).
Изменение активной кислотности и чистоты сыворотки после ионирования приведено на рис. 2.58.
Рисунок 2.58.
Рисунок 2.58. – Изменение активной кислотности (а) и чистоты (б) при деминерализации осветленной молочной сыворотки: 1 – катионит КУ-2-8; 2 – анионит КУ-2-8ч(2); 3 – анионит АМУ-1
Кинетика изменения рН полностью отражает обменные процессы в разных анионитах и позволяет устанавливать момент проскока ионов:
в КУ-2-8 – между 2000 и 2500 мл; в АМЦ-1 – на уровне 500 мп; в АВ-17-8ч – на уровне 900 мл. Степень деминерализации сыворотки по содержанию золы составляет: КУ-2-8 + АВ-17-8ч = 83%, а КУ-2-8 + АМЦ-1 = 93 %. Сыворотка после АМЦ-1 была прозрачной, без запаха аминов, характерного для АВ-17-8ч. Содержание золы в порциях элюата находилось на уровне 0,05—0,08%. Изменение чистоты фильтрата показывает, что высокие обменные свойства и фильтрующая способность АМЦ-1 позволяют получать почти в 2 раза больше деминерализованной сыворотки чистотой 97 ед.
На сыворотку молочную, деминерализованную методом ионного обмена, разработана и утверждена нормативно-техническая документация.
В последнее время все больший интерес представляет переработка молочной сыворотки после изменения рН. Повышение кислотности молочной сыворотки необходимо, например, для приготовления гидролизованного сиропа, состоящего из лактозы, глюкозы и галактозы, отличающегося более высокой усвояемостью, большей пищевой ценностью и сладостью. Это позволяет разработать и освоить новые виды кондитерских, хлебобулочных, пищеконцентратных и других изделий, безалкогольных напитков с частичной заменой основного сырья — свекловичного сахара, молочных продуктов, плодово-ягодных соков, лимонной кислоты и др.
Нейтрализованная молочная сыворотка с титруемой кислотностью 10 —18 Т применяется в продуктах детского питания в кондитерской и парфюмерной промышленности.
При гомогенном способе для раскисления сыворотки используют различные химические реагенты или их растворы: NаОН, КОН, Nа2СО3, Са(ОН)2 и др. Недостаток способа — введение сравнительно больших количеств катионов и анионов, что существенно изменяет минеральный состав молочных продуктов.
При гетерогенном способе с помощью различных марок анионных смол, в частности отечественного сильноосновного макропористого анионита АВ-17-2П с рабочим диапазоном рН от 0 до 14, возможно провести нейтрализацию молочной сыворотки до 13 ˚Т без изменения ее солевого состава. Существует зависимость между кислотностью исходной исходной сыворотки и количеством ионита, необходимого для ее нейтрализации (рис. 2.59.).
Рисунок 2.59.
Рисунок 2.59. – Зависимость массы ионита, необходимого для нейтрализации исходной сыворотки, от ее кислотности
Дата: 2019-05-29, просмотров: 500.