10 г препарата растворяют в 100 мл свсжепрокипяченной и охлаж-
денной воды. Полученный раствор должен быть бесцветным и прозрачным.
Кислотность или щелочность
К 50 мл того же раствора прибавляют 5 капель раствора бромтимоло-
вого синего и разливают на две части. К 25 мл прибавляют 1 каплю 0,02
моль/л раствора едкого натра; должно появиться голубое окрашивание. К
другим 25 мл прибавляют 1 каплю 0,02 моль/л раствора соляной кислоты;
должно появиться желтое окрашивание.
Интервал перехода цвета индикатора: pH = 6,0 — 7,6
Изменение цвета индикатора:
щелочная среда нейтральная среда кислая среда
синий зеленый желтый
КАЛЬЦИЙ
4аммиака и 1 мл раствора оксалата аммония, перемешивают и через 10 минут сравнивают с эталоном, к которому прибавлено такое же количество реактивов.
COONH4 СОО
Са2+ + │ = | Ca ↓+ 2NH4+
COONH4 COO
бел.
Муть, появившаяся в испытуемом растворе, не должна превышать эталон.
МАГНИЙ
5 мл того же раствора не должны давать мути от прибавления 0,5 мл раствора аммиака и раствора гидрофосфата натрия.
NH4CI
Mg2‘ + Na2HPO4 + NН4ОН = MgNH4PO4 ↓+ H20 + 2Na‘
БАРИЙ
10 мл того же раствора не должны давать помутнения с разведенной серной кислотой при наблюдении в течение 2-х часов.
ЖЕЛЕЗО
10 мл того же раствора не должны содержать железа более, чем 1 мл эталонного раствора, разведенный водой до 10 мл (не более 0,0003% в препарате).
К 10 мл испытуемого раствора прибавляют 2 мл раствора сульфоса- лициловой кислоты и 1 мл раствора аммиака и через 5 мин сравнивают с эталоном, к которому прибавлено такое же количество реактивов.
Растворы солей Fe2+ и Fe3+ в зависимости от концентрации образуют с раствором сульфосалициловой кислоты в аммиачной среде коричнево-красные растворы феррилсульфосалицилатных комплексов.
ТЯЖЕЛЫЕ МЕТАЛЛЫ
10 мл того же раствора должны выдерживать испытание на тяжелые металлы (не более 0,0005 % в препарате).
К 10 мл испытуемого раствора прибавляют 1 мл разведенной уксусной кислоты, 2 капли раствора сульфида натрия, перемешивают и через 1 мин сравнивают с эталоном, состоящим из 1 мл эталонного раствора, 9 мл воды и такого же количества прибавленных реактивов.
СН3СООН
Pb2+ + Na2S = PbS ↓ + 2Na2+
черный
Наблюдение окраска проводят по оси пробирок диаметром 1,5 см, помещенных на белой поверхности. В испытуемом растворе не должно появиться черное или бурое окрашивание. В сравниваемых растворах допускается лишь слабая опалесценция от серы, выделяющейся из сульфида натрия.
СУЛЬФАТЫ
Раствор 2 г препарата в 10 мл воды должен выдерживать испытание на сульфаты (не более 0,005 % в препарате).
К 10 мл испытуемого раствора прибавляют 0,5 мл разведенной хлористоводородной кислоты и 1 мл раствора хлорида бария, перемешивают и через 10 минут сравнивают с эталоном, состоящим из 10 мл эталонного раствора и такого же количества реактивов, какое прибавлено к испытуемому раствору. Муть, появившаяся в испытуемом растворе, не должна превышать эталон.
SO42- + BaCl2 = BaSO4 ↓+ 2Cl-
КАЛИЙ
Раствор 0,5 г препарата и 5 мл воды не должен давать мути от прибавления раствора виннокаменной кислоты.
СООН COOK
│ │
СНОН СНОН
│ + к+ -> │ ↓ + н+
СНОН СНОН
│
СООН COOH
H2C4H4O6 + K+ = KHC4H4O6 ↓+ H+
СОЛИ АММОНИЯ
Раствор 0,5 г препарата в 10 мл воды должен выдерживать испытание на соли аммония (не более 0,004 % в препарате).
К 10 мл испытуемого раствора прибавляют 3 капли реактива Несслера, перемешивают и через 5 минут сравнивают с эталоном, к которому прибавлено такое же количество реактива.
2K2[HgI4] + ЗКОН + NH3 -> [ОHg2 NH2]I↓+ 7KI + 2H20 ,
желто-бурый
Соли аммония в зависимости от концентрации образуют с реактивом Несслера желто-бурый осадок или желтое окрашивание. Окраска, появившаяся в испытуемом растворе, не должна превышать эталон.
МЫШЬЯК
1 г препарата должен выдерживать испытание на мышьяк (не более 0,00005 % в препарате).
Потери в весе при высушивании
Около 1 г препарата (точная навеска) сушат при 110 С0 до постоянного веса. Потеря в весе не должна превышать 0,5 %.
Количественное определение
Аргентометрия. Метод осаждения по Мору
Около 1 г препарата (точная навеска) растворяют в воде в мерной колбе емкостью 50 мл и доводят объем раствора водой до метки. 5 мл полученного раствора разбавляют водой до 40 мл и титруют 0,1 моль/л раствором нитрата серебра до оранжево-желтого окрашивания осадка. Индикатор — хромат калия.
1 мл 0,1 моль/л раствора нитрата серебра соответствует 0,005844 г NaCl, которого в пересчете на сухое вещество должно быть не менее 99,5 %.
NaCl + AgN03 —> AgCl ↓+ NaN03
0,1 моль/л
2AgN03 + K2CrO4 -> Ag2Cr04 ↓+ 2KN03
лишняя желто-оранж.
капля
Формула расчета: % = V×K×T×100%
a
ЗАНЯТИЕ 2
АНАЛИЗ РАСТВОРА НАТРИЯ БРОМИДА 2 % — 100 МЛ, ИЗГОТОВЛЕННОГО В АПТЕКЕ ПО ИНДИВИДУАЛЬНОМУ РЕЦЕПТУ
Задачи
1. Освоить внутриаптечный контроль жидкой лекарственной формы, изготовленной в аптеке по индивидуальному рецепту.
2. Научиться делать обзор возможных методов химического анализа и выбирать наиболее экономически выгодный.
3. Совершенствовать навыки титриметрического количественного определения однокомпонентных растворов.
4. Научиться рассчитывать отклонения, сравнивать с допустимой нормой, делать заключение и оформлять результаты анализа.
5. Научиться рассчитывать навеску, ориентировочный объем титранта.
Вопросы для самоподготовки
1. Назовите виды внутриаитечного контроля, обязательные по приказу М3 РФ №751 для данной лекарственной формы. Какие виды контроля проводятся выборочно с целью проверки работы фармацевта? Составьте общий алгоритм всех видов контроля данной лекарственной формы.
2. Назовите специфические показатели качества, проверяемые в жидких лекарственных формах.
3. Приведите обзор методов качественного анализа лекарственной формы. Выберите наиболее убедительную реакцию для качественного экспресс-анализа.
4. Приведите обзор возможных методов количественного определения лекарственной формы. Дайте оценку методам. Выберите наиболее экономически выгодный метод количественного экспресс-анализа.
5. Как рассчитать навеску и ориентировочный объем титранта? Титр? Содержание натрия бромида при титриметрическом и рефрактометрическом определениях? Отклонения и сравнение с допустимой нормой?
6. Как произвести оценку качества проверенной лекарственной формы?
Назовите документ, где делаются отметки о произведенной проверке.
Материальное обеспечение
Реактивы и растворители:
• кислота азотная;
• кислота хлористоводородная;
• раствор белильной (хлорной) извести или раствор хлорамина;
• хлороформ;
• кислота уксусная.
Титрованные растворы и индикаторы:
• 0,1 моль/л раствор нитрата серебра;
• раствор хромата калия
• раствор бромфенолового синего.
Посуда, приборы, оборудование:
• титровальная установка;
• мерная пипетка 1 мл;
• сахарный стаканчик или колба для титрования;
• часовое стекло;
• пробирки;
• вата.
АНАЛИЗ РАСТВОРА НАТРИЯ БРОМИДА, ПРИГОТОВЛЕННОГО ПО ИНДИВИДУАЛЬНОМУ РЕЦЕПТУ
Rp: Solutionis Natrii bromidi 2 %-100ml
D.S. По 1 ст. л. 3 p. в день после еды
Свойства
Бесцветная прозрачная жидкость без запаха соленого вкуса нейтральной реакции среды.
Определение подлинности
1. Na+
К 2 каплям раствора прибавляют 2 капли раствора дигидропироантимоната калия ( гексагидроксоантимоната калия). Наблюдают выделение белого кристаллического осадка.
2NaBr +K2H2Sb2O7 = Na2H2Sb2O7 ↓+ 2KBr
NaBr + K[Sb(OH)6 ] = Na[Sb(OH)6]↓ + KBr
1. Вг-
а) К 1-2 каплям раствора бромида натрия на часовом (предметном) стекле прибавляют 1 -2 капли раствора нитрата серебра. Образуется желтоватый осадок, частично растворимый в растворе аммиака.
NaBr + AgNO3 —> AgBr↓ + NaNO3
бл.-желт.
б) К 0,5 мл раствора натрия бромида добавляют по 0,5 мл хлороформа, кислоты хлористоводородной и несколько капель раствора белильной (хлорной) извести или раствора хлорамина, взбалтывают. Хлороформный слой окрашивается в желто-оранжевый цвет.
СаОС12 + 2НCl -> СаС12 + Н20 + С12
2NaBr + Cl2 -> Br2 + 2NaCl
Количественное определение
1. Аргентометрия no Мору
1 мл раствора натрия бромида помешают в склянку для титрования, добавляют 5-7 капель раствора хромата калия и титруют 0,1 моль/л раствором нитрата серебра до оранжево-желтого цвета.
NaBr + AgN03 —> AgBr↓ + NaNO3
0,1 моль/л
2AgNO3 + K2Cr04 -» Ag2Cr04 ↓+ 2KN03
лишняя кирп.-красн.
капля
2 Аргентометрия по Фаянсу с применением поверхностно действующего индикатора бромфенолового синего.
1 мл препарата помещают в склянку для титрования, добавляют 2 -3 капли раствора бромфенолового синего, по каплям разведенную уксусную кислоту до получения зеленовато-желтого окрашивания (~3 капли) и титруют 0,1 моль/л раствором нитрата серебра до коагуляции сине-фиолетового осадка.
NaBr + AgNO3 —» AgBr ↓ + NaN03
0,1 моль/л
1. Меркуриметрический метод
1 мл препарата помещают в склянку для титрования, добавляют 3 капли раствора дифенилкарбазона и титруют 0,1 моль/л раствором нитрата окисной ртути до фиолетового окрашивания.
2NaBr + Hg(N03)2 -> HgBr2 ↓+ 2NaN03
0,1 моль/л
1 мл 0,1 моль/л раствора нитрата серебра или 0,1 моль/л раствора нитрата окисной ртути соответствует 0,01029 г натрия бромида.
Расчеты при титриметрическом титровании
Расчет ориентировочного объёма титранта определяется делением массы анализируемого вещества, находящемся в анализируемой навеске на титр, т.е.
V= m | T V = 0,02 | 0,01029 = 1,94 мл
допуст. отк. для 2,0 составляют ± 5 % (приказ М3 РФ № 751)
АЛГОРИТМ ВНУТРИАПТЕЧНОГО КОНТРОЛЯ РАСТВОРА НАТРИЯ БРОМИДА, ИЗГОТОВЛЕННОГО ПО ИНДИВИДУАЛЬНОМУ РЕЦЕПТУ
1. Работа с рецептом
• бланк формы 107У
• штамп ЛПУ, личная печать и подпись врача, срок действия рецепта 60 дней
• назначение врача: по 1 ст. л. 3 раза в день после еды
1. Письменный контроль
Дата № рецепта
ППК
Aqua purificata 100 ml
Natrii bromidum 2,0
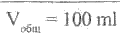
Приготовил:
Проверил: № анализа
Подпись провизора-аналитик
Органолептический контроль
• бесцветная прозрачная жидкость без запаха и механических включений.
Физический контроль (выборочно)
Vo6„i = 100 мл, доп. откл. - ± 3 %
Проверка герметичности укупорки.
Химический контроль (выборочно)
Качественный химический контроль:
• доказательство наличия Вг-
Количественное определение:
• аргентометрия. m = 2,0
• содержание NaBr допуст. откл, = ± 5 %
• Оформление результатов анализа:
заполнить «Журнал регистрации результатов органолептического, физического и химического контроля .....
Контроль при отпуске
· В соответствии с физико-химическими свойствами отпускается в герметически укупоренном флаконе;
· основная этикетка «Внутреннее», дополнительная «Хранить в недоступном для детей месте»;
· на этикетке указаны номер и место нахождения аптеки, номер рецепта, фамилия и возраст больного, назначение врача, дата изготовления, цена, срок годности;
· номер и фамилия больного на рецепте соответствуют номеру и фамилии на этикетке;
· поставить подпись на обратной стороне рецепта (лицо, отпустившее лекарственное средство).
| АО «Петербургские аптеки» Аптека № 116г. Санкт Петербург ул. Типанова д.3 Гр. Сергеевой М.Т. 48лет рец. № 34251 !!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!В Н У Т Р Е Н Н Е Е11111111111111111111111111111 Раствор натрия бромида 2% 100мл По 1 столовой ложке 3 раза в день после еды Дата…………… Годен до………………………… Цена……………. Хранить в недоступном для детей месте Хранить в прохладном темном месте |
Перед употреблением взбалтывать
| Хранить в прохладном месте |
| Хранить в защищенном от света месте |
ЗАНЯТИЕ 3
АНАЛИЗ РАСТВОРА КИСЛОТЫ ХЛОРИСТОВОДОРОДНОЙ ДЛЯ ВНУТРЕННЕГО УПОТРЕБЛЕНИЯ
Задачи
1. Освоить внутриаптечный контроль кислоты хлористоводородной для внутреннего употребления.
2. Совершенствовать навыки титриметрического определения..
3. Научиться делать расчеты с использованием условного титра и оформлять результаты анализ
Вопросы для самоподготовки
1. Назовите виды контроля, обязательные для раствора кислоты хлористоводородной для внутреннего употребления. Какие виды контроля проводятся выборочно? Составьте алгоритм всех видов внутриаптечного контроля.
2. Приведите обзор возможных методов определения подлинности и количественного определения кислоты хлористоводородной. Какие из них целесообразно использовать во внутриаптечном контроле?
1. Особенности расчета содержания кислоты хлористоводородной. Оценка качества лекарственной формы.
Материальное обеспечение
Реактивы:
• раствор гидроксида аммония;
• раствор нитрата серебра;
• раствор танина;
• раствор натрия гидрокарбоната 5 %.
Титрованные растворы и индикаторы:
• 0,1 моль/л раствор гидроксида натрия;
• метиловый оранжевый.
Посуда, оборудование:
• титровальная установка;
• пипетки 5 мл;
• мерный цилиндр;
• пробирки.
Общие указания
Фармакопейными стандартными растворами являются кислота хлористоводородная разведенная (Acidum hydrochloricum dilutum), содержащая 8,3% НС1 (8,2-8,4 %), и кислота хлористоводородная (Acidum hydro- chloricum), содержащая 25 % НС1 (24,8-25,2 %).
Если в рецепте прописан раствор кислоты без обозначения концентрации, то отпускают кислоту хлористоводородную разведенную.
Если в рецепте прописан раствор кислоты с обозначением концентрации, то при расчетах разведенную хлористоводородную кислоту (8,3 %) принимают за 100%.
В ассистентских комнатах не рекомендуется хранить даже разведенную хлористоводородную кислоту. Поэтому разведенную хлористоводородную кислоту разводят водой в соотношении 1 : 10 (10 % раствор) и этот концентрированный раствор используют для изготовления растворов и других жидких лекарственных средств. Наиболее частой является комбинация с пепсином. Пепсин — протеолитический фермент желудочного сока, является альбумином, поэтому микстуру с пепсином относят к растворам ВМС (высокомолекулярных соединений). Хлористоводородная кислота активирует и стабилизирует пепсин (оптимальные pH = 1,8-2).
Во внутриаптечном контроле для расчета содержания хлористоводородной кислоты используется условный титр. Это связано с тем, что указанное в рецепте содержание НС1 обозначает содержание 8,3 % фармакопейного раствора, из которого и была приготовлена лекарственная форма.
Соотношение титра и условного титра
Тфакт. = c(fNaOH)*MHCl*fHCl|1000 = 0,1*36,46*1|1000=0,003646г/мл
Тусловн.= Тфакт*100/8,3 = 0,003646 *100/8,3=0,043927г/мл
Rp: Solutionis Acidi hydrochlorici 1 % — 100 ml
Pepsini 1,0
M.D.S. По 1 чайн. ложке 3 раза в день. Ребенку 10 лет.
Свойства
Бесцветный прозрачный, слегка опалесцирующий раствор со слабым
своеобразным запахом и кислым вкусом.
Подлинность
1. Сl-
а) К 2-3 каплям раствора добавляют 2-3 капли раствора нитрата серебра.
Образуется белый творожистый осадок, растворимый в растворе аммиака.
НС1 + AgNO3 = AgCl↓+ НNO3
AgCl↓ + 2NH4OH = [Ag(NH3)2]Cl + 2H20
[Ag(NН3)2]Cl + 2HNO3 = AgCl↓ + 2NH4NO3
б) К 2-3 каплям раствора прибавляют 2-3 капли 5%раствора натрия гидрокарбоната. Выделяются пузырьки углекислого газа.
НCl + NaHCO3 = NaCl + Н20 + СО2↑
1. Пепсин
К 1 мл микстуры прибавляют 0,5 мл раствора танина. Постепенно образуется белый студенистый осадок.
Количественное определение
Метод нейтрализации (алкалиметрия)
5 мл микстуры титруют 0,1 моль/л раствором гидроксида натрия до желтого окрашивания (индикатор — метиловый оранжевый).
1 мл 0,1 моль/л раствора гидроксида натрия соответствует 0,04393 г кислоты хлористоводородной разведенной (Т условный).
V× К ×Т× 100
m = 5
доп. отк = ± 6%
АЛГОРИТМ ВНУТРИАПТЕЧНОГО КОНТРОЛЯ
МИКСТУРЫ КИСЛОТЫ ХЛОРИСТОВОДОРОДНОЙ С ПЕПСИНОМ
1. Работа с рецептом
· бланк формы 107У;
· штамп ЛУ, личная печать и подпись врача, срок действия рецепта 60 дней;
· компоненты микстуры совместимы;
· дозы в соответствии с возрастом больного не превышены
· назначение врача указано в рецепте.
Письменный контроль
Дата № рецепта
Ппк д
Aqua purificata 90 ml
Solutio Acidi hydrochlorici 1 : 10 — 10 ml
Pepsinum 1,0
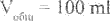
Приготовил:
Проверил: № анализа
Подпись ировизора-аналитика
2. Органолептический контроль
Бесцветный слегка опалесцирующий раствор без механических включений.
3. Физический контроль (выборочно)
V общ = 100 мл доп. отк. = + 3 % [97 -103мл]
Проверка герметичности укупорки.
4. Химический контроль
По приказу М3 РФ № 751 растворы кислоты хлористоводородной для внутреннего употребления подлежат полному химическому (качественному и количественному) контролю обязательно.
Качественный химический контроль:
• доказательство Сl- и пепсина.
Количественное определение:
• метод алкалиметрии.
Содержание НС1 = 1,0 доп. откл = ± 6 % [0,94 - 1,06]
Оформление результатов анализа:
• заполнить «Журнал регистрации результатов органолептического, физического и химического контроля внутриаптечной заготовки, лекарственных форм, изготовленных по индивидуальным рецептам (требованиям лечебных учреждений), концентратов, полуфабрикатов, тритураций, спирта этилового и фасовки»;
• поставить номер анализа и подпись провизора-аналитика на обратной стороне рецепта и ППК.
Контроль при отпуске
• В соответствии с физико-химическими свойствами отпускается в герметически укупоренном флаконе;
• основная этикетка: «Внутреннее», дополнительные; «Хранить в прохладном месте», «Перед употребление взбалтывать», ««Хранить в недоступном для детей месте»;
«Детское»;
• дозы в соответствии с возрастом больного не превышены;
• номер и фамилия больного на рецепте соответствуют номеру и фамилии на этикетке;
• указать срок годности;
• поставить подпись на обратной стороне рецепта (отпустил « подпись).
| АО «Петербургские аптеки» Аптека № 116г. Санкт Петербург ул. Типанова д.3 Гр. Смирнову С.Т. 10лет рец. № 10291 |
| В Н У Т Р Е Н Н Е Е |
| Раствор кислоты хлористоводородной 1% 100мл Пепсина 1,0 По 1 чайной ложке 3 раза в день во время еды Дата…………… Годен до………………………… Цена……………. Хранить в недоступном для детей месте |
| Д Е Т С К О Е |
Перед употреблением взбалтывать
| Хранить в прохладном месте |
| Хранить в защищенном от света месте |
ЗАНЯТИЕ 4
АНАЛИЗ РАСТВОРА ЛЮГОЛЯ 2 % - 100 МЛ ДЛЯ ВНУТРЕННЕГО УПОТРЕБЛЕНИЯ, ИЗГОТОВЛЕННОГО В АПТЕКЕ ПО ИНДИВИДУАЛЬНОМУ РЕЦЕПТУ
Задачи
1. Освоить внутриаптечный контроль раствора Люголя.
2. Освоить химический контроль компонентов лекарственной формы с учетом их влияния на анализ друг друга.
3. Совершенствовать навыки в расчетах и оформлении отчетной документации.
Вопросы для самоподготовки
1. Назовите обязательные и выборочные виды внутриаптечного контроля раствора Люголя. Какие особенности количественного состава компонентов и изготовления лекарственной формы необходимо отметить при проверке паспорта письменного контроля? Составьте алгоритм внутриаптечного контроля данной лекарственной формы.
2. Качественный химический контроль. Каковы особенности его проведения.
3. Количественный химический контроль. Влияют ли компоненты на анализ друг друга? Каковы особенности методики количественного определения компонентов смеси и расчета их содержания?
Материальное обеспечение
Реактивы:
• раствор крахмала;
• разведенная уксусная кислота.
Титрованные растворы и индикаторы:
§ 0,1 моль/л раствор тиосульфата натрия;
§ 0,1 моль/л раствор нитрата серебра;
§ раствор эозината натрия.
Посуда, оборудование:
· титровальная установка;
· склянка с притертой пробкой;
· пробирки;
· мерная пипетка на 1 мл.
Rp: Solutionis Lugoli 2 % — 100 ml
D.S. По 5 капель 3 раза в день на молоке после еды.
Состав
Иода — 2,0
Калия иодида - 4,0
Воды очищенной до 100 мл
Свойства
Прозрачная жидкость красно-бурого цвета со специфическим запахом.
Подлинность
1. I2
К 1 капле раствора добавляют 2 мл воды и 1-2 капли раствора крахмала. Появляется синее окрашивание.
1. KI и I2
К 1 мл раствора прибавляют 2-3 капли разведенной уксусной кислоты, 1-2 капли раствора гексонитрокобальтата(III) натрия (кобалътинитрита натрия), 1-2 мл хлороформа и взбалтывают. Слой хлороформа окрашивается в фиолетовый цвет, а в водном слое наблюдается желтый кристаллический осадок.
2 KI + Na3[Co(NO2)6] -> K2Na[Co(NO2)6] ↓+ 2NaI
Количественное определение
1. Количественное определение иода
Метод иодометрии
1 мл раствора помещают в склянку с притертой пробкой и титруют 0,1 моль/л раствором тиосульфата натрия без индикатора до обесцвечивания.
I2 + 2Na2S203 → 2NaI + Na2S406
V1× K1× T × 100
m, = 1
Mолярная масса йода =253,8г/моль f=1/2
1 мл 0,1 моль/л раствора тиосульфата натрия соответствует 0,0129 г иода,
доп. отк = ± %?
2. Количественное определение калия иодида
Аргентометрия. Метод осаждения по Фаянсу с поверхностно действующим индикатором эозинатом натрия.
К выше оттитрованной жидкости прибавляют 0,5 мл разведенной уксусной кислоты, 2 капли раствора эозината натрия и титруют 0,1 моль/л раствором нитрата серебра до коагуляции ярко-розового осадка.
При расчете из объема 0,1 моль/л раствора AgNO3 вычитают объем 0,1 моль/л раствора Na2S203, так как при титровании иода образуется натрия иодид. На его титрование расходуется объем 0,1 моль/л AgN03, эквивалентный объему 0,1 моль/л раствора Na,S203, ушедшего на титрование иода. KI + AgN03 -> AgI↓↓ + KNO3
NaI + AgN03 -> AgI ↓ + NaN03
(V2K, - V1 К ) × T × 100
mrKJ = 1
MKI. = 166 fKI= 1 TkI =0,0166г/мл
T.e.1 мл 0,1 моль/л раствора нитрата серебра соответствует 0,0166 г калия иодида.
доп. отк. = ± %?
Составьте алгоритм внутриаптечного контроля раствора Люголя. Оформите результаты анализа в дневнике и соответствующем журнале.
| АО «Петербургские аптеки» Аптека № 116г. Санкт Петербург ул. Типанова д.3 Гр. Смирновой Т. А.65лет рец. № 2865
| ||
| В Н У Т Р Е Н Н Е Е | ||
| МИКСТУРА |
Раствор Люголя 2 % 100мл Состав йода 2,0 Калия йодида 4,0 Воды очищенной до 100мл По 5 капель в молоке 3 раза в день после еды Дата…………… Годен до………………………… Цена……………. Хранить в недоступном для детей месте | |
| Хранить в прохладном месте | ||
| Хранить в защищенном от света месте |
ЗАНЯТИЕ 5
Дата: 2019-04-23, просмотров: 766.