Азотистая кислота сама по себе при обычной температуре неустойчива, поэтому ее генерируют в момент проведения реакции из солей:
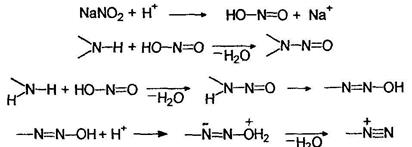
Первичные (1°), вторичные (2 °) и третичные (3°) амины как жирного, так и ароматического рядов различаются по своему поведению в реакциях с азотистой кислотой. Первичные алифатические амины реагируют с азотистой кислотой с образованием совершенно неустойчивых солей диазония, разлагающихся с выделением азота и образованием карбокатионов:
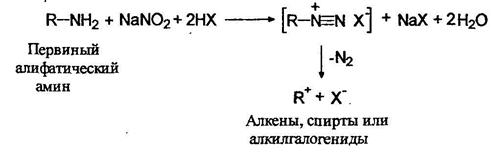
Первичные ароматические амины реагируют с азотистой кислотой с образованием относительно устойчивых солей диазония:
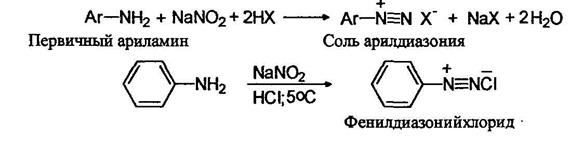
Названия солей диазония образуются путем добавления окончания диазоний к названию арильного радикала с указанием названия аниона. При взаимодействии вторичных алифатических и ароматических аминов с азотистой кислотой реакция останавливается на стадии образования нитрозоминов:
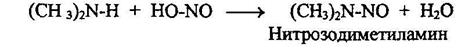
При нагревании ароматических нитрозоаминов они изомеризуются с переходом нитрозогруппы от азота к кольцу (перегруппировка Фишера-Хеппа):
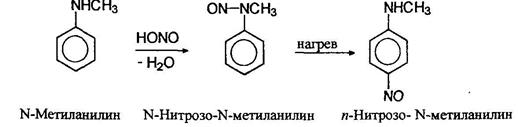
Третичные алифатические амины на холоде образуют с азотистой кислотой соли. Третичные жирноароматические амины при действии азотистой кислоты претерпевают реакцию замещения в кольцо с образованием окрашенных в зеленый цвет нитрозоариламинов:
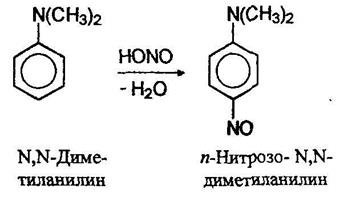
Диазо- и азосоединения
Органические соединения, содержащие в молекуле два атома азота, связанные кратной связью и не входящие в циклическую систему, могут относиться как к азо-, так и диазо соединениям. В случае диазосоединений два атома азота соединены лишь с одним углеводородным радикалом Ar-N2+Cr, а в случае азосоединений - с двумя Ar-N=N-Ar Азосоединения интенсивно окрашены. В зависимости от структуры молекулы они могут быть окрашены в интенсивно желтый, оранжевый, красный, синий или даже зеленый цвет. Примерно половина используемых в настоящее время красителей являются азокрасителями. Диазосо единения называют как соли арилдиазониев. Азосоединения называют двумя путями - как производные азобензола;
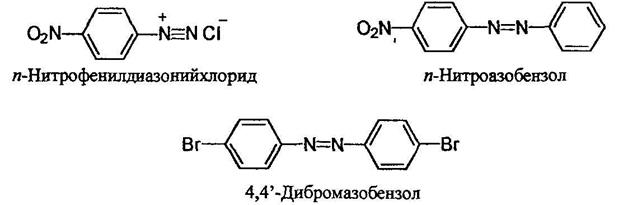
Более сложные соединения называют, рассматривая арилазогруппу Ar-N=N- как заместитель:
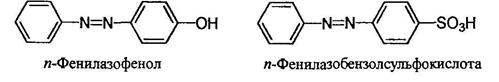
Реакции солей арилдиазония
Все реакции солей арилдиазониев можно разделить на две группы: реакции с выделением азота и реакции без выделения азота.
Реакции замещения
Диазогруппа может быть замещена на разнообразные группы, это является одним из самых лучших путей введения функциональных групп в ароматическое ядро:
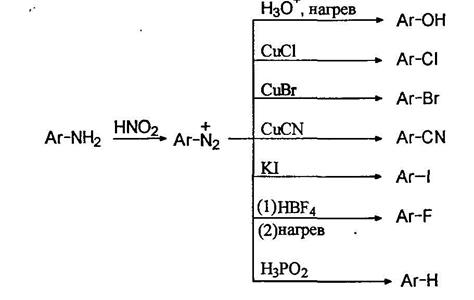
При нагревании водных растворов сульфатов диазониев происходит отщепление азота и образуются фенолы. Таким образом можно получать фенолы с различными заместителями в ароматическом кольце, например:
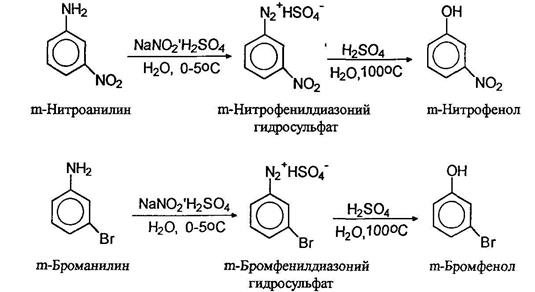
Соли арилдиазониев реагируют с иодидами натрия или калия образуя арилиодиды:
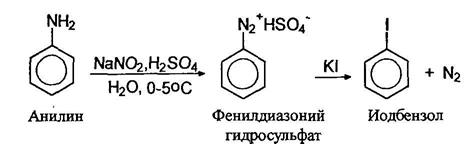
Для замещения диазогруппы на фтор к раствору соли диазония прибавляют тетрафторборную кислоту, при этом осаждается борфториды диазония, которые отфильтровывают, промывают и сушат. При осторожном нагревании борфториды диазония разлагаются с образованием арилфторидов:
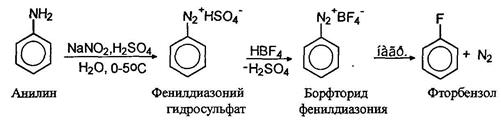
Замещение диазогруппы на хлор и бром осуществляется действием на свежеприготовленный раствор соли диазония хлоридом или бромидом одновалентной меди. Считают, что реакция проходит по радикальному механизму (реакция Зандмеера):
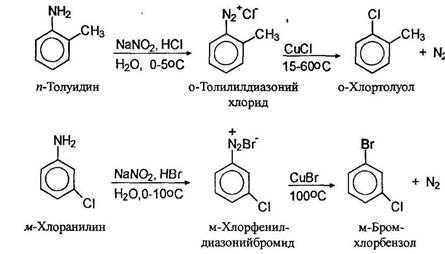
Замещение диазогруппы на нитрильную осуществляется также по реакции Зандмеера использованием цианида одновалентной меди.
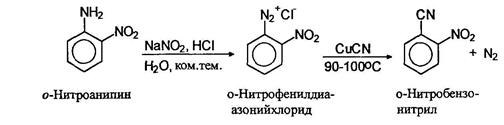
Вместо солей меди (I) в качестве катализатора можно использовать свежеосажденную порошкообразную металлическую медь.
Азосочетание
Замещение диазогруппы на водород можно осуществлять с помощью нескольких реагентов. Наиболее широкое применение получила фосфорноватистая (гипофосфористая) кислота. Соли диазония просто оставляют стоять в присутствии фосфорноватистой кислоты. С помощью этой оеакпии удаляют аминогруппу с ароматического кольца.
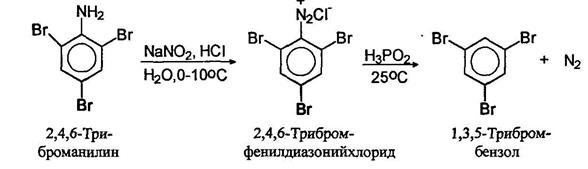
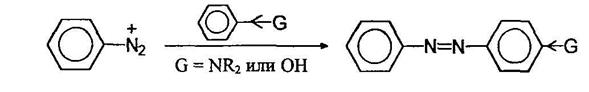
Азосочетанием получают красители. Окрашенные вещества поглощают из падающего на них видимого света некоторые лучи и отражают все остальные - цвет отраженных лучей и определяет окраску вещества. Чем длиннее цепь сопряжения, тем глубже окраска вещества.
Согласно одной из теорий цветности, окрашенное соединение должно содержать так называемую хромофорную группировку - это может быть, например, пара атомов соединенных двойной связью: ОС, C=N, N=N. Очень полезно присутствие в молекуле так называемой ауксохромной группировки, несущей одну или несколько подвижных электронных пар: при ее наличии цвет вещества углубляется. Пример такой групприровки диметиламиногруппа - N(CH3)2- Вот, к примеру, краситель метиловый оранжевый, очень широко применяемый как индикатор на кислоты. Его получают из сульфаниловой кислоты и К,К-диметиланилина:
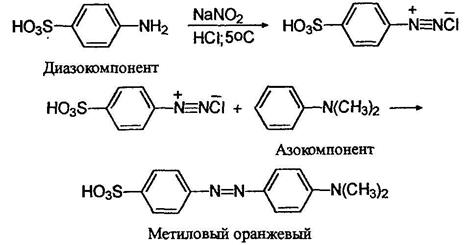
В молекуле этого красителя присутствует хромофорная двойная азот-азотная связь и ауксохромная диметиламиногруппа.
 Азокрасители, получаемые диазотированием сульфаниловой кислоты и последующим азосочетанием продукта с азакомпонентами в виде солей широко используются в качестве химических индикаторов.
Азокрасители, получаемые диазотированием сульфаниловой кислоты и последующим азосочетанием продукта с азакомпонентами в виде солей широко используются в качестве химических индикаторов.
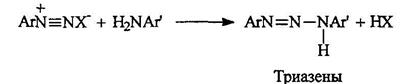
Триазены существуют в двух таутомерных формах:
В средах, близких к нейтральной, катионы диазония электрофильно атакуют неподеленную пару электронов азота первичной аминогруппы. Образующиеся при этом аминоазосоединения называют триазенами.

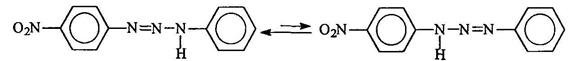
Равновесие смещено в сторону образования триазена, в молекуле которого протон находится у более основного атома азота, т. е. связанного с более электронодонорным радикалом:
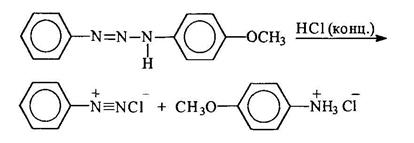
При действии минеральных кислот триазены расщепляются. При этом если триазен несимметричный, расщепление происходит таким образом, что отщепляется амин, являющийся более сильным основанием, а из "азофрагмента" образуется соответствующая соль диазония:
Список литературы
1. "Справочник химика" т.2, Л.-М.: Химия, 1964 стр. 418-419.
2. Бандман А.Л., Волкова Н.В. и др. Вредные химические вещества. Неорганические соединения элементов V–VIII групп. Справочное издание. Под ред. В.А.Филова и др. Л.: Химия, 1989, 592 с
3. Петров А.А., Бальян Х.В., Трощенко А.Т. Органическая химия. – М.: Высш. шк., 1973. - 623 с.
4. Препаративная органическая химия. Изд. 2-е, М., Госхимиздат, 1964.
5. Мельниченко Г.Ф., Кирсанова В.Ф., Биткова Н.П. Выращивание экологически чистой овощной продукции: томаты, перец, баклажаны. Благовещенск, 1993, 62.
6. Богословский Б.Н., Щитова Э.П. Опыты по химии с экологической направленностью. Благовещенск, 1993, 27 с..
7. Терней А. Современная органическая химия: В 2 т. - М.: Мир, 1981. - Т.1 - 670 с; Т.2 - 615 с.
8. В. Ф. Травень. Органическая химия. Том 1. – М.: Академкнига, 2004, - 708 с.
Дата: 2019-05-28, просмотров: 340.