Ферменту и ионам кальция
| Фракция казеина | Степень чувствительности | |
| к сычужному ферменту | к ионам кальция | |
| αs1-Казеин αs2-Казеин β-Казеин ϰ-Казеин | + - + +++ | ++ +++ + - |
Казеин в молоке содержится в основном в виде казеиновых мицелл (около 95%) со средним размером около 100 нм и лишь незначительная часть (около 5 %) – в виде мономеров, полимеров фракций казеина и субмицелл, имеющих размер менее 20–40 нм.
Основными компонентами минеральной части мицелл казеина являются кальций (2,7–2,8 %), фосфор (0,9 %) и цитрат (0,4 %), в небольших количествах содержатся также магний (0,1–0,2 %), калий (0,2 %) и натрий (0,1 %).
Кальций в казеиновых мицеллах содержится в двух формах: органический кальций, присоединенный к фосфатным и карбоксильным группам казеина, и неорганический кальций, входящий в состав коллоидного фосфата и цитрата кальция. По аналогии фосфор коллоидного фосфата кальция считают неорганическим фосфором в отличие от органического фосфора, входящего в состав казеина.
Ионы органического кальция взаимодействуют с остатками фосфорной кислоты, соединяясь с одной или двумя ее гидроксильными (ОН─) группами; кроме того, они присоединяются к карбоксильным группам (СОО─) казеина. Во втором случае кальций имеет свободную связь и может образовывать кальциевый мостик между расположенными друг против друга серинфосфатными группами (R) двух молекул казеина:
2R– COOH + Ca2+ → 2R–COO–Ca+ + 2H+;
2R–COOH + Ca2+ → R–COO–Ca–OOC–R + 2H+.
Такой кальций играет определенную роль при образовании казеиновых мицелл и называется структурообразующим, так как объединяет две молекулы казеина. Кальциевые мостики способствуют агрегации коллоидных частиц казеина при сычужной и кальциевой коагуляции. Соединять молекулы казеина между собой наподобие кальциевых мостиков может и неорганический фосфор в виде коллоидного фосфата кальция, который наряду с ионами кальция может присоединяться к серинфосфатным группам молекул казеина.
Комплекс органического кальция с казеином называется казеинатом кальция, а комплекс казеината кальция с коллоидным фосфатом кальция – к азеинаткальцийфосфатным комплексом (ККФК). Мицеллы казеина представляют собой почти сферические, рыхлые, пористые, сильно гидратированные частицы. В настоящее время известно несколько моделей казеиновых мицелл, однако ни одна из них не может считаться доказанной.
Все модели мицелл можно разделить на две группы: модели типа ядро – оболочка, которые, как правило, предполагают, что гидрофобное ядро мицелл состоит из αs1- и β-казеинов, а роль защитной гидрофильной оболочки выполняет ϰ-казеин, и модели субмицеллярного строения рыхлых мицелл, предусматривающие их построение из сферических субмицелл. Модели второго типа получили большее число сторонников.
Авторы этих моделей полагают, что казеиновые мицеллы состоят из плотно упакованных субмицелл, построенных по типу ядро-оболочка. Сферическая субмицелла состоит из 25–30 мономеров казеина, ее диаметр 10–20 нм.
Последняя модель, предложенная Штидтом (рис.2.2), предполагает, что в состав субмицелл входят четыре фракции казеина – αs1-, αs2-, β- и ϰ-казеин в соотношении 3:1:3:1. Фракции казеина связаны фосфатом кальция. Гидрофобные остатки фракций казеина находятся внутри ядра, а заряженные группы – на его поверхности. В поверхностном слое содержатся много остатков фосфосерина и гликомакропептидная часть ϰ-казеина. ϰ-Казеин занимает часть поверхности субмицеллы. Субмицеллы объединяются в мицеллы с помощью коллоидного фосфата кальция, гидрофобных и электростатических взаимодействий. Субмицеллы с небольшим содержанием ϰ-казеина или без него расположены внутри мицеллы, а с большим содержанием ϰ-казеина – на ее поверхности.
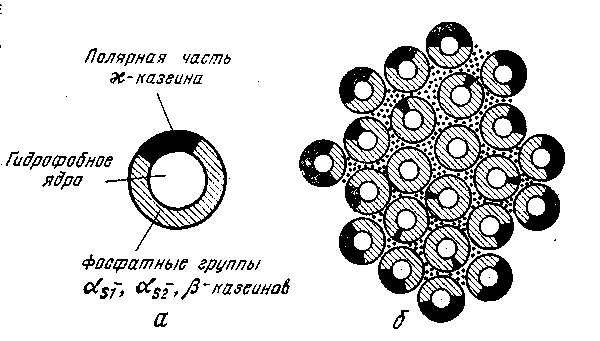
Рис. 2.2. Модель мицеллы казеина по Шмидту
На поверхности казеиновых мицелл имеются положительно и отрицательно заряженные частицы (−СООН, −ОН, >СО, НN< ,−NН2, −SH и др.). Суммарный электрический заряд казеиновых мицелл – отрицательный. Заряженные группы адсорбируют молекулы воды, которые распределяются на поверхности электрически заряженной частицы мономолекулярным слоем. На образовавшемся слое адсорбируются другие частицы воды. По мере утолщения слоя связанной воды новые молекулы воды все слабее удерживаются мицеллой казеина. Количество воды, связанной частицами казеина, вдвое превышает их массу.
Стойкость ККФК определяется степенью гидратации и суммарным поверхностным зарядом частицы: чем они выше, тем больше стойкость комплекса.
Для того, чтобы вызвать агрегацию и коагуляцию мицелл казеина, необходимо снизить их отрицательный заряд, т.е. перевести мицеллы в изоэлектрическое или близкое к нему состояние, а также разрушить их гидратные оболочки.
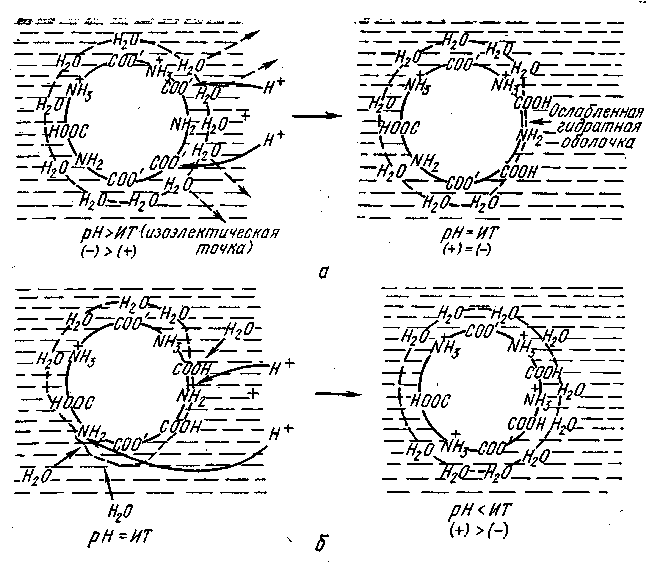
Если постепенно снижать величину рН, то ионы водорода в соответствии с условиями равновесия будут связываться заряженными СОО−-группами, образуя незаряженные карбоксильные группы. Число отрицательных зарядов уменьшится (рис. 2.3). При определенной величине рН количество положительных зарядов будет равно количеству отрицательных зарядов на поверхности белковых частиц (изоэлектрическая точка). Если величина рН снижается за пределы изоэлектрической точки, то ионы водорода протонизируют незаряженные аминогруппы и суммарный заряд вновь повышается.
Следовательно, в изоэлектрической точке количество зарядов оказывается самым незначительным, поэтому гидратация белка в таких условиях проявляется наиболее слабо и стабильность его самая низкая. В изоэлектрической точке ККФК обладает выраженной способностью к осаждению.
|
|
Рис. 2.3. Выравнивание зарядов на поверхности белковой частицы при снижении величины рН (схематически)
а – снижение рН до изоэлектрической точки; б – снижение рН за пределы изоэлектрической точки.
Сывороточные белки. Под термином «сывороточные белки» обычно принято считать группу белков, которые остаются в плазме молока (сыворотке) после осаждения казеина при рН 4,6–4,7. Они составляют около 20 % всех белков молока. К ним относятся β-лактоглобулин (52 %), α-лактальбумин (23 %), иммуноглобулины (16 %), альбумин сыворотки крови (8 %), лактоферрин и другие минорные белки (1 %).
По сравнению с казеином сывороточные белки содержат больше незаменимых аминокислот, поэтому с точки зрения физиологии питания их следует считать наиболее полноценными.
В сывороточных белках серы больше, чем в казеине. Технологическое значение имеет сера, образующая свободные сульфгидрильные группы. Наличие серы в сывороточных белках обусловлено присутствием серосодержащих аминокислот – метионина, цистина, цистеина. Они влияют на изменения белков в процессе переработки молока, например, на денатурацию и органолептические показатели при тепловой обработке.
В нативном состоянии сывороточные белки вследствие прочной гидратной оболочки и высокой степени дисперсности образуют относительно устойчивые коллоидные растворы. Средний размер коллоидных частиц составляет от 15 до 50 нм. Из-за малого размера их количество в молоке превышает число казеиновых мицелл приблизительно в 1500 раз.
Сывороточные белки не гидролизуются сычужным ферментом, по сравнению с казеином менее чувствительны к кальцию, но более чувствительны к нагреванию. Нагревание молока вызывает денатурацию сывороточных белков, затем наступает взаимодействие белок-белок с образованием димеров и полимеров. Кроме того, тепловая обработка способствует взаимодействию денатурированного β-лактоглобулина с ϰ-казеином казеиновых мицелл.
Главные представители сывороточных белков – β-лактоглобулин и α-лактальбумин – синтезируются в клетках молочной железы, альбумин сыворотки крови, иммуноглобулины переходят в молоко из крови.
Иммунные глобулины выполняют функцию антител, содержание этих белков в молозиве очень велико (50–75 % общего содержания белка).
Липиды. Липиды молока синтезируются в молочной железе. Они состоят в основном из молочного жира (более 98 %) и жироподобных веществ (фосфолипидов, стеринов, жирорастворимых витаминов и др.). Молочный жир является наиболее энергетически ценным компонентом молока, кроме того, он обусловливает определенный вкус и консистенцию молочных продуктов, их высокую пищевую ценность. Фосфолипиды помимо известной физиологической роли выполняют структурную и защитную функции, стабилизируя жировую эмульсию и усиливая стойкость жира к окислению и гидролизу.
Молочный жир. По химическому составу представляет собой смесь глицеридов: три-, ди- и моноглицеридов. Основная доля приходится на триглицериды (97 %). В состав молочного жира входит свыше 100 жирных кислот, состав и структура которых определяют свойства жира. От содержания ненасыщенных и насыщенных жирных кислот в триглицеридах зависят консистенция и такие физические свойства молочного жира, как температура плавления, отвердевания.
Триглицериды с ненасыщенными низкомолекулярными жирными кислотами характеризуются более высокой температурой плавления, чем триглицериды с насыщенными высокомолекулярными кислотами. Температура плавления молочного жира понижается по мере увеличения содержания ненасыщенных жирных кислот в триглицеридах.
Зимой в молочном жире увеличивается количество тринасыщенных и динасыщенно-мононенасыщенных триглицеридов. Летом их содержание снижается и возрастает количество легкоплавких триглицеридов, содержащих ненасыщенные жирные кислоты.
Ненасыщенные жирные кислоты более реакционноспособны, чем насыщенные, из-за чего в большей степени подвержены воздействию ферментов, поэтому масло, выработанное из летнего молока, хуже хранится, быстрее подвергается порче во время хранения, чем масло из зимнего молока.
Молочный жир находится в молоке в виде жировых шариков, окруженных защитными пленками (белково-лецитиновыми оболочками), и представляет собой эмульсию жира в воде.
Размер жировыых шариков колеблется от 1 до 10 мкм (средний диаметр равен 2,5–4,5 мкм), он зависит от стадии лактации, кормовых рационов, породы животного.
Размеры жировых шариков имеют практическое значение, так как определяют степень перехода жира в продукт при производстве сливок, масла, сыра, творога.
Физическая стабильность шариков жира в молоке и молочных продуктах, их поведение при отстое сливок и технологической обработке в основном зависят от состава и свойств их оболочек.
Состав и структура оболочек жировых шариков. Основными структурными элементами оболочки жировых шариков (ОЖШ) являются липиды и белки. Эти компоненты, ориентированные определенным образом на поверхности шариков, стабилизируют жировую эмульсию молока.
Толщина оболочки составляет 10−15 нм (иногда 20−30 нм). Она представляет собой сложный комплекс структурных белков, ферментов, фосфолипидов, холестерина каротина, витамина А и других компонентов. Существует несколько моделей структурной организации оболочек (Кинг, Мортон, Макферсон и Китчен, Дженсен и др.).
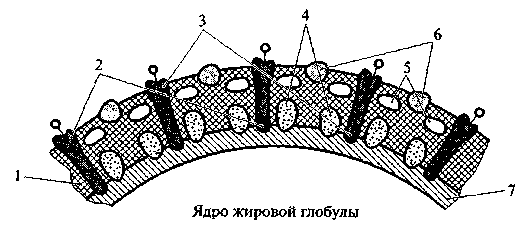
По данным электронно-микроскопических исследований, ОЖШ состоит из двух слоев различного состава – внутреннего тонкого, плотно прилегающего к жировой глобуле, и внешнего рыхлого (диффузного), легко десорбируемого при технологической обработке молока. К внутреннему слою прилегает слой высокоплавких глицеридов, опоясывающий ядро жировой глобулы. Оболочку жирового шарика пронизывают гликопротеиды – один их конец взаимодействует со слоем высокоплавких триглицеридов глобулы, к другому прикреплены углеводы, выступаающие из мембраны и ориентированные к водной фазе (рис. 2.4).
|
|
Рис. 2.4. Модель оболочки жирового шарика по Макферсону и Китчен:
1 − фосфолипиды; 2 − гликопротеиды; 3 − гидрофобный белок; 4 − слой высокоплавких триглицеридов; 5 − ядро жировой глобулы
ОЖШ содержат на поверхности полярные группы (фосфатные группы фосфолипидов, карбоксильные группы, аминогруппы), создается суммарный отрицательный электрический заряд (изоэлектрическая точка около 4,3). К отрицательно заряженным группам присоединяются катионы кальция, магния и др. В результате образуется двойной электрический заряд.
Дополнительное стабилизирующее действие оказывает гидратная оболочка, образующаяся вокруг полярных групп компонентов ОЖШ.
Среди всех структурных компонентов ОЖШ особенно важны для стабилизации жировой эмульсии молока гликопротеиды и фосфолипиды. После обработки оболочек протеазами, разрушающими гликопротеиды, стабильность эмульсии снижается, а после удаления полярных групп фосфолипидов с помощью фосфолипазы С, она резко падает и наступает коалесценция шариков жира.
Таким образом, вторым фактором устойчивости ОЖШ является структурно-механический фактор.
Следовательно, для обеспечения устойчивости жировой эмульсии молока и сливок в процессе выработки молочных продуктов необходимо стремиться сохранить неповрежденными ОЖШ и не снижать степень их гидратации. Для этой цели необходимо сокращать до минимума механические воздействия на жировую фазу молока при транспортировке, хранении и обработке, избегать его вспенивания, правильно проводить тепловую обработку.
Углеводы. Углеводы молока синтезируются в молочной железе. В молоке содержатся моносахариды (глюкоза, галактоза и др.), их производные, дисахарид – лактоза (молочный сахар) и более сложные олигосахариды. Основным углеводом молока является лактоза.
Лактоза. Лактоза обусловливает пищевую ценность молока, служит исходным веществом при молочнокислом брожении в процессе производства кисломолочных продуктов и сыров, влияет на свойства молочных консервов в процессе хранения, а также на вкус и цвет молочных продуктов, при выработке которых применяется высокотемпературная обработка.
Содержание лактозы в молоке зависит от индивидуальных особенностей и физиологического состояния животных.
Лактоза (С12Н22О11) является дисахаридом, построенным из остатков глюкозы и галактозы. В молоке лактоза образует истинный раствор, присутствует в молекулярно-дисперсном виде в двух основных формах – α и β, которые различаются пространственным расположением групп ОН у первого углеродного атома молекулы глюкозы и легко переходят одна в другую.
По сравнению с сахарозой лактоза в 5–6 раз менее сладкая и хуже растворяется в воде. Растворимость β-лактозы выше, чем α-лактозы. Из пересыщенных растворов лактоза кристаллизуется. Кристаллизация лактозы при выработке сгущенного молока с сахаром – очень важная технологическая операция, обусловливающая качество молочных консервов.
Лактоза содержит различные функциональные группы, вследствие чего вступает в реакции со многими веществами.
Под действием ферментов происходит распад лактозы на низкомолекулярные соединения. В молочной промышленности регулируемое расщепление лактозы в результате деятельности микроорганизмов, называемое брожением, является важнейшей технологической операцией при производстве кисломолочных продуктов.
Минеральные вещества. Минеральные вещества поступают в организм животного и переходят в молоко главным образом из кормов и минеральных добавок. Поэтому их количество в молоке находится в прямой зависимости от рационов кормления, окружающей среды (состава почвы, воды и т. д.), времени года, а также породы животного и его физиологических особенностей.
В молоке содержится более 50 элементов, из них около 30 определены количественно. Все минеральные вещества, входящие в состав молока, можно подразделить на макро- и микроэлементы. Макроэлементы содержатся в относительно больших количествах – 10–100 мг/кг, содержание микроэлементов исчисляется микрограммами.
Макроэлементы. К макроэлементам молока относятся калий, натрий, кальций, магний, фосфор и хлор.
Калий, кальций, натрий и магний находятся в молоке в основном в виде солей фосфорной и лимонной кислот. Около 95 % калия и натрия присутствуют в истинном растворе в виде легко диссоциирующих солей, остальное их количество связано с казеином и находится, таким образом, в коллоидном состоянии.
Кальций присутствует в основном в коллоидной форме (около 30 % – в виде коллоидного фосфата кальция и около 40 % – в виде ККФК). На долю истинного раствора приходится 29–33 % всего кальция и лишь 7–10 % его ионизировано. Нормальной концентрацией ионизированного кальция считается величина, равная 110 мг/кг, если она уменьшается до 80 мг/кг, молоко становится «сычужно-вялым»; при концентрации его более 160 мг/кг – молоко нестабильно и легко свертывается при повышении температуры.
Магний в основном присутствует в истинном растворе (73–82 % всего магния), однако лишь 16 % всего магния ионизировано. Остальное количество магния входит в состав коллоидного фосфата магния, а также связано с казеином.
Фосфор – в виде истинного раствора около 40 % всего фосфора, остальное количество в коллоидном состоянии (38 % – неорганические соли, ККФК – 20 %).
Микроэлементы. К микроэлементам относятся: железо, медь, цинк, марганец, кобальт, йод, молибден, фтор, алюминий, кремний, селен, олово, хром, свинец и др. В молоке они связаны с оболочками жировых шариков (железо, медь), казеином и сывороточными белками (йод, селен, цинк, алюминий и др.), входят в состав ферментов (железо, молибден, марганец, цинк, селен), витаминов (кобальт), гормонов (йод, цинк, медь).
Их количество в молоке значительно колеблется в зависимости от состава кормов, почвы, воды, состояния здоровья животных, а также условий обработки и хранения молока. В связи с этим микроэлементы молока можно подразделить на «естественные», то есть поступившие в молоко из молочной железы коровы, и «внесенные», то есть попавшие в молоко с поверхности тары и оборудования.
Микроэлементы, как известно, имеют огромное физиологическое значение для новорожденного теленка и взрослых животных, а также обусловливают пищевую и биологическую ценность молока для человека. Они обеспечивают построение и активность жизненно важных ферментов, витаминов и гормонов. Чувствительны к содержанию некоторых микроэлементов в молоке как питательной среде и многие молочнокислые бактерии, входящие в состав бактериальных заквасок.
Количество внесенных микроэлементов может в несколько раз превышать количество натуральных. В результате большого содержания, например, меди и железа снижается качество молока и молочных продуктов: окисляется аскорбиновая кислота, появляются посторонние привкусы, снижается устойчивость сливочного масла при хранении и т. д. Кроме того, загрязнение молока токсичными элементами (медью, цинком, оловом, хромом и, особенно, свинцом, ртутью, кадмием, мышьяком), а также радионуклидами представляет угрозу для человека, особенно детей.
Ферменты. Ферменты – это биологические катализаторы, ускоряющие химические реакции. По химическому строению они являются простыми или сложными белками.
В молоке, полученном при нормальных условиях от здорового животного, содержится около 100 ферментов различного происхождения.
В молоке имеются нативные (истинные) ферменты, попадающие в него в процессе молокообразования из секреторных клеток молочной железы или непосредственно поступающие из крови. Кроме нативных, в молоке содержатся микробные ферменты, поступающие в него вследствие инфицирования молочной железы или жизнедеятельности микроорганизмов, попадающих в молоко из воздуха, с доильной аппаратуры, емкостей для хранения и с рук в процессе получения, хранения и транспортирования.
Ферменты имеют большое практическое значение. Так, на их действии основано производство кисломолочных продуктов и сыров. Многие ферменты вызывают глубокие изменения составных частей молока во время выработки и хранения молочных продуктов, что может привести к снижению их пищевой ценности и возникновению пороков. Кроме того, по активности некоторых ферментов можно судить о санитарно-гигиеническом состоянии сырого молока или эффективности его пастеризации.
Редуктаза . Редуктаза накапливается в молоке при размножении в нем бактерий, с увеличением количества бактерий активность редуктазы возрастает. На предприятиях молочной промышленности с помощью редуктазной пробы устанавливают общую бактериальную обсемененность молока.
Пероксидаза. Является нативным ферментом, бактериями не выделяется. Она окисляет с помощью пероксида водорода различные полифенолы и ароматические амины. Инактивируется при температуре около 80 °С без выдержки. Реакцией на пероксидазу контролируют эффективность высокотемпературной пастеризации (ГОСТ 3623). Технологического значения пероксидаза не имеет.
Каталаза – фермент, способствующий разложению пероксида водорода. Нативная каталаза переходит в молоко из клеток молочной железы, фермент также вырабатывают содержащиеся в молоке бактерии и лейкоциты. Количество каталазы в молоке непостоянно. В молозиве и в молоке, полученном от больных животных или бактериально загрязненном, ее количество резко увеличивается. Поэтому определение активности каталазы используют как метод обнаружения анормального молока и выявления его обсемененности психротрофной и гнилостной микрофлорой.
Липаза. Катализирует расщепление жиров. В молоке содержится нативная и микробная липаза. Ферменты связаны главным образом с казеином и иммуноглобулинами (плазменная липаза), и лишь небольшая часть адсорбирована оболочками жировых шариков (мембранная липаза).
В результате охлаждения, перекачивания, гомогенизации молока происходит перераспределение липазы с белков на оболочку шарика жира. При этом наступает гидролиз жира, выделяются низкомолекулярные жирные кислоты (масляная, капроновая и др.), и молоко прогоркает.
Микробные липазы обладают высокой активностью, по сравнению с нативными они более термостабильны, разрушаются при температуре 85–90 °С (нативные – 74–80 °С).
Фосфатаза. Катализирует гидролиз эфиров фосфорной кислоты, этот фермент попадает в молоко из клеток молочной железы. В свежем молоке обнаружены щелочная и кислая фосфатазы.
Щелочная фосфатаза молока чувствительна к повышенной температуре. Температуры, вызывающие тепловую денатурацию щелочной фосфатазы, сопоставимы с температурами, вызывающими денатурацию белков клеток патогенной микрофлоры молока при пастеризации (63 °С в течение 30 мин, 72 °С в течение 15 с и 80 °С без выдержки). Кислая фосфатаза термостабильна. Высокая чувствительность щелочной фосфатазы к нагреванию положена в основу метода контроля эффективности пастеризации молока и сливок (фосфатазная проба, ГОСТ 3623).
Лактаза катализирует гидролиз лактозы с образованием глюкозы и галактозы, которые, в свою очередь, распадаются впоследствии на более простые соединения: кислоты, спирт, углекислый газ и др. Этот процесс является основополагающим при производстве кисломолочных продуктов и сыров. В молоке находится лактаза микробного происхождения. Действие лактазы оптимально при температуре 40 ºС.
Лизоцим – очень важный фермент, обнаруженный в молоке, он катализирует гидролиз полисахаридных цепей клеточной оболочки бактерий, что приводит к их гибели. Таким образом лизоцим обеспечивает бактерицидные свойства свежевыдоенного молока. Молочнокислые бактерии менее чувствительны к действию лизоцима, чем микроорганизмы, неблагоприятные в санитарном отношении.
Витамины. Молоко содержит все жизненно важные витамины, хотя и в небольших количествах (табл. 2.2.). Их содержание не постоянно и зависит от кормового рациона, времени года, физиологического состояния, породы и индивидуальных особенностей животного.
Для молочной промышленности основной интерес представляют витамины А, Д, Е, В1, В2, В9, С. Часть витаминов влияет на ход окислительно-восстановительных процессов, протекающих в молоке, и играет роль антиокислителей липидов. Многие витамины являются необходимыми факторами роста микроорганизмов заквасок, а каратиноиды, витамин В2 – природными красителями молочных продуктов.
Таблица 2.2.
Дата: 2019-04-23, просмотров: 748.