М ЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ
Для лабораторных занятий
| Специальность | 5В 110 300 - «Фармация» |
| Курс | 3 |
| Семестр | IV |
Шымкент
201 8
Обсуждены на заседании кафедры фармацевтической и токсикологической химии
Протокол №16 от 31.05.2018 г.
Зав. кафедрой, профессор Ордабаева С.К.
1. Тема: Фармакопейные испытания лекарственных веществ по показателям качества: описание, растворимость, подлинность на примере лекарственных средств, производных VIII-V групп периодической системы Д.И.Менделеева.
2. Цель: Научиться проводить оценку качества изучаемых лекарственных средств на основе общих и частных свойств препаратов в соответствии с требованиями нормативной документации. При оценке качества лекарственных средств использовать государственные принципы и положения, регламентирующие качество лекарственных средств.
3. Задачи обучения:
· дать обучающимся методологию проведения фармацевтического анализа изучаемых лекарственных средств на этапах получения, хранения и применения;
· научить обучающихся применять общие фармакопейные методы исследования к анализу изучаемых лекарственных средств;
· сформировать у обучающихся умения и навыки проведения фармацевтического анализа в соответствии с требованиями нормативно-технических документов по контролю за качеством и безопасностью изучаемых лекарственных средств.
· научить обучающихся определять качество лекарственных препаратов по разделам частных статей ГФ РК или другой НД «описание», «растворимость», «идентификация».
4. Основные вопросы темы:
1. Фармацевтический анализ, специфические особенности в связи с целевым названием лекарственных средств и профессиональная ответственность провизора.
2. Фармакопейный анализ, его особенности, требования, предъявляемые к фармакопейному анализу.
3. Унификация и стандартизация однотипных испытаний в группах лекарственных средств.
4. Общие положения, общие и частные статьи фаркокопеи, их взаимосвязь.
5. Описание внешнего вида лекарственных средств.
6. Значение показателей “описание” и “растворимость” для оценки качественных изменений лекарственных средств, для выполнения отдельных этапов фармацевтического анализа.
7. Внешние факторы, влияющие неблагоприятно на внешний вид лекарственного препарата.
8. Типы химических реакций, приводящих к изменению внешнего вида лекарственных препаратов при неправильном хранении.
9.Комплексный характер оценки качества лекарственных средств. Показатели «описание» и «растворимость» как общая ориентировочная характеристика испытуемого вещества при выполнении отдельных этапов фармацевтического анализа.
10. Принципы определения запаха и вкуса лекарственных препаратов по ГФ РК (т.1, стр. 120).
11. Цвет как относительный показатель подлинности и чистоты лекарственных препаратов.
12. Как характеризуется термин «растворимость» ГФ РК.
13. Способы выражения растворимости, принятые ГФ РК.
Идентификация лекарственных средств в соответствии с общей статьей ГФ РК «Реакции идентификации на ионы и функциональные группы», т.1, стр.112
Методы обучения и преподавания: Контроль знаний, лабораторная работа, написание и защита протокола анализа
Объекты изучения:
Вода дистиллированная – ГФ РК, т. 2, стр. 168
Вода для инъекций – ГФ РК, т. 2, стр. 165
Раствор перекиси водорода 3%– ГФ РК, т. 2, стр. 171
Иод – ГФ РК, т. II, стр. 248
Калия иодид – ГФ РК, т. II, стр. 253
Натрия иодид – ГФ РК, т. II, стр. 360
Кислота хлороводородная – ГФ РК, т. II, стр. 535
Калия хлорид – ГФ РК, т. II, стр. 255
Натрия хлорид – ГФ РК, т. II, стр. 377
Натрия бромид – ГФ РК, т. II, стр. 356
Калия бромид – ГФ РК, т. II, стр. 250
На проведение лабораторного занятия отводится 200 минут, которые распределены следующим образом:
| № п/п | Этапы занятия | Время, мин |
| 1 | исходный контроль знаний по теме лабораторного занятия (устно) | 15 |
| 2 | проверка готовности к выполнению лабораторной работы, согласно рабочих мест | 15 |
| 3 | выполнение лабораторной работы | 110 |
| 4 | написание протокола | 20 |
| 5 | защита протокола | 15 |
| 6 | контроль знаний по теме лабораторного занятия (тестирование) | 15 |
| 7 | подведение итогов (выставление оценок) | 10 |
Содержание занятия:
Рабочее место № 1
Провести оценку качества препарата по разделам:
а) описание
б) растворимость
Данные исследования оформить в виде таблицы 1 и 2.
Литература
Основная:
на русском языке:
1. Арыстанова Т.А. Фармацевтическая химия, учебник, том I: - Алматы: «Эверо», 2015.-572 с.
2. Арыстанова Т.А. Фармацевтическая химия, учебник, том II:- Алматы: «Эверо», 2015.-640 с.
3. Государственная фармакопея Республики Казахстан.-Алматы:«Жибек жолы», 2008.-Том 1.- 592 с.
4. Государственная фармакопея Республики Казахстан.- Алматы:«Жибек жолы», 2009.-Том 2.- 804 с.
5. Государственная фармакопея Республики Казахстан.-Алматы:«Жибек жолы», 2014.-Том 3.-729 с.
6. Контроль качества и стандартизация лекарственных средств: методическое пособие / под ред. Раменской Г. В., Ордабаевой С. К.-М: I МГМУ; - Шымкент: ЮКГФА, 2015. - 285 с.
7. Ордабаева С.К. Анализ лекарственных препаратов, производных ароматических соединений: учебное пособие.-Шымкент: «Әлем», 2012.-250 с.
8. Раменская Г.В. Фармацевтическая химия: учебник.-М.: БИНОМ. Лаборатория знаний, 2015.-467 с.
9. Руководство к лабораторным занятиям по фармацевтической химии под редакцией Г.В. Раменской.-М.: Пилот, 2016.-352 с.
10. Халиуллин, Ф. А. Инфракрасная спектроскопия в фармацевтическом анализе: учебное пособие / - М.: ГЭОТАР-Медиа, 2017. - 160 с.
11. Method validation in pharmaceutical analisis: a guide to best practice / editors dr. Joachim Ermer. - 2nd ed. - Germany: Wiley-VCH, 2015. - 418 p.
12. Watson, David G. Pharmaceutical analysis: a textboor for pharmacy students and pharmaceutical chemists / David G. Watson. - 4th ed. - Philadelphia: Elsevier, 2017. - 459 p.
7. Контроль:
1. Раздел НД “Описание”-это характеристика:
а) физических свойств
б) химических свойств
в) фармакологических свойств
г) физических и химических свойств
д) технологических свойств
2. Определение цвета в лекарственных препаратах проводится:
а) визуально
б) органолептически
в) в сравнении с эталонами цветности
г) физико-химическими методами
д) в сравнении с эталонами мутности
3. Какие факторы приводят к нарушению дозировки (увеличению количества основного вещества в навеске) лекарственных средств, имеющих структуру кристаллогидратов:
а) выветривание
б) свет, влага
в) контакт с тяжелыми металлами
г) химические реакции различных типов
д) перепады температуры
4. Изменение растворимости лекарственного вещества указывает:
а) на присутствие примесей
б) на отсутствие примесей
в) на изменение физических свойств
г) ни о чем не говорит
д) на изменение химических свойств
5. Бесцветное пламя горелки окрашивает в фиолетовый цвет ион:
а) натрия
б) кальция
в) калия
г) лития
д) магния
6. Соль кальция окрашивает бесцветное пламя горелки в:
а) кирпично-красный цвет
б) карминно-красный цвет
в) зеленый цвет
г) желтый цвет
д) оранжевый цвет
7. По посинению красной лакмусовой бумаги обнаруживают:
а) аммиак
б) диоксид углерода
в) сульфиды
г) кислород
д) мышьяк
8. Реакцию образования берлинской лазури используют для обнаружения:
а) растворов солей железа (111)
б) растворов солей железа (11)
в) растворов солей магния
г) растворов солей ртути
д) растворов тетрайодомеркуриата калия
9. Для обнаружения нитратов и нитритов используют реакцию с:
а) дифениламином
б) раствором калия перманганата
в) гексацианоферрат-ионом
г) цинкуранилацетатом
д) с раствором хлорида бария
10.С раствором серебра нитрата желтый творожистый осадок, нерастворимый в азотной кислоте и в растворе аммиака образуют:
а) йодиды
б) хлориды
в) бромиды
г) сульфиды
д) сульфаты
11.Отличить карбонаты от гидрокарбонатов можно по реакции:
а) с фенолфталеином
б) с кислотой хлороводородной
в) с гексанитрокобальтом натрия
г) с гидрофосфатом натрия
д) с кислотой серной
12. Белый осадок с сульфид-ионом образуют:
а) цинк
б) медь
в) висмут
г) железо
д) мышьяк
13. С оксалат – ионом образуют белый осадок растворы солей:
а) кальция
б) калия
в) магния
г) аммония
д) лития
14.При действии щелочей на водные растворы солей образуется желтый осадок оксида:
а) ртути
б) серебра
в) цинка
г) меди
д) железа
15. Дайте название реакции, механизм которой приведен ниже:
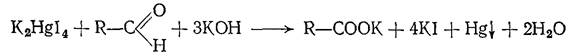
а) с реактивом Несслера
б) с реактивом Марки
в) с реактивом Фелинга
г) с реактивом Драгендорфа
д) с реактивом Розенхейма
16. Лекарственные препараты, процесс растворения которых длится более 10 минут относятся:
а) к медленно растворимым
б) к легко растворимым
в) к растворимым
г) к не растворимым
д) к практически нерастворимым
17. Запах лекарственного вещества определяют на расстоянии:
а) 4-6 см
б) 10-15 см
в) 10-12 см
г) 20-25 см
д) 30 см
18. С раствором хлорида бария определяют:
а) сульфат-ион
б) хлорид-ион
в) карбонат-ион
г) бромид-ион
д) гидрокарбонат - ион
19. С тиоцианат-ионом окрашиваются в красный цвет растворы солей:
а) железа(111)
б) натрия
в) калия
г) кальция
д) магния
20. Амины ароматические первичные дают реакцию образования:
а) азокрасителя
б) серебряного зеркала
в) берлинской лазури
г) кровавой соли
д) турнбулиевой сини
Тема 2 : Фармакопейные испытания рН среды , кислотности или щелочности, прозрачности и цветности раствора на примере лекарственных средств, производных VIII-V групп периодической системы Д.И.Менделеева.
2. Цель: Научиться проводить оценку качества изучаемых лекарственных средств на основе общих и частных свойств препаратов в соответствии с требованиями нормативной документации. При оценке качества лекарственных средств использовать государственные принципы и положения, регламентирующие качество лекарственных средств.
3. Задачи обучения:
· дать обучающимся методологию проведения фармацевтического анализа изучаемых лекарственных средств на этапах получения, хранения и применения;
· научить обучающихся применять общие фармакопейные методы исследования к анализу изучаемых лекарственных средств;
· сформировать у обучающихся умения и навыки проведения фармацевтического анализа в соответствии с требованиями нормативно-технических документов по контролю за качеством и безопасностью изучаемых лекарственных средств.
· научить обучающихся определять качество лекарственных препаратов по разделам частных статей ГФ РК или другой НД НД «Кислотность или/щелочность», рН, «Испытания на предельное содержание примесей», «Определение прозрачности и степени опалесценции жидкостей», «Определение степени окраски жидкостей».
4. Основные вопросы темы:
1. Фармацевтический анализ, специфические особенности в связи с целевым названием лекарственных средств и профессиональная ответственность провизора.
2. Фармакопейный анализ, его особенности, требования, предъявляемые к фармакопейному анализу.
3. Унификация и стандартизация однотипных испытаний в группах лекарственных средств.
4. Определение прозрачности и степени опалесценции жидкостей в соответствии с требованиями ГФ РК.
5. Значение показателей “прозрачность и степень опалесценции” для оценки качественных изменений лекарственных средств, как критерий чистоты лекарственных препаратов
6. Унификация испытаний. Общие и частные методы обнаружения примесей.
7. Общий характер определения содержания примесей по показателям «прозрачность и степень опалесценции жидкостей» и «определение степени окраски жидкостей» и др.
8. Значение физических констант в анализе лекарственных веществ и определении их относительной чистоты (величина рН раствора).
9. Способы установления рН среды.
10. Определение наличия примесей свободных кислот и щелочей в лекарственных препаратах.
11. рН среды, «кислотность», «щелочность» как параметры чистоты лекарственных веществ.
12. Определение степени окраски жидкостей в соответствии с требованиями ГФ РК.
13. Какая жидкость по требованиям ГФ РК считается прозрачной и бесцветной?
14. Приготовление исходных растворов и растворов сравнения для определения степени окраски жидкостей.
15. Определение степени окраски жидкостей по статье ГФ РК в ряду цветов коричневый- желтый – красный.
16. Приготовление исходного красного, голубого, желтого раствора по ГФ РК для определения степени окраски жидкостей.
Объекты изучения:
1. Вода дистиллированная – ГФ РК, т. 2, стр. 168
2. Вода для инъекций – ГФ РК, т. 2, стр. 165
3. Раствор перекиси водорода 3% – ГФ РК, т. 2, стр. 171
4. Иод – ГФ РК, т. II, стр. 248
5. Калия иодид – ГФ РК, т. II, стр. 253
6. Натрия иодид – ГФ РК, т. II, стр. 360
7. Кислота хлороводородная – ГФ РК, т. II, стр. 535
8. Калия хлорид – ГФ РК, т. II, стр. 255
9. Натрия хлорид – ГФ РК, т. II, стр. 377
10. Натрия бромид – ГФ РК, т. II, стр. 356
11. Натрия тиосульфат – ГФ РК,т.II, стр.375
12. Калия бромид – ГФ РК, т. II, стр. 250
Содержание занятия:
Р а б о ч е е м е с т о 1
Провести испытания лекарственных средств по разделам:
а) прозрачность и степень опалесценции
б) степень окраски жидкостей
Результаты испытаний лекарственных средств на прозрачность и степень мутности окраску оформить в виде таблице 1.
Р а б о ч е е м е с т о 2.
Провести оценку качества лекарственных средств по разделу «кислотность или щелочность».
Данные исследований оформить в виде таблице 2
Результаты исследований кислотности и щелочности препарата
Т а б л и ц а 2
| Русское, латинское название, химичес-кая формула | Индикатор | Окраска индикатора Начальная конечная | мл титрованного раствора | Заключение в соответствии с требованиями НД |
Р а б о ч е е м е с т о 3.
Провести испытания по определению рН растворов лекарственных препаратов
Данные исследования оформить в виде таблице 3 и 4
Результаты определения рН раствора колориметрическим методом
Та б л и ц а 3
| Русское, латинское назв. хим. формула. | Ориентировочное значение рН раствора по универсальному индикатору | Подбор буферных растворов с указанием интервала рН | Соответствие требованиям НД с указанием рН испытуемого раствора. |
Результаты определения pH раствора потенциометрическим методом
Таблица 4
| Русское, латинское название, химическая формула | Ориентировочное значение рН раствора по универсальному индикатору | Результаты измерений рН 1 2 3 среднее | Соответствие Требованиям НД |
Рабочее место 4
Провести испытания лекарственных препаратов на содержание примеси органических веществ, примеси восстанавливающих веществ.
Результаты испытаний оформить в виде таблице 5.
Испытания на содержание примеси органических веществ, примеси восстанавливающих веществ в лекарственных препаратах
Таблица 5
| Русское, латинское название, хим. формула | Требование НД к содержанию примеси | Результаты испытаний | Соответствие требованиям НД |
7. Контроль:
1.Какие примеси попадают в лекарственный препарат извне:
| случайные
| специфические
| общетехнологические
| токсические
| нейтральные
2. Исходный желтый раствор по ГФ РК для определения степени окраски жидкостей получают при растворении ... в смеси кислоты хлороводородной и воды.
|железа хлорида
|кобальта хлорида
|меди сульфата
|калия бихромата
|натрия тиосульфата
3. Исходный красный раствор по ГФ РК для определения степени окраски жидкостей получают при растворении ... в смеси кислоты хлороводородной и воды.
|кобальта хлорида
|железа хлорида
|меди сульфата
|калия бихромата
|натрия тиосульфата
4. Исходный голубой раствор по ГФ РК для определения степени окраски жидкостей получают при растворении ... в смеси кислоты хлороводородной и воды.
|меди сульфата
|железа хлорида
|кобальта хлорида
|калия бихромата
|цинка сульфата
5.Определение степени окраски жидкостей по статье ГФ РК проводят в ряду цветов ... .
|коричневый- желтый - красный
|зеленый- желтый - красный
|коричневый- красный
|желтый - красный
|коричневый- зеленый-голубой
6. В воде дистиллированной допустимы примеси
| нитратов и нитритов
| солей аммония
| восстанавливающих веществ
| хлоридов, сульфатов, тяжелых металлов
| диоксида углерода
7. В воде очищенной по отсутствию помутнения в течение 1 ч с известковой водой определяют примеси
| диоксида углерода
| апирогенных веществ
| аммиака
| хлорид-иона
| восстанавливающих веществ
8. Нормативная документация рекомендует определение примесей нитратов и нитритов в воде очищенной
| по обесцвечиванию раствора калия перманганата
| по реакции с кислотой серной концентрированной
| по обесцвечиванию раствора калия перманганата в кислой среде
| по реакции с раствором дифениламина
| по реакции с раствором дифениламина в среде кислоты серной концентрированной
9. Дополнительное испытание при контроле качества воды для инъекций
| определение пирогенных веществ
| определение восстанавливающих веществ
| определение диоксида углерода
| определение хлоридов
| определение сухого остатка
10. Для стабилизации раствора пероксида водорода используют
| натрия метабисульфит
| кислоту хлороводородную
| ацетанилид
| стабилизатор Вейбеля
| спирт этиловый
11. Лекарственный препарат быстро разлагается на свету, при нагревании, соприкосновении с окисляющими или восстанавливающими веществами, некоторыми металлами, выделяя кислород
| натрия тиосульфат
| натрия гидрокарбонат
| натрия нитрит
| лития карбонат
| пероксид водорода
12. Обеззараживающим свойством обладает лекарственный препарат
| калия йодид
| калия хлорид
| раствор пероксида водорода
| натрия хлорид
| натрия бромид
13. Фармакопейный метод количественного определения раствора пероксида водорода
| перманганатометрия
| комплексонометрия
| рефрактометрия
| алкалиметрия
| ацидиметрия
14. Для установления подлинности препаратов пероксида водорода используют реакцию с:
| калия бихроматом в среде кислоты серной
| кислотой хлороводородной
| серебра нитратом
| натрия фторидом
| кислотой винной
15. В воде очищенной по обесцвечиванию раствора с калия перманганатом в кислой среде определяют примеси:
| восстанавливающих веществ
| нитратов и нитритов
| сульфат-ионов
| диоксида углерода
| хлорид-ионов
16. Ингибитором разложения перекиси водорода в гидроперите является:
| кислота фосфорная
| мочевина
| ацетанилид
| кислота мочевая
| кислота щавелевая
17. Мочевину в гидроперите определяют:
| по продуктам гидролиза
| с натрия тиосульфатом
| гидроксамовой пробой
| биуретовой реакцией
| c раствором бихромата калия
18. Количественное содержание воды в лекарственных средствах определяют по ниже приведенной реакции с помощью реактива … .
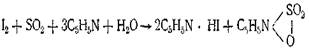
| 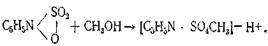
|
|Фишера
|Майера
|Несслера
|Марки
|Толленса
19. Для стабилизации раствора пероксида водорода используют … .
| ацетанилид
| кислоту хлороводородную
| натрия метабисульфит
| стабилизатор Вейбеля
| спирт этиловый
20. При количественном определении перекиси водорода перманганатометрическим методом по приведенной реакции индикатором является … .
2KMnO4 + 5H2O2+3 H2SO4 à 2MnSO4 + K2SO4 + 8H2O + 5O2
|титрант
|метиловый красный
|метиловый оранжевый
|фенолфталеин
|крахмал
21. Приведенную ниже реакцию окисления дифениламина в кислой среде используют для обнаружения в воде очищенной … .
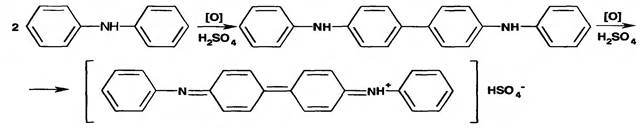
|нитратов и нитритов
|бромидов и иодидов
|сульфатов и сульфидов
|фторидов и хлоридов
|сульфитов и броматов
22. Приведенная ниже химическая структура соответствует лекарственному препарату … .
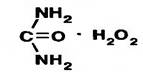
| гидроперит
| перекись водорода
| кислота глютаминовая
| меглюмин
| омнискан
23. Кислотность или щелочность определяют:
| по изменению окраски индикатора, титриметрическим методом
| колориметрическим методом
| химическими реакциями
| потенциометрическим методом
| кулонометрическим методом
24.рН – реакция среды, является характеристикой:
| химических свойств
| физических свойств
| фармакологических свойств
| физических и химических свойств
| технологических свойств
25 рН исследуемого препарата может измениться:
| при хранении
| при изготовлении
| при транспортировке
| при отпуске
| не изменяется, т.к. это постоянная величина
26. Величину рН определяют:
| потенциометрически
| титриметрическим методом
| колориметрическим методом
| рефрактометрическим методом
| спектрофотометрическим методом
27. Бесцветным считают жидкости:
| по цвету не отличающиеся от воды или растворителя
| по цвету не отличающиеся от эталона мутности
| по цвету не отличающиеся от эталона цветности
| по цвету не отличающиеся эталона прозрачности
| не имеющие окраски
28. Окраску в исследуемом растворе определяют:
| при дневном отраженном свете на матово-белом фоне
| при дневном отраженном свете на черном фоне
| органолептически
| не определяют
| при солнечном освещении на черном фоне
Тема 3 : Фармакопейные испытания на наиболее часто встречающиеся примеси (хлориды, сульфаты и т.п.) на примере лекарственных средств, производных IV-I групп периодической системы Д.И.Менделеева.
2. Цель: Научиться проводить фармакопейные испытания на наиболее часто встречающиеся примеси (хлориды, сульфаты и т.п.) на примере лекарственных средств, производных IV-I групп периодической системы Д.И.Менделеева в соответствии с требованиями нормативной документации
3. Задачи обучения:
· дать обучающимся методологию проведения фармацевтического анализа изучаемых лекарственных средств на этапах получения, хранения и применения;
· научить обучающихся применять общие фармакопейные методы исследования к анализу изучаемых лекарственных средств;
· сформировать у обучающихся умения и навыки проведения фармацевтического анализа в соответствии с требованиями нормативно-технических документов по контролю за качеством и безопасностью изучаемых лекарственных средств.
4. Основные вопросы темы:
1. Фармацевтический анализ, специфические особенности в связи с целевым названием лекарственных средств и профессиональная ответственность провизора.
2. Фармакопейный анализ, его особенности, требования, предъявляемые к фармакопейному анализу.
3. Унификация и стандартизация однотипных испытаний в группах лекарственных средств.
4. Общие замечания к испытаниям препаратов на предельное содержание примесей.
5. Требования, предъявляемые к реакциям, применяемым для анализа ионов, находящихся в препаратах в виде примесей.
6. Унификация испытаний. Общие и частные методы обнаружения примесей.
7. Источники попадания и способы обнаружения примесей в препаратах изучаемой группы
8. Свойства, определяющие применение бария сульфат для рентгеноскопии в медицине. Требования к чистоте и хранению.
9. Требования к чистоте бария сульфата в зависимости от способа применения в медицине.
10. Допустимые и не допустимые примеси в бария сульфате для рентгеноскопии.
11. Для чего проводят солянокислые, азотнокислые и водные вытяжки из бария сульфата.
12. Какие примеси предусматриваются по НД в магния окиси. Укажите источники примесей и рассчитайте примесь железа в препарате.
13. Обоснуйте наличие примесей в препарате магния сульфата.
14. Какие дополнительные испытания на чистоту проводятся в препаратах магния, исходя из способов получения.
15. Какое отличие в требовании на чистоту магния сульфата и магния сульфата для инъекций.
16. Требования к чистоте препаратов кальция в зависимости от способа и области применения.
17. Выделите допустимые и недопустимые примеси кальция хлориде.
18. Почему примесь железа в кальция хлориде одновременно регламентируется как допустимая и недопустимая.
19. Как проводятся испытания на примеси магния и других щелочноземельных металлов кальция хлориде.
20. Определение недопустимых примесей солей меди, сульфидов, мышьяка в изучаемых препаратах.
Объекты изучения:
· Натрия гидрокарбонат- ГФ РК,т.II, стр.358
· Натрия тетраборат - ГФ РК,т.II, стр. 374
· Цинка окись – ГФ РК, том II, стр. 561
· Цинка сульфат – ГФ РК, том II, стр. 562
· Бария сульфат для рентгеноскопии – ГФ РК, т.II. стр.128
· Кальция хлорид– ГФ РК, т.II. стр.263
· Кальция сульфат
· Магния окись– ГФ РК, т.II. стр.317
· Магния сульфат– ГФ РК, т.II. стр. 321
· Меди сульфат – ГФ РК, том II, стр. 328
· Висмута нитрат основной
· Алюминия гидроксид
Рабочее место 1
Провести испытания лекарственных препаратов на содержание примесей хлоридов и сульфатов.
Результаты испытаний оформить в виде таблице 1.
Испытания на содержание допустимых примесей в лекарственных препаратах Таблица 1
| Русское, латинское название, хим. формула | Требование НД к содержанию допусти-мой примеси | Методика испытания по ГФ РК Уравнения реакций | Соответствие требованиям НД |
Рабочее место 2
Провести испытания лекарственных препаратов на недопустимые примеси:
Результаты испытания оформить в виде таблице 2.
Объекты изучения:
· Натрия гидрокарбонат- ГФ РК,т.II, стр.358
· Натрия тетраборат - ГФ РК,т.II, стр. 374
· Цинка окись – ГФ РК, том II, стр. 561
· Цинка сульфат – ГФ РК, том II, стр. 562
· Кальция хлорид– ГФ РК, т.II. стр.263
· Магния окись– ГФ РК, т.II. стр.317
· Магния сульфат– ГФ РК, т.II. стр. 321
· Меди сульфат – ГФ РК, том II, стр. 328
· Алюминия гидроксид
Рабочее место №1 Провести количественное определение цинка сульфата в субстанции
Рабочее место № 2 Провести количественное определение меди сульфата в субстанции.
Рабочее место № 3 Провести количественное определение натрия гидрокарбоната в субстанции.
Рабочее место № 4 Провести количественное определение магния сульфата в субстанции.
7. Контроль:
1. Для количественного анализа лекарственных средств, имеющих в молекуле первичную ароматическую аминогруппу применяют метод … .
a. нитритометрии
b. нейтрализации в безводной среде
c. аргентометрии
d. комплексонометрии
e. нейтрализации в водной среде
2. Количественное определение серебра нитрата проводят методом ... .
a. аргентометрии по Фольгарду
b. комплексонометрии
c. иодометрии
d. нейтрализации
e. нитритометрии
3 Количественное определение меди сульфата по нормативной документации проводят методом ... .
a. йодометрии
b. аргентометрии
c. нейтрализации
d. нитритометрии
e. перманганатометрии
4 При количественном определении натрия гидрокарбоната ацидиметрическим методом используют индикатор … .
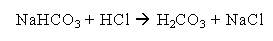
a. метиловый оранжевый
b. метиловый красный
c. фенолфталеин
d. кислотный хром черный
e. тропеолин 00
5 Приведенная ниже реакция используется в анализе магния сульфата для определения … .

a. количественного содержания
b. чистоты
c. подлинности
d. стабильности
e. растворимости
6. Назовите препарат, количественное содержание которого проводится методом комплексонометрии при рН 2-3, индикатор пирокатехиновый фиолетовый:
a. сульфат меди;
b. висмута нитрат основной;
c. сульфат цинка;
d. нитрат серебра;
e. сульфат железа
7 Количественное определение цинка сульфата по нормативной документации проводят методом … .
a. комплексонометрии
b. прямой нейтрализации
c. рефрактометрии
d. аргентометрии по Фольгарду
e. ацидиметрии
8 Для количественного определения … используют метод прямой комплексонометрии в среде аммиачного буферного раствора (рН 9.5-10.0), индикатор эриохром черный.
a. магния сульфата
b. висмута нитрата основного
c. меди сульфата
d. алюминия гидроксида
e. серебра нитрата
Объекты изучения:
1. хлорэтил
2. хлороформ
3. йодоформ
Рабочее место № 1. Провести сравнительный анализ физических свойств следующих препаратов: хлорэтила, хлороформа
Результаты оформить в виде таблицы.
| Название препаратов
| Описание
| Растворимость | Т кип
| Плот- ность
| Соответ ствие НД
| |||
| Вода | Спирт | эфир | Бен-зол | |||||
Рабочее место № 2 Провести полный фармакопейный анализ хлорэтила
Рабочее место № 3 Провести полный фармакопейный анализ хлороформа
Рабочее место № 4 Провести полный фармакопейный анализ йодоформа
7. Контроль:
1. Введение галогена в молекулу производных углеводородов
| повышает растворимость и снижает токсичность препарата
| снижает биологическую активность и токсичность препарата
| повышает биологическую активность и токсичность препарата
| снижает биологическую активность, уменьшает растворимость
| приводит к полной потере фармакологической активности препарата
2. Лекарственный препарат горит зеленым пламенем, образуя углекислоту, воду и хлористый водород
| хлороформ
| эфир диэтиловый
| спирт этиловый
| хлористый этил
| глицерин
3. В хлороформ для наркоза добавляют спирт этиловый
| в качестве консерванта для обезвреживания примеси фосгена
| для снижения летучих свойств
| для снижения токсичности
| для уменьшения неприятного запаха и вкуса
| для снижения воспламенения
4. Органические примеси в хлороформе для наркоза определяют по реакции с
| кислотой серной конц.
| натрия нитропруссидом
| бромной водой
| аммиачным раствором серебра нитрата
| реактивом Розенхейма
5. Приведенная ниже химическая формула соответствует лекарственному препарату
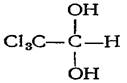
| хлоралгидрат
| хлористый этил
| хлороформ
| уротропин
| формальдегид
6. Количественное определение хлороформа по нормативной документации проводят методом
| аргентометрии
| сухой минерализации
| сжигания в токе кислорода
| влажной минерализации
| не проводят
7. Идентификацию хлороформа по нормативной документации проводят по
| температуре кипения и плотности
| реакции конденсации с анилином
| реакции конденсации с резорцином
| после минерализации с серебра нитратом
| по продуктам щелочного гидролиза
8. Описание «мелкие, пластинчатые, блестящие кристаллы лимонно-желтого цвета с резким характерным запахом» соответствует препарату
| калия иодид
| кислота аскорбиновая
| натрия иодид
| калия ацетат
| йодоформ
9. Формула хлористого этила:
| С2Н5СI;
| СНCI3;
| СН3СН2СI2;
| СF3CHCIBr;
| С2Н5ОН
10 Какое влияние оказывает введение галогена в молекулу углеводорода?
| снижает токсичность и активность препарата;
| увеличивает наркотические свойства и повышает токсичность препарата;
| повышает растворимость и снижает токсичность препарата;
| снижает наркотические свойства, уменьшает растворимость;
| приводит к полной потере фармакологической активности препарата;
11. Зачем для идентификации хлористый этил нагревают со спиртовым раствором щелочи:
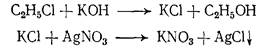
| минерализация для перевода хлора в ионогенное состояние;
| для отделения примесей;
| для создания щелочной среды;
| для устранения возможных побочных продуктов реакции;
12. Описание «прозрачная бесцветная жидкость, легко летучая, со своеобразным фруктовым запахом, температура кипения 12—13°, вследствие чего он быстро испаряется и вызывает сильное охлаждение, чем обусловлено его местноанестезирующее действие» соответствует препарату:
| хлороформ;
| йодоформ;
| спирт этиловый;
| хлористый этил;
| фторотан;
13. Горит зеленым пламенем, образуя углекислоту, воду и хлористый водород:
| спирт этиловый;
| этиловый эфир;
| хлористый этил;
| хлороформ;
| глицерин;
14.Укажите требование Государственной фармакопеи для испытания на присутствие органической примеси в лекарственных препаратах:
| с концентрированной серной кислотой (при наличии органических примесей происходит их осмоление и пожелтение раствора);
| с реактивом Несслера (побурение раствора за счет освобождения свободной ртути);
| с реактивом Толленса (почернение раствора за счет выделения свободного серебра);
| с реактивом Марки;
| с хромотроповой кислотой;
15.Укажите лекарственный препарат и назовите примесь, которую определяют в этом препарате по нижеприведенной реакции:
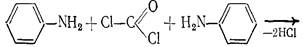

| хлороформ для наркоза, фосген;
| йодоформ, анилин;
| спирт этиловый, дифенилмочевина;
| эфир для наркоза, соляная кислота;
| хлористый этил, восстанавливающие вещества;
16 Назовите консервант, который добавляют к хлороформу для наркоза:
| тимол;
| резорцин;
| метабисульфит натрия;
| спирт этиловый;
17 Приведенная ниже химическая формула соответствует лекарственному препарату … .

|хлорэтил
|фторотан
|галотан
|хлороформ
|йодоформ
18 Приведенная ниже химическая формула соответствует лекарственному препарату … .
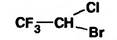
|фторотан
|хлорэтил
|эфир диэтиловый
|хлороформ
|йодоформ
19 Описание «прозрачная, бесцветная, легко летучая жидкость со своеобразным запахом, температура кипения 12-13◦С» соответствует … .
|хлорэтилу
|фторотану
|эфиру
|хлороформу
|йодоформу
20 Рациональное название лекарственного препарата «трихлорметан» соответствует … .
|хлороформу
|фторотану
|эфиру
|хлорэтилу
|йодоформу
21 Приведенная ниже реакция окисления хлороформа протекает при … .

|неправильных условиях хранения
|идентификации
|количественном определении
|определении примесей органических примесей
|определении примесей альдегидов
22 Приведенная ниже реакция обнаружения фосгена используется в анализе … .
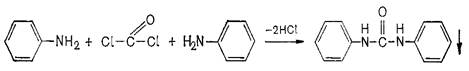
|хлороформа
|фторотана
|эфира
|хлорэтила
|йодоформа
23 Примеси альдегидов в хлороформе по приведенной ниже реакции определяют с реактивом … .
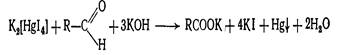
|Несслера
|Марки
|Толленса
|Фелинга
|Майера
24 Испытания на отсутствие органических примесей в хлороформе проводят по … .
| отсутствию пожелтения от добавления кислоты серной конц.
| пожелтению раствора от добавления кислоты серной конц.
|выпадению хлопьев от добавления реактива Несслера
|окрашиванию крахмала при добавлении калия иодида
|выпадению осадка от добавления анилина
25 Примеси свободного хлора в хлороформе обнаруживают по … .
|окрашиванию крахмала в синий цвет при добавлении калия иодида
|пожелтению раствора от добавления кислоты серной конц.
|выпадению хлопьев от добавления реактива Несслера
|выделению бурого газа от добавления кислоты серной конц.
|выпадению осадка от добавления анилина
26 Примеси фосгена в хлороформе обезвреживаются в присутствии спирта этилового за счет … .
|образования нетоксичного диэтилового эфира угольной кислоты
|разложения фосгена до хлороводорода и углекислого газа
|образования угольной кислоты и воды
|переведения фосгена в осадок
|разложения фосгена до газообразных продуктов
27 Описание «прозрачная, бесцветная, тяжелая подвижная, легко летучая жидкость с характерным запахом, температурой кипения 59,5-62◦С, пары не воспламеняются и не взрываются» соответствует … .
|хлороформу
|фторотану
|хлоралгидрату
|хлорэтилу
|йодоформу
28 Приведенные ниже рациональное название и химическая формула соответствуют лекарственному препарату … .
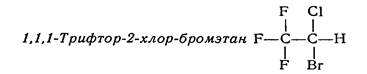
|фторотан
|хлороформ
|хлоралгидрат
|хлорэтил
|йодоформ
29 Сущность пробы Бельштейна заключается в образовании … .
|летучих галогенидов меди при нагревании галогенсодержащих препаратов на медной проволоке
|неорганических соединений при сжигании в токе кислорода
|неорганических ионов при сплавлении галогенсодержащих препаратов с натрия карбонатом
|галогенидов меди при обработке галогенсодержащих препаратов кислотой серной конц.
|мышьяковистого водорода
30 Проба Бельштейна служит для идентификации атома … в молекуле органического вещества.
|галогена
|азота
|серы
|фосфора
|щелочных металлов
31 При нагревании препаратов … в сухом виде на медной проволоке пламя окрашивается в синевато-зеленый цвет.
|брома и йода
|хлора
|серы
|фтора
|форсфора
32 При внесении в пламя горелки на медной проволоке препаратов, содержащих ионы … пламя окрашивается в желтый цвет.
|хлора
|брома
|йода
|фтора
|серы
33 При нагревании галогенсодержащих препаратов … в сухом виде на медной проволоке пламя окрашивается для брома и йода в…цвет.
|синевато-зеленый цвет
|желтый
|красный
|бурый
|зеленый
34 Образование летучих галогенидов меди при нагревании галогенсодержащих препаратов на медной проволоке используют в … .
|пробе Бельштейна
|методе Къельдаля
|методе сжигания в колбе с кислородом
|методе Зангера-Блека
|пробе Лассеня
35 Рациональное название «трийодметан» соответствует лекарственному препарату … .
| йодоформ
|хлороформ
|хлоралгидрат
|хлорэтил
|фторотан
36 Нагревание препарата в присутствии кислоты серной конц. с выделением фиолетовых паров используют для идентификации …
|йодоформа
|хлороформа
|бромкамфоры
|хлорэтила
|кислоты глютаминовой
37 При идентификации … нагреванием в присутствии кислоты серной конц. образуются фиолетовые пары.
|йодоформа
|хлороформа
|бромкамфоры
|хлорэтила
|кислоты глютаминовой
38 Йодоформ применяют как… средство.
|антисептическое
|ингаляционное
|витаминное
|кардиотоническое
|косметическое
39 Фторотан применяют в медицинской практике для … .
|ингаляционного наркоза
|кратковременного наркоза
|дезинфицирования ран
|обработки инструментов
|лечения кишечных инфекций
Объекты изучения:
1. спирт этиловый – ГФ РК, том II, стр. 581
2. глицерин – ГФ РК, том II, стр. 195
3. нитроглицерин
4. эфир для наркоза – ГФ РК, том II, стр.595
Рабочее место № 1 Провести полный фармакопейный анализ спирта этилового 95%
Рабочее место № 2 Провести полный фармакопейный анализ эфира для наркоза
Рабочее место №3 Провести полный фармакопейный анализ глицерина
Рабочее место №4 Провести полный фармакопейный анализ таблеток нитроглицерина
7. Контроль:
1.Дайте название лекарственного вещества, формула которого приведена ниже:

|нитроглицерин;
|маннит;
|валидол;
|глицерин;
|эфир медицинский;
2. Для какого лекарственного вещества характерна реакция идентификации образования акролеина:
|нитроглицерина;
|глицерина;
|хлористого этила;
|хлороформа;
|спирта этилового;
3. Укажите метод количественного определения спирта этилового:
|нитритометрия;
|нейтрализация;
|перманганатометрия;
|комплексонометрия;
|концентрацию спирта определяют по величине его плотности;
4. Реакция идентификации характерна для: 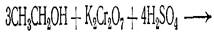
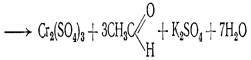
|спирта этилового;
|бихромата калия;
|альдегидов;
|глицерина;
|эфира медицинского;
5. Химическая формула соответствует:
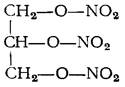
|глицерину;
|нитроглицерину;
|эфиру медицинскому;
|фторотану;
|хлороформу;
6. Описание «прозрачная, бесцветная, летучая жидкость с характерным запахом и жгучим вкусом. Кипит при 78°С. Легко воспламеняется, горит синеватым светящимся бездымным пламенем» соответствует препарату
|эфир диэтиловый
|спирт этиловый
| хлористый этил
|хлоралгидрат
|хлороформ
7. Примесь фурфурола определяют в лекарственном препарате
|фторотан
|хлороформ
|спирт этиловый
|хлористый этил
|глицерин
8. Реакцию образования акролеина рекомендуют для идентификации
|йодоформа
|глицерина
|хлористого этила
|хлороформа
|спирта этилового
9. Описание «прозрачная, бесцветная сиропообразная жидкость без запаха, сладкого вкуса, нейтральной реакции» соответствует:
|спирту этиловому 96%
|глицерину
|нитроглицерину
|хлороформу
|меди сульфату
10. Количественное определение глицерина в соответствии с НД проводят:
|нитритометрией
|алкалиметрией
|не проводят
|перманганатометрией
|спектрофотометрией
11. Нитрат-ионы нитроглицерина идентифицируют:
|с кислотой серной концентрированной
|с раствором дифениламина
|с кислотой азотной концентрированной
|с раствором гидроксида натрия
|после гидролиза с раствором дифениламина
13. Спиртовую часть молекулы нитроглицерина идентифицируют:
|после омыления, нагревая с гидросульфатом калия
|после гидролиза с дифениламином
|с кислотой серной концентрированной
|с раствором иодидов
|с раствором хлорангидрида уксусной кислоты
14. Объемную концентрацию спирта этилового определяют методом:
|нитритометрии
|нейтрализации
|перманганатометрии
|комплексонометрии
|ареометрии
15. Реакция идентификации, химизм которой приведен ниже, характерна для препарата:
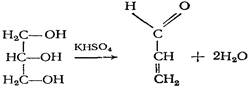
|глюкоза;
|хлоралгидрат;
|салициловая кислота;
|спирт этиловый;
|глицерин
16. Примеси метилового спирта в спирте этиловом определяют по реакции:
|с кислотой хромотроповой
|с кислотой серной конц.
|с калия перманганатом
|с реактивом Толленса
|с кислотой уксусной
17. Примеси сивушных масел обнаруживают в препарате:
|хлороформ
|хлористый этил
|спирт этиловый
|хлоралгидрат
|эфир диэтиловый
18. Примесь фурфурола в спирте этиловом определяют реакцией:
|образования шиффового основания
|с хромотроповой кислотой
|образования акролеина
|образования этилацетата
|образования йодоформа
19 При взаимодействии спирта этилового с кислотой уксусной по приведенной ниже реакции образуется … .

|этилацетат с приятным фруктовым запахом
|желтый осадок с характерным запахом
|ацетальдегид
|белый осадок, растворимый в избытке реактива
|акролеин с неприятным запахом
20 При взаимодействии спирта этилового с йодом в щелочной среде по нижеприведенной реакции образуется … .

| желтый осадок с характерным неприятным запахом
| белая опалесценция
| осадок черного цвета, пузырьки газа
| аморфный осадок белого цвета
| осадок синего цвета
21 При взаимодействии глицерина с водоотнимающими средствами по нижеприведенной реакции образуется … .
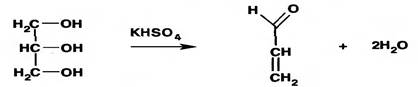
| акролеин с неприятным запахом
| этилацетат с приятным фруктовым запахом
| ацетальдегид с характерным запахом
| аморфный осадок белого цвета
| осадок бурого цвета
22 Приведенная ниже реакция образования глицерата меди используется для … глицерина.

|идентификации
|количественного определения
|определения примесей сивушных масел
|определения стабильности
|определения чистоты
23 Приведенную ниже реакцию используют для обнаружения примеси ... в спирте этиловом.
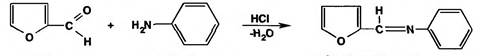
|фурфурола
|сивушных масел
|дубильных веществ
|альдегидов
|органических веществ
24 Приведенная ниже химическая структура соответствует лекарственному препарату … .
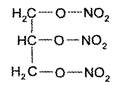
|нитроглицерин
|спирт этиловый
|диэтиловый эфир
|глицерин
|формалин
25 При взаимодействии спирта этилового с бихроматом калия по приведенной ниже реакции образуется … .
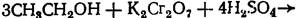
| 
|
|ацетальдегид с запахом свежих яблок
|желтый осадок с характерным запахом
|этилацетат с приятным фруктовым запахом
|бурый осадок, растворимый в избытке реактива
|акролеин с неприятным запахом
26 Примесь спирта метилового в этаноле определяют по реакции с … .
|кислотой хромотроповой
|аммония оксалатом
| натрия сульфидом
|меди сульфатом
|кислотой серной
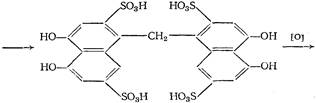
27 Приведенную ниже реакцию используют для обнаружения примеси … в анализе чистоты спирта этилового.
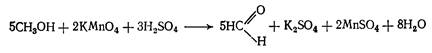
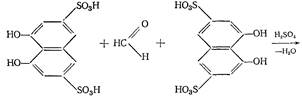
| 
|
|
| |
|метилового спирта
|альдегидов
|органических веществ
|дубильных веществ
|сивушных масел
Объекты изучения:
1. Формальдегид – ГФ РК, том II, стр. 523
2. Гексаметилентетрамин
3. Хлоральгидрат
Рабочее место № 1 Провести полный фармакопейный анализ раствора формальдегида
Рабочее место № 2 Провести полный фармакопейный анализ субстанции гексаметилентетрамина
Рабочее место № 3 Провести полный фармакопейный анализ субстанции хлоралгидрата
Рабочее место № 4 Провести полный фармакопейный анализ раствора гексаметилентетрамина 40% для инъекций
7. Контроль:
1Примесь параформа в формальдегиде образуется в условиях
| низкой температуры (ниже 9°С)
| влияния света и кислорода воздуха
| хранения в присутствии влаги
| высокой температуры (выше 20°С)
| длительного хранения
2 Реакция, приведенная ниже, используется для идентификации лекарственного препарата


| метионин
| глюкоза
| формальдегид
| гексаметилентетрамин
| цистеин
3 Приведенная ниже химическая формула соответствует лекарственному препарату
|
| ремантадин
| левомицетин
| гексаметилентетрамин
| стрептоцид
| мидантан
4 Наличие альдегидной группы в лекарственных препаратах приводит к:
| снижению фармакологической активности
| снижению токсичности
| повышению фармакологической активности и токсичности
| усилению летучести
| не влияет на фармакологическую активность
5 Реакции идентификации альдегидов, основанные на их окислительно-восстановительных свойствах проводят с:
| реактивом Толленса, Феллинга, Несслера;
| фуксинсернистой кислотой, с бисульфит натрия;
| реактивом Марки, Драгендорфа;
| реактивом Розенхейма;
| солями тяжелых металлов
|
| формальдегид
| кислота ацетилсалициловая
| новокаин
| резорцин
| левомицетин
7 Для какого препарата характерно образование параформа при хранении:
| хлоралгидрат
| глюкоза
| формальдегид
| спирт этиловый
| хлорэтил
8 Способ снижения токсичности альдегидной группы в молекуле лекарственного препарата:
| образование гидратной формы альдегида;
| удлинение алкильного радикала;
| введение непредельных связей;
| окисление до карбоксильной группы
| введение галогена в молекулу альдегида
9 НД рекомендует определение кислотности в формальдегиде с целью определения:
| примеси муравьиной кислоты, образующейся при получении и при дисмутации препарата;
| промежуточных примесей синтеза;
| предупреждения возможных процессов полимеризации;
| примеси кислоты хлороводородной;
| предупреждения деструкции препарата
10 Применение гексаметилентетрамина как антисептического средства основано на:
| способности возгоняться
| способности осаждаться пикриновой кислотой
| гидролизе в водных растворах с образованием формальдегида
| осаждаться бромной водой
| растворяться в спирте
11 Гидратная форма хлораля применяется в медицине под названием:
| хлороформ
| хлорэтил
| хлоралгидрат;
| формальдегид;
| глюкоза
12 Количественное содержание формальдегида проводят в соответствии с приведенной ниже химической реакцией методом … .
I2 + 2NaOH à NaIO + NaI + H2O
HCHO + NaIO + NaOH à HCOONa + NaI + H2O
NaI + NaIO + H2SO4 à I2 + Na2SO4 + H2O
I2 + Na2S2O3 à 2NaI + Na2S4O6
|йодометрии, обратным титрованием
|йодометрии, прямым титрованием
|йодатометрии, обратным титрованием
|Мора, прямым титрованием в шелочной среде
|Мора, прямым титрованием в нейтральной среде
13 При количественном определении хлоралгидрата методом обратной алкалиметрией используют индикатор … .
Cl3C-CH(OH)2 + NaOH изб à CHCl3 + HCOONa
NaOH изб+HClàNaCl+H2O
|фенолфталеин
|натрия эозинат
|бромтимоловый синий
|кислотный хром черный
|тропеолин 00
14 Гексаметилентетрамин образует цветные осадки с … за счет содержания в структуре третичного атома азота.
|общеалкалоидными осадительными реактивами
|кислотами
|щелочами
|галогенами щелочных металлов
|солями кальция
15 Гексаметилентетрамин образует желтый осадок с пикриновой кислотой за счет содержания в структуре … .
|третичного атома азота
|метиленовых групп
|аминных групп
|аминной группы в С1
|метиленовой группы в С2
16 Приведенная ниже реакция используется в анализе хлоралгидрата для … .
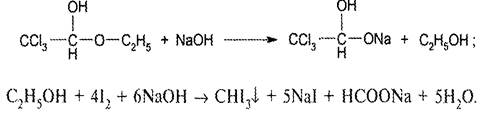
|обнаружения специфической примеси хлоралалкоголята
|идентификации
|количественного определения
|исследования стабильности
|обнаружения общетехнологических примесей
Объекты изучения:
o Кальция глюконат - ГФ РК, том II, стр. 258
o Кальция лактат
Рабочее место № 1 Провести фармакопейный анализ субстанции кальция глюконата
Рабочее место № 2 Провести фармакопейный анализ субстанции кальция лактата
7. Контроль:
1.Окислительно-восстановительная реакция с калия перманганатом лежит в основе количественного определения препарата
A) кальция лактат
B) кальция глюконат
C) натрия цитрат
D) калия ацетат
E) натрия оксибутирата
2. Химическая формула соответствует лекарственному препарату
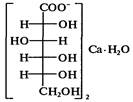
A) кальция пантотенату
B) кальция ацетату
C) кальция пангамату
D) кальция глюконату
E) кальция лактату
3. Приведенная ниже химическая структура соответствует лекарственному препарату … .

|кальция глюконат
|кальция ацетат
|кальция пангамат
|кальция пантотенат
|кальция лактат
4. Приведенная ниже реакция образования ацетальдегида используется при идентификации … .

| кальция лактата
| кальция глюконата
| натрия цитрата
| ацетилцистеина
| пирацетама
5. При идентификации кальция лактата окисление лактат – иона калия перманганатом сопровождается образованием … .
| ацетальдегида с характерным запахом
| окрашенного осадка
| кислоты молочной
| этилацетата с яблочным запахом
| комплексных солей молочной кислоты
6. Идентификацию ионов кальция в кальция лактате проводят с … .
| аммония оксалатом
| кислотой виннокаменной
| цинка уранилацетатом
| натрия кобальтинитритом
| реактивом Несслера
7. Количественное определение кальция лактата проводят методом … .
| комплексонометрии в среде аммиачного буфера
| нейтрализации
| комплексонометрии в среде кислоты азотной
| перманганатометрии
| гравиметрии
8. Реакцию образования солей светло-зеленого цвета с хлоридом окисного железа используют для идентификации … .
| кальция глюконата
| диэтилового эфира
| аминолона
| ацетилцистеина
| пирацетама
9. При идентификации кальция лактата окисление лактат – иона калия перманганатом сопровождается образованием … .
| ацетальдегида с характерным запахом
| окрашенного осадка
| кислоты молочной
| этилацетата с яблочным запахом
| комплексных солей молочной кислоты
10. Идентификацию ионов кальция в кальция лактате проводят с … .
| аммония оксалатом
| кислотой виннокаменной
| цинка уранилацетатом
| натрия кобальтинитритом
| реактивом Несслера
11. Количественное определение кальция лактата проводят методом … .
| комплексонометрии в среде аммиачного буфера
| нейтрализации
| комплексонометрии в среде кислоты азотной
| перманганатометрии
| гравиметрии
Объекты изучения:
3. Глюкоза – ГФ РК, том II, стр. 523
4. Левовист
3. Сахароза
Рабочее место № 1 Провести полный фармакопейный анализ раствора субстанции глюкозы
Рабочее место № 2 Провести полный фармакопейный анализ субстанции сахарозы
Рабочее место № 3 Провести полный фармакопейный анализ субстанции левовиста
7. Контроль:
~Поляриметрическим методом определяют … глюкозы.
|удельное вращение
|показатель преломления
|интенсивность флюоресциенции
|удельный показатель поглощения
|оптическую плотность
~Восстановительные свойства глюкозы связаны с наличием в молекуле … .
|полуацетального гидроксила
|пиранозного цикла
|гидроксильной группы в положении С3
|гидроксильной группы в положении С4
|спиртовой группы в положении С6
~Как многоатомный спирт глюкоза взаимодействует с … .
|меди гидроксидом с образованием комплексных соединений синего цвета
|общеалкалоидными реактивами с образованием окрашенных осадков
|реактивом Толленса с образованием бурого осадка
|реактивом Марки с образованием ауринового красителя
|реактивом Фелинга с образованием Cu2 O красно-фиолетового цвета
~В окислительно-восстановительные реакции с реактивами Фелинга и Толленса глюкоза вступает за счет наличия … .
|альдегидной группы
|гидроксильных групп
|пиранозного цикла
|гидроксильной группы в положении С3
|гидроксильной группы в положении С4
~Олигосахарид … состоит из α-D-глюкопиранозы и β-D-фруктофуранозы.
|сахароза
|глюкоза
|мальтоза
|лактоза
|крахмал
~Сахароза не вступает в реакцию с реактивом …, так как не содержит полуацетальный гидроксил, переходящий в альдегидную группу.
|Фелинга
|Марки
|Майера
|Вагнера
|Драгендорфа
~Глюкоза образует озазоны с четкой температурой плавления при нагревании с … .
|фенилгидразином
|реактивом Марки
|кислотой серной конц.
|кислотой хромотроповой
|меди гидроксидом
~Олигосахарид … состоит из β-D-галактопиранозы – и (1→)-α-D-глюкопиранозы.
|лактоза
|глюкоза
|мальтоза
|сахароза
|крахмал
~Примеси декстрина определяют в препарате … .
|глюкоза
|формальдегид
|лактоза
|хлоралгидрат
|спирт этиловый
~Поляриметрическим методом определяют … глюкозы.
|удельное вращение
|показатель преломления
|интенсивность флюоресциенции
|удельный показатель поглощения
|оптическую плотность
~Восстановительные свойства глюкозы связаны с наличием в молекуле … .
|полуацетального гидроксила
|пиранозного цикла
|гидроксильной группы в положении С3
|гидроксильной группы в положении С4
|спиртовой группы в положении С6
~Как многоатомный спирт глюкоза взаимодействует с … .
|меди гидроксидом с образованием комплексных соединений синего цвета
|общеалкалоидными реактивами с образованием окрашенных осадков
|реактивом Толленса с образованием бурого осадка
|реактивом Марки с образованием ауринового красителя
|реактивом Фелинга с образованием Cu2 O красно-фиолетового цвета
~В окислительно-восстановительные реакции с реактивами Фелинга и Толленса глюкоза вступает за счет наличия … .
|альдегидной группы
|гидроксильных групп
|пиранозного цикла
|гидроксильной группы в положении С3
|гидроксильной группы в положении С4
~Олигосахарид … состоит из α-D-глюкопиранозы и β-D-фруктофуранозы.
|сахароза
|глюкоза
|мальтоза
|лактоза
|крахмал
~Сахароза не вступает в реакцию с реактивом …, так как не содержит полуацетальный гидроксил, переходящий в альдегидную группу.
|Фелинга
|Марки
|Майера
|Вагнера
|Драгендорфа
~Глюкоза образует озазоны с четкой температурой плавления при нагревании с … .
|фенилгидразином
|реактивом Марки
|кислотой серной конц.
|кислотой хромотроповой
|меди гидроксидом
~Олигосахарид … состоит из β-D-галактопиранозы – и (1→)-α-D-глюкопиранозы.
|лактоза
|глюкоза
|мальтоза
|сахароза
|крахмал
~Примеси декстрина определяют в препарате … .
|глюкоза
|формальдегид
|лактоза
|хлоралгидрат
|спирт этиловый
~Реакцию образования озазонов используют для идентификации … .
|глюкозы
|кислоты аскорбиновой
|кислоты глютаминовой
|лактозы
|сахарозы
~При взаимодействии глюкозы с фенилгидразином по приведенной ниже реакции образуется … .
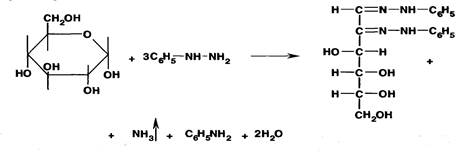
|осадок озазона желтого цвета с характерной температурой плавления
|ауриновый (арилметановый) краситель красного цвета
|основание Шиффа розового цвета
|индофеноловый краситель синего цвета
|диазокраситель красного цвета
~Приведенная ниже реакция преобразования глюкозы в оксиметилфурфурол протекает при … .
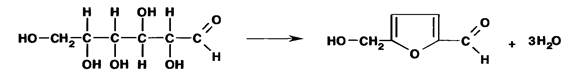
|неправильных условиях стерилизации и хранения
|идентификации
|количественном определении
|определении удельного вращения
|определении примеси декстрина
М ЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ
Для лабораторных занятий
| Специальность | 5В 110 300 - «Фармация» |
| Курс | 3 |
| Семестр | IV |
Шымкент
201 8
Обсуждены на заседании кафедры фармацевтической и токсикологической химии
Протокол №16 от 31.05.2018 г.
Зав. кафедрой, профессор Ордабаева С.К.
1. Тема: Фармакопейные испытания лекарственных веществ по показателям качества: описание, растворимость, подлинность на примере лекарственных средств, производных VIII-V групп периодической системы Д.И.Менделеева.
2. Цель: Научиться проводить оценку качества изучаемых лекарственных средств на основе общих и частных свойств препаратов в соответствии с требованиями нормативной документации. При оценке качества лекарственных средств использовать государственные принципы и положения, регламентирующие качество лекарственных средств.
3. Задачи обучения:
· дать обучающимся методологию проведения фармацевтического анализа изучаемых лекарственных средств на этапах получения, хранения и применения;
· научить обучающихся применять общие фармакопейные методы исследования к анализу изучаемых лекарственных средств;
· сформировать у обучающихся умения и навыки проведения фармацевтического анализа в соответствии с требованиями нормативно-технических документов по контролю за качеством и безопасностью изучаемых лекарственных средств.
· научить обучающихся определять качество лекарственных препаратов по разделам частных статей ГФ РК или другой НД «описание», «растворимость», «идентификация».
4. Основные вопросы темы:
1. Фармацевтический анализ, специфические особенности в связи с целевым названием лекарственных средств и профессиональная ответственность провизора.
2. Фармакопейный анализ, его особенности, требования, предъявляемые к фармакопейному анализу.
3. Унификация и стандартизация однотипных испытаний в группах лекарственных средств.
4. Общие положения, общие и частные статьи фаркокопеи, их взаимосвязь.
5. Описание внешнего вида лекарственных средств.
6. Значение показателей “описание” и “растворимость” для оценки качественных изменений лекарственных средств, для выполнения отдельных этапов фармацевтического анализа.
7. Внешние факторы, влияющие неблагоприятно на внешний вид лекарственного препарата.
8. Типы химических реакций, приводящих к изменению внешнего вида лекарственных препаратов при неправильном хранении.
9.Комплексный характер оценки качества лекарственных средств. Показатели «описание» и «растворимость» как общая ориентировочная характеристика испытуемого вещества при выполнении отдельных этапов фармацевтического анализа.
10. Принципы определения запаха и вкуса лекарственных препаратов по ГФ РК (т.1, стр. 120).
11. Цвет как относительный показатель подлинности и чистоты лекарственных препаратов.
12. Как характеризуется термин «растворимость» ГФ РК.
13. Способы выражения растворимости, принятые ГФ РК.
Идентификация лекарственных средств в соответствии с общей статьей ГФ РК «Реакции идентификации на ионы и функциональные группы», т.1, стр.112
Дата: 2019-03-05, просмотров: 900.