Аминоалкилзамещенные бензолы составляют группу биологически важных веществ. Так, 2-аминопропильный фрагмент сообщает производным бензола свойства стимуляторов нервной системы. Большая часть из них (соединения (1-) содержит первичную или вторичную аминогруппу. Родоначальником этих
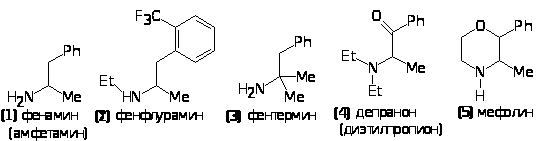
психостимуляторов был фенамин (1),который (как и депранон (4) в настоящее время используют только как анорексигенные лекарственные вещества, способствующие снижению аппетита (анорексия - отсутствие аппетита) в комплексном лечении ожирения. Установлено, что фенфлурамин 2 не возбуждает ЦНС, а повышает уровень потребления сахара в мышцах. Синтез фенамина осуществляют
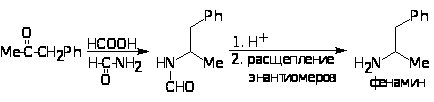
аминированием метилбензилкетона по методу Лейкарта-Валлаха (действием муравьиной кислоты и ее амида) с последующим кислым гидролизом промежуточного 2-(N-формил)аминопропилбензола и расщеплением оптических изомеров.
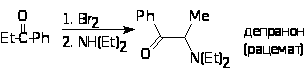
Депранон 4 получают бромированием фенилэтилбензола по альфа-метиленовому положению и последующим нуклеофильным замещением атома брома на диэтиламинную группу.
К этой же группе психостимуляторов относится алкалоид эфедрин (6) [(-)-форма], который стимулирует рецепторы адреналина (адреномиметик), повышает
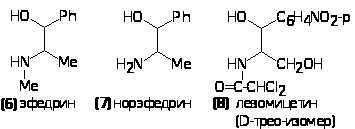
артериальное давление за счет сужения сосудов и расширяет бронхи. Его применяют при аллергиях (бронхиальной астме, сенной лихорадке и др.) так же, как и адреналин. Синтезируют рацемический эфедрин (псевдоэфедрин) действием ме-тиламина на 1-фенил-1,2-пропандион с последующим восстановлением промежуточного имина. Адренэргическим и сосудосуживающим действием обладает также и норэфедрин (6). Первая стадия его синтеза заключается в конденсации бензальдегида с нитроэтаном, которая проводится в присутствии водного карбоната калия при комнатной температуре в атмосфере азота. Полученный при этом нитроспирт затем восстанавливают в амин (7) в системе Zn/AcOH.
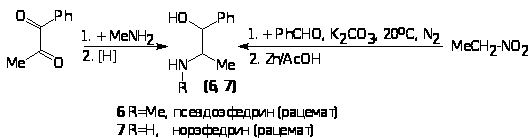
Природный антибиотик левомицетин (хлорамфеникол, 8) также со-
держит 2-амидопропильную боковую группу в бензольном кольце. Он относится к редко встречаемым в природе соединениям, содержащим в своей молекуле нитрогруппу и атом галогена. Этот антибиотик эффективен в отношении многих грамположительных и грамотрицательных бактерий (активен только D-(-)-трео-изомер). Его применяют для лечения брюшного тифа, дизентерии, коклюша, пневмонии и др. заболеваний. Для увеличения водорастворимости левомицетин используют в виде сукцината натрия, а для пролонгирования его действия получают левомицетина стеарат. Его антимикробное действие связано с ингибированием синтеза белка у патогенных организмов. Промышленное производство левомицетина начинается с хлорирования стирола в метаноле с получением 2-хлор-1-метоксиэтилбензола (9), который нитруют и выделяют пара-нитроизомер (10). Последний дегидрохлорируют щелочью, а промежуточный метоксиалкен затем омыляют в кислой среде, что приводит к образованию нитроацетофенона (11а).
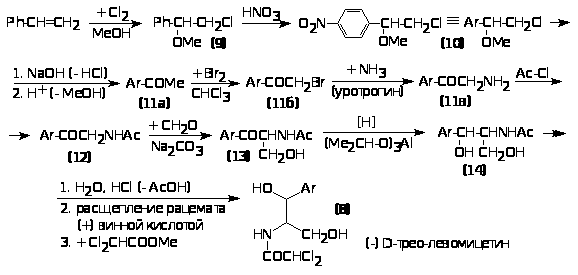
Бромированием этого соединения получают 2-бромацетофенон (11б) последующая обработка которого аммиаком (или уротропином) и защитой аминогруппы промежуточного амина (11в) приводит к амидоацетофенону (12). Его гидроксиметилируют формальдегидом до (13) и восстанавливают последний в присутствии изопропилата алюминия в 1,3-диоламид (14). После гидролитического снятия ацильной защиты рацемический диоламин расщепляют (+)-винной кислотой, выделяя D-(-)-трео-изомер, который затем ацилируют метиловым эфиром дихлоруксусной кислоты с получением левомицетина 8.
Адреналин (16) - гормон надпочечников - содержит 2-(N-метил-амино)этильный заместитель в дигидроксибензольном кольце, а его предшественники - нейромедиаторы норадреналин (17) и дофамин (18),- первичную аминогруппу (все три биогенных амина носят название катехоламинов). Если адреналин применяют при аллергиях, то норадреналин - для повышения артериального давления. В промышленности норадреналин и адреналин получают из
пирокатехина (19), ацилируя его хлоруксусной кислотой в присутствии AlClз до хлорметилкетона (20), который затем аминируют аммиаком или метиламином с получением аминокетонов (21). В случае N-метилпроизводного 21 восстановление на никеле Ренея с последующим расщеплением энантиомеров с помощью (+)-винной кислоты приводит к D-(-)адреналину 16. В случае каталитического гидрирования первичного амина 21 синтезируют норадреналин 17. В альтернативном подходе осуществляют формилирование пирокатехина в системе
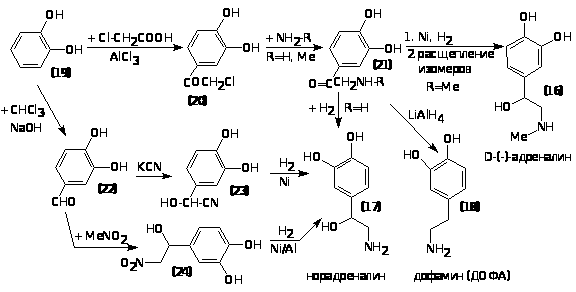
CHClз/NaOH до альдегида (22), который либо цианируют до цианпроизводного (23) либо конденсируют с нитрометаном до нитроспирта (24). Затем оба соеди-
нения 23 и 24 превращают каталитическим гидрированием в норадреналин 17. Восстановлением первичного амина 21 с помощью комплексных гидридов получают дофамин 18.
Дата: 2019-02-25, просмотров: 523.