Движение нейтрофильных лейкоцитов к очагу воспаления начинается внутри кровеносных сосудов. Приближаясь к участку сосуда, расположенному в непосредственной близости от центра воспалительного очага, лейкоциты замедляют свое движение относительно скорости кровотока и начинают процесс проникновения (диапедеза) через сосудистую стенку. И движение лейкоцитов, и их адгезия к сосудистой стенке, и последующее проникновение через стенку сосуда – это сложный, многоэтапный процесс (Рис.3).
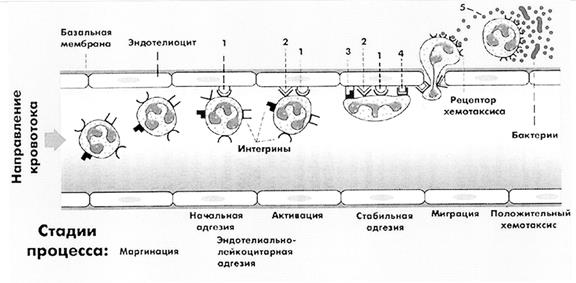
Рис. 3. Маргинация, адгезия и миграция (диапедез) лейкоцитов
(по W.Bocher, H.Denk, Ph.Heitz)
1 – Р-селектин; 2 – Фактор активации тромбоцитов; 3 – Е-селектин;
4 – иммуноглобулиновый комплекс; 5 – хемотаксические цитокины
Появление на поверхности лейкоцитов и эндотелиоцитов молекул адгезии начинается только после контакта этих клеток с рядом медиаторов воспаления и цитокинов. До этого контакта молекулы адгезии (L-селектины и бета-2-интегрины в лейкоцитах; Р-селектины и Е-селектины в эндотелиоцитах) содержатся во внутриклеточных гранулах и не функционируют. На первых этапах и движение, и адгезия лейкоцитов и эндотелиоцитов обеспечивается в основном за счет селектинов и, частично, интегринов которые соединяются с соответствующими рецепторами на поверхности лейкоцитов и клеток эпителия сосуда. В последующем происходит «слущивание» (шеддинг) селектинов с поверхности лейкоцитов и их место занимают бета-2-интегрины, резко увеличивающие адгезию лейкоцитов к сосудистой стенке. Молекулы адгезии оказывают содействие лейкоцитам и при их прохождении через сосудистую стенку. В дальнейшем, при движении лейкоцитов к центру очага воспаления, их «привлечение» обеспечивают молекулы (цитокины) хемотаксиса.
Электротаксис – движение отрицательно заряженных лейкоцитов по направлению к эпицентру очага воспаления (где накапливаются положительно заряженные частицы – ионы из разрушенных клеток, мицеллы белка, погибшие или поврежденные клетки и др).
Важнейшей составной частью воспалительного процесса является фагоцитоз, в котором принимают участие как фагоциты крови (лейкоциты), так и фагоциты, находящиеся вне сосудистого русла (например, тканевые макрофаги).
Фагоцитоз - это процесс поглощения и переваривания клеткой различных корпускулярных агентов (частиц) которые являются или становятся инородными для всего организма или для отдельных его частей.
При фагоцитозе происходит процесс поглощения и переваривания не только частиц, изначально являющихся чужеродными для организма, но и тех, которые могут стать таковыми при определенных условиях (Например, микроорганизмы, составляющие нормальную микрофлору кишечника, при их парентеральном проникновении в ткани становятся объектами фагоцитоза, или эритроциты в кровеносном русле для организма не чужеродны, но если они попадут в ткани при кровоизлиянии, то могут стать объектами фагоцитоза.).
Захват клетками капель жидкости и использование этих жидкостей в процессах внутриклеточного пищеварения носит название пиноцитоза. Кроме того, чужеродные частицы могут поглощаться фагоцитами и за счет эндоцитоза (так называемое – рецептор-опосредованное взаимодействие).
Процесс фагоцитоза включает в себя несколько стадий.
Первая стадия – стадия маргинации, адгезии и диапедеза лейкоцитов нами уже была рассмотрена выше.
Вторая стадия - передвижение фагоцита к объекту фагоцитоза. Наиболее известные хематтрактанты для лейкоцитов -интерлейкин 8, моноцитарный хемотаксический фактор, лейкотриен В4.
Механизм таксиса:
- скопление хеморецетпоров (кэппинг) на стороне лейкоцита, обращенной в сторону наибольшей концентрации хемотаксинов. Этот полюс становится ведомым.
- изменение коллоидного состояния цитозоля лейкоцита – переход из состояния золя в состояние геля.
- снижение поверхностного натяжения на обращенной в сторону очага воспаления области мигрирующего лейкоцита («головной полюс»), что стимулирует перемещение цитозоля лейкоцита именно в головной конец.
- сокращение актиновых филаментов хвостового полюса и перестройка структур цитоскелета лейкоцита.
- выталкивание цитозоля к головному концу и движение лейкоцита в очаг воспаления.
Третья стадия – опсонизация объектов фагоцитоза. Опсонизация – это процесс взаимодействия опсонинов (иммуноглобулинов IgG1, IgG3, IgM, белков системы комплемента С3b, C4, C5a, С-реактивного белка) с рецепторным аппаратом инфекционной частицей. На фагоцитах есть рецепторы к Fc-фрагментам иммуноглобулинов и к белкам системы комплемента. В результате инфекционные частицы плотно прикрепляются к оболочке фагоцитов, а иммуноглобулины, белки комплемента и С-реактивный белок служат как бы «мостиком», прочно соединяющим фагоцит и фагоцитируемый объект.
Четвертая стадия - погружение объекта в фагоцит, которая может осуществляться двумя путями. Во-первых, фагоцит, подобно амебе, способен выпускать псевдоподии, которые смыкаются над объектом фагоцитоза, и он оказывается внутри фагоцита. Во-вторых, это погружение может происходить путем инвагинации клеточной оболочки фагоцита: в нем образуется все увеличивающаяся впадина, в которую и погружается объект; затем края впадины смыкаются над объектом, и он оказывается внутри фагоцитирующей клетки. В процессе погружения объекта в фагоцит важную роль играют электрические заряды объекта и фагоцита, интенсивность хемотаксиса и величина поверхностного натяжения в месте соприкосновения фагоцита и фагоцитируемого объекта.
Пятая стадия – переваривание. Вначале живой объект, попавший в фагоцит и находящийся в его пищеварительной вакуоли, должен быть убит. Живые объекты фагоцит не переваривает. Основную роль в гибели живых объектов, попавших в фагоцит, играет резкий сдвиг рН протоплазмы фагоцита в кислую сторону. После того, как объект убит, пищеварительная вакуоль, в которой он находится, сливается с одной или несколькими лизосомами фагоцита, и лизосомные ферменты осуществляют процесс пищеварения в этой полости.
Живой объект может быть фагоцитирован и иным путем: в гранулах лейкоцита содержатся бактерицидные вещества (например, активные кислородные радикалы, появляющиеся в результате респираторного взрыва), которые выбрасываются в окружающую среду, и, таким образом, лейкоцит убивает микроорганизм (механизм «нейтрофильной ловушки»). Затем осуществляется процесс его погружения и переваривания.
Таковы процессы, лежащие в основе завершенного фагоцитоза.
Если микроорганизмы - объекты фагоцитоза либо обладают мощной полисахаридной капсулой (например, микобактерии туберкулеза), защищающей их от кислой реакции среды, либо выделяют вещества, которые препятствуют слиянию лизосом с пищеварительной вакуолью, в результате чего процесс внутриклеточного пищеварения не может быть осуществлен. В этом случае имеет место так называемый незавершенный фагоцитоз. Он заканчивается тем, что через некоторое время живые микроорганизмы либо выбрасываются из фагоцита, либо фагоцит гибнет.
3. Стадия воспаления- пролиферация
Острое воспаление всегда завершается фазой пролиферации, хотя пролиферативные процессы в той или иной степени выражены с самого начала воспалительного процесса. Интенсивная пролиферация начинается только тогда, когда полностью завершается альтерация и экссудация, а патогенный агент уничтожен или выведен за пределы организма. В противном случае (если патогенный агент не уничтожен) острое воспаление может трансформироваться в хроническое.
Фазе пролиферации предшествует период накопления противовоспалительных медиаторов. Основное место среди них занимают:
- гепарин, который связывает биогенные амины, ингибирует комплемент, является мощным антикоагулянтом, инактивирует кининовые системы;
- ингибиторы протеаз – вещества, подавляющие активность лизосомальных гидролаз и, тем самым, резко снижающие повреждение клеток и тканей;
- антифосфолипазы, ингибирующие фосфолипазу А2 и за счет этого уменьшающие синтез арахидоновой кислоты и ее продуцентов – простагландинов и простациклинов. Следует указать, что выработка антифосфолипаз стимулируется глюкокортикоидными гормонами;
- антиоксиданты – металлосодержащие белки, инактивирующие кислородные радикалы и липоперекиси;
- инактиваторы воспалительных медиаторов, например, гистаминаза и кининаза, разрушающие гистамин и кинины;
- медиаторы клеточного происхождения: факторы роста эндотелия, тромбоцитов, эпидермальный фактор роста, трансформирующий ростовой факитор-в (TGF- в).
Репаративные процессы могут идти по двум направлениям: по пути регенерации (замещение погибших клеток клетками точно такого же типа) и по пути фиброплазии (замещение клеточного дефекта соединительной тканью). И регенерация, и фиброплазия осуществляются как за счет усиления пролиферации, так и за счет снижения уровня апоптоза .
В регуляции процессов репарации принимают участие и гормоны: тиреотропный, соматотропный, соматомедины, инсулин. Процессы регенерации костной ткани стимулируются половыми гормонами, а заживление ран – гормонами щитовидной железы.
Дата: 2019-02-02, просмотров: 410.