О биологической активности почвы можно судить по скорости разложения растительных остатков. Для этого растительные остатки (солома, корни, листья и др.) в пакетах из капроновой сетки помещают в разные горизонты почвенного профиля. О скорости разложения растительных остатков судят по потере массы за определенное время (месяц, сезон). При проведении исследований рекомендуется пятикратная повторность опыта. Если необходимо исключить в части вариантов деятельность животных, их посыпают нафталином, который отпугивает микро- и мезофауну, но не угнетает бактерии и грибы. В опытах можно вычленить влияние микрофлоры и микрофауны на процессы разложения растительных остатков.
Сравнительную оценку биологической активности разных объектов можно дать по интенсивности разложения льняной ткани, натянутой на стеклянную пластинку и помещенной в почву. Об интенсивности процесса судят по потере массы льняной ткани.
О скорости минерализационных процессов можно судить по скорости накопления аминокислот в почве. Для этого стеклянные пластинки, обшитые хлопчатобумажной тканью, помещают в почву. После десяти-, тридцатидневной экспозиции их извлекают из разреза и очищают щеточкой. Пластины обрабатывают раствором нингидрина в ацетоне и сушат при комнатной температуре в течение 24 ч до появления окраски. Проводят определение свободных аминокислот, сравнивая с эталонами (стандартные растворы аминокислот).
7. Функциональные группы гумусовых веществ и методы их определения.
Гумусовые кислоты содержат большой набор кислородсодержащих функциональных групп. Экспериментально можно обнаружить спиртовые и фенольные гидроксильные группы, альдегидные и кетонные группы, хиноидные карбонилы, карбоксильные, метоксильные, сложноэфирные группы и гетероциклический кислород. Группы могут находиться в свободном состоянии или связаны внутримолекулярными и межмолекулярными водородными связями.
О содержании кислородсодержащих групп в различных гуминовых кислотах можно узнать из данных Тсутсуки и Куватсука (1978) (таблица 1).
Таблица 1 - Содержание кислородсодержащих функциональных групп в гуминовых кислотах
| Группы | Минимальное содержание | Максимальное содержание |
| Карбоксильные СООН | 2,73 | 5,06 |
| Карбонильные С=О | 3,07 | 8,13 |
| Фенольные гидроксилы | 1,94 | 3,25 |
| Спиртовые гидроксилы | 0,74 | 3,30 |
| Метоксильные группы | 0,25 | 1,29 |
| Кислород функциональных групп, % к общему содержанию кислорода в ГК | 69,6 | 97,4 |
Наибольшее значение в реакциях органо-минерального взаимодействия имеют карбоксильные и фенольные группы. При взаимодействии с ионами металлов образуются соли (гуматы) или комплексные соединения, которые могут образоваться по схеме
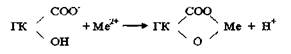
Эти же группы играют важную роль и при взаимодействии ГК и ФК с минералами, например, при образовании сложных железистых или железо-фосфатных мостиков между поверхностью частицы глинистого минерала и молекулой гумусовой кислоты. Определение функциональных групп гуминовых кислот в теоретическом отношении представляет довольно сложную задачу. Даже группы одного типа, например, карбоксильные, находятся в разных положениях и характеризуются различными константами кислотности. Они вступают в реакции нейтрализации или замещения при различных значениях рН. Наличие фенольных групп еще более осложняет задачу. Аналитические реакции протекают в гетерогенной среде, отсюда следует вероятная неполнота реакции и побочные процессы, например, адсорбция. При титровании гуминовых кислот щелочными реагентами можно обнаружить широкий спектр кислых функциональных групп со значениями рКа от <3 до 14.
Для определения общего количества кислых функциональных групп применяют титриметрические методы. Для определения карбоксильных групп используется их способность вступать в реакцию при нейтральной реакции среды, для этого применяется метод Кухаренко - реакция гуминовых кислот с ацетатом кальция. Для разделения гидроксильных и карбоксильных групп применяют метилирование и ацилирование гуминовых кислот. Хиноидные группы можно найти по реакции восстановления гуминовых кислот растворами хлорида олова (II) или хлорида титана (III). Разработаны и другие методы, например, высокочастотное титрование в неводных средах.
Дата: 2019-02-02, просмотров: 415.