Определение элементного состава является необходимым условием исследования любых органических соединений и служит для идентификации, составления простейших формул и изучения изменений, происходящих в веществе под действием химических реагентов. Элементный анализ гумусовых веществ позволяет вскрыть особенности гумификации в почвах различных природных зон, для чего вычисляют обычно атомные отношения С:Н и С:О. Простейшие формулы для гумусовых веществ составляют редко, что связано со сложностью веществ и условностью понятия молекулярной массы применительно к ним. Атомные доли различных элементов, устанавливаемые анализом, не находятся в простых кратных отношениях. Сведения об элементарном составе необходимы для обоснованного отнесения природных органических соединений различного происхождения к группе гумусовых веществ. Методы элементного анализа разнообразны. Содержание углерода может быть найдено одним из рассмотренных выше методов, азота - методом Кьельдаля. Наилучшие результаты дает применение модифицированных методов Прегля, получивших широкое распространение в почвенно-химических лабораториях.
Для проведения элементного анализа используют гуминовые и фульвокислоты в твердом состоянии, высушенные при температуре не выше 70°С и растертые в порошок. Предварительно проводится очистка гумусовых веществ. Взятие навески для микроопределений осуществляется на аналитических весах.
Применяемые методы определения углерода и водорода основаны на количественном сожжении органического вещества до углекислого газа и воды с последующим количественным определением образующихся продуктов сгорания. Окисление может проводиться кислородом воздуха, чистым кислородом, твердыми окислителями в присутствии катализаторов и при различных температурах. Наиболее часто применяют кислород, оксид меди, хромат свинца, пероксид марганца. Для количественного определения образующихся углекислого газа и паров воды можно применять различные методы (газометрические, кондуктометрические, гравиметрические и т.д.).
Для определения азота может быть использован микрометод Дюма. В его основу положено разложение органического вещества в присутствии оксида меди в атмосфере углекислого газа. Газообразные продукты горения, состоящие из элементарного азота, оксида азота, углекислого газа, паров воды, паров сернистой кислоты и др., увлекаемые током углекислого газа, проходят через раскаленную зону восстановленной меди, оксида меди и металлического серебра. Восстановленная медь способствует восстановлению оксидов азота до элементарного азота. Элементарный азот собирается в микроазотометре и количественно определяется по объему. Сожжение вещества длится 10-15 мин.
Элементный состав гумусовых веществ может быть определен на элементарном анализаторе. Погрешность определения не превышает 0,3%, время проведения одного анализа - не более 10 мин, для анализа достаточна навеска - 0,5-2,5 мг. Для разделения и количественного определения СО2, Н2, N2 используется принцип адсорбционной газовой хроматографии.
Результаты элементного анализа позволяют характеризовать особенности гумусовых веществ различного происхождения и дают некоторые сведения о принципах их строения. Атомные отношения показывают количество атомов углерода, приходящееся в молекуле на один атом водорода, кислорода, азота. Чем больше эти отношения, тем большую роль играет углерод в построении молекулярной структуры. Повышение соотношений указывает на возрастание доли бензоидных фрагментов и снижение доли алифатических боковых цепей в молекулах гумусовых веществ. По величине соотношения С:О судят о степени окисленности органического вещества. Атомное отношение Н:С четко характеризует класс углеводородов; отношения Н:С>2 свойственны парафинам, отношения Н:С от 1,5 до 1,8-2,0 - циклопарафинам, отношение Н:С <1 - ароматическим углеводородам. Для гуминовых кислот отношение Н:С колеблется в пределах 0,6-1,0, что формально указывает на преобладание ароматических структур.
Атомные отношения позволяют решать некоторые вопросы механизмов трансформации растительных остатков и отдельных групп гумусовых веществ. Для этого удобно использовать диаграммы атомных отношений Н:С-О:С. По оси ординат отношения О:С отложены в масштабе вдвое меньше, чем отношение О:С по оси абцисс. При таком способе построения графика реакции гидратации и дегидратации выражаются прямыми линиями, проходящими под углом 45° к координатным осям. Если на диаграмме атомных отношений отложить результаты анализа элементного состава отдельных групп гумусовых веществ, то по их взаимному расположению можно судить о тех химических процессах, которыми связаны эти вещества. На рисунке 1 показаны области, отвечающие элементному составу гуминовой кислоты, фульвокислоты и растительных остатков различного происхождения. Сопоставление этих областей показывает, что переход от растительных остатков к фульвокислотам химически выражается потерей групп СН3. Превращение растительных остатков в гуминовые кислоты химически может быть описано реакциями дегидратации и деметилирования.
Диаграмма атомных отношений позволяет сделать вывод о суммарном итоге процесса трансформации, но не раскрывает его стадий.
4. Методы изучения структуры и определения молекулярной массы гумусовых веществ
Наиболее полную характеристику гумусовых веществ дает их структурная формула. К настоящему времени предложено несколько формул, но все они имеют гипотетический характер, хотя и позволяют объяснить многие свойства гумусовых веществ.
Исследования М.М. Кононовой и Н.П. Бельчиковой показали четкую связь между оптическими свойствами гумусовых веществ и условиями их образования. Спектры поглощения гумусовых веществ в УФ- (ультрафиолетовой) и видимой областях спектра применяют:
- для сравнительной характеристики гумусовых веществ различного происхождения;
- как метод изучения особенностей свойств и строения гуминовых кислот и фульвокислот;
- для быстрого количественного определения содержания гуминовых кислот и фульвокислот в почвах;
- для количественного определения некоторых компонентов, обнаруживаемых в щелочных и спиртобензольных экстрактах(например, хлорофилл);
- в экспериментальных работах - для контроля за растворимостью ГК и ФК, условиями их осаждения, образованием соединений с катионами металлов.

Рисунок 1. Диаграмма атомных отношений Н:С - О:С: ГК — гуминовые кислоты, ФК - фульвокислоты, РО - растительные остатки, 1 - потеря СН2, 2 — дегидратация, 3 — декарбоксилирование
Характер спектров поглощения гумусовых веществ в УФ-(200-400 нм) и видимой областях (400-750 нм) электромагнитного спектра однотипен. Зависимости имеют вид монотонных кривых без максимумов поглощения с резким возрастанием оптической плотности при длинах волн короче 400 нм.
ИК-спектры существенно отличаются от спектров в УФ- и видимой областях. В интервале от 2,5 до 10-12 мкм спектры ГК и ФК характеризуются довольно большим набором полос поглощения, обусловленных присутствием в молекулах этих веществ ряда атомных группировок. Хорошо идентифицируются полосы, относимые за счет групп СН, СН2, СН3, ОН, СООН, С=С, NH2, C=N и др. Для качественной характеристики ИК-спектра (инфракрасного спектра) пользуются длиной волны X (мкм) или волновым числом v (см1). ИК-спектры называются молекулярными, спектры в УФ- и видимой области спектра - электронными. Для количественной характеристики используют те же показатели, что и в других областях спектра: пропускание, поглощение, оптическую плотность. Для количественного определения могут быть использованы только те системы, светопоглощение которых подчиняется закону Бугера-Ламберта-Бера.
При работе в ИК-области спектра нельзя использовать водные растворы, так как вода интенсивно поглощает ИК-излучение. Органические растворители не поглощают излучения в ИК-области, гумусовые вещества в них нерастворимы. В связи с этим гуминовые и фульвокислоты изучают в твердом состоянии. Применяют два основных метода подготовки: растирание в минеральном масле (например, вазелиновое масло) до получения однородной массы и запрессовывание растертых препаратов в солевые пластины.
Важной задачей при изучении гумусовых веществ является определение молекулярных масс гумусовых кислот. Гумусовые кислоты полидисперсны, в отдельных фракциях молекулярные массы колеблются около некоторого среднего значения. Все молекулы такой фракции образуют статистически однородную совокупность по молекулярным массам, распределение которых подчиняется нормальному закону. Гуминовые кислоты, выделенные из какой-либо почвы, представлены несколькими такими совокупностями молекул. При анализе молекулярно-массового распределения суммарная картина выражается кривой, имеющей полимодальный характер. Все методы определения молекулярных масс позволяют получить только средние значения.
В зависимости от метода определения и способа усреднения различают два типа средних молекулярных масс.
1. Среднечисловое значение молекулярной массы Мп (получают при определении молекулярной массы химическим, крио-скопическим, эбулиоскопическим методами)
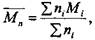 (9)
(9)
где М i ( - молекулярная масса i-го компонента препарата, ni - число молекул с молекулярной массой Mi .
 2. Средневесовая молекулярная масса Mw (получают при определении методом светорассеяния или гель-фильтрации)
2. Средневесовая молекулярная масса Mw (получают при определении методом светорассеяния или гель-фильтрации)
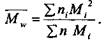 (10)
(10)
Средневесовая молекулярная масса в наибольшей степени отражает вклад той фракции, которая количественно преобладает (по массе) в исследуемом препарате. Среднечисловая молекулярная масса этого не учитывает.
Дата: 2019-02-02, просмотров: 599.