Ответ: в соответствии с рядом стандартных электродных потенциалов разбавленные кислоты (кроме HNO 3 ) взаимодействуют только с металлами, у которых 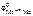 < 0. так как (см. табл. 11.1)
< 0. так как (см. табл. 11.1) 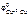 = +0,34 В,
= +0,34 В, 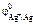 = +0,8 В,
= +0,8 В,  = –2,34 В,
= –2,34 В, 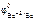 = –2,90 В, то с хлороводородной кислотой взаимодействуют только Mg и Ba .
= –2,90 В, то с хлороводородной кислотой взаимодействуют только Mg и Ba .
Mg + 2HCl = MgCl2 + H2.
Ba + 2HCl = BaCl2 + H2.
3. Можно ли получить серебро и магний из водных растворов солей AgNO 3 и Mg ( NO 3 )2 восстановлением цинком при стандартных условиях? Написать уравнение реакции.
Ответ: в соответствии с рядом стандартных электродных потенциалов металлы, у которых меньшее значение стандартных электродных потенциалов, вытесняют металлы с большим значением стандартных электродных потенциалов из водных растворов их солей. Находим стандартные электродные потенциалы (см. табл. 11.1):
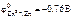 ,
,
, 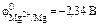 .
.
Так как 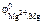 <
< 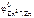 <
< 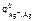 , то цинк восстанавливает серебро из раствора AgNO 3 , а магний из раствора Mg ( NO 3 )2 цинком не восстанавливается:
, то цинк восстанавливает серебро из раствора AgNO 3 , а магний из раствора Mg ( NO 3 )2 цинком не восстанавливается:
Zn + 2AgNO3 = 2Ag + Zn(NO3)2.
КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
УРОВЕНЬ А
1. Назвать следующие комплексные соединения: K 3 [ Fe ( CN )6]; [ PtCl 3 ( NH 3 )3] Cl ; [ Co ( NO 2 )3( NH 3 )3].
Ответ:
а) K 3 [ Fe ( CN )6] – гексацианоферрат ( III ) калия.
б) [ Pt ( NH 3 )3 Cl 3 ] Cl – хлорид трихлоротриамминплатины ( IV ).
в) [ Co ( NH 3 )3( NO 2 )3] – тринитротриамминкобальт.
Написать формулы следующих химических соединений:
Сульфат тетрааминмеди ( II ), гексахлороплатинат ( IV ) калия, тетрахлороамминакваплатина.
Ответ:
а) [ Cu ( NH 3 )4] SO 4 ;
б ) K2[PtCl6];
в ) [PtNH3H2OCl4].
3. Записать выражение константы устойчивости комплексных ионов [ Fe ( CN )6]4-; [ Pt ( NH 3 )2 Cl 2 ]2+.
Ответ :
Fe2+ + 6CN- <=> [Fe(CN)6]4-;
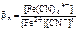 .
.
Pt4+ + 2NH3 + 2Cl- <=> [Pt(NH3)2Cl 2]2+;
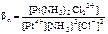 .
.
ЖЕСТКОСТЬ ВОДЫ
УРОВЕНЬ А
1. Какие из указанных соединений: Fe ( HCO 3 )2, CaCl 2 , MgSO 4 , Ca ( HCO 3 )2, Fe ( NO 3 )2, Mg ( HCO 3 )2, обусловливают:
а) постоянную жесткость воды;
б) временную жесткость воды?
Ответ: а) постоянная (некарбонатная) жесткость воды обусловлена присутствием в воде CaCl2, MgSO4, Fe(NO3)2;
б) временная (карбонатная) жесткость воды обусловлена присутствием в воде гидрокарбонатов Fe(HCO3)2, Ca(HCO3)2, Mg(HCO3)2.
Какие из указанных уравнений реакций протекают при устранении временной жесткости воды:
а ) MgCl2 + Na2CO3 + H2O = Mg(OH)2↓+ 2NaCl + CO2↑;
б ) 3CaSO4 + 2Na3PO4 = Ca3(PO4)2↓ + 3Na2SO4;
в) Fe(HCO3)2 + 2Ca(OH)2 = Fe(OH)2↓ + 2CaCO3↓ + 2H2O;
4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3↓?
Ответ: для устранения временной жесткости в воду добавляют гашеную известь С a ( OH )2; при этом протекает реакция.
Fe(HCO3)2 +2Ca(OH)2 = Fe(OH)2↓ + 2CaCO3↓ + 2H2O:
4 Fe ( OH )2 + 2 H 2 O + O 2 = 4 Fe ( OH )3↓ (вторичный процесс).
Какие из указанных уравнений реакций протекают при устранении постоянной жесткости воды:
а) Mg ( HCO 3 )2 + 2 Ca ( OH )2 = Mg ( OH )2↓+ 2 CaCO 3 ↓ + 2 H 2 O ;
б ) CaSO4 + Na2CO3 = CaCO3↓ + Na2SO4;
в) Ca(HCO3)2 = CaCO3↓ + CO2↑ + H2O?
Ответ: для устранения постоянной жесткости в воду добавляют техническую соду ( Na 2 CO 3 ), при этом протекает реакция
б ) CaSO4 + Na2CO3 = CaCO3↓ + Na2SO4 .
ВЫСОКОМОЛЕКУЛЯРНЫЕ СОЕДИНЕНИЯ (ПОЛИМЕРЫ). СПОСОБЫ ПОЛУЧЕНИЯ
УРОВЕНЬ А
Дата: 2018-12-28, просмотров: 325.