При взаимодействии бромоводорода с 1,3-бутадиеном соотношение количеств получающихся продуктов 1,2- и 1,4-присоединения зависит от температуры и времени реакции.
При низкой температуре (минус 80 оС) образуется смесь, с массовой долей продукта 1,4-присоединения 20 % и продукта 1,2-присоединения - 80 %. При температуре 40 оС - продукта 1,4-присоединения 80 % и продукта 1,2-присоединения - 20 %.
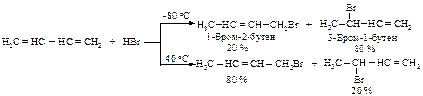
Каждый изомер совершенно устойчив при низкой температуре:
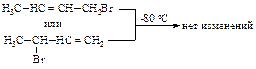
Однако любой из продуктов 1,2- или 1,4-присоединения при нагревании до 40 оС превращается в смесь изомеров, получаемую в реакции I,3-бутадиена с бромоводородом при температуре 40 оС:
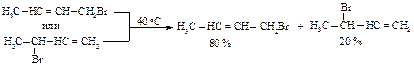
При минус 80 оС оба продукта устойчивы, не превращаются друг в друга. Следовательно, соотношение, в котором их выделяют, и есть то соотношение, в котором они образуются: 20 % продукта 1,4-присоединения и 80 % продукта 1,2-присоединения. Значит, при низкой температуре 1,2-присоединение происходит быстрее, чем 1,4-присоединение, т.е. количества продуктов определяются энергиями активации реакций их образования.
Если при нагревании любой из продуктов превращается в одну и ту же смесь, то смесь эта является равновесной, и в ней преобладает более устойчивый продукт 1,4-присоединения. Это означает, что при высокой температуре соотношение продуктов определяется равновесием.
Рассмотрим механизм реакции. На первой стадии образуется аллильный карбокатион. При минус 80 оС бромид-ион, вероятно, не может быстро отойти от только что возникшего карбокатионного центра. Он быстро присоединяется к соседнему атому углерода и образует 3-бром-1-бутен.
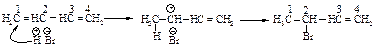
Энергия активации присоединения аниона брома к атому C2 должна быть меньше, чем энергия активации присоединения аниона брома к концевому атому углерода (С4). Этот продукт при минус 80 оС образуется быстрее. Его называют кинетически контролируемым продуктом реакции.
При 40 оС скорость 1,2-присоединения увеличивается, но вместе с ней растет и скорость обратной реакции, т.к. и ее энергетический барьер невысок.
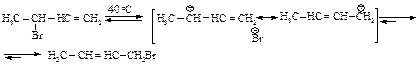
При повышенной температуре становится возможным присоединение BrӨ к концевому атому углерода и образование продукта 1,4-присоединения. Таким образом, увеличивается скорость образования продукта 1,2-присоединения, его ионизации [низкий энергетический барьер Еа(1,2)] и скорость его превращения в продукт 1,4-присоединения. Последний может также ионизироваться, но отщепление иона BrӨ от этого изомера будет происходить гораздо труднее из-за его устойчивости [высокий энергетический барьер Еа(1,4)]. При высокой температуре продукт 1,4-присоединения будет накапливаться. Ввиду большей устойчивости продукта 1,4-присоединения его называют термодинамически контролируемым продуктом реакции.
Термодинамически контролируемый продукт – это более устойчивый продукт, который накапливается не в результате более быстрого образования, а в результате равновесия.
Термодинамический контроль выступает на первый план при увеличении времени реакции и температуры (контроль равновесием).
Обратите внимание, что в реакции Ad Е сопряженных диенов более устойчивый продукт образуется с меньшей скоростью. Это характерно для ряда других реакций, например, электрофильного сульфирования и алкилирования ароматических углеводородов (аренов). Изучение присоединения к сопряженным диенам дает объяснение, почему при разных температурах из одних и тех же исходных веществ образуются разные продукты.
Дата: 2018-12-21, просмотров: 395.