При планировании комбинаторного синтеза для оптимизации строения известного лидера необходимо учитывать различные факторы, такие, как биологические и физические свойства соединения, связывающие взаимодействия с мишенью. Для примера, если связывающие взаимодействия с обычными лигандами известны, то эти сведения необходимо учитывать для определения размера, типа и относительного положения функциональных групп вводимых в синтез. Так, если мишень является цинк-содержащей протеазой, то библиотека должна содержать карбоксильные или тиольные группы. Кроме того, известно, что половина известных лекарственных средств содержат только 32 типа центроидов. При этом только относительно небольшие заместители представляют собой основное множество в боковых цепях известных лекарственных средств. Это дает возможность моделировать аналоги молекулы лекарственного средства и использовать компьютер для направленного дизайна библиотек. Применяются методы молекулярной механики и, в основном, полуэмпрические методы квантовой химии. Для описания молекул используются дескрипторы, характеризующие такие свойства молекулы как log P, молекулярный вес, число Н-доноров, число Н-ацепторов, число конформационно подвижных связей, ароматичность, степень разветвления связей и присутствие или отсутствие специфических функциональных групп
Определение активности
Высокопроизводительный скрининг
Поскольку комбинаторный синтез позволяет получать большое число соединений за очень короткое время, то испытания биологической активности также должны вестись быстро и автоматически. Этот процесс носит название выскопроизводительного скрининга (ВПС) (high throughput screening). В традиционной методике соединения тестируются и анализируются на плате, содержащей 96 небольших ячеек с емкостью 0,1 мл. В ВПС появились платы с 1536 ячейками объемом 1-10 микролитров. Для идентификации активных соединений используются методы флуоресценции и хемолюминисценции. Дальнейшее уменьшение объема (менее 1 микролитра) создает проблемы при упаривании малых объемов. Однако ведутся работы в направлении испытаний в тонких пленках, которые можно анализировать с помощью капиллярного электрофореза. Кроме того, ведутся работы по созданию машин для ультрамалых объемов синтеза и анализа. На кремневой подложке размером 10 х 10 см можно будет создать 105 отдельных ячеек объемом 10-9 литра.
Скрининг на грануле
Иногда структуры удается тестировать прямо на твердой фазе. Такой скрининг на грануле предполагает взаимодействие с мишенями, которые мечены ферментами, флюоресцирующей меткой, радионуклидами или хромофорами. Положительная реакция регистрируется по флюоресценции или изменению окраски. Такой метод является очень быстрым и дает возможность анализировать 108 гранул. Активные гранулы могут быть отсортированы микроманипуляцией с последующим установлением строения активного соединения. Однако, может наблюдаться так называемая фальшивая отрицательная активность из-за пространственных трудностей взаимодействия твердой фазы с мишенью. Поэтому все же надежнее удалять синтезированную молекулу с гранулы. Однако иногда бывает, что соединение становится нерастворимым в пробе и дает отрицательный результат, тогда как оно давало положительный эффект находясь на твердой фазе.
Примеры комбинаторного синтеза
Комбинаторная химия удовлетворяет требованиям быстрого получения новых лидеров в различных областях. Большинство ранних работ по комбинаторной химии были в области получения пептидов с использованием твердофазных процедур. Это привело к получению новых ингибиторов протеаз HIV, антимикробных препаратов, лигандов опиатных рецепторов и ингибиторов протеаз аспартамовой кислоты. Однако, пептиды не идеальные кандидаты для лекарственных средств, они обычно обладают слабой оральной активностью, поскольку неустойчивы для пищеварительных ферментов.
Первым опытом получения иных соединений явилась попытка использования таких процедур для получения пептидов на основе неприродных аминокислот. Кроме того, пептиды могут быть модифицированы путем различных превращений, например реакциями N‑метилирования. Пептиды могут быть получены также связыванием N‑замещенных глицинов, давая продукты, которые известны как пептоиды, в которых боковые цепи связаны с азотом, а не с α‑углеродом. Некоторые из них могу служить лигандами для различных важных рецепторов и демонстрируют повышенную метаболическую стабильность.
Ациклические библиотеки
Кроме библиотек пептидов и пептидоподобных структур в ряду ациклических соединений в качестве примера можно привести библиотеку на основе четырехкомпонентной реакции Уги. Синтезирована методом ОГОС на смоле Ринка 96-членная библиотека N-ациламиноалкиламидов из четырех компонентов: 32 карбоновых кислот, одного амина, восьми альдегидов и одного изоцианида:
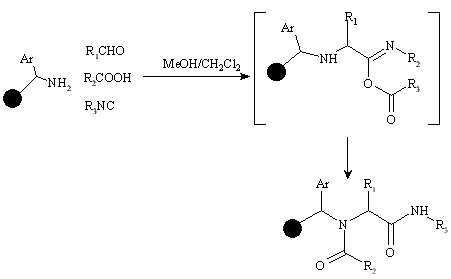
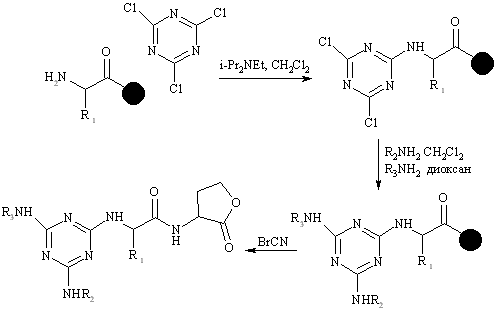
Описана библиотека 12000 триазинов. Избыток цианурхлорида реагирует с иммобилизованнм амином с образованием замещенного хлортриазина. Затем второй атом хлора замещается на аминогруппу, а третий, менее реакционно способный, атом хлора замещается при повышенной температуре.
Дата: 2018-12-21, просмотров: 362.