Третья стадия включает улучшение фармацевтических и фармакокинетических свойств таким образом, чтобы сделать лекарство удобным для клинического использования, например, повысить его растворимость в воде и химическую стабильность, пролонгировать его действие и т.д.
Под термином фармакокинетика понимают судьбу вещества в организме, т.е. все то, что делает организм с лекарством. Эти исследования включают изучение всасывания, распределение вещества в тканях и органах, метаболизм и выведение из организма.
Фармакодинамика – изучение изменений, производимых лекарством в функциях организма, остаются ли они неизменными или нарушаются, т.е. все то, что делает лекарство в организме.
При разработке лекарственного препарата всегда приходиться прибегать к структурной модификации – это специальный метод создания новых структур. Рассмотрим, какие существуют подходы.
Создание биоизостерических соединений.
Биоизостер - химическая группа, которая способна заменить другую химическую группу, не сильно изменив при этом трехмерную молекулярную структуру и тем самым физиологическую активность
Создание пролекарств ( pro drug), соединений, не обладающих выраженной биологической активностью, но способных превратиться в активные соединения либо посредством ферментативной реакции, либо химическим путем без участия белкового катализатора.
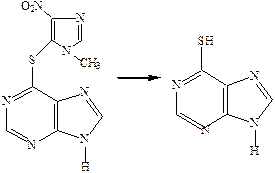
В организме азатиоприн медленно превращается в 6-меркаптопурин (иммунодепрессант), что приводит к пролонгированию действия последнего.
Создание мягких препаратов ( soft drug), фармакологический эффект которых локализован в определенном месте, а их распределение в других местах приводит к быстрой деструкции или инактивации.
Создание двойных лекарств ( twin drug) – фармакологически активных соединений, содержащих две фармакоформные группы, объединенных ковалентно в одну молекулу. Двойные лекарства могут быть неидентичными, имеющими в качестве составляющих различные структуры.
Каждый из упомянутых типов модификаций, улучшающих активность, приводит к созданию новой химической структуры, а она может также обладать меньшей активностью или иметь другой фармакологический профиль, поэтому эта часть исследований часто неотделима от QSAR стадии.
Комбинаторный синтез
В недавнем прошлом открытие лекарственного средства начиналось с индивидуального синтеза сотен, а иногда и тысяч аналогов малоактивного препарата, в надежде повысить его активность и селективность, с одновременным снижением токсичности. В среднем, для достижения поставленной цели необходимо было синтезировать более 10 000 соединений, а чтобы получить это молекулярное множество, один человек должен был бы работать около 1000 лет.
В настоящее время поиск новых лекарственных препаратов строится на принципиально новой основе.
Теперь все начинается с расшифровки структуры генов, кодирующих белки, ответственные за проявление тех или иных биологических функций. Затем эти “мишени” (targets) получают в чистом виде и создают специальные тестовые системы, позволяющие уже не in vivo, а микрометодами, in vitro, определять биологическую активность как давно синтезированных так и вновь получаемых веществ.
Таким образом находят биологически активную структуру (hit compounds), которую модифицируя преобразуют в соединение-лидер (lead compounds), в результате оптимизации свойств которого получают лекарственное соединение (clinical candidate). Схематично этот процесс можно выразить следующим образом:
Идентификация мишени
Синтез молекулярного множества, скрининг
Определение строения и идентификация хита
Оптимизация хита
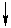
Создание соединения-лидера
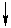
Оптимизация соединения-лидера
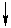
Потенциальное лекарственное средство
Успехи геномики свидетельствуют о том, что в ближайшее десятилетие будет получено около 2000 новых мишеней и темп скрининга придется повышать, несмотря на то, что уже в настоящее время удается подвергнуть скринингу до 100 тысяч соединений в расчете на одну мишень. Поэтому если ранее скрининг отставал от синтеза, то теперь ситуация изменилась: вдобавок к образцам сотен тысяч уже известных органических веществ, составляющих так называемые исторические библиотеки, понадобилось быстро получать миллионы соединений.
Подобную задачу способно решить только особое направление в органической химии, так называемый комбинаторный синтез, позволяющий специальными приемами быстро синтезировать обширные коллекции веществ с похожей структурой, так называемые библиотеки.
Комбинаторный синтез – это одна из наиболее быстро развивающихся в последнее время областей фармацевтической индустрии. Он является наиболее важным инструментом для создания новых лекарственных препаратов. Что же такое комбинаторный синтез и почему он так важен?
Говоря попросту, комбинаторный синтез является способом получения большого числа соединений за короткое время. При этом используются обычные реакционные пути и традиционный набор исходных материалов и реагентов.
Обычно химик получает соединение, которое он выделяет, очищает и идентифицирует. При комбинаторном синтезе делается акцент на получение смеси. Строение соединения необязательно устанавливать. Необязательно выделять и очищать. Вместо этого каждую смесь тестируют на биологическую активность целиком. Если смесь не проявляет активность, то нет необходимости эту смесь более изучать и ее сохраняют. Если активность проявляется, то уже требуется идентификация каждого компонента смеси. В известном смысле комбинаторный синтез выглядит как синтетический эквивалент природного первичного океана-бульона, в котором происходил в течение эволюции случайный синтез различных химических молекул, немногие из которых проявляли биологическую активность.
Комбинаторный синтез используется в основном в двух направлениях:
Дата: 2018-12-21, просмотров: 411.