4.2.1 Обратное алкалиметрическое титрование.
Метод основан на образовании натриевых солей за счет незамещенных карбоксильных групп. Титрант нейтрализует карбоксильную группу в γ-положении:
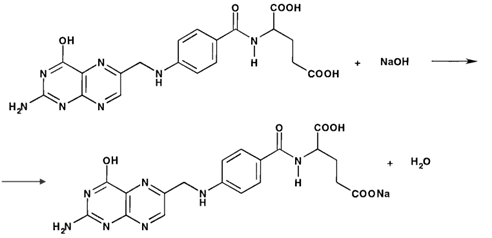
Для проведения определения навеску порошка растертых таблеток фолиевой кислоты массой 0,5 г (точная навеска) растворяем в избытке 0,1 М раствора гидроксида натрия (25 мл), а затем медленно титруем несвязавшееся количество щелочи 0,1 М раствором хлороводородной кислоты в присутствии индикатора тимолфталеина:
NaOH + HCl → NaCl + H2O
В КТТ синий раствор индикатора обесцвечивается (рис. 10).
На титрование избытка щелочи израсходовано соляной кислоты (К=1,01):
1) 24,2 мл;
2) 24,2 мл;
3) 24,1 мл,
что в среднем дает
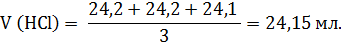
Титр раствора натрия гидроксида (К=0,98) по фолиевой кислоте:
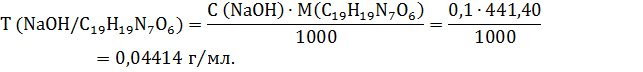

Рисунок 10. Окраска индикатора тимолфталеина.
Для определения средней массы одной таблетки фолиевой кислоты (Р) взвешиваем на аналитических весах 20 таблеток и делим полученное значение на 20:
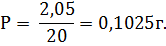
При использовании метода заместительного титрования содержание кислоты фолиевой (Х, г) в расчете на одну таблетку найдем по формуле:
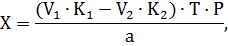
где V1 и V2 – соответственно объемы титрованных растворов, взятого в избытке и пошедшего на титрование, мл;
К1 и К2 – поправочные коэффициенты титровальных растворов;
Т – титр раствора по определяемому веществу, г/мл;
Р – средняя масса одной таблетки, г;
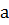 – навеска лекарственного вещества, взятая на анализ, г.
– навеска лекарственного вещества, взятая на анализ, г.
Подставляем значения:
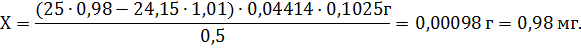
4.2.2. Фотоколориметрическое определение.
Количественное определение содержания фолиевой кислоты в препарате проводили на фотоколориметре модели APEL AP-101 фирмы Медтехкор, Санкт-Петербург, РФ (рис. 11).

Рисунок 11. Фотоколориметр APEL AP-101
Около 1 г порошка растертых таблеток (точная навеска) помещаем в мерную колбу емкостью 100 мл, прибавляем 50 мл воды, 2 мл концентрированного раствора аммиака и перемешиваем. После этого доводим объём раствора водой до метки и фильтруем, отбрасывая первые 15 мл фильтрата. 10 мл полученного фильтрата помещаем в мерную колбу емкостью 100 мл, доводим объём до метки 3%-ным раствором гидрофосфата калия и перемешиваем.
Параллельно готовим стандартный раствор фолиевой кислоты. Для этого около 0,05 г стандартного образца фолиевой кислоты (точная навеска) растворяем в смеси 50 мл воды и 2 мл концентрированного раствора аммиака в мерной колбе ёмкостью 100 мл. Доводим объем раствора водой до метки и перемешиваем. 1 мл полученного раствора помещаем в мерную колбу емкостью 50 мл и доводят объем раствора до метки 3%-ным раствором гидрофосфата калия.
В две пробирки наливаем по 5 мл стандартного раствора фолиевой кислоты (пробирки 1 и 2). В две другие пробирки наливаем по 5 мл испытуемого раствора (пробирки 3 и 4). В 5-ю пробирку наливают 5 мл 3%-ного раствора гидрофосфата калия.
В пробирки 1 и 3 наливаем по 1 мл 0,4%-ного раствора перманганата калия, а в пробирки 2, 4 и 5 - по 1 мл воды. Содержимое пробирок перемешиваем и оставляем на 3 мин.
При этом в пробирках 1 и 3 протекают реакции окислительного гидролиза с образованием птерин-6-карбоновой кислоты и n-аминобензоилглутаминовой кислоты:
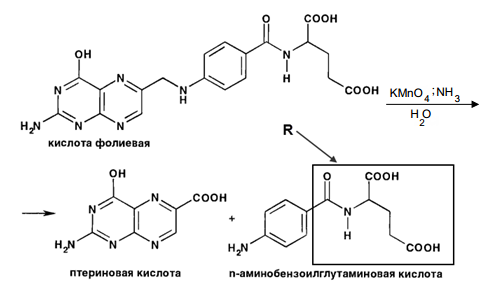
Затем во все пробирки приливаем по 1 мл 2%-ного раствора нитрита натрия и по 1 мл 25%-ного раствора хлористоводородной кислоты, хорошо перемешиваем и оставляем на 2 мин. При этом происходит образование сои диазония:
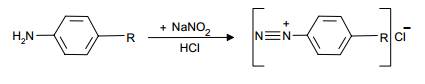
Во все пробирки приливаем по 1 мл 5%-ного раствора сульфамата аммония и осторожно перемешивают до прекращения выделения пузырьков газа:

Во все пробирки приливаем по 1 мл 0,1%-ного раствора N-(1-нафтил)-этилендиамина дигидрохлорида, перемешивают и оставляют на 10 мин. В результате происходит образование азокрасителя:
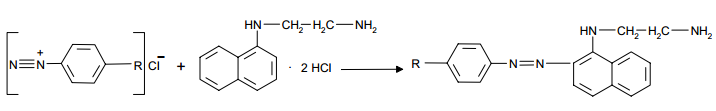
Измеряем оптическую плотность растворов на фотоколориметре при длине волны 550 нм в кювете толщиной 1 см относительно контрольного раствора (пробирка 5).
Содержание фолиевой кислоты в одной таблетке, г, вычисляем по формуле:
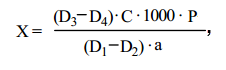
где D1, D2, D3, D4 – оптические плотности растворов в пробирках 1, 2, 3. 4;
С – концентрация стандартного раствора фолиевой кислоты, мг/мл;
а – навеска препарата, г;
Р – средняя масса таблетки, г.
При расчетах использовали полученные значения оптической плотности исследуемых растворов:
D1 = 0,889;
D2 = 0,441;
D3 = 0,883;
D4 = 0,440.
Концентрация стандартного раствора фолиевой кислоты равна 0,05/100/50 = 0,00001 г/мл.
На основание полученных значений находим содержание кислоты фолиевой в таблетке (г):
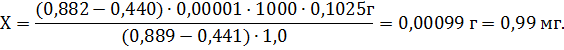
5. Заключение, выводы, рекомендации
Важным свойством фолиевой кислот является се способность к окислительно-восстановительным превращениям. Это свойство позволяет ей выполнять определенные биологические функции в организме (участие в обмене одноуглеродных радикалов) и может быть использовано в анализе препаратов, ее содержащих.
В результате проведенного исследования, нами были изучены методы синтеза препаратов, являющихся производными птерина, их классификация и фармакологическое применение. Из производных птерина витаминной активностью обладает только фолиевая кислота и кальция фолат, используемые для профилактики авитаминоза и предотвращения негативных последствий применения метотрексата.
Быль проведен литературный обзор с целью изучения классических, методов анализа производных птерина, и новых альтернативных разработок.
Химические методы идентификации отличаются простотой выполнения и хорошей наглядностью, но несколько уступают в простоте методу УФ-спектроскопии. Методы количественного определения, при чем как химические, так и физико-химические, являются достаточно трудоемкими.
Химический метод алкалиметрического титрования, будучи относительно простым в выполнении, не обладает высокой точностью, что еще усугубляется невысоким содержанием фолиевой кислоты в одной таблетке. Спектрофотометрическое определение дает более точные результаты, но требует большой затраты времени и расхода реактивов.
На основании проведенного исследования можно сделать выводы:
1) Исследуемый препарат является фолиевой кислотой.
2) Содержание кислоты фолиевой в одной таблетке соответствует требования ФС (0,9-1,1 мг).
3) Качество фармацевтического препарата «Фолиевая кислота» Борисовского ЗМП (Беларусь) удовлетворяет требованиям НД.
6. Источники:
1. Абакшонок А.В., Еремин А.Н., Агабеков В.Е. Взаимодействие фолиевой кислоты с наночастицами серебра. // Известия Национальной Академии наук Беларуси. – Мн., 2014. № 2, С. 19-26.
2. Абдуева Ф. М., Бычкова О. Ю., Бондаренко И. А. Терапевтическая фармакология: Практическое пособие для студентов и врачей. Харьков: ХНУ им. В.Н. Каразина 2011.
3. Арзамасцев Л. П. Фармацевтическая химия: Учеб. Пособие. – М.: ГЭОТАР-МЕД, 2004.
4. Бауэр Г., Энгельгард Х., Хеншен А., Высокоэффективная жидкостная хроматография в биохимии: Пер. с англ./Под ред. А. Хеншен и др.—М.: Мир, 1988.
5. Беликов В.Г. Фармацевтическая химия. – М.: МЕДпресс-информ, 2007.
6. Березов Т.Т., Коровкин Б.Ф. Биологическая химия. – М.: Медицина, 1998.
7. Венгеровский А.И. Лекции по фармакологии, М.: Физико-математическая литература, 2007
8. Витамины и минеральные вещества: Полная энциклопедия. Сост.: Т.П.Емельянов. – СПб. 2001.
9. Горбачев В.В., Горбачева В.Н. Витамины, микро- и макроэлементы. Справочник. — Мн.: Книжный Дом; Интерпрессервис, 2002.
10. Государственная фармакопея СССР. X-е издание. – М.: медицина, 1968.
11. Ерина О.В., Хохлов В.Ю., Селеменев В.Ф. Спектрофотометрическое определение рутина, аскорбиновой, никотиновой и фолиевой кислот в их смесях. // «Заводская лаборатория. Диагностика материалов». № 8, 2011. Том 77. С. 20-23.
12. Зыков А.В. Экстракция витаминов группы В и их определение в фармацевтических препаратах. Автореф. дис. канд. хим. наук. – Воронеж, 2013.
13. Иванова А.А. Влияние модифицированных витаминов с антиоксидантным действием на эффективность и токсичность противоопухолевой терапии в эксперименте. Автореф. дис. канд. мед. наук. – Томск, 2009.
14. Крыльский Д.В., Сливкин А.И., Брежнева Т.А. Практикум по фармацевтической химии. – Воронеж: Издательско-полиграфический центр Воронежского государственного университета, 2008.
15. Кулешова М. И. и др. Анализ лекарственных форм, изготовляемых в аптеках/М. И. Кулешова, Л. Н. Гусева, О. К. Сивицкая. – Пособие. 2-е изд., перераб. и доп. – М.: Медицина, 1989.
16. Кухта В.К., Морозкина Т.С., Таганович А.Д. Биологическая химия. – М.: Медицина, 2008.
17. Лифляндский В. Г. Витамины и минералы. – М: ОЛМА Медиа Групп; 2010.
18. Масякова Е. Н. Спектрофотометрический анализ смесей водорастворимых витаминов с применением хемометрических алгоритмов. Автореф. дис. канд. хим. наук. – Томск, 2009.
19. Международная Фармакопея. 3-е издание, том 2. Спецификация для контроля качества лекарственных препаратов. – Женева: ВОЗ, 1983.
20. Морозкина Т. С. Витамины. Краткое рук. для врачей и студентов мед., фармацевт. и биол. Специальностей /Т. С. Морозкина, А. Г. Мойсеёнок. — Мн.: ООО«Асар», 2002.
21. Патент № 2497825 РФ, МПК7 C07F5/00. Конъюгат фолиевой кислоты и способ его получения / Павич Т.А., Воробей А. В., Соловьев К. Н.
22. Племенное В. В. Введение в химию природных соединений. Казань, 2001.
23. Ровбуть Т.И. Показатели витаминной обеспеченности и окислительного стресса у детей Гродненской и Гомельской областей Беларуси. Автореф. дис. канд. мед. наук. – Минск, 2007.
24. Салахов И.А. Унифицированные подходы к анализу метаболитов, химиотерапевтических, анальгезирующих и противовоспалительных лекарственных средств методом ВЭЖХ Автореф. дис. канд. мед. наук. – Казань, 2010.
25. Сирицо С.И. Обращено-фазовая изократическая ВЭЖХ для аналитического контроля водорастворимых витаминов в многокомпонентных рецептурах. Автореф. дис. канд. хим. наук. – Москва, 2008.
26. Сливкин А. И., Селеменев В. Ф., Суховерхова Б. А. Физико-химические и биологические методы оценки качества лекарственных средств: Учеб. пособие / Под ред. В. Г. Артюхова, А. И. Сливкина. — Воронеж: Издательство Воронежского государственного университета, 1999.
27. Смирнов В.А., Климочкин Ю.Н. Витамины и коферменты: Учеб. пособие – Самара: Самар. гос. техн. ун-т, 2008.
28. Солдатенков А. Т., Колядина Н.М., Шендрик И.В. Основы органической химии лекарственных веществ. – М: Химия, 2001.
29. Тыжигирова В.В., Филиппова С.Ю. Применение ИК– и УФ– спектроскопических методов в фармацевтическом анализе. Учебное пособие по фармацевтической химии. ГОУ ВПО Иркутский государственный медицинский университет РОСЗДРАВА РФ, 2010.
30. Челнакова Н.Г. Экспериментальное обоснование и практическая реализация программы коррекции массы тела с использованием фактора питания (БАД). Автореф. дис. канд. тех. наук. – Кемерово, 2014.
31. Шаповалова Е.М. Механизмы гемостатических сдвигов при отсутствии, дефиците и избытке витаминов с антиоксидантными свойствами в рационе питания. Автореф. дис. канд. биол. наук. – Челябинск, 2010.
32. Шелеметьева О.В. Определение витаминов методом высокоэффективной жидкостной хроматографии в премиксах, биологически активных добавках и пищевых продуктах. Автореф. дис. канд. хим. наук. – Томск, 2009.
33. Материалы сайта http://www.provisor.com.ua.
34. Материалы сайта http://ribeyebar.ru.
35. Материалы сайта https://ru.wikipedia.org.
Дата: 2018-12-21, просмотров: 754.