4.1.1. Реакция образования птериновой кислоты.
Для проведения анализа помещаем 10 таблеток (0,01 г кислоты фолиевой) в фарфоровую ступку (рис. 2, а) и растираем их до гомогенного состояния (рис.2, б).


а б
Рисунок 2. Подготовка ЛП к проведению анализа.
Полученную навеску препарата растворяем в 5 мл раствора гидроксида натрия (0,1 моль/л), приливаем 5 мл раствора хлороводородной кислоты (0,1 моль/л) и 1 мл раствора калия перманганата. Реакционную смесь помещаем на 3 минуты на водяную баню с температурой 80-85°С. После охлаждения приливаем по каплям 0,2 мл раствора пероксида водорода (для удаления избытка реактива) и фильтруем. Фильтрат имеет голубую флюоресценцию в УФ-свете, обусловленную образованием птериновой кислоты:
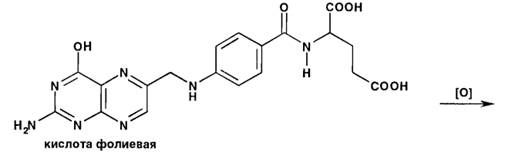
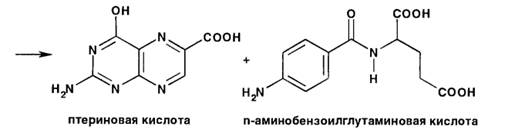
4.4.2. Реакция образования окрашенных комплексных солей фолиевой кислоты.
Наличие в птериновой части молекулы кислоты фолиевой подвижного атома водорода в гидроксильной группе и третичных атомов азота позволяет получить нерастворимые в воде окрашенные внутрикомплексные соли с катионами меди (II), свинца, серебра, кобальта, железа (III) общей формулой:
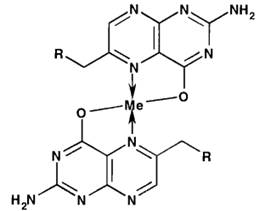
0,01 г препарата растертых таблеток фолиевой кислоты взбалтываем в течение 2-3 минут с 1-1,5 мл раствора натрия гидроксида (0,1 моль/л) и фильтруем. Помещаем 3 капли фильтрата на предметное стекло и прибавляем по 3 капли раствора солей металлов.
Образуются осадки комплексных солей:
Со свинца ацетатом – лимонно-желтый (рис. 3);
С кобальта нитратом – темно-желтый (рис. 4);
С серебра нитратом – желто-оранжевый (рис. 5);
С меди (II) сульфатом – зеленый (рис. 6);
С железа (III) хлоридом – красно-желтый (рис. 7).

Рисунок 3. Рисунок 4.
Осадок комплексной соли свинца. Осадок комплексной соли кобальта.


Рисунок 5. Рисунок 6.
Осадок комплексной соли серебра. Осадок комплексной соли меди.

Рисунок 7. Осадок комплексной соли железа
4.4.3. Реакция образования азокрасителя.
При восстановлении фолиевой кислоты в солянокислом растворе цинковой пылью в числе других продуктов отщепляется n- аминобензолглутаминовая кислота, которую диазотируют нитритом натрия:
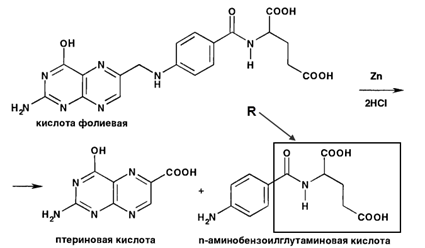
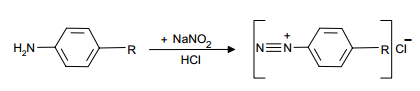
Полученная соль диазония сочетается с β-нафтолом: по реакции:
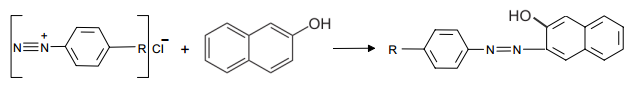
Для проведения опыта 0,01 г препарата растертых таблеток фолиевой кислоты растворяем в 1 мл 0,1 М раствора натрия гидроксида, прибавляют 0,02-0,03 г цинковой пыли, оставляем смесь на 3 мин. и фильтруем. При подкислении кислотой хлороводородной до кислой реакции среды и прибавлении нескольких капель раствора натрия нитрита получается соль диазония, которая образует со щелочным раствором β-нафтола азокраситель красного цвета (рис. 8):

Рисунок 8. Окраска полученного раствора азокрасителя.
4.4.4. УФ-спектроскопия.
Идентификацию препарата фолиевой кислоты проводили на спектрофотометре UV модели РВ 2201 ЗАО «СОЛАР», Беларусь (рис. 9).

Рисунок 9. Спектрофотометр универсальный РВ 2201.
УФ-спектр 0,001%-ного раствора препарата в 0,1М растворе гидроксида натрия имеет максимумы поглощения при 256, 283, 365 нм.
Отношение оптических плотностей составляет
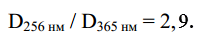
Дата: 2018-12-21, просмотров: 772.