В технике чистые металлы находят ограниченное применение. Основными конструкционными материалами, которые широко применяются в промышленности, являются металлические сплавы, которые часто обладают более высокими свойствами, чем чистые металлы.
Сплавом называется вещество, полученное сплавлением двух и более элементов. Металлические сплавы получают сплавлением металлов или преимущественно металлов с неметаллами. При этом металлический сплав сохраняет комплекс характерных металлических свойств.
В теории сплавов основными понятиями являются компонент, фаза и система. Системой называют металлы и металлические сплавы. Компонентами называют вещества, образующие систему. Ими могут быть элементы (металлы и неметаллы) и химические соединения элементов. Например: чистый металл является однокомпонентной системой, сплав двух металлов – двухкомпонентной системой.
Фазой называется однородная часть системы, отделенная от другой части системы (то есть другой фазы) поверхностью раздела. При переходе через эту поверхность раздела сильно (скачком) изменяются химический состав или структура. Например, при кристаллизации чистого металла в системе имеются только две фазы: жидкая – из расплавленного металла; твёрдая – из закристаллизовавшихся зерен этого же металла.
Фазы в металлических сплавах. В твердых в агрегатном состоянии сплавах фазами могут быть: зёрна чистого металла, зёрна твёрдого раствора, зёрна химического соединения.
Твердыми растворами называют фазы, в которых один из компонентов сплава сохраняет свою кристаллическую решетку, а атомы другого компонента располагаются в решетке первого компонента, изменяя ее размеры. Все твердые растворы однофазны и имеют металлический тип связи. Различаются твердые растворы внедрения и твердые растворы замещения (рис. 2.14).
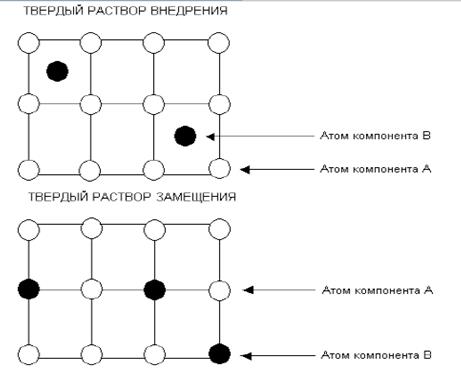
Рис.2.14. Схема формирования твердых растворов
Твердые растворы внедрения возникают при сплавлении металлов с неметаллами, имеющими малый атомный радиус – C, N, B, H. Такие твердые растворы всегда имеют ограниченную растворимость второго компонента в первом. Например, с углеродом железо образует твердые растворы: феррит с ОЦК-решеткой и аустенит с ГЦК-решеткой.
Твердые растворы замещения образуются, когда атомные радиусы металлов отличаются менее, чем на 15%. Такие твердые растворы могутбыть ограниченными и неограниченными. Чем больше различие в атомных радиусах компонентов, тем меньше растворимость. Неограниченные твердые растворы образуют компоненты, имеющие одинаковый тип кристаллической решетки, например: Cu –Au, Si – Ge, Cu – Ni, Co – Ni, Ti – V.
Химические соединения образуются при химическом взаимодействии компонентов. В химическом соединении элементы находятся в строгом соотношении друг с другом, то есть соблюдается соответствие стехиометрической пропорции, выраженной формулой вида AmBn. Химические соединения имеют свою кристаллическую решетку, отличную от решеток компонентов. Химические соединения имеют постоянную температуру плавления, как и чистые металлы, и играют роль самостоятельного компонента.
Свойства химического соединения сильно отличаются от свойств исходных элементов. Как правило, оно обладает высокой твёрдостью и хрупкостью.
Примерами химических соединений являются:
1. соединения металлов с металлами, так называемые интерметаллиды, например, CuAl2, Ni3Al, MoFe2, Mg2Sn.
2. соединения металлов с неметаллами, так называемые металлические соединения, например: карбиды Fe3C, VC, WC, TiC; нитриды TiN, Cr2N, Fe2N; бориды CrB, Ni3B, TiB2, а также гидриды элементов. Такие соединения очень тугоплавки и обладают высокой твердостью.
Некоторые химические соединения могут формировать твердые растворы. В этом случае сохраняется решетка химического соединения AmBnс замещенными в ее узлах атомами А или В, а так же замещенными или внедренными атомами третьего компонента С.
Рис 2.15 Схема структуры механической смеси
При образовании сплавов в процессе затвердевания или полиморфного превращения в структуре может формироваться особая структурная составляющая, называемая механическая смесь (рис. 2.15). Механическая смесь не является фазой, это смесь двух фаз, сформированная при определенной постоянной температуре и определенном постоянном химическом составе сплава. Фазами, входящими в механическую смесь, могут быть чистые компоненты, твердые растворы и химические соединения.
Если механическая смесь формируется при одновременной кристаллизации зерен двух фаз из жидкости – она называется эвтектика, а такое превращение называется эвтектическим. Если механическая смесь формируется из твердой фазы при ее полиморфном превращении из высокотемпературной модификации в низкотемпературную модификацию с выделением второй фазы – такая механическая смесь называется эвтектоидом, а такое превращение называется эвтектоидным.
Диаграммы состояния сплавов
Диаграмма состояния – это графическое изображение состояния сплава в зависимости от температуры и концентрации компонентов. Диаграммы состояния показывают равновесные (устойчивые) состояния, то есть такие, которые обладают минимальной свободой энергий. Диаграмма строится в координатах: температура – концентрация компонентов.
С построения и анализа диаграммы состояния начинается изучение любого сплава. Диаграмма состояния позволяет изучать фазы и структурные составляющие сплава. Пользуясь диаграммой состояния можно определять при любой температуре нагрева сплава число составляющих фаз, их состав и количественное соотношение, температуры начала и конца плавления. Используя диаграмму состояния сплава, можно установить возможность проведения термической обработки и её режимы, температуру литья и горячей пластической деформации, и т.д.
Диаграмма состояния строится различными экспериментальными методами: по кривым охлаждения сплава (термический анализ); измерением удлинения образцов при охлаждении; наблюдением микроструктуры; рентгеновским методом и др.
Имеется 4 основных типа диаграмм состояния, на которых основывается теория сплавов.
Диаграмма состояния сплавов с полной нерастворимостью компонентов в твердом состоянии (механических смесей компонентов). Компоненты таких сплавов в жидком состоянии неограниченно растворимы друг в друге, а в твердом не вступают в химическое взаимодействие друг с другом и не растворяются друг в друге. Такая форма сплава возникает при большом различии в свойствах образующих его металлов. К сплавам с полной нерастворимостью компонентов в твердом состоянии относятся сплавы Al – Si, Pb – Sb, Be – Al, Sn –Zn и др.
На диаграмме (рис. 2.16) линия АДВ является линией ликвидус, выше неё сплав находится в жидком состоянии; линия СДЕ является линией солидус, ниже неё сплав находится в твердом состоянии и представляет собой механическую смесь компонентов А и В. Выше линии солидус, но ниже линии ликвидус сплав состоит из жидкости (ж) и кристаллов А – левее точки Д; из жидкости (ж) и кристаллов В – правее точки Д.
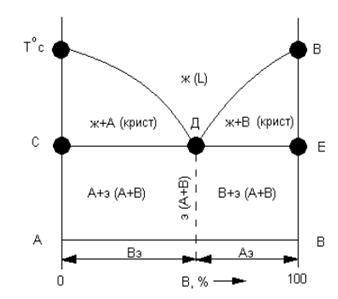
Рис. 2.16. Диаграмма состояния сплавов с полной нерастворимостью компонентов
При концентрации компонентов Аэ и Вэ – в точке Д – на диаграмме происходит кристаллизация из жидкости механической смеси кристаллов А и В – эвтектики. Эвтектика имеет наименьшую температуру плавления (кристаллизации) в данной системе и представляет собой сложную структуру чередующихся фаз А и В.
В соответствии с данной диаграммой в зависимости от концентрации компонентов могут формироваться доэвтектические, эвтектические и заэвтектические сплавы (рис. 2.17).
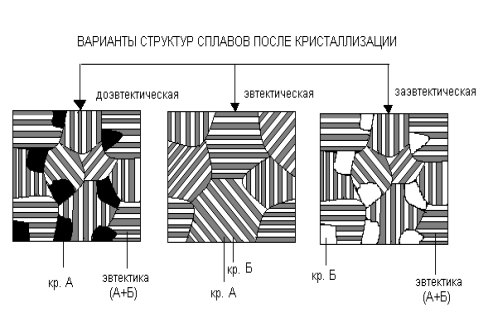
Рис. 2.17. Схематические изображения структуры сплавов с полной нерастворимостью компонентов
Доэвтектические сплавы – левее точки Д, ниже линии СД; заэвтектические – правее точки Д, ниже линии ДЕ; эвтектические – при эвтектической концентрации компонентов А и Б, ниже точки Д.
Диаграмма состояния сплавов с неограниченной растворимостью компонентов в твердом состоянии. Эта диаграмма соответствует сплавам, у которых компоненты и в жидком, и в твердом состоянии образуют растворы. Причем в твердом состоянии формируется твердый раствор замещения с полной растворимостью компонентов. К сплавам, имеющим такую диаграмму, относятся Cu-Ni, Fe-Cr, Co-Cr и др.
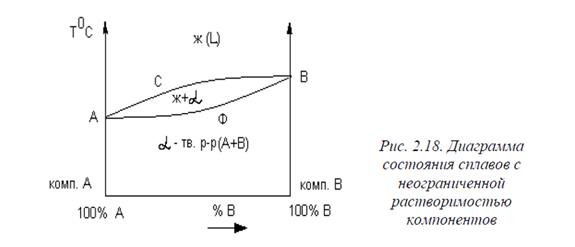
На диаграмме (рис. 2.18): линия АСВ – ликвидус; линия АФВ – солидус; точки А и В – температуры кристаллизации компонентов А и В, соответственно; α – неограниченный твердый раствор компонентов А и В друг в друге (рис. 2.19).
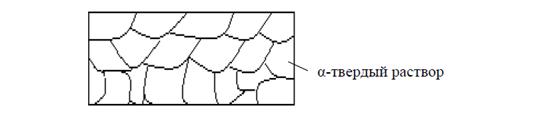
Рис. 2.19. Схематическое изображение структуры сплава с неограниченной растворимостью компонентов при любой концентрации компонентов
При любом составе сплава (кроме состава чистых компонентов), на линии ликвидуса начинается процесс формирования первых кристаллитов твердого состава. На линии солидуса кристаллизация заканчивается.
Кристаллиты твердого раствора, сформированные при разной температуре имеют разный химический состав. При медленной, так называемой равновесной кристаллизации, за счет диффузионных процессов состав кристаллов выравнивается. Однако реальные условия охлаждения сплавов в технологическом производстве изделий не обеспечивают протекание диффузионных процессов. Неравновесная кристаллизация создает внутри сплава так называемую дендритную (внутрикристаллитную) ликвацию. Чем больше температурный интервал кристаллизации сплава, то есть, чем больше расстояние между линиями ликвидус и солидус, тем сильнее проявляется дендритная ликвация, снижающая свойства.
Диаграмма состояния сплавов с ограниченной растворимостью компонентов в твердом состоянии. Эта диаграмма характеризует систему сплавов двух компонентов, обозначающих твёрдые растворы в ограниченных областях сплавов, за пределами которых образуется механическая смесь из кристаллов твёрдых растворов.
Диаграмма представляет собой комбинацию диаграмм: диаграмму с полной нерастворимостью компонентов в твёрдом состоянии (с эвтектикой – механической смесью) и диаграмму с неограниченной растворимостью компонентов в твёрдом состоянии (рис. 2.20).
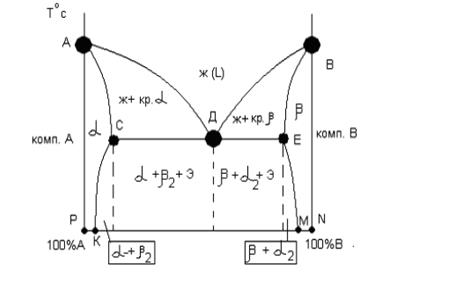
Рис. 2.20. Диаграмма состояния сплавов с
ограниченной растворимостью компонентов
Несмотря на сложный, на первый взгляд, вид, используя закономерности, характерные для двух предыдущих диаграмм, можно легко разобраться в этой диаграмме.
На этой диаграмме: линия АДB – ликвидус; линия ACДEB – солидус; область ACKРA – область существования твердого раствора α (твердого раствора компонента в кристаллической решетке компонента А); область BEMNB – область существования твердого раствора β (твердого раствора компонента А в кристаллической решетке компонента В); область КСДEM – область существования механической смеси двух твёрдых растворов, α и β. Линии КС и ЕМ являются линиями переменной растворимости. Ниже этих линий из твердых растворов α и β выделяются вторичные кристаллы β2 и α2.
Физические и химические свойства этих вторичных кристаллов такие же, что и первичных кристаллов той же фазы. Отличие заключается в размерах и форме. При высокой температуре превращения и медленном охлаждении сплава вторичные фазы выделяются по границам зерен твердых растворов α и β (рис. 2.21а). При низкой температуре превращения или быстром охлаждении вторичные фазы выделяются внутри зерен твердых растворов α и β в виде дисперсных (мелких) включений (рис. 2.21б). Эти вторичные зерна (твердого раствора β2) приводят к упрочнению сплава – так называемому дисперсионному твердению.
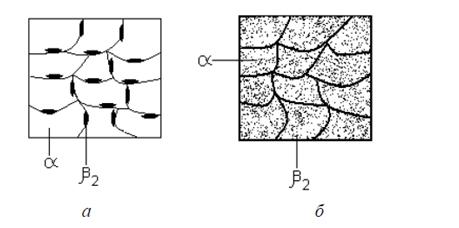
Рис. 2.21. Схематическое изображение выделения вторичных фаз: а – при равновесном охлаждении; б – при неравновесном охлаждении
Чем больше скорость охлаждения, тем меньше образуется вторичных кристаллов β2 и α2 фаз. При определенных, выше критических, скоростях охлаждения выделений вторичных фаз вообще не происходит, а происходит закалка сплава и образуется пересыщенный твердый раствор α или β.
При охлаждении сплава эвтектического состава (точка Д – на диаграмме) из жидкости одновременно выделяются кристаллы твердыхрастворов α и β, и образуется эвтектика (α + β), то есть механическая смесь растворов.
При охлаждении доэвтектических сплавов с концентрацией компонента Вв пределах между точками С и Д ниже линии солидус (СД) остатки жидкости (ранее не закристаллизовавшейся как твердый раствор α) кристаллизуются с образованием эвтектики (α + β). Сплав имеет структуру: эвтектика + отдельные зерна α - фазы (рис. 2.22а).
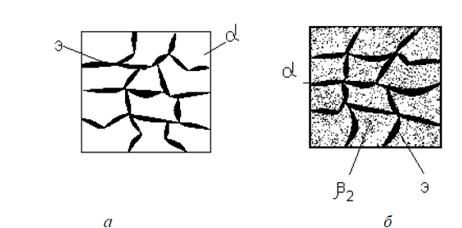
Рис. 2.22. Схематическое изображение строения доэвтектического сплава: а – до начала дисперсионного твердения; б – после дисперсионного твердения
Соотношение зерен эвтектики и твердого раствора α зависит от исходной концентрации сплава. Чем ближе состав сплава к эвтектическому, тем больше зерен эвтектики. Кроме того, при охлаждении сплава из твердого раствора α происходит выделение мелких вторичных зерен β2 (рис. 2.22б).
При охлаждении заэвтектических сплавов с концентрацией компонента в пределах между точками D и Е происходят аналогичные процессы с выделением α2 кристаллов.
Указанная диаграмма характерна для сплавов типа Pb – Sn, которые используют в качестве припоев в электронике (из-за низкой температуры плавления ~ 183 °С).
Диаграмма состояния сплавов с устойчивым химическим соединением. Устойчивым называется такое химическое соединение, которое при нагреве до температуры плавления не диссоциирует. Такие химические соединения, как говорилось выше, играют роль компонентов в сплавах и описываются диаграммами состояния с устойчивым химическим соединением (рис. 2.23).
Если химическое соединение AmBn обозначить как компонент С, то данная диаграмма разделится на 2 части, которые аналогичны уже рассмотренным нами ранее. Исключением является то, что одним из компонентов является химическим соединением. Таким образом, одна
часть диаграммы (левее точки С) – простая эвтектическая диаграмма с полной нерастворимостью компонентов в твердом состоянии, а другая (правее точки С) – эвтектическая диаграмма с ограниченной растворимостью компонента С в решетке компонента В, то есть AmBn.
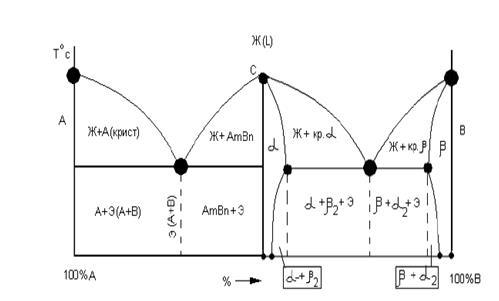
Рис. 2.23. Диаграмма состояния сплавов с
устойчивым химическим соединением
Поэтому, по аналогии с диаграммой с ограниченной растворимостью компонентов, α-фаза является твердым раствором компонента В вкристаллической решетке химического соединения AmBn, а β-фаза является твердым раствором химического соединения AmBn в кристаллической решетке компонента В.
Физические и механические свойства сплавов. Свойства сплавов в значительной степени определяются фазовым составом, о котором можно судить по диаграмме состояния. Для систем, образующих непрерывные твердые растворы, зависимость свойств от состава изображается кривыми, а для двухфазных смесей – прямыми линиями (рис. 2.24).
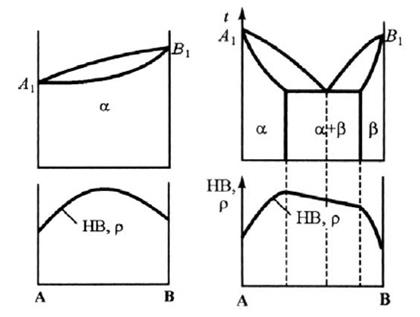
Рис. 2.24 Закономерности изменения свойств сплавов
Эти закономерности указывают на то, что у твердых растворов такие свойства, как твердость HB, удельное сопротивление ρ, всегда превосходят аналогичные свойства исходных компонентов.
Сохранение пластичности твердых сплавов используется на практике. Например, при растворении в меди 5% алюминия прочность увеличивается в два раза, а пластичность остается на уровне пластичности чистой меди. Твердые растворы обладают и другими уникальными физическими и химическими свойствами. Например, при растворении в железе 30% никеля теряются его ферромагнитные свойства.
Строение сплава определяет и технологические свойства. Сплавы в состоянии твердых растворов хорошо обрабатываются давлением (деформируемые сплавы), но трудно – резанием. Эвтектические сплавы обладают наилучшей жидкотекучестью и являются литейными сплавами.
Дата: 2018-11-18, просмотров: 1089.