Существуют различные типы электродов, мембранный потенциал которых селективно зависит от активности определенного иона (или ионов), например, в случае стеклянного электрода мембранный потенциал зависит от активности ионов водорода. Такие электроды очень важны для определения некоторых ионов, особенно при низких концентрациях. Многие ИСЭ, применяемые для определения различных ионов, устроены аналогично стеклянному. В отличие от других электродов, их как правило, не «отравляют» белки, поэтому такие электроды идеально подходят для проведения измерений в биологических средах. Особенно это справедливо для стеклянных ионоселективных электродов. Ни один из этих электродов не специфичен относительно данного иона, но каждый из них обладает определенной селективностью относительно данного иона или ионов, поэтому их следует называть ионоселективными электродами (ИСЭ).Существуют и другие типы ИСЭ в частности, электроды с кристаллической и жидкой мембраной. Общий принцип работы этих электродов тот же, что и что и у стеклянного. Однако они отличаются от стеклянного электрода с точки зрения природы электродной мембраны. Главное же отличие всех ИСЭ от металлических состоит в том, что на ИСЭ не протекает никакой ОВР-ции. Зависимость потенциала ИСЭ от состава раствора обусловлена равновесиями ионного обмена, комплексообразования, распределения и равновесиями осадок-раствор.
ИСЭ позволяют определять активность ионов. В сильно разбавленных растворах различия между активностями и концентрациями невелики. В других случаях ИСЭ следует градуировать по значениям концентраций определяемых ионов, поддерживая ионную силу раствора постоянной. В то же время в ряде случаев требуется определение именно активностей, и для решения этой задачи ИСЭ очень удобны. Другой важной сферой применения ИСЭ является определение отдельных химических форм вещества, например, отдельных степеней оксления или свободных ионов металла в присутствии их комплексов.
Механизм возникновения потенциала мембранных ионоселективных электродов менее изучен по сравнению со стеклянными электродами для измерения рН, и поэтому гораздо меньше известно о том, за счет чего возникает потенциал и чем он определяется. Тем не менее механизмы должны быть аналогичны В мембране электрода обычно содержится определяемый ион, селективно связанный реагентом либо в малорастворимое соединение, либо в комплекс. Или же электрод необходимо предварительно кондиционировать в растворе определяемого иона, и тогда этот ион также будет селективно связан реагентом мембраны. Последний случай аналогичен образованию слоя гидратированного геля – SiО-H+ при выдерживании стеклянного электрода в воде. При погружении ионоселективного электрода в анализируемый раствор на поверхности раздела мембрана – раствор возникает граничный потенциал. Возможный механизм его возникновения обусловлен стремлением ионов диффундировать из более концентрированного раствора в более разбавленный, как в случае возникновения жидкостной границы и, соответственно, потенциала жидкостного соединения. Диффузия катионов приведет к появлению положительного заряда и к увеличению потенциала электрода, в случае же диффузии анионов, наоборот, возникает отрицательный заряд и потенциал уменьшается.
Из этого следует, что при изготовлении ионселективного электрода очень важно подобрать материал с центрами связывания с высоким сродством к определяемому иону. Так, кальций-селективный электрод с жидкой мембраной обладает гораздо более высокой селективностью по отношению к иону кальция по сравнению с ионами магния и калия из-за высокого сродства к кальцию используемого органического катионообменника. На границе раздела мембрана – раствор устанавливается равновесие с участием ионов кальция, и величина потенциала электрода определяется отношением активностей ионов кальция в анализируемом растворе и фазе мембраны.
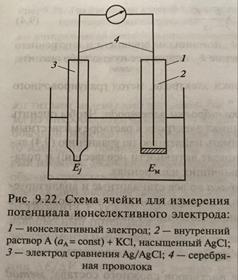
Измерение потенциала ионселективного электрода

Дата: 2019-11-01, просмотров: 561.