В клетке в определенных субклеточных частицах постоянно протекают сложные биохимические процессы в присутствии определенных ферментов.
Так гидролазы и лиазы сосредоточены преимущественно в лизосомах. Сложные окислительно-восстановительные ферменты располагаются в митохондриях, здесь же располагаются ферменты цикла ди – и трикарбоновых кислот. Ферменты активирования аминокислот располагаются в цитоплазме, они есть и в ядерном соке. В цитоплазме также находятся ферменты гликолиза. Ферменты, катализирующие синтез белка, в основном, находятся в рибосомах. В ядре локализованы ферменты катализирующие синтез нуклеиновых кислот.
Таким образом, системы ферментов, локализованных в различных субклеточных структурах, обеспечивают осуществление отдельных циклов реакций. Будучи связаны друг с другом эти циклы реакций обеспечивают жизнедеятельноть клеток, органов, тканей и организма в целом.
Задания для самостоятельного изучения
1. История открытия ферментов
2. Определение активности ферментов.
5. Механизм действия ферментов. Теория Фишера. Теория индуцированного соответствия Кошланда
6. Применение ферментов
.
Тема «ГОРМОНЫ»
Гормоны химические агенты с весьма высокой биологической активностью, присутствующие в организме в малых количествах. Их действие многосторонне. Они регулируют не только клеточный метаболизм, но и работу внутренних органов, кровяное давление. Их действие на тот или другой орган достигается благодаря присутствию в определенных клетках специфических рецепторов.
Принято выделять три класса гормонов: пептидные, стероидные и амины. Полипептидные гормоны, или просто пептидные гормоны это гормоны, состоящие из аминокислот, выделяемых эндокринной системой и распределяемых по нервным окончаниям через циркуляцию крови. Эндокринные органы, которые выделяют пептидные гормоны это гипоталамус, гипофиз, щитовидная железа, надпочечники, яичники, поджелудочная железа, эндокринная и жировая ткань. Органы, которые не считаются частью эндокринной системы, такие как сердце и желудочнокишечный тракт, также могут секретировать пептидные гормоны.
Пептидами являются, например, окситоцин, вазопрессин. Среди белковых гормонов имеются как простые белки (инсулин, глюкагон, соматотропин, пролактин и др.), так и сложные гликопротеины (фоллитропин, лютропин).
Гормоны полипептидной или белковой природы хранятся в секреторных пузырьках, пока не будут востребованы. Гормоны бывают разных размеров: от маленьких полипептидов, содержащих 3 аминокислоты (тироксин-рилизинг фактор), до 200 аминокислот (гормон роста и пролактин). Обычно полипептиды, содержащие от 100 и более аминокислот, называют белками, а включающие менее 100 аминокислот - полипептидами. Гормоны белковой и полипептидной природы синтезируются в шероховатом эндоплазматическом ретикулуме различных эндокринных клеток, как и прочие белки. Первоначально они синтезируются в виде крупных полипептидов, не обладающих биологической активностью (прегормоны), затем расщепляются в эндоплазматическом ретикулуме до более мелких прогормонов. Отсюда они транспортируются в аппарат Гольджи, где упаковываются в секреторные пузырьки. В ходе этого процесса ферменты пузырьков расщепляют прогормоны, формируя биологически активные гормоны и неактивные фрагменты. Пузырьки хранятся в цитоплазме, многие из них связаны с мембраной клеток до тех пор, пока не возникнет потребность в гормоне. Секреция гормонов (как и неактивных фрагментов) осуществляется в том случае, когда секреторные пузырьки растворяются в мембране и содержащиеся в них гормоны попадают в интерстициальное пространство или напрямую в кровоток путем экзоцитоза. Во многих случаях стимулом для экзоцитоза является увеличение концентрации ионов кальция в цитозоле клетки, вызываемое деполяризацией плазматической мембраны. В других случаях стимуляция поверхностных рецепторов эндокринной клетки приводит к увеличению циклического аденозинмонофосфата и последующей активации протеинкиназ, стимулирующих секрецию гормона. Пептидные гормоны водорастворимы, что позволяет им легко проникать в кровеносную систему, доставляющую их к тканям-мишеням.
Амины объединяют гормоны, близкие по структуре аминокислотам - тирозину и триптофану (тиреоидные гормоны, адреналин, норадреналин). Две группы гормонов являются производными тирозина: гормоны щитовидной железы и мозгового вещества надпочечников, формирующиеся под действием ферментов в цитоплазме железистых клеток. Тиреоидные гормоны синтезируются и хранятся в щитовидной железе, включаясь в макромолекулы белка тиреоглобулина, который размещается в больших фолликулах щитовидной железы. Секреция гормона осуществляется при условии отщепления аминов от тиреоглобулина, свободные гормоны выделяются в кровоток.
Стероидные гормоны – это вещества, которые обладают высокой биологической активностью. Они чаще бывают животного происхождения, реже растительного. Предшественниками стероидов являются изопреноидные вещества. Наличие особенной системы строения значительно отличается данный класс веществ от других. В его основе – система гонана, которая представляет собой насыщенный углеводород. Ядро стероида может быть частично ненасыщенно или насыщенно, включать в свой состав алкильные и функциональные группы. Благодаря особым качествам, стероидные гормоны могут легко проникать в кровь через плазматические мембраны в клетки мишени. Для попадания в такие клетки гормоны связываются с транспортными белками, которые и доставляют их в необходимое место.
Синтез стероидных гормонов происходит в коре надпочечников из холестерина, в желтом теле и фолликулах яичников, в плаценте. К стероидным гормонам относятся: половые гормоны: женские (эстрогены), мужские (андрогенные) гормоны, среди которых метилтестостерон, тестостерон, андростерон; а также кортикостероиды, к которым относятся альдостерон, прегнан, кортикостерон, кортизон и т.д.
Стероидные гормоны занимают важное место в нормализации обмена веществ в организме человека. Некоторые синтетические гормоны даже способны превосходить натуральные аналоги, к ним можно отнести преднизолон.
Все гормоны функционируют в системе эндокринных связей, координирующим центром которой является гипоталамус. Регуляция гормональных процессов, связанных с эндокринной системой, осуществляется по принципу обратной связи. Для гормонов характерна строгая специфичность их действия.
Задания для самостоятельного изучения
1. Дать определение гормонам.
2. Классификация гормонов по химическому строению.
3. Механизм действия гормонов.
4. Участие циклической АМФ в механизме действия гормонов на обмен веществ и функции клетки.
5. Гормоны щитовидной железы.
6. Гормоны мозгового вещества.
7. Гормоны поджелудочной железы.
8. Половые гормоны.
9. Гормоны надпочечников.
Тема: «ОБМЕН ВЕЩЕСТВ, ЕГО БИОЛОГИЧЕСКАЯ РОЛЬ.
БИОЭНЕРГЕТИКА КЛЕТКИ»
Обмен веществ или метаболизм – это сложная цепь биохимических реакций, заключающаяся в усвоении веществ из окружающей среды, сложных превращений в организме и выделении в окружающую среду продуктов расщепления этих веществ. Все реакции обмена веществ – это ферментативные реакции. Обмен веществ является источником энергии всех жизненных процессов. Обмен веществ обеспечивает процессы роста и развития, самообновление всех клеточных структур, энергообеспечение функций, постоянство внутренней среды. Поэтому при прекращении обмена веществ нарушается или прекращается жизнедеятельность организма.
Основу обмена веществ в клетке составляют:
· Химические превращения веществ, поступающих в организм;
· Изменение их энергетических свойств;
· Информационное взаимодействие отдельных элементов биологической системы.
Химические превращения веществ в организме объединяют два неразрывно связанных между собой и противоположных по направленности процесса – анаболизм и катаболизм
Анаболизм (ассимиляция, биосинтез) – это фаза, в которой из простых веществ синтезируются новые, необходимые клетке биомолекулы. Процесс требует затрат энергии.
Катаболизм (диссимиляция) – это фаза, в которой происходит расщепление сложных органических молекул до простых. Углеводы, белки, жиры, поступающие в клетку, распадаются до углекислого газа, аммиака, воды, молочной кислоты. При распаде этих веществ выделяется энергия, которую называют свободной.
Свободная энергия является частью внутренней энергии (энтальпии), которая может быть превращена в полезную работу. Высокий уровень свободной энергии присущ потенциально неустойчивым системам, которые могут переходить на более низкий уровень этой энергии; изменение свободной энергии (ее убыль) будет отрицательным, а реакция называется экзергонической. Напротив, биохимические реакции, требующие затраты энергии, характеризуются переходом веществ из устойчивого состояния с низкой свободной энергией к менее устойчивому состоянию с большой свободной энергией. Изменение свободной энергии (ее приход) будет положительным. Такие реакции называются эндергоническими.
Для большинства биохимических реакций энтальпия близка к свободной энергии. Этим определяется калорийность пищи как приближенной меры работы, совершаемой в результате усвоения пищи организмом.
Важную роль в передаче химической энергии внутри клетки играют вещества, известные под названием высокоэнергетических (макроэргических) соединений, при превращении их освобождается большое количество энергии, расходуемое на различные процессы жизнедеятельности. К числу таких соединений относится обширный класс фосфоорганических соединений. Центральное место среди них занимает АТФ (аденозинтрифосфат). АТФ занимает промежуточное положение между высокоэнергетическими и низкоэнергетическими веществами и выполняет роль посредника в передаче энергии от высокоэнергетического к низкоэнергетическому соединению, что имеет большое значение в синтезе белков, нуклеиновых кислот, углеводов.
АТФ был впервые получен К.Лиманом в 1929 году из мышц лягушки. Это сильная четырехосновная кислота, хорошо растворимая в воде, содержит два высокоэнергетических остатка фосфорной кислоты.
При гидролизе АТФ образуются АДФ и АМФ с выделением большого количества химической энергии:
АТФ ↔АДФ↔АМФ
АТФ вместе с АДФ и АМФ образуют адениловую систему. Энергия, накопленная в виде АТФ, используется в огромном числе различных эндергонических процессов клетки, к числу которых относятся биосинтез белков, нуклеиновых кислот, углеводов, жиров, транспорт веществ через мембраны, различные формы движения.
АТФ образуется в ходе эндергонической реакции, называемой реакцией фосфорилирования:
АДФ + H 3 PO 4 →АТФ
В этой реакции используется либо энергия, извлекаемая при окислении фрагментов питательных веществ, связанном с субстратным фосфорилированием, либо энергия, выделяющаяся при переносе электронов по дыхательной цепи, сопряженном с окислительным фосфорилированием, либо энергия, получаемая за счет фотосинтетического фосфорилирования.
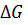 гидролиза АТФ достаточно велика и составляет – 30,5 кДж·моль-1; близкая величина найдена для гидролиза АТФ с образованием АМФ и пирофосфата. В то же время величина
гидролиза АТФ достаточно велика и составляет – 30,5 кДж·моль-1; близкая величина найдена для гидролиза АТФ с образованием АМФ и пирофосфата. В то же время величина 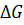 гидролиза АМФ на аденозин и фосфорную кислоту составляет – 12,6 кДж·моль-1, т.е. почти в 2,5 раза ниже энергии макроэргической связи. В живой клетке с учетом реальных концентраций реагентов, изменение
гидролиза АМФ на аденозин и фосфорную кислоту составляет – 12,6 кДж·моль-1, т.е. почти в 2,5 раза ниже энергии макроэргической связи. В живой клетке с учетом реальных концентраций реагентов, изменение 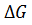 может составлять – 50 кДж·моль-1 и выше.
может составлять – 50 кДж·моль-1 и выше.
К группе высокоэнергетических соединений относятся также тиоэфиры – промежуточные продукты обмена жирных кислот. В природе основным тиоэфирным соединением является кофермент А (соединение аденозин – 3',5' – дифосфорной кислоты с фосфопантотениламиноэтантиолом) – Н S - СоА.
Кофермент А взаимодействует с АТФ с образованием тиоэфира (Р 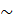 Р
Р 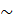 S – СоА)
S – СоА)
Н S – СоА + АТФ ↔ Р 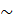 Р
Р 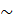 S – СоА + АМФ
S – СоА + АМФ
Данное высокоэнергетическое соединение легко вступает в реакцию ацилирования с жирной кислотой:
R-CH2-COOH + Р 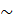 Р
Р 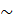 S – СоА ↔ R-CH2-CO- S – СоА + РР
S – СоА ↔ R-CH2-CO- S – СоА + РР
В результате этой реакции существенно возрастает реакционная способность атома углерода тиоэфирной связи. При участии кофермента А протекает ряд промежуточных реакций клеточного дыхания, биосинтеза и окисления высших жирных кислот.
К числу высокоэнергетических соединений также относятся 1,3- дифосфоглицериновая кислота (дФГК) и фосфоенолпируват (ФЕП). Эти вещества являются промежуточными продуктами гликолиза и с их превращениями сопряжен процесс субстратного фосфорилирования 1,3 – дифосфоглицериновая кислота передает одну фосфатную группу на АДФ, в результате чего образуется АТФ и 3 – фосфоглицериновая кислота:
1,3 – дФГК + АДФ→ 3 – ФГК + АТФ
Фосфоенолпируват также легко передает свою фосфатную группу молекуле АДФ:
ФЕП +АДФ → ПВК + АТФ
Фосфоенолпируват и 1,3 – дифосфоглицериновая кислота не только играют роль доноров химической энергии, но и являются важными интермедиатами гликолиза.
Два других высокоэнергетических фосфорилированных соединения – креатинфосфат и аргининфосфат – важны как «аккумуляторы» химической энергии.
При обмене веществ в организме человека протекают окислительно – восстановительные реакции. Процесс окисления любого вещества связан с отдачей электронов окисляемым веществом, а процесс восстановления – присоединения электронов к какому–то веществу (акцептору электронов). В живых организмах выделение энергии происходит постепенно, порциями. Выделяемая энергия может рассеиваться в виде теплоты или улавливаться в процессе синтеза высокоэнергетических соединений. Поэтому выделяют свободное и сопряженное окисление.
Свободное окисление не связано с переходом энергии биологического окисления в энергию макроэргических соединений. Выделяющаяся энергия рассеивается в виде теплоты. Этот вид энергообразования в клетках важен для теплорегуляции и детоксикации вредных продуктов обмена веществ.
Сопряженное окисление связано с переходом свободной энергии, выделяющейся в процессе биологического окисления, в доступную для использования форму энергии – макроэргические связи АТФ или другие виды энергии, например, ионный градиент. Различают такие виды сопряженного окисления, как окислительное фосфорилирование на уровне субстрата и окислительное фосфорилирование на уровне дыхательной цепи ферментов. В первом случае синтез АТФ идет за счет переноса высокоэнергетического фосфата от окисляемого субстрата к АДФ. Такое фосфорилирование, в основном, происходит в мышцах в процессе гликолиза.
Во втором случае синтез идет за счет энергии, которая выделяется при переносе электронов по дыхательной цепи ферментов, локализованных в митохондриях, от окисляемых веществ к атомарному кислороду в процессе дыхания. Этот процесс не связан непосредственно с синтезом АТФ и вначале используется для образования протонного потенциала на мембране, который в дальнейшем приводит к синтезу АТФ. Энергия протонного потенциала может затрачиваться и на другие виды работы, поэтому образование АТФ не является единственным и обязательным следствием окисления.
Задания для самостоятельного изучения
1. Клеточный метаболизм, его биологическая роль.
2. Пути передачи энергии от катаболических процессов к анаболическим
4. Регуляция метаболических путей.
5. Строение и свойства АТФ, ее особенности.
6. Роль АТФ в передаче энергии. АТФ – цикл в клетке.
7. Высоко– и низкоэнергетические соединения, их биологическая роль.
Тема: «ОБМЕН НУКЛЕИНОВЫХ КИСЛОТ»
Дата: 2019-07-30, просмотров: 390.