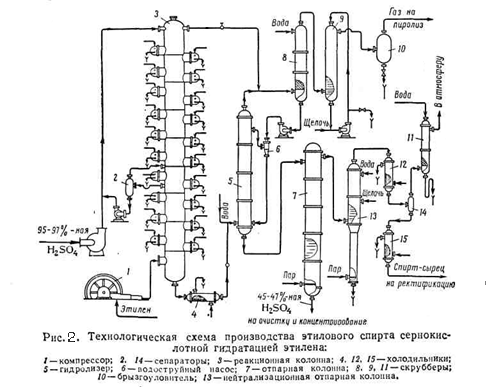
Схема установки получения этилового спирта сернокислотной гидратацией этилена приведена на (рис.2)
|
|
Исходным сырьём служит газообразная этан этиленовая фракция, содержащая 30 – 50 % этилена, и 95 – 97% серная кислота. Этиленсодержащий газ подают в реактор – абсорбционную колонну 3, орошаемую серной кислотой и имеющую 25 тарелок. Газ в виде мелких пузырьков барботирует на тарелках через слой жидкости, где происходит поглощение этилена. Для отвода тепла реакции на каждой тарелке имеется змеевик водяного охлаждения. В колонне поддерживается температура 65 – 75 °C и давление 25 кгс/см2 . Газ, покидающий колонну содержит 2 – 6 % этилена. Он проходит скрубберы 8 и 9 орошаемые соответственно водой и 5 – 10% раствором едкого натра, для отмывки серной кислоты и нейтрализации. Отмытый газ (этан) направляют на пиролиз.
Из нижней части колонны 3 непрерывно вытекает реакционная масса, имеющая примерно следующий состав (%): этилсульфат – 60-80, серная кислота – 10-30, диэтилсульфат – 2-8, полимеры – 1-7, вода и прочие примеси -2. Эта смесь охлаждается в холодильнике 4 и направляется в гидролизёр 5, куда поступает и вода. Гидролиз проводится при 92 - 96°C и давлении 4,5 - 5 кгс/см2. из нижней части гидролизёра 5 реакционная масса поступает в верхнюю часть отпарной колонны 7, в низ которой подаётся острый пар. В нижней части колонны поддерживается температура 125 °C, в верхней 110°C и давление 0,5 кгс/см2. Из нижней части колонны 7 отводится 45 – 47 % серная кислота, поступающая на упаривание до 90 % концентрации. Пары спирта и других продуктов направляются в колонну 13, где отгоняется спирт – сырец. В эту колонну для нейтрализации серной кислоты вводят 5% раствор едкого натра.
Спирт – сырец содержит 25 – 35% этанола, 3 – 5% диэтилового эфира, 60 – 65% воды и 0,05% полимеров. Его направляют на ректификацию для получения 95 - 96% концентрации спирта. Выход этанола ректификата составляет 85% от стехиометрического. Кроме того, получается диэтиловый эфир с выходом до 7%.
Сернокислотная гидратация олефинов – самый распространённый метод получения спиртов. Однако недостатком метода является участие больших количеств серной кислоты и её разбавление, а отсюда необходимость её упаривания, перекачки больших объёмов и так далее. Всё это связано с коррозией аппаратуры и большими капитальными затратами на сооружение заводов. [2,5]
ПРОИЗВОДСТВО СПИРТОВ ПРЯМОЙ ГИДРАТАЦИЕЙ ОЛЕФИНОВ
Теоретические сведения
В промышленности методом прямой гидратации получают этиловый и изопропиловый спирты. Прямая гидратация олефинов заключается в непосредственном присоединении воды к олефином:
С2Н4 + H2O ↔ C2H5OH
Синтез этилового спирта удалось осуществить лишь после того, как были изысканы достаточно активные катализаторы процесса. При газофазной гидратации в качестве катализаторов применяются фосфорная кислота или окись вольфрама на носителях. На последнем катализаторе процесс проводят и в жидкой фазе.
Газофазная реакция прямой гидратации олефинов обратима и идёт с выделением тепла. Тепловой эффект зависит от строения исходных олефинов и их молекулярного веса:
С2Н4 + H2O ↔ C2H5OH + 10,9 ккал/моль (45,6 кДж/моль);
Поскольку реакция идёт с выделением тепла и уменьшением объёма, ей благоприятствуют пониженные температуры и повышенные давления. Константа равновесия реакции равна: lgKр = (2100/T) – 6,195, где Т – температура, К. Практический выбор условий связан со скоростью реакции и, следовательно, с активностью катализатора. Реакцию удаётся реализовать при температурах от 200 до 300 °C, но эти условия термодинамически неблагоприятны для этилена. Поэтому на промышленных катализаторах степень конверсии олефинов в спирт низка.
Также, как и в случае сернокислотной гидратации, присоединение воды происходит по правилу Марковникова.
Механизм прямой гидратации олефинов в присутствии фосфорной кислоты был предложен Н.М.Чирковым. Первая стадия заключается в физическом растворении этилена в плёнке фосфорной кислоты на поверхности носителя. Затем происходит отщепление протона от молекулы кислоты:
H3PO4 ↔ Н+ + H2PO4-
Известно, что олефины, как и ароматические углеводороды являются слабыми основаниями, поэтому прямую гидратацию олефинов можно рассматривать как реакцию электрофильного замещения. Этилен образует с протоном π-комплекс, который переходит в более стабильный ион карбония. Далее ион карбония взаимодействует с водой за счёт неподелённой электронной пары атома кислорода; в данном случае проявляется нуклеофильность воды, обладающей амфотерными свойствами. В результате образуется ион алкоксония, который отщепляет протон с образованием спирта:
С2Н4 + Н+↔π-комплекс↔CH2+CH3 + H2O↔CH2(H2O) +CH3 + Н+↔C2H5OH
В производстве этилового спирта прямой гидратацией этилена наиболее широкое применение получил фосфорнокислотный катализатор на твёрдом носителе.
Катализаторы прямой гидратации не должны разрушаться под действием влаги, поэтому такой катализатор, как фосфорная кислота на кизельгуре, не применим – он не имеет скелета и легко разрушается. В качестве носителя для фосфорной кислоты применяют силикагель и алюмосиликат. Обычный шариковый алюмосиликат обрабатывают 20% -ной серной кислотой; при этом содержание оксида алюминия в нём снижается, а содержание оксида кремния повышается (излишнее количество оксида алюминия приводит к образованию малоактивных фосфатов алюминия). Затем носитель пропитывают 65%-ной фосфорной кислотой и сушат при 100°C. Готовый катализатор содержит 35-40% фосфорной кислоты. Если (как это и принято чаще всего) в качестве носителя используют шариковый силикагель, его обрабатывают водяным паром с целью пассивации.
В условиях реакции фосфорная кислота, осаждённая на носителе, растворена в плёнке воды, адсорбированной на поверхности пор, и реакция фактически протекает в жидкой плёнке фосфорной кислоты. Кислотный катализ, таким образом, сводится к гомогенному катализу в жидкой плёнке катализатора.
Как и в случае сернокислотной гидратации, при прямой гидратации этилена протекает ряд других реакций приводящих к побочным продуктам. За счёт взаимодействия иона карбония со спиртом образуется диэтиловый эфир:
C2H5OH + CH2 +CH3  (С2Н5)2О + H2
(С2Н5)2О + H2
За счёт дегидрирования спирта образуется ацетальдегид
C2H5OH  C2H4O+ H2
C2H4O+ H2
Причём реакция сопровождается образованием этана. Путём полимеризации этилена образуются полимеры:
CH2+CH3 + CH2CH2  CH2+CH3CH2CH2 и т.д.
CH2+CH3CH2CH2 и т.д.
По топытным данным конвертированный этилен расходуется на образование различных продуктов таким образом (в масс.%): на этанол – 94,5; на диэтиловый эфир – 2,5; на ацетальдегид – 2,0; на полимеры и сложные эфиры – 1,0.
Реакция прямой гидратации этилена описывается следующим интегральным уравнением при Т, рH2O, рC2H4 – const:
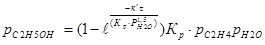
Влияние температуры
Реакцию прямой гидратации олефинов желательно проводить при невысоких температурах. Однако практически выбор температуры лимитируется скоростью реакции и активностью применяемых катализаторов.
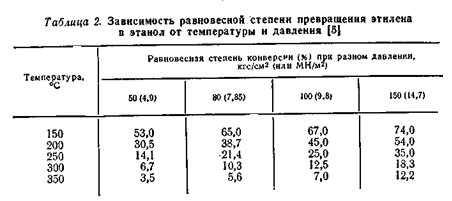
В таблице 2 приведена зависимость равновесной степени превращения этилена в этанол от температуры при разных давлениях.
Из приведённых данных видно, что с повышением температуры равновесная стиепень превращения этилена в спирт снижается. Однако, при низких температурах активность фосфорнокислотного катализатора мала. Так, степень конверсии этилена при 280 – 290 °C достигает лишь 4 – 5%, а при более низких температурах она ещё меньше (рис.3.)
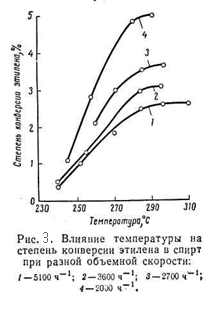
На практике процесс прямой гидратации в паровой фазе в присутствии фосфорнокислотного катализатора ведут в интервале 260 - 300°C.
Влияние мольного соотношения воды и этилена
Согласно термодинамическим данным, с увеличением отношения вода/этилен с 0,5/1 до 1/1 значительно повышается степень конверсии олефина

Однако экспериментальные данные отличаются от термодинамических (рис) с увеличением отношения вода/этилен до 0,7/0,75 степень конверсии этилена действительно возрастает, но при дальнейшем его увеличении она снижается.
Установлено также, что от соотношения вода/этилен зависит и активность катализатора гидратации. Оптимальная концентрация фосфорной кислоты в жидкостной плёнке на пористом носителе составляет 83 – 85%. Эта величина зависит от парциального давления водяного пара, которое определяется общим давлением в системе и мольным отношением вода/этилен. Оптимальная концентрация фосфорной кислоты наблюдается при отношении вода/этилен = 0,75/1. с дальнейшим ростом этого отношения возрастает количество воды в плёнке, уменьшается концентрация кислоты и снижается степень конверсии этилена. Поэтому в промышленных условиях принято мольное отношение вода/этилен = (0,6 – 0,7)/1.
Влияние давления
Повышение давления благоприятствует реакции гидратации, причём оптимальное давление составляет 70 – 80 кгс/см2. это давление связано с процессом абсорбции этилена фосфорной кислотой. Оптимальное парциальное давление водяных паров равно 27 – 30 кгс/см2; оно и определяет мольное соотношение водяных паров и этилена. Оптимальное парциальное давление этилена составляет 36 – 38 кгс/см2.

Общее давление складывается из парциальных давлениях воды, этилена и примесей. Прои концентрации этилена в циркулирующем газе 80 – 85% общее давление системы получается равным 70 - 80 кгс/см2.
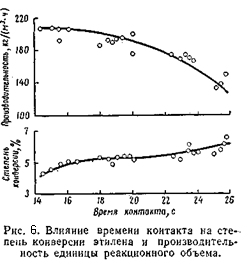
Влияние времени контакта
С увеличением времени контакта степень конверсии этилена возрастает, а производительность единицы объёма снижается. Оптимальное время контакта 17 – 19 с, что соответствует объёмной скорости 1 800 – 2 000 (1/час). В оптимальных условиях степень конверсии этилена не превышает 4,2 – 4,5 %, а селективность его использования достигает 95%. [2,3]
Дата: 2019-07-24, просмотров: 451.