ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ
Пензенский государственный педагогический университет им. В.Г. Белинского
Факультет естественно-географический
Кафедра химии и теории и методики обучения химии
ДИПЛОМНАЯ РАБОТА
Использование цифровой лаборатории «Архимед» в школьном химическом эксперименте
Студент Макарова О.Е.
Руководитель Фирстова Н.В.
К защите допустить.
Протокол № от «___» ____2009 г.
Зав. Кафедрой Керимов Э.Ю.
Пенза, 2009
Содержание
Введение
Глава 1. Обзор литературы
1.1 Информатизация системы образования
1.2 Информатизация химического образования
1.3 Цифровая лаборатория «Архимед» – новое поколение школьных естественно-научных лабораторий
Цифровая лаборатория «Архимед» в преподавании химии
1.3.2 Анализ методических разработок и материалов по применению цифровой лаборатории «Архимед» на уроках химии
Глава 2. Методы исследования
2.1 Настройка работы и регистрация данных с помощью цифровой лаборатории «Архимед»
2.2 Анкетирование
Глава 3. Результаты и их обсуждение
3.1 Методические разработки опытов, с использованием цифровой лаборатории «Архимед», для урочной деятельности
3.2 Методические разработки опытов, с использованием цифровой лаборатории «Архимед», для элективных курсов и исследовательской работы учащихся
3.2.1 Методические разработки опытов, с использованием цифровой лаборатории «Архимед», для элективного курса «Химия и медицина»
3.2.2 Методические разработки опытов, с использованием цифровой лаборатории «Архимед», для элективного курса «Химия и экология»
3.3 Апробация методических разработок опытов с использованием цифровой лаборатории «Архимед» в урочной деятельности и на элективных курсах
Выводы
Список литературы
Приложение 1. Примерное календарно-тематическое планирование учебного материала по химии в 9 классах
Приложение 2. Примерное календарно-тематическое планирование учебного материала по химии в 8 классах
Приложение 3. Примерное календарно-тематическое планирование учебного материала по химии в 11 классах
Приложение 4. Тематическое содержание программы элективного курса «Химия и медицина»
Приложение 5. Тематическое содержание программы элективного курса «Химия и экология»
Приложение 6. Конспект занятия «Анализ качества пищевых продуктов»
Приложение 7. Анкета для учащихся перед выполнением эксперимента
Приложение 8. Анкета для учащихся после выполнения работы
ВВЕДЕНИЕ
Сегодня в условиях развития информационного общества одним из ключевых элементов, позволяющих максимально индивидуализировать учебный процесс, является информатизация обучения, основанная на применении информационно-коммуникационных технологий (ИКТ), на организации учебного процесса в специализированной открытой информационно-образовательной среде, в которой посредством ИКТ происходит обмен учебной информацией.
В мировой практике имеется много примеров успешного использования информационно-коммуникационных технологий в образовании. Новые условия развития образования, реализация федеральных и региональных целевых программ и проектов вызывают необходимость разработки новой среднесрочной программы информатизации системы образования.
Для реализации принятой Правительством РФ «Концепции модернизации российского образования» разрабатывается проект «Информатизация системы образования» (2004-2009 гг.) Федерального агентства по образованию РФ. Основная идея проекта «Информатизация системы образования» – это создание условий для системного внедрения и активного использования ИКТ в работе школы. Участвующие в проекте школы перейдут на новую ступень использования ИКТ в учебном процессе, начнут активно использовать современные цифровые образовательные ресурсы.
Анализ состояния дел в области информатизации, проведенный в ходе подготовки проекта, выявил острую нехватку специалистов, способных создавать практически эффективные цифровые образовательные ресурсы и грамотно использовать их на практике. В связи с вышеизложенным, актуальным представляется создание новых моделей подготовки будущих учителей, работающих с использованием создаваемых в проекте цифровых учебно-методических материалов.
Одним из примеров реализации идей проекта «Информатизация системы образования» в естественно-научном образовании является создание и установка в школах цифровых лабораторий, которые позволят перевести школьный практикум естествознания на качественно новый уровень; подготовить учащихся к самостоятельной творческой работе в любой области знаний; осуществить приоритет деятельностного подхода к процессу обучения; развить у учащихся широкий комплекс общих учебных и предметных умений; овладеть способами деятельности, формирующими познавательную, информационную, коммуникативную компетенции.
Цифровая лаборатория «Архимед» – это новое поколение естественно-научных лабораторий – оборудование для проведения широкого спектра исследований, демонстраций, лабораторных работ. Входящие в состав цифровой лаборатории «Архимед» цифровые образовательные ресурсы и цифровые лабораторные комплексы, направлены на выполнение следующих задач: комплексное использование материально-технических средств обучения на основе современных технико-педагогических принципов; переход от репродуктивных форм учебной деятельности к самостоятельным, поисково-исследовательским видам работы; перенос акцента на практико-ориентированный компонент учебной деятельности; формирование коммуникативной культуры учащихся; развитие умений работы с различными типами информации и ее источников.
Сегодня цифровые лаборатории «Архимед» используются в практике обучения по физике, химии, биологии, экологии и пр. во многих школах России; учителями создан и опробован целый ряд методик применения КПК на уроках. Институт новых технологий проводит конкурсы подобных методических разработок [2]; материалы по применению цифровых лабораторий «Архимед» стали все чаще появляться в трудах образовательных конференций и конгрессов и в публикациях прессы.
Объект исследования: учебно–воспитательный процесс в средних общеобразовательных учреждениях.
Предмет исследования: методическая деятельность учителя химии по использованию современных средств обучения в химическом эксперименте.
Целью нашей работы было исследование возможностей цифровой лаборатории «Архимед» для применения в урочной и внеурочной деятельности по химии.
Цель, предмет и объект исследования предполагают решение следующих задач:
1. Обобщить и систематизировать материалы по основным направлениям развития информационных и коммуникационных технологий в современном естественно-научном образовании, в частности в обучении химии.
2. Освоить технику работы с использованием цифровой лаборатории «Архимед».
3. Провести методический анализ разработок опытов по химии создателей цифровой лаборатории «Архимед».
4. Разработать методики и теоретическое обоснование результатов экспериментов с использованием цифровой лаборатории «Архимед» в урочной и внеурочной деятельности (элективные курсы «Химия и медицина», «Химия и экология») по химии.
5. Апробировать самостоятельно разработанные, модифицированные и предложенные разработчиками цифровой лаборатории «Архимед» опыты в урочной и внеурочной деятельности по химии.
6. Провести анкетирование в группе учащихся, использовавших в своей работе цифровую лабораторию «Архимед», с целью исследования эффективности её применения для процесса обучения.
7. Составить пособие к практикуму для учащихся – слушателей элективных курсов «Химия и экология» и «Химия и медицина» в форме рабочей тетради.
Глава 1. Обзор литературы
1.1 Информатизация системы образования
Человечество стремительно вступает в принципиально новую для него информационную эпоху. Существенным образом меняются все слагаемые образа жизни людей.
Мир меняется стремительно, меняются и требования к системе образования. Она уже сегодня должна ориентироваться на те потребности общества, которые появятся через 10-15 лет. Необходима целостная стратегия совершенствования системы общего образования в условиях глобальных процессов информатизации всех сфер жизни общества.
Цель и принципы информатизации системы образования [18]
Стратегическая цель – подготовка детей и молодежи к полноценной жизни в информационном обществе за счет повышения качества образования посредством формирования единой информационно-образовательной среды и интенсивного внедрения информационно-коммуникационных технологий в образовательный процесс.
Концептуальными принципами информатизации образования являются:
· принцип приоритетности – информатизация образования должна стать приоритетной областью государственной политики в области информатизации, что будет выражаться в усиленном ресурсном обеспечении;
· принцип системности – процесс информатизации должен обеспечить изменение системных свойств системы;
· принцип направляемого развития – так как реальные процессы внедрения информационно-коммуникационных технологий в систему образования будут развиваться в силу внутренних и внешних факторов, то цель управления информатизацией образования – направлять, корректировать объективно протекающие процессы саморазвития;
· принцип учета ограниченности ресурсов – так как ресурсы образовательной системы ограничены, то управление информатизацией образования предполагает оптимальный выбор и комбинирование ресурсов;
· принцип культуросообразности – информатизация образования должна строиться на учете национально-культурных особенностей, уклада жизни, ценностных ориентаций и норм поведения населения.
Основная идея проекта «Информатизация системы образования» – это создание условий для системного внедрения и активного использования ИКТ в работе школы. Участвующие в проекте школы перейдут на новую ступень использования ИКТ в учебном процессе, начнут активно использовать современные цифровые образовательные ресурсы. В них создадутся условия для творчества учителей, активной самостоятельной работы учащихся, гибкую организацию процессов учения и обучения. Сложившаяся в нашей стране модель массовой школы ориентирована, прежде всего, на унификацию учебного процесса. Информационные технологии ХХ века, на которых она построена, требовали использовать закрытую учебную архитектуру [32].
Постановка новых образовательных задач, связанных с преодолением кризиса Тоффлера [31] требуют перехода к открытой учебной архитектуре [33]. Это невозможно без смены технологического базиса общего образования. Проект информатизации системы образования будет создавать условия для соответствующей трансформации [34]. В рамках проекта:
· разрабатываются качественно новые учебные и методические материалы (компонент 1);
· трансформируется существующая система переподготовки и текущей методической поддержки педагогов (компонент 2);
· создаются межшкольные методические центры (компонент 3), обеспечивающие постепенную трансформацию муниципальной методической службы и внедрение новых учебных материалов в практику работы школы.
Второй компонент проекта (подготовка педагогов) включает в себя:
· переподготовку работников управления образованием пилотных регионов (на региональном и муниципальном уровнях), которые разрабатывают и проводят в жизнь региональные и муниципальные планы преобразования работы школы,
· переподготовку членов базовых (проектных) школьных команд, которые разрабатывают и проводят в жизнь планы информатизации своей школы,
· переподготовку предметных команд педагогов, которые будут обучать школьников на основе нового поколения цифровых образовательных материалов для шести предметных областей,
· создание новых моделей подготовки будущих учителей, подготовку их к работе с использованием создаваемых в проекте цифровых учебно-методических материалов,
· разработка системы управления качеством подготовки, переподготовки и повышения квалификации педагогов в области информатизации образования, с использованием универсальной (единой) системы учебных планов и модульных курсов подготовки, которая обеспечивает фиксацию, сохранение и распространение полученных в ходе проекта результатов на всю систему образования.
Анализ состояния дел в области информатизации, проведенный в ходе подготовки проекта, выявил острую нехватку специалистов, способных создавать практически эффективные цифровые образовательные ресурсы и грамотно использовать их на практике. Для успеха программы информатизации школы необходимо существенное развитие отечественного потенциала в области разработки и эффективного использования цифровых учебных материалов нового поколения. С этой целью, в рамках второго компонента предусмотрены меры по дополнительной подготовке специалистов в области педагогического дизайна, подготовке и изданию необходимых учебных и информационных материалов, широкой подготовке и информированию педагогов в области педагогического дизайна.
На всей территории РФ будут доступны как учебные материалы нового поколения для работы школьников и подготовки педагогов, так консультации по использованию этих материалов. Будет сформирован корпус методистов, которые смогут оказывать необходимую поддержку педагогам и после завершения проекта. Базой для переподготовки и последующей методической поддержки учителей станут межшкольные методические центры (компонент 3). Особенность предлагаемых программ обучения состоит в том, что они основываются на представлениях компетентностного подхода. Обучение педагогов включает в себя не только передачу соответствующих знаний и умений в ходе серии последовательных учебных мастерских, но и практическое использование этих знаний и умений педагогами в реальном учебном процессе, их постоянную консультационную поддержку, формирование (в том числе, с использованием Интернета) сетевых групп методической поддержки учителей. В результате должно произойти не только повышение квалификации педагогов, но и появиться практические изменения практики учебной работы в школах и профессиональных училищах, распространиться опыт и материалы для осуществления аналогичной трансформации в школах других регионов страны [34].
Структура массовой переподготовки педагогов включает пять основных процессов:
· Формирование у педагогов интереса к использованию ИКТ в учебном процессе еще до включения учителя в подготовку. Эта подготовка – добровольное дело педагога, желающего принять участие в решение наиболее противоречивых и острых задач современного образования, получать большее удовлетворение от своей работы [34].
· Ознакомление учителей с соответствующими способами педагогической работы с использованием ИКТ и специально разработанных учебно-методических материалов. Эта работа проводится в рамках специально организуемых мастерских. Содержание занятий мастерской определяется в соответствии с целевой группой обучаемых. Основной упор делается на поддержку дальнейшей самостоятельной работы педагогов. Например, при ознакомлении с ИКТ демонстрируются не столько основные приемы работы, сколько использование документации, обучающих программ, мастеров и подсказок для самостоятельного освоения соответствующих программных и технических средств [34].
· Оперативная поддержка, создание «среды сотрудничества» для прошедших подготовку педагогов: образование малых сетевых (в том числе, с помощью Интернет) групп взаимопомощи, постоянная в течение учебного года поддержка работы таких групп методистом, который проводил подготовку учителей [34].
· Анализ результатов практической работы и рефлексия процессов саморазвития учителя. Работа проводится в рамках мастерских и способствует закреплению и развитию методов профессионального саморазвития педагогов. Она является обязательной составной частью каждой из мастерских, наряду со знакомством с опытом передовых школ и учителей, педагогическими и поддерживающими их информационными технологиями. В ходе этой работы также стимулируется и поддерживается «растущая снизу» ассоциация преподавателей, где каждый педагог чувствует поддержку коллег, стремится и имеет реальную возможность достичь высших уровней педагогического мастерства [34].
Организационно переподготовка учителей проводится в форме краткосрочных семинаров (мастерских), которые проводятся 2-3 раза в год, а также методически и консультационно поддержанной практической работы педагогов в классе между этими семинарами. Вводный семинар предваряется «вступительным тестом», который помогает познакомиться с курсантами, определить их учебные стили и специфические нужды, что следует учесть в процессе переподготовки (знакомство с педагогическими техниками, уровень владения компьютером, тип интеллекта и т.п.). (Интенсивный семинар ориентирован на 6-12 дней занятий и проводится до начала учебного года). Успешно завершив вводный семинар, преподаватель возвращается к практической работе в школе, получая необходимую методическую поддержку. За нее отвечает методист, участвовавший в проведении семинара. Там, где есть технические условия, эту работу можно организовать с использованием Интернет. Сетевые группы взаимопомощи должны облегчить применение полученных знаний, способствовать созданию среды для формирования профессионального сообщества [34].
Составной частью методической поддержки являются семинарские занятия, проводимые в две сессии: в середине учебного года и по его окончании. Первая часть основного семинара проходит во время зимних каникул, как интенсивный пятидневный цикл занятий. Содержание работы семинара включает в себя подробный анализ работы в классе в первом полугодии (рефлексия, разбор удачных случаев), рассмотрение особенностей проведения занятий во втором полугодии. На этом семинаре участники проходят также цикл различных обязательных занятий. Основной результат семинара – индивидуальный план работы в классе на второе полугодие. Вторая часть основного семинара проводится по окончании учебного года. Содержание занятий включает анализ работы во втором полугодии и планирование занятий на следующий учебный год. На этом семинаре участники проходят цикл различных обязательных занятий. Участники завершают семинар отчетом о результатах учебного года и планом работы на следующий учебный год. В итоге, все участники, которые прошли основной цикл подготовки, включающий в себя три семинара и один учебный год моделируемой практической работы в школе, получают соответствующие сертификаты. При желании учитель может (и должен) модифицировать имеющиеся в его распоряжении новые методы работы. Для тех педагогов, которые хотят совершенствоваться в этом направлении, предлагается следующая ступень переподготовки [34].
Мастерская учителей организуется по окончании второго учебного года. Программа мастерской включает в себя анализ работы в прошедшем учебном году (рефлексия, разбор удачных случаев модификации и проектирования модулей) и ряд обязательных курсов. Мастерская завершается подготовкой учителями индивидуальных образовательных проектов для реализации в предстоящем учебном году. Успешное завершение мастерской учителей служит основанием для соответствующей сертификации педагогов, прошедших продвинутый цикл подготовки, который состоит из основного цикла и мастерской учителей, предваряемой одним дополнительным учебным годом моделируемой практической работы в школе [34].
После трех лет практической работы учителя могут пройти специальную подготовку и стать методистами по использованию ИКТ в учебной работе. Программа семинара методистов (Методический семинар) предусматривает участие курсанта в качестве ассистента в работе семинара по подготовке учителей (помощь работающему методисту, рефлексия работы). После стажировки в качестве методиста в течение учебного года (проведение семинаров, поддержка участников по компьютерной сети) курсант, успешно завершивший семинар, получает сертификат учителя-методиста с правом участвовать в подготовке учителей [34].
Обязательной составной частью сетевой поддержки педагогов являются:
– ведение списка рассылки и ленты новостей сетевого объединения педагогов;
– обмен видеофрагментами своих достижений (уроки, ученические конференции и т.п.) между участвующими в работе педагогами;
– регулярная подготовка сетевых методических бюллетеней, а также периодический выпуск интегрированных «бумажных» изданий.
Постоянно действующая сетевая поддержка, как составная часть массовой подготовки педагогов, представляет собой элемент системы управления содержательными преобразованиями в работе школы [34].
Проблемы и противоречия информатизации системы общего образования
Оценка реализации Государственной программы развития образования, анализ образовательной ситуации показывают, что, несмотря на значительные результаты информатизации системы общего образования, имеются проблемы, требующие разрешения [18]:
1. Отраслевой характер информатизации в России, рассогласованность действий по различным отраслям значительно усложняет и снижает эффективность принимаемых мер.
2. Отсутствие системности организации и координации процесса информатизации.
3. Процессы информатизации идут в большей степени стихийно, нет четкой координации и согласования управленческих действий на разных уровнях. Темпы и уровень информатизации зависят от компетентности руководителей образовательных учреждений и органов управления образованием.
4. Недостаточная разработанность нормативно-правового обеспечения процесса информатизации.
5. Отсутствие республиканского компонента в содержании школьного курса информатики, контроля за качеством образования учащихся по информатике.
6. Слабая развитость информационных каналов оперативного управления образованием; недостаточная оснащенность образовательных учреждений современными обучающими компьютерными программами.
7. Малоэффективное использование имеющейся компьютерной техники в образовательном процессе.
8. Недостаточная разработанность механизмов стимулирования труда учителей информатики и учителей, использующих ИКТ.
Наличие широкого спектра проблем указывает на сложившиеся в системе общего образования противоречия [18]:
- между приоритетностью информатизации и обособленность и отраслевым характером информатизации образования;
- между многообразием существующих средств образовательных технологий, высоким уровнем обеспеченность компьютерной техникой и малоэффективным использованием имеющихся информационных ресурсов в образовательном процессе; дефицитом квалифицированных кадров в области ИКТ;
- между необходимостью широкого использования ИКТ, высоким уровнем потребности в дистанционном образовании и несформированностью информационной образовательной среды, которая позволила бы эту потребность реализовать;
- между широкой реализацией республиканских и муниципальных программ и проектов информатизации образования и неразработанностью механизмов управления комплексной информатизацией систем образования, критериев определения эффективности использования ИКТ, механизмов оценки результативности, эффективности и социального влияния программ информатизации.
Потенциально информатизация системы общего образования может обеспечить повышение уровня качества образования, эффективности и информационной привлекательности деятельности образовательных учреждений. Однако, такой прорыв предполагает наличие четкой стратегии информатизации образования, последовательных и скоординированных действий в этой сфере.
1.2 Информатизация химического образования
В последнее десятилетие отмечается активное внедрение компьютерных и телекоммуникационных технологий в учебно-воспитательный процесс школы. В системе государственного управления образованием этому вопросу уделяют самое пристальное внимание.
Каждый день информационное сообщество российских учителей пополняется новыми именами, в сети появляются новые сетевые ресурсы, в школы приходят новые программные педагогические средства. Современный учитель химии не может находиться в стороне от этих процессов. Неуклонно растёт интерес преподавателей к проблеме информатизации: они принимают самое активное участие в создании образовательных ресурсов, их отладке, тестировании, апробации и внедрении. Сейчас уже никто не сомневается в том, что использование программных педагогических средств в учебно-воспитательном процессе существенно расширяет возможности учителя [11].
Можно выделить три основных направления развития информационных и коммуникационных технологий в современном естественно-научном образовании, в частности в обучении химии [36]:
· дистанционное и открытое образование;
· виртуальные лаборатории;
· библиотеки мультимедиа-объектов
· применение метода компьютерных проектов в обучении химии;
· использование цифровых лабораторий как современного информационного оборудования в проведении химического эксперимента, в частности использование цифровой лаборатории «Архимед» [20].
Дистанционное и открытое образование.
В основе концепции открытого образования лежит творческий характер обучения. Такая форма образовательного процесса включает ученика в развёрнутые системы информационных баз данных, снимает пространственно-временные ограничения в работе с различными источниками информации, что очень актуально в современном постиндустриальном информационном обществе [36].
Одним из наиболее динамично развивающихся направлений открытого образования является дистанционное образование (ДО), которое позволяет реализовать следующие принципы [36]:
· доступность обучения, в частности преодоление физических ограничений человека, расширение аудитории обучающихся;
· личностная направленность обучения, создание комфортных условий для школьников и учителей, учёт индивидуальных психологических особенностей (восприятия, памяти, мышления), индивидуальный темп обучения;
· развитие информационной культуры, навыков работы с современными средствами информатизации и телекоммуникации;
· социализация обучения, учёт личностно-коммуникативных особенностей учащихся.
Безусловный плюс – несомненная важность для психологического развития ребёнка – его вовлечение в систематическую учебную деятельность под непосредственным руководством взрослого, процесс овладения культурой и социализация проходят при посредничестве учителя.
Вместе с тем нельзя упускать из виду и обратную сторону дистанционного обучения. К проблемам дидактического плана следует отнести адаптацию сетевых образовательных ресурсов к возможностям, условиям, уровню подготовки каждого школьника [15].
Сложность состоит в том, что затруднено общение: между субъектами образовательного процесса нет непосредственного живого контакта. Посредником выступает компьютер. Для дистанционного обучения очень важна оперативность связи со школьником. Поэтому к учителю в системе ДО – компьютеру – предъявляются серьёзные требования:
- отвечать очень быстро на все письма;
- поощрять оперативность своих слушателей;
- установить чёткий график общения в режиме on-line и неукоснительно соблюдать его;
- создать атмосферу психологического комфорта
В настоящее время в системе ДО можно выделить следующие основные формы:
- электронные сетевые учебники;
- обучающие и контролирующие задания;
- электронные практикумы;
- исследовательские проектные работы;
- информационные ресурсы [2];
- дистанционные олимпиады и конкурсы;
- форумы, конференции, общение on-line;
- повышение квалификации и обмен опытом.
Виртуальные лаборатории.
Информационные технологии, включающие в себя современные мультимедиасистемы, могут быть использованы для поддержки процесса активного обучения. Именно они в последнее время привлекают повышенное внимание. Примером таких обучающих систем являются виртуальные лаборатории, которые могут моделировать поведение объектов реального мира в компьютерной образовательной среде и помогают учащимся овладевать новыми знаниями и умениями при изучении научно – естественных дисциплин, таких, как химия, физика, биология. Особо следует отметить значение виртуальных экспериментов для химического образования [24].
Преимущества работы с виртуальными лабораториями [24]:
· Подготовка учащихся к химическому практикуму в реальных условиях:
1) отработка основных навыков работы с оборудованием;
2) обучение выполнению требований техники безопасности в безопасных условиях виртуальной лаборатории;
3) развитие наблюдательности, умения выделять главное, определять цели и задачи работы, планировать ход эксперимента, делать выводы;
4) развитие навыков поиска оптимального решения, умения переносить реальную задачу в модельные условия и наоборот;
5) развитие навыков оформления своего труда.
· Проведение экспериментов, недоступных в школьной химической лаборатории.
· Дистанционный практикум и лабораторные работы, в том числе с детьми, имеющими ограниченные возможности, и взаимодействие с территориально удалёнными школьниками.
· Быстрота проведения работы, экономия реактивов.
· Усиление познавательного интереса.
Недостатки работы с виртуальными лабораториями [24]:
При использовании виртуальных лабораторий школьник, в силу своей неопытности, не сможет отличить виртуальный мир от реального, то есть модельные объекты, созданные компьютером, полностью вытеснят объекты реально существующего окружающего мира.
Запись данных.
Для начала записи данных в меню Регистратор выберите команду Пуск.
Анкетирование
Для реализации цели работы – исследования возможностей цифровой лаборатории «Архимед» для применения в урочной и внеурочной деятельности по химии нами был применен метод анкетирования. Анкетирование – метод сбора первичного материала в виде письменного опроса респондентов с целью сбора информации с помощью анкеты о состоянии тех или иных сторон воспитательного процесса, отношения к тем или другим явлениям [12].
Мы использовали сплошное (опрос всех представителей выборки) анкетирование. По числу респондентов и типов контактов респондентов анкетирование‚ проводимое нами следует отнести к групповому (несколько респондентов) и очному (в присутствии исследователя-анкетёра) соответственно. Вопросы, предложенные учащимся были составлены в закрытой (содержит полный набор возможных ответов) и открытой (ответ целиком и полностью формулирует сам респондент) форме (Приложение 7, 8). В закрытых вопросах респонденту предлагалось выбрать один или несколько из данных ему вариантов (количество выборов оговаривалось после формулировки вопроса). В наших анкетах для закрытых вопросов предъявлялись поливариантная (предусматривает список ответов) или шкальная (с ранжированием степени убеждения, отношения, впечатления и т.д.) форма вариантов ответов.
Задание.
1. Сделать вывод о свежести использованного молока
2. Чем вызвана кислотность молока, какая кислота образуется при скисании молока? Напишите уравнения реакции образования этой кислоты и её нейтрализацию гидроксидом натрия.
Опыт № 3. Определение кислотности хлеба [19]
Цель опыта: определить кислотность разных видов хлебобулочной продукции, проследив за изменением рН при титровании.
Форма работы: индивидуальная (в группах).
Оборудование и реактивы: хлебобулочная продукция (хлеб Дарницкий, хлеб пшеничный из сортовой муки, батон, хлеб пшеничный, приготовленном на жидких дрожжах, хлеб пшеничный обойный, хлеб ржаной из сеяной муки), 0,1 М раствор гидроксида натрия, бюретка, воронка, колбы для титрованиия, мешалка, фенолфталеин, датчик рН, соединительный провод для датчика, цифровая лаборатория «Архимед».
Настройка параметров измерения:
1) частота измерений – каждую секунду;
2) число замеров – 1000
Ход опыта:
Подготовка к анализу. Образцы разрезают пополам по ширине и от одной половины отрезают кусок (ломоть) массой около 70 г, у которого срезают корки и подкорочный слой общей толщиной 1 см. Для изделий массой менее 200 г берут целые булки, с которых срезают корки слоем приблизительно 1 см. Из кусков приготовленных изделий удаляют все включения (повидло, варенье,, изюм и т.п.), затем их быстро измельчают и перемешивают.
25 г измельченного мякиша отвешивают с погрешностью до 0,05 г. Навеску помещают в сухую бутылку (типа молочной) вместимостью 500 см3, с хорошо пригнанной пробкой. Мерную колбу вместимостью 250 см3 наполняют до метки дистиллированной водой, подогретой до температуры 60 °С. Около 1/4 взятой дистиллированной воды переливают в бутылку с хлебом, который после этого быстро растирают деревянной лопаточкой до получения однородной массы, без заметных комочков нерастертого хлеба.
К полученной смеси прибавляют из мерной колбы всю оставшуюся дистиллированную воду. Бутылку закрывают пробкой и энергично встряхивают в течение 3 мин. После встряхивания дают смеси отстояться в течение 1 мин и отстоявшийся жидкий слой осторожно сливают в сухой стакан через чистое сито или марлю.
Из стакана отбирают пипеткой по 50 см3 раствора в три конические колбы вместимостью по 100-150 см3 каждая. Затем опускают датчик рН и начинают по каплям из бюретки прибавлять 0,1 М раствор едкого натра, при включённой мешалке, до рН 8,2 (по показаниям прибора), фиксируя при этом цвет индикатора (появление розоватой окраски). Полученные данные занести в таблицу 2. Опыт повторяют 3 раза.
Таблица 2 - Кислотность хлеба
| Образец хлеба | Объём хлебной вытяжки, мл | Объём, прилитого раствора NaOH, мл | Среднее значение объёма, прилитого раствора NaOH, мл | Кислотность хлеба, град |
| Хлеб пшеничный из сортовой муки | ||||
| Образец 1 |
|
| ||
| Образец 2 | ||||
| Образец 3 | ||||
| Хлеб пшеничный, приготовленном на жидких дрожжах | ||||
| Образец 1 |
|
| ||
| Образец 2 | ||||
| Образец 3 | ||||
| Хлеб пшеничный обойный | ||||
| Образец 1 |
|
| ||
| Образец 2 | ||||
| Образец 3 | ||||
| Хлеб ржаной из обойной муки | ||||
| Образец 1 |
|
| ||
| Образец 2 | ||||
| Образец 3 | ||||
| Хлеб ржаной из обдирной муки | ||||
| Образец 1 |
|
| ||
| Образец 2 | ||||
| Образец 3 | ||||
| Хлеб ржаной из сеяной муки | ||||
| Образец 1 |
|
| ||
| Образец 2 | ||||
| Образец 3 | ||||
Результаты измерений: вычислить кислотность образцов хлеба по формуле [29]:
Кислотность хлеба = 25·50·4·V/(250·10),
где V – объем 0,1 моль/дм3 раствора гидроксида натрия, см3; 1/10 – приведение 0,1 моль/дм3 раствора гидроксида натрия или гидроксида калия к 1 моль/дм3; 4 – коэффициент, приводящий к 100 г навески; 25 – масса навески испытуемого продукта, г; 250 – объем воды, взятый для извлечения кислот, см3; 50 – объем испытуемого раствора, взятый для титрования, см3.
Проведённое нами испытание с образцом хлеба «Сеянный», показало следующий результат: (таблица 3)
Таблица 3 - Кислотность хлеба «Сеяный»
| Образец хлеба | Объём хлебной вытяжки, мл | Объём, прилитого раствора NaOH, мл | Среднее значение объёма, прилитого раствора NaOH, мл | Кислотность хлеба, град |
| Хлеб ржаной из сеяной муки | ||||
| Образец 1 | 50 | 4,95 |
5 | 6,25 |
| Образец 2 | 50 | 5,0 | ||
| Образец 3 | 50 | 5,05 | ||
По нашему мнению использование цифровой лаборатории «Архимед» для исследования кислотности хлеба помогает в определении, поскольку слабо-розового окрашивания фенолфталеина не появляется, даже при приливании большого избытка гидроксида натрия.
Опыт №4. Определение кислотности муки [19]
Цель опыта: определить кислотность разных сортов и видов муки, проследив за изменением рН при титровании.
Форма работы: индивидуальная (в группах).
Оборудование и реактивы: разные сорта и/или виды (пшеничная, ржаная, кукурузная) муки, 0,1 М раствор гидроксида натрия, бюретка, воронка, колбы для титрованиия, мешалка, фенолфталеин, датчик рН, соединительный провод для датчика, цифровая лаборатория «Архимед».
Настройка параметров измерения:
1) частота измерений – каждую секунду;
2) число замеров – 1000
Ход опыта: В колбу для титрования помещают 5 г муки, затем прибавляют 40 мл воды, 5-6 капель фенолфталеина. Затем опускают датчик рН, начинают регистрацию данных и приливание (по каплям) 0,1 М раствор едкого натра при включённой мешалки до рН 8,2. Опыт повторяют 3 раза. Полученные данные занести в таблицу 4.
Таблица 4 - Кислотность муки
| Образец муки | Масса муки в образце, г | Объём, прилитого раствора NaOH, мл | Среднее значение объёма, прилитого раствора NaOH, мл | Кислотность муки, град |
| Мука пшеничная | ||||
| Образец 1 |
|
| ||
| Образец 2 | ||||
| Образец 3 | ||||
| Мука ржаная | ||||
| Образец 1 |
|
| ||
| Образец 2 | ||||
| Образец 3 | ||||
| Мука кукурузная | ||||
| Образец 1 |
|
| ||
| Образец 2 | ||||
| Образец 3 | ||||
Результаты измерений: вычислить кислотность образцов муки по формуле:
Кислотность муки = V ( NaOH ) · 20 / 10
Опыт №4. Определение свежести творога [19]
Цель опыта: определить кислотность разных видов творога, проследив за изменением рН при титровании.
Форма работы: индивидуальная (в группах).
Оборудование и реактивы: разные виды творога, 0,1 М раствор гидроксида натрия, бюретка, воронка, колбы для титрованиия, мешалка, фенолфталеин, датчик рН, соединительный провод для датчика, цифровая лаборатория «Архимед».
Настройка параметров измерения:
1) частота измерений – каждую секунду;
2) число замеров – 1000
Ход опыта: В колбу для титрования помещают 10 г творога (очистить от изюма и др. включений) и небольшими порциями приливают 20 мл воды, нагретой до 30-40 0С. Творог тщательно перемешивают стеклянной палочкой. Прибавляют 5 капель спиртового раствора фенолфталеина. Помещают в раствор датчик рН, начинают регистрацию данных, одновременно прибавляя 0,1 н. раствор гидроксида натрия до рН 8,2 (появления розовой окраски). Опыт повторяют 3 раза. Полученные данные занести в таблицу 5.
Таблица 5 - Кислотность творога
| Образец творога | Масса творога в образце, г | Объём, прилитого раствора NaOH, мл | Среднее значение объёма, прилитого раствора NaOH, мл | Кислотность творога, град |
| Образец творога 1 | ||||
| 1 |
|
| ||
| 2 | ||||
| 3 | ||||
| Образец творога 2 | ||||
| 1 |
|
| ||
| 2 | ||||
| 3 | ||||
| Образец творога 3 | ||||
| 1 |
|
| ||
| 2 | ||||
| 3 | ||||
Результаты измерений: вычислить кислотность образцов творога по формуле:
Кислотность творога = V ( NaOH ) · 20
Опыт 2. Коррозия металлов
Данный эксперимент может быть проведён на элективном курсе «Химия и экология», в рамках подготовки к ученическим конференциям и в урочной деятельности в 9 классе при изучении темы «Металлы» на уроке № 13 «Общие понятия о коррозии металлов» (Приложение 1).
Цель работы: изучить влияние продуктов коррозии на развитие водных растений, используя при этом возможности цифровой лаборатории «Архимед» (насадка рН-метр).
Форма работы: фронтальная (демонстрационный эксперимент).
Опыт 1. Влияние продуктов коррозии металлов на развитие водных растений
Опыт закладывают за 4 дня до урока (можно на предыдущем уроке). Значения рН регистрируют в одно и тоже время один раз в день. Полученные по водородному показателю данные представляют учащимся в виде графика. А сами опытные образцы демонстрируют на уроке.
Реактивы и оборудование: вода, железный гвоздь, кусочек меди (цинка, олова), водоросли; 3 химических стакана.
Ход работы: Три химических стакана вместимостью 100 мл наполняют водой и помещают в них водоросли. Во 2-й стакан опускают гвоздь, в 3-й – гвоздь и кусочек меди (цинка, олова), а 1-й стакан оставляют в качестве контрольного. В течение 4 дней делают контрольные замеры pН воды во всех стаканах, проводят обнаружение ионов металлов (Fe2+, Fe3+, Zn2+, Cu2+, Sn2+).
Наблюдения:
Через 5 дней можно наблюдать резкое изменение pН воды во 2-м и 3-м стаканах по сравнению с контрольным, а также внешнего вида растений: они буреют, сильно ослизняются, отмирает корневая система.
Ход опыта: Четыре химических стакана вместимостью 50 мл наполняют водой и:
В стакан № 1: помещают водоросли – контрольный образец
В стакан №2: помещают водоросли и железный гвоздь
В стакан № 3: помещают водоросли и железный гвоздь, с медной проволокой
В стакан № 4: помещают водоросли и железный гвоздь, с цинковой стружкой
· В течение 4 дней делают контрольные замеры pН воды во всех стаканах
· Значения рН регистрируют в одно и тоже время один раз в день.
· Полученные по водородному показателю данные представляются учащимся в виде графика.
· Сами опытные образцы растений демонстрируют на последнем элективе.
Наблюдения:
Через 5 дней можно наблюдать изменение pН воды во 2-м, 3-м,4-м стаканах по сравнению с контрольным, а также внешнего вида растений: они буреют, сильно ослизняются. ( таблица 7)
Таблица 7 - Водородный показатель при прохождении процессов коррозии металлов в воде
| Дата измерения | Стакан №1 | Стакан №2 | Стакан №3 | Стакан №4 |
| Первый день | 8,38 | 8,37 | 8,30 | 8,33 |
| Второй день | 9,07 | 9,26 | 8,95 | 8,43 |
| Третий день | 9,10 | 9,68 | 9,15 | 8,58 |
| Четвёртый день | 9,14 | 9,75 | 9,20 | 8,63 |
| Пятый день | 9,15 | 9,75 | 9,47 | 8,68 |
Теоретическое обоснование процесса
Коррозия – это самопроизвольное разрушение металлических материалов, происходящее под химическим воздействием окружающей среды [42].
В результате электрохимической коррозии окисление металла может приводить как к образованию нерастворимых продуктов (например ржавчины), так и к переходу металла в раствор в виде иона. Ржавчина представляет собой гидратированный оксид железа – Fe2O3· xH2O. Ржавление протекает под воздействием воды и кислорода. Это электрохимический процесс, при котором одни частицы железа играют роль катода, а другие – анода.
Важнейшими окислителями, вызывающими электрохимическую коррозию являются кислород и ионы водорода.
О2 + 2Н+ + 4e = 2Н2О
2Н+ + 2e = Н2
Образец в стакане № 2:
В анодной области:
Fe(тв) – 2е → Fe2+(водн),
В катодной области:
О2(водн) + 2Н2О(ж.) + 4е → 4ОН-(водн)
При контакте катодной и анодной областей происходит осаждение Fe(OH)2. Воздух окисляет его и образуется ржавчина:
Fe(OH)2(тв.) + 0,5О2 + Н2О → Fe2O3· xH2O
Образец в стакане № 3 (катодное покрытие): металл включения (Cu) имеет больший потенциал, чем основной металл (Fe)
В анодной области:
Fe(тв) – 2е → Fe2+(водн)
В катодной области:
2Н+ + 2e → Н2
О2(водн) + 2Н2О(ж.) + 4е → 4ОН-(водн)
При контакте катодной и анодной областей происходит осаждение Fe(OH)2. Воздух окисляет его и образуется ржавчина:
Fe(OH)2(тв.) + 0,5О2 + Н2О → Fe2O3· xH2O
Поток электронов от железа направляется к меди и разряжает ионы водорода, а железо разрушается быстрее, чем без меди.
Образец в стакане № 4 (анодное покрытие): металл включения (Zn) имеет меньший потенциал, чем основной металл (Fe)
В анодной области:
Zn(тв) – 2е → Zn2+(водн)
В катодной области:
2Н+ + 2e → Н2
2Н2 + О2(водн) → 2 Н2О
О2(водн) + 2Н2О(ж.) + 4е → 4ОН-(водн)
При контакте катодной и анодной областей происходит осаждение Zn(OH)2(осадок белого цвета)
Значения электродных потенциалов металлов подтверждают предложенное выше объяснение процесса:
Fe3+ + 3e = Fe, Е0 = - 0,036 В
Сu2+ + 2e = Cu, Е0 = 0,337 В
Zn2+ + 2e = Zn, Е0 = - 0,763 В
Таким образом, медь будет увеличивать скорость электрохимической коррозии. Это подтверждают результаты эксперимента, а именно в 3-м стакане изменение значения рН более интенсивно по сравнению с 4-м стаканом.
Опыт № 3. Определение рН (водородного показателя) питьевой неминерализованной воды, минеральной воды, газированных окрашенных напитков
Активная реакция среды, является одним из параметров качества питьевой воды, наряду с такими характеристиками как температура, мутность, цветность, запах и привкус, прозрачность, общая жёсткость, содержание ионов, окисляемость.
На величину рН воды влияет содержание карбонатов, гидроокисей, солей, подверженных гидролизу, гуминовых веществ и т. п. Данный показатель является индикатором загрязнения открытых водоемов при выпуске в них кислых или щелочных сточных вод, а также питьевой воды. В результате происходящих в воде химических и биологических процессов и потерь углекислоты рН воды открытых водоемов может быстро изменяться, и этот показатель следует определять сразу же после отбора пробы, желательно на месте отбора. Измерение рН цветных растворов и суспензий индикаторным способом невозможно.
Цель работы: Определить характер среды (кислая, щелочная, нейтральная) различных пробы воды (хозяйственно-питьевая вода, вода из водоёма, вода из родника) и напитков (Кока-кола, Фанта) и сделать вывод об их пригодности для потребления в качестве питьевой воды.
Форма работы: фронтальная (демонстрационный эксперимент).
Оборудование и реактивы: пробы воды и напитков (хозяйственно-питьевая вода, вода из водоёма, вода из родника, Кока-кола, Фанта); химические стаканы, лабораторный штатив, датчик рН, цифровая лаборатория «Архимед».
Настройка параметров измерения:
1) частота измерений – каждую секунду;
2) число замеров – 50
Ход работы: каждую из предложенных для анализа вод прилить в химический стакан. Погрузить датчик рН, начать измерение.
Результаты работы: представить полученные результаты в форме таблицы (Таблица 8)
Таблица 8 - Активная реакция среды рН проб воды и напитков
| Пробы воды и напитков | Объём пробы воды и напитков | Активная реакция среды, рН | Среднее значение рН |
| Хозяйственно-питьевая вода | |||
| Проба 1 | |||
| Проба 2 | |||
| Проба 3 | |||
| Вода из водоёма | |||
| Проба 1 | |||
| Проба 2 | |||
| Проба 3 | |||
| Вода из родника | |||
| Проба 1 | |||
| Проба 2 | |||
| Проба 3 | |||
| «Кока-кола» | |||
| Проба 1 | |||
| Проба 2 | |||
| Проба 3 | |||
| «Фанта» | |||
| Проба 1 | |||
| Проба 2 | |||
| Проба 3 | |||
Вывод: Сделайте вывод о пригодности исследуемых вод по показателю рН, если согласно требованиям ГОСТ активная реакция (рН) питьевой воды должна составлять 6,5-9,5.
Выводы
1. Проведён методический анализ материалов по основным направлениям развития информационных и коммуникационных технологий в современном естественно-научном образовании, в частности в обучении химии.
2. Освоена техника работы с использованием цифровой лаборатории «Архимед».
3. Проведён методический анализ разработок опытов по химии создателей цифровой лаборатории «Архимед».
4. Разработаны методики и теоретическое обоснование результатов экспериментов с использованием цифровой лаборатории «Архимед» в урочной и внеурочной деятельности (элективные курсы «Химия и медицина», «Химия и экология») по химии.
5. Проведена апробация самостоятельно разработанных, модифицированных и предложенных разработчиками цифровой лаборатории «Архимед» опытов в урочной и внеурочной деятельности по химии.
6. Для исследования эффективности применения цифровой лаборатории «Архимед» в процессе обучения применяли метод выборочного‚ группового‚ очного анкетирования.
7. Составлено пособие к практикуму для учащихся – слушателей элективных курсов «Химия и экология» и «Химия и медицина» в форме рабочей тетради.
Список Литературы
1. Аксёнова Э.Н., Андрианова О.П. Руководство к лабораторным занятиям по фармацевтической химии. – 3-е изд., перераб. и доп. – М.: Медицина, 2001. – 384 с.
2. Анисимова Г.А. Библиотека сетевых образовательных ресурсов для современного учителя химии // Современные информационные технологии в обучении химии: Материалы III областной научно- практической конференции учителей химии и преподавателей вузов (Пенза, ПГПУ им. В. Г. Белинского, 2006). – Пенза: ПГПУ, 2006. – С. 20 –21.
3. Архимед 2004. Первый шаг (http: //www.9151394. ru/projects/arhimed/ arhkonkurs_040315/pobediteli.html).
4. Беспалько, В. П. Персонифицированное образование / В. П. Беспалько // Педагогика. – №2. – 1998. – С. 17.
5. Бондарев А.С., Дмитриева Н.В., Терехин М.Б. Цифровые лаборатории «Архимед» в обучении биологии (http://sputnik.mto.ru/Docs_35/Kongress/6.html).
6. Габриелян О.С. Химия. 8-9 класс: Методическое пособие. – М., Дрофа, 1999-2001. – 128с.
7. Габриелян О.С.‚ Остроумов Г. Химия 9 класс: Настольная книга учителя. – М.: Дрофа, 2003. – 400с.
8. О.С. Габриелян. Химия. 8 кл.: тетрадь для лабораторных опытов и практических работ к учебнику О.С. Габриеляна « Химия. 8 класс» / О.С. Габриелян, А.В. Яшукова. – 3-е изд., стереотип. – М.: Дрофа, 2008. – 96 с.
9. Габриелян О.С. и др. Химия. 9 класс: Учебник для общеобразовательных учреждений. М.: Дрофа, 2003. – 224с.
10. Додонов Е.Д. «Живой калейдоскоп» информационных технологий / Международный педагогический мастер-класс 2004 Цифровая школьная четверть. 2004 (http://www.bgpu.ru/intel/Material/mc_04/text/dodonov.htm).
11. Дорофеев М.В. Информатизация школьного курса химии // Химия. Первое сентября. – 2002. – №37. С.35 –38.
12. Дружинин В. Н. Экспериментальная психология. – СПб.: Питер, 2002. – 45 с.
13. Дунин С.М., Федорова Ю.В. «Живая физика» плюс цифровая лаборатория «Архимед» (материалы Педагогического марафона – 2005) // Физика. Приложение к газете «Первое сентября». – 2005. – № 11.
14. Дунин С.М., Федорова Ю.В. Совместное использование программы «Живая физика» и цифровой лаборатории «Архимед» (http://www.9151394.ru/projects/arhimed/arhkonkurs_040315/dunin/sovm_isp.htm).
15. Закурдаева С.Ю. Цифровая лаборатория «Архимед». Исследовательская деятельность учащегося (материалы Педагогического марафона – 2004) // Физика. Приложение к газете «Первое сентября». – 2004. – № 22, Новые технологии в образовании / Семинар в Центре информационных технологий и учебного оборудования (http://pedsovet.edu.ru/nfpk_web/start.htm)
16. Intel® “Обучение для будущего” (при поддержке Microsoft® ) – М.: «Русская редакция», 2005. – 368с.
17. Каталог образовательных средств и решений. Школьные лаборатории. Цифровая лаборатория «Архимед» / Институт новых технологий (http://www.int-edu.ru/arhimed/).
18. Концепция информатизации системы общего образования республики Саха (Якутия).
19. Кузнецова А.В. Практикум по прикладной химии: Учебное пособие ( ПГПУ им. В.Г. Белинского). – Пенза, 2004. – 108 с.
20. Линьков В.М. // Современные информационные технологии в обучении химии: Материалы III областной научно- практической конференции учителей химии и преподавателей вузов (Пенза, ПГПУ им. В. Г. Белинского, 2006). – Пенза: ПГПУ, 2006. – C. 7 –8.
21.Мелентьева Г.А., Антонова Л.А. Фармацевтическая химия. – М.: Медицина, 1985. – 480 с.
22.Мещерякова Е. А. Метод компьютерных проектов в практике обучения химии // Современные информационные технологии в обучении химии: Материалы III областной научно- практической конференции учителей химии и преподавателей вузов (Пенза, ПГПУ им. В. Г. Белинского, 2006). – Пенза: ПГПУ, 2006. – С. 72 –75.
23.Мещерякова О. А. Организация проектной деятельности в локальной сети // Современные информационные технологии в обучении химии: Материалы III областной научно- практической конференции учителей химии и преподавателей вузов (Пенза, ПГПУ им. В.Г. Белинского, 2006). – Пенза: ПГПУ, 2006. – С. 70 –72.
24.Морозов М.Н., Танаков А.И., Герасимов А.В., Быстров Д.А., Цвирко В.Э., Дорофеев М.В. Разработка виртуальной химической лаборатории для школьного образования. Educational Technology & Society, 2004, №3 – С. 155 –164.
25.Новые технологии в образовании / Семинар в Центре информационных технологий и учебного оборудования (http://pedsovet.edu.ru/nfpk_web/start.htm).
26. Подьячева Е.А., Ашкеева Г.Х., Макеева Е.Е. и др. Практикум по химии: ( для подготовительных отделений). – Алма-Ата: Мектеп, 1987. – 160 с.
27. Полат Е. С. Новые педагогические технологии / Пособие для учителей – М.: 1997. – С. 55 –58.
28. Программа курса химии для 8-11 классов общеобразовательных учреждений. – М.: Дрофа, 2000-2002. –160с.
29.Роева Н. Н., Клячко Ю. А, Кирничная В. К. Методы исследования свойств сырья и продуктов питания. Лабораторный практикум для студентов технологических специальностей. – М.: 2000. – С. 24 –26.
30.Таирова Е. А. Обзор учебников и пособий по химии на электронных носителях // Современные информационные технологии в обучении химии: Материалы III областной научно- практической конференции учителей химии и преподавателей вузов (Пенза, ПГПУ им. В. Г. Белинского, 2006). – Пенза: ПГПУ, 2006. – С. 22 –31.
31.Уваров А.Ю. Два кризиса образования, учебная архитектура и Интернет // Организационные инновации в управлении интегрированными образовательными учреждениями: Материалы Всероссийской научно-практической конференции (Барнаул, 2002). – Барнаул. – 2002. - С. 16-17.
32.Уваров А.Ю. О конструктивных элементах открытой учебной архитектуры // «Информационные технологии в непрерывном образовании»: Тезисы докладов Международной конференции (Петрозаводск, Петрозаводский государственный университет, 1995). – Петрозаводск.: Изд-во Петрозаводского государственного университета, 1995 г. – С. 15.
33.Уваров А.Ю.Открытая учебная архитектура для школы информационного века // Образование и информатика: Труды Международного конгресса ЮНЕСКО. Т. 4, М.: 1997.
34.Уваров А.Ю. Подготовка педагогов в проекте «Информатизация системы образования» // «Телематика'2003»: Материалы X Всероссийской научно-методической конференции. – СПб.: 2003. С. 25 –27.
35.Федорова Ю.В., Трактуева С.А., Шапиро М.А., Панфилова А.Ю. Цифровые лаборатории «Архимед» // Информационные технологии в образовании-2003. Сборник трудов конференции (http://www.bitpro.ru/ito/2003/II/1/II-1-2863.html; http://www.ito.su/2003/tezis/II-1-2863-Ustniy.html
36.Филиппова В.М, Тихомирова В. П. Фрагменты коллективной монографии под общей редакцией В. М. Филиппова и В.П. Тихомирова. http: / /academy.odoportal.ru/documents/academ/bibl/russia/1/html.
37. Фирстова Н. В., Мещерякова О. А. Практикум к элективному курсу «Химия и экология». – Пенза: ПГПУ‚ 2007. – 50 с.
38. Цифровая лаборатория « Архимед». Методические материалы. Институт новых технологий. – М.: 2007. – 375 с.
39. Штремплер Г.И. Химия на досуге: Домашняя хим. лаб.: Кн. для учащихся. – М.: Просвещение: « Учеб. лит.», 1996. – 94 с.
40.sota –as.ru
41.www. FIZfaq 1502.narod.ru./ arhimed.)
42. Эпштейн Д.А., Ходаков Ю.В. Неорганическая химия. Учебник для 9 класса. – М.: Просвещение, 1986. – С. 112 – 116.
Приложение 1. Примерное календарно-тематическое планирование учебного материала по химии в 9 классах
| № урока | Содержание учебного материала |
| 1-2 | Характеристика химического элемента на основании его положения в Периодической системе Д.И. Менделеева |
| 3 | Амфотерные оксиды и гидроксиды |
| 4 | Периодический закон и система элементов Д.И.Менделеева |
| Раздел 1.Скорость химических реакций. Химическое равновесие(6ч) по учебнику 8 класса | |
| 5 | Скорость химических реакций |
| 6 | Зависимость скорости химических реакций от природы реагирующих веществ, концентрации и температуры |
| 7 | Катализ и катализатор |
| 8 | Обратимые и необратимые реакции |
| 9 | Химическое равновесие и способы его смещения |
| 10 | Обобщение и систематизация знаний по теме |
| Раздел 2 . Металлы (15 ч) | |
| 11 | Положение элементов металлов в Периодической системе Д.И.Менделеева и особенности строения их атомов Физические свойства металлов |
| 12 | Химические свойства металлов |
| 13 | Общие понятия о коррозии металлов |
| 14 | Сплавы |
| 15 | Металлы в природе. Общие способы их получения |
| 16 | Общая характеристика элементов главной подгруппы I группы |
| 17 | Соединения щелочных металлов |
| 18 | Общая характеристика элементов главной подгруппы II группы |
| 19 | Соединения щелочноземельных металлов |
| 20 | Алюминий, его физические и химические свойства |
| 21 | Соединения алюминия |
| 22 | Железо, его физические и химические свойства |
| 23 | Генетические ряды Fe2+ и Fe3+ |
| 24 | Обобщение по теме «Металлы» |
| 25 | Контрольная работа по теме «Металлы» |
| Раздел 3 . Неметаллы (20ч.) | |
| 26 | Общая характеристика неметаллов |
| 27 | Общая характеристика галогенов |
| 28 | Соединения галогенов |
| 29 | Сера, ее физические и химические свойства |
| 30 | Оксиды серы (IV) и (VI) |
| 31 | Серная кислота и ее соли |
| 32 | Азот и его свойства |
| 33 | Аммиак и его свойства |
| 34 | Соли аммония |
| 35 | Азотная кислота и ее свойства |
| 36 | Соли азотистой и азотной кислот. Азотные удобрения |
| 37 | Фосфор |
| 38 | Соединения фосфора |
| 39 | Углерод |
| 40 | Оксиды углерода(II) и (IV) |
| 41 | Карбонаты |
| 42 | Кремний |
| 43 | Силикатная промышленность |
| 44 | Обобщение по теме «Неметаллы» |
| 45 | Контрольная работа по теме «Неметаллы» |
| Раздел 4. Практикум по неорганической химии (5 ч) | |
| 46 | Получение амфотерного гидроксида и изучение его свойств |
| 47 | Получение аммиака и исследование |
| 48-49 | Решение экспериментальных задач на распознавание важнейших катионов и анионов |
| 50 | Решение экспериментальных задач на распознавание важнейших катионов и анионов |
| Раздел 5 . Органические вещества (12ч.) | |
| 51 | Предмет органической химии. Строение атома углерода |
| 52 | Алканы. Химические свойства и применение алканов |
| 53 | Алкены. Химические свойства этилена |
| 54 | Понятие о спиртах на основе реакции гидратации этилена и взаимодействия этилена с раствором перманганата калия |
| 55 | Окисление альдегида в кислоту и понятие об одноосновных карбоновых кислотах |
| 56 | Понятие о сложных эфирах. Жиры |
| 57 | Понятие об аминокислотах |
| 58 | Реакция поликонденсации аминокислот. Белки |
| 59 | Углеводы |
| 60 | Полимеры |
| 61 | Обобщение знаний учащихся по органической химии |
| 62 | Решение экспериментальных задач на распознавание органических веществ с использованием качественных реакций на альдегиды, многоатомные спирты, крахмал и непредельные соединения |
| Тема 7. Обобщение знаний по химии за курс основной школы (6ч.) | |
| 63 | Периодический закон и Периодическая система химических элементов Д. И. Менделеева в свете учения о строении атома |
| 64 | Строение вещества (виды химических связей и типы кристаллических решеток) |
| 65 | Химические реакции |
| 66 | Классы химических соединений в свете ТЭД. |
| 67 | Контрольная работа по теме «Органические вещества» и «Обобщение знаний по химии за курс основной школы» |
| 68 | Подведение итогов |
Приложение 2. Примерное календарно-тематическое планирование учебного материала по химии в 8 классах
| № урока |
Содержание учебного материала
Раздел 1. Атомы химических элементов (10 часов)
Приложение 3. Примерное календарно-тематическое планирование учебного материала по химии в 11 классах
| № | Содержание учебного материала | Примерные сроки | ||
| 11А | 11Б | |||
| Раздел №1 Строение атома | ||||
| 1. | Основные сведения о строении атома. | 2.09 | 5.09 | |
| 2. | Электронная оболочка. Особенности строения электронных оболочек переходных элементов. | 6.09 | 6.09 | |
| 3. | Периодический закон и периодическая система химических элементов Д.И.Менделеева. | 9.09 | 12.09 | |
| 4. | Значение периодического закона Д.И. Менделеева. | 13.09 | 13.09 | |
| 5. | Виды химической связи. Ионная связь. | 16.09 | 19.09 | |
| 6. | Ковалентная полярная и неполярная химическая связь. | 20.09 | 20.09 | |
| 7. | Металлическая связь. | 23.09 | 26.09 | |
| 8. | Водородная химическая связь. | 27.09 | 27.09 | |
| 9. | Повторение и обобщение знаний по теме «Строение атома. Химическая связь» | 30.09 | 3.10 | |
| 10. | Контрольная работа №1 по теме «Строение атома» | 4.10 | 4.10 | |
| Раздел №2 Строение вещества и их свойства | ||||
| 11. | Полимеры. | 7.10 | 10.10 | |
| 12. | Органические полимеры. Волокна. | 11.10 | 11.10 | |
| 13. | Органические полимеры. Волокна. | 14.10 | 17.10 | |
| 14. | Неорганические полимеры. | 18.10 | 18.10 | |
| 15. | Вещества молекулярного строения. Газообразные вещества. | 21.10 | 24.10 | |
| 16. | Жидкие вещества. | 25.10 | 25.10 | |
| 17. | Твердые вещества. | 28.10 | 31.10 | |
| 18. | Чистые вещества и смеси. | 1.11 | 1.11 | |
| 19. | Дисперсные системы. | 11.11 | 14.10 | |
| 20. | Состав смесей. Разделение смесей. | 15.11 | 15.11 | |
| 21. | Истинные растворы. Способы выражения концентрации. | 18.11 | 21.10 | |
| 22. 23. 24. 25. | Решение задач на массовую долю растворимого вещества. Решение задач на массовую долю растворимого вещества. Решение задач на массовую долю растворимого вещества. Решение задач на массовую долю растворимого вещества. | 22.11 25.11 29.11 2.12 | 22.11 28.10 29.11 5.12 | |
| 26. | Урок-зачет «Решение задач» | 6.12 | 6.12 | |
| 27. | Классификация химических реакций. Реакции, которые идут без изменения состава. | 9.12 | 12.12 | |
| 28. | Классификация химических реакций, которые идут с изменением состава вещества. | 13.12 | 13.12 | |
| 29. | Тепловой эффект химической реакции. | 16.12 | 19.12 | |
| 30. | Скорость химической реакции. | 20.12 | 20.12 | |
| 31. | Обратимость химических реакций. Химическое равновесие. | 23.12 | 26.12 | |
| 32. | Условия смещения химического равновесия. | 27.12 | 27.12 | |
| 33. | Электролитическая диссоциация. | |||
| 34. | Реакции ионного обмена. | |||
| 35. | Гидролиз. Гидролиз неорганических веществ. | |||
| 36. | Гидролиз органических веществ. | |||
| 37. | Среда водных растворов. Водородный показатель. | |||
| 38. 39. | Окислительно-восстановительные реакции. | |||
| 40. 41. | Электролиз. | |||
| 42. | Обобщение знаний по теме «Строение вещества и их свойства» | |||
| 43. | Контрольная работа №2 по теме «Строение вещества и их свойства» | |||
| Раздел №3 Вещества и их свойства | ||||
| 44. | Металлы и их свойства. |
| ||
| 45. | Металлотермия. Коррозия металлов |
| ||
| 46. | Общие способы получения металлов |
| ||
| 48 | Общая характеристика инертных газов. |
| ||
| 49 | Общая характеристика галогенов. |
| ||
| 50 | Классификация неорганических и органических веществ. |
| ||
| 51 | Оксиды. |
| ||
| 52 | Кислоты. Химические свойства кислот. Неорганические и органические кислоты. |
| ||
| 53. | Особые свойства серной кислоты. |
| ||
| 54. | Особые свойства азотной кислоты. |
| ||
| 55. | Основания. |
| ||
| 56. | Соли. |
| ||
| 57. | Химические свойства солей. |
| ||
| 58. | Генетическая связь между классами неорганических соединений |
| ||
| 59. | Генетическая связь между классами органических соединений |
| ||
| 60. | Повторение и обобщение темы «Вещества и их свойства» |
| ||
| 61. | Урок-зачет по теме «Вещества и их свойства». |
| ||
| 62. | Контрольная работа №3 по теме «Вещества и их свойства» |
| ||
| 63. | Практическая работа №1 |
| ||
| 64. | Практическая работа №2 |
| ||
| 65. | Химия в жизни общества (урок- конференция) · Химия и промышленность · Химия и сельское хозяйство · Химия и экология · Химия и повседневна жизнь человека |
| ||
| Резерв | ||||
| 66. 67. 68 | Решение задач и упражнений |
| ||
| Общее число по курсу | 68 | |||
| Демонстрации | 5 | |||
| Лабораторные опыты | 22 | |||
| Практические работы | 2 | |||
| Контрольные работы | 3 | |||
Приложение 4. Тематическое содержание программы элективного курса «Химия и медицина»
| № | Наименование тем курса | Количество часов |
| I | Теоретический курс | 11 |
| 1 | Химия и лекарства | 1 |
| 2 | Здоровое питание | 1 |
| 3 | Пищевые добавки | 1 |
| 4 | Витамины | 1 |
| 5 | Гормоны | 1 |
| 6 | Ферменты | 1 |
| 7 | Антибиотики | 1 |
| 8 | Анестезирующие средства | 1 |
| 9 | Полимеры в медицине | 1 |
| 10 | Неорганические вещества как лекарства | 1 |
| 11 | Экскурсия в домашнюю аптечку | 1 |
| II | Практикум | 4 |
| 12 | Изучение свойств веществ, производных салициловой кислоты | 1 |
| 13 | Изучение свойств лекарственных веществ, производных п-аминофенола | 1 |
| 14 | Обнаружение витаминов | 1 |
| 15 | Решение экспериментальных задач с использованием лекарственных веществ | 1 |
| III | Подведение итогов | 2 |
| 16 | Экскурсия в центр сертификации контроля и качества лекарственных препаратов. | |
| 17 | Защита проектов | 1 |
Приложение 5. Тематическое содержание программы элективного курса «Химия и экология»
| № | Наименование тем курса | Количество часов |
| I | Теоретический курс | 24 |
| 1 | История экологии, значение экологии, прикладная экология. | 1 |
| 2 | "Страхи" современного мира. | 1 |
| 3 | Современные проблемы утилизации мусора (Экологическая ситуация в городе и условия жизни населения). | 1 |
| 4 | Современные экологические проблемы с точки зрения химика. | 1 |
| 5 | Яды вокруг нас! Решение задач. | 1 |
| 6 | Диоксины и окружающая среда. Решение задач. | 1 |
| 7 | Медь и окружающая среда. | 1 |
| 8 | Изучение белков в связи с охраной природы. | 1 |
| 9 | Бензин и кислотные загрязнители. | 1 |
| 10 | Эпидемиология. | 1 |
| 11 | Решение задач с экологическим содержанием. | 1 |
| 12 | Работа в Интернет-классе по отбору информации для проектов и сообщений. | 1 |
| 13 | Решение задач с экологическим содержанием. | 1 |
| 14 | Нужно ли бояться Леонидовки? | 1 |
| 15 | Экология воды. Решение задач. | 1 |
| 16 | Чистая вода для хвори беда! | 1 |
| 17 | Экология почв | 1 |
| 18 | Экологические проблемы в добыче полезных ископаемых | 1 |
| 19 | Источники загрязнения атмосферы. | 1 |
| 20 | Экология воздуха. | 1 |
| 21 | Пластмасса вчера, сегодня и завтра. | 1 |
| 22 | Экология питания. | 1 |
| 23 | Консерванты, красители в пищевых продуктах. | 1 |
| 24 | Решение задач с экологическим содержанием. | 1 |
| II | Практикум. | 6 |
| 25 | Методы экологии. | 1 |
| 26 | Мониторинг водных сред (1). | 1 |
| 27 | Мониторинг водных сред (2). | 1 |
| 28 | Мониторинг почвы. | 1 |
| 29 | Минеральные удобрения как возможные загрязнители почв и сельхозпродукции | 1 |
| 30 | Медико-экологические исследования Определение нитратов в пищевых продуктов (овощных культурах). | 1 |
| III | Подведение итогов. | 4 |
| 31 | Экскурсия в Росприроднадзор Пензенской области. | 1 |
| 32 | Экскурсия в ЦЛАТИ по Пензенской области. | 1 |
| 33 | Защита проектов. | 1 |
| 34 | Защита проектов. | 1 |
Приложение 6. Конспект занятия «Анализ качества пищевых продуктов»
Цель: освоение методов анализа качества продуктов питания и сырья, с использованием возможностей цифровой лаборатории «Архимед».
Задачи:
1. Сформировать у учащихся представление о водородном показателе растворов на основе выполнения опытов по определению рН.
2. Познакомить школьников с методикой титрования.
3. Сформировать у учащихся интерес к проблеме здорового питания.
4. Активизировать познавательную активность учеников в процессе проведения эксперимента.
Форма работы: фронтальная (демонстрационный опыт)
Тип занятия: изучение нового материала
Ведущий метод: объяснительно-иллюстративный
Реактивы и оборудование: молоко, творог, хлеб, мука, 2% спиртовой раствор фенолфталеина, дистиллированная вода, 0,1 М раствор едкого натра; цифровая лаборатория «Архимед», датчик рН, химический стакан, бюретка, конические колбы для титрования,.
План занятия
1. Презентация «Цифровая лаборатория «Архимед»
2. Анкетирование № 1 (Приложение 7)
3. Знакомство учащихся с методикой проведения анализа качества пищевых продуктов без цифровой лаборатории «Архимед».
4. Знакомство учащихся с методикой проведения анализа качества пищевых продуктов с цифровой лабораторией «Архимед».
5. Анкетирование № 2 (Приложении 8)
Ход занятия
Каждый опыт проводится сначала с использованием индикатора (фенолфталеина) – опыт А, а затем с использованием возможностей цифровой лаборатории «Архимед» - опыт Б.
| Смысловые блоки | Основное содержание |
| 1. Мотивация учащихся | 1. Вопрос обеспечения пищей был одним из самых существенных для человека. С развитием техники возможности для увеличения количества производимой пищи постоянно возрастали. Продукты питания расходовались на удовлетворение спроса растущего населения и требовались во всё возрастающем количестве. Хотя основная проблема обеспечения пищей не перестала быть актуальной‚ содержание её изменилось. На сегодняшний день остро встал вопрос о качестве потребляемой нами пищи. Кто из Вас может с уверенностью сказать о том, что употребляет пищу, удовлетворяющую стандартам качества? |
| 2. Изучение нового материала | 2. В настоящее время существуют специальные организации, которые следят за качеством производимых продуктов питания. При этом все эти учреждения используют в своей работе различные методики проведения анализа. На сегодняшнем занятии мы с Вами возьмём на себя роль экспертов качества. В своей работе мы также рассмотрим различные способы выполнения анализа продуктов питания. Мы будем использовать для анализа молоко, творог, хлеб и муку. В нашей работе мы будем исследовать кислотность этих продуктов. Согласно исследованиям Т. Пауль, кислый вкус кислых жидких веществ зависит не от количества кислоты, а от концентрации водородных ионов. Концентрацию ионов водорода называют водородным показателем – рН. рН = - lg [Н+] Величина водородного показателя характеризует реакцию среды: кислую (рН < 7), нейтральную (рН = 7) и щелочную (рН > 7) Водородный показатель и реакция среды могут быть определены с помощью индикаторов (метилоранжа, фенолфталеина, лакмуса), а также, при этом точнее с помощью специальных приборов рН-метров. |
| Анализ качества пищевых продуктов. Анализ кислотности молока | - Молоко содержит в своем составе жиры (в виде эмульсии), белки – казеин, альбумин, глобулин (в виде коллоидного раствора), растворённые в воде азотистые небелковые вещества, соли и молочный сахар – лактозу (формулу на доске).
Процесс скисания молока связан с образованием молочной кислоты (С3Н6О3) в результате молочнокислого брожения, образующейся из лактозы, глюкозы.
Схема на доске:
Лактоза → гидролиз → глюкоза → брожение → молочная кислота
Реакция молочнокислого брожения глюкозы:
С6Н12О6 → 2 СН3 – СН (ОН) – СООН
Определение кислотности молока основано на методе кислотно-основного титрования.
Объяснить суть процесса кислотно-основного титрования (используя схему).
 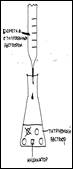  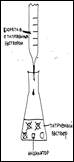 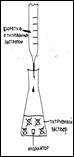 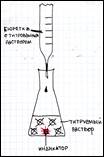 В процессе работы мы определяем какое количество гидроксида натрия пошло на полную нейтрализацию молочной кислоты и по формуле высчитываем кислотность.
В процессе работы мы определяем какое количество гидроксида натрия пошло на полную нейтрализацию молочной кислоты и по формуле высчитываем кислотность.
|
| Опыт №1. Определение кислотности молока. Форма работы: индивидуальная (в группах) | Оборудование и реактивы: молоко пастеризованное и не пастеризованное, 0,1 М раствор гидроксида натрия, бюретка, воронка, колбы для титрованиия, фенолфталеин, цифровая лаборатория «Архимед», насадка – рН-метр, мешалка. А) Ход опыта: В колбу для титрования наливают 10 мл молока, 20 мл дистиллированной воды, 5 капель 2% раствора фенолфталеина. Смесь хорошо перемешивают. Затем по каплям прибавляют 0,1 М раствор едкого натра, фиксируя при этом цвет индикатора (появление розоватой окраски). Б) Настройка параметров измерения «Архимеда»: 1) частота измерений – каждую секунду; 2) число замеров – 1000 Ход опыта: В колбу для титрования наливают 10 мл молока, 20 мл дистиллированной воды, 5 капель 2% раствора фенолфталеина. Смесь хорошо перемешивают при помощи магнитной мешалки. Затем опускают датчик рН и начинают по каплям из бюретки прибавлять 0,1 М раствор едкого натра, при включённой мешалке, до рН 8,2 (по показаниям прибора), фиксируя при этом цвет индикатора (появление розоватой окраски). Полученные данные занести в таблицу №1 .Опыт повторяют 3 раза. |
Таблица №1 - Кислотность молока
| Образец молока | Объём молока, мл | Объём, прилитого раствора NaOH, мл | Среднее значение объёма, прилитого раствора NaOH, мл | Кислотность молока, град |
| Пастеризованное молоко | ||||
| Пастеризованное молоко, образец 1 |
|
| ||
| Пастеризованное молоко, образец 2 | ||||
| Пастеризованное молоко, образец 3 | ||||
| Не пастеризованное молоко | ||||
| Не пастеризованное молоко, образец 1 |
|
| ||
| Не пастеризованное молоко, образец 2 | ||||
| Не пастеризованное молоко, образец 3 | ||||
Результаты измерений: вычислить кислотность пастеризованного и не пастеризованного молока в условных градусах Тёрнера по формуле:
Кислотность молока = V р ( NaOH ) · 10
Свежее молоко имеет 16-18 градусов кислотности по Тёрнеру. Предельная кислотность свежего молока 20 градусов.
Задание.
1. Сделать вывод о свежести использованного молока
2. Чем вызвана кислотность молока, какая кислота образуется при скисании молока? Напишите уравнения реакции образования этой кислоты и её нейтрализации гидроксидом натрия.
Кислоты как продукт кислотного брожения находятся в хлебе в довольно большом количестве. Их содержание колеблется естественно в зависимости от способов изготовления хлеба и особенно брожения теста. Особенно важны молочная и уксусная кислоты, есть следы муравьиной и масляной кислот.
Приготовленный на дрожжах после краткого и быстрого брожения разрыхленный пшеничный хлеб содержит то же количество кислоты, что и мука; оно соответствует количеству содержащихся в последней кислых фосфатов. В хлебе на закваске, особенно в кислом ржаном черном хлебе, кислотность возрастает в зависимости от продолжительности брожения.
Градусом кислотности называется то количество кислоты в 100 г хлебного мякиша, которое требует для своей нейтрализации 1см2 щелочи.
Таким образом, кислотность хлеба обусловлена наличием уксусной и молочной кислоты.
В процессе титрования мы определяем количество щёлочи, которое необходимо для нейтрализации кислот в хлебной вытяжке (процесс связан с изменением окраски индикатора) и по формуле рассчитываем кислотность хлеба.
Оборудование и реактивы: хлебобулочная продукция (хлеб Дарницкий, хлеб пшеничный из сортовой муки, батон, хлеб пшеничный, приготовленном на жидких дрожжах, хлеб пшеничный обойный, хлеб ржаной из сеяной муки), 0,1 М раствор гидроксида натрия, бюретка, воронка, колбы для титрованиия, фенолфталеин, цифровая лаборатория «Архимед», насадка – рН-метр, мешалка.
Ход опыта:
Подготовка к анализу. Образцы разрезают пополам по ширине и от одной половины отрезают кусок (ломоть) массой около 70 г, у которого срезают корки и подкорочный слой общей толщиной 1 см. Для изделий массой менее 200 г берут целые булки, с которых срезают корки слоем приблизительно 1 см. Из кусков приготовленных изделий удаляют все включения (повидло, варенье,, изюм и т.п.), затем их быстро измельчают и перемешивают.
25 г измельченного мякиша отвешивают с погрешностью до 0,05 г. Навеску помещают в сухую бутылку (типа молочной) вместимостью 500 см3, с хорошо пригнанной пробкой. Мерную колбу вместимостью 250 см3 наполняют до метки дистиллированной водой, подогретой до температуры 60 °С. Около 1/4 взятой дистиллированной воды переливают в бутылку с хлебом, который после этого быстро растирают деревянной лопаточкой до получения однородной массы, без заметных комочков нерастертого хлеба.
К полученной смеси прибавляют из мерной колбы всю оставшуюся дистиллированную воду. Бутылку закрывают пробкой и энергично встряхивают в течение 3 мин. После встряхивания дают смеси отстояться в течение 1 мин и отстоявшийся жидкий слой осторожно сливают в сухой стакан через чистое сито или марлю.
А) Ход опыта: Из стакана отбирают пипеткой по 50 см3 раствора в три конические колбы вместимостью по 100-150 см3 каждая. Затем начинают по каплям из бюретки прибавлять 0,1 М раствор едкого натра, фиксируя при этом цвет индикатора (появление розоватой окраски).
Б) Настройка параметров измерения:
1) частота измерений – каждую секунду;
2) число замеров – 1000
Ход опыта: Из стакана отбирают пипеткой по 50 см3 раствора в три конические колбы вместимостью по 100-150 см3 каждая. Затем опускают датчик рН и начинают по каплям из бюретки прибавлять 0,1 М раствор едкого натра, при включённой мешалке, до рН 8,2 (по показаниям прибора), фиксируя при этом цвет индикатора (появление розоватой окраски). Полученные данные занести в таблицу №2. Опыт повторяют 3 раза.
Таблица № 2 - Кислотность хлеба
| Образец хлеба | Объём хлебной вытяжки, мл | Объём, прилитого раствора NaOH, мл | Среднее значение объёма, прилитого раствора NaOH, мл | Кислотность хлеба, град |
| Хлеб пшеничный | ||||
| Образец 1 |
|
| ||
| Образец 2 | ||||
| Образец 3 | ||||
| Хлеб ржаной | ||||
| Образец 1 |
|
| ||
| Образец 2 | ||||
| Образец 3 | ||||
Результаты измерений: вычислить кислотность образцов хлеба по формуле:
Кислотность хлеба = 25·50·4·V/(250·10),
где V – объем 0,1 моль/дм3 раствора гидроксида натрия, см3; 1/10 – приведение 0,1 моль/дм3 раствора гидроксида натрия или гидроксида калия к 1 моль/дм3; 4 – коэффициент, приводящий к 100 г навески; 25 – масса навески испытуемого продукта, г; 250 – объем воды, взятый для извлечения кислот, см3; 50 – объем испытуемого раствора, взятый для титрования, см3.
Задание.
1. Сделать вывод о соответствии кислотности использованного образца хлебобулочной продукции, если известно, что кислотность:
· Хлеба пшеничного из сортовой муки – не более 2 - 4°
· Хлеба пшеничного, приготовленного на жидких дрожжах – 3-5°,
· Хлеба пшеничного обойного – не более 7°,
· Хлеба ржаного из обойной муки – не более 12°,
· Хлеба ржаного из обдирной муки – 11°,
· Хлеба ржаного из сеяной муки – 7°.
2. Чем вызвана кислотность хлеба.
Виды муки:
1. обойная (цельнозерновая) мука - мука грубого помола. Обойная мука содержит большое количество оболочек, поэтому она имеет цвет с сероватым или коричневым оттенком. Размер частиц неоднородный
Хлеб из цельнозерновой муки по праву назван лечебным продуктом против ожирения, сахарного диабета, атеросклероза, пониженной моторики кишечника. Зерновой хлеб эффективно удаляет вредные вещества из организма - соли тяжелых металлов, радиоактивных вещества, ядовитые компоненты, остатки продуктов биологического происхождения, увеличивает продолжительность жизни.
Ученым США удалось доказать, что смертность людей, потребляющих продукты из цельного зерна, снижается на 15-20%. В большинстве западных странах Комитеты Национального Питания рекомендуют взрослым прием 25-35 г диетического пищевого волокна. Съедая один кусочек цельнозернового хлеба, вы получаете 5г клетчатки. Ежедневно включая в свой рацион хлеб из цельнозерновой муки, вы полностью удовлетворяете потребность организма в клетчатке и пищевых волокнах.
2. обдирная мука – состоит в основном из наружных частей зерна. Обдирную муку получают грубым помолом; она содержит больше оболочек, цвет ее белый с серым оттенком, частицы отрубей хорошо заметны.
3. Сеяная мука – состоит в основном из эндосперма зерна с включением 1.2% периферийных его частей, самая полезная, ценная по содержанию белков, углеводов, незаменимых аминокислот, витаминов, минеральных веществ.
Мука высшего сорта вырабатывается из центральных слоев эндосперма; размер ее частиц однородный до 0,05 мм, цвет белый с кремовым оттенком.
Муку 1-го сорта получают из внутренних слоев эндосперма, цвет ее белый с желтоватым оттенком. Размер частиц - до 0,1 мм.
Мука 2-го сорта имеет более грубый помол; цвет белый с сероватым оттенком, частицы более крупные - 0,03-0,20 мм.
Кислотность свежей муки зависит от ее сорта и вида. Она обусловлена содержанием белков (продуктов гидролиза белков), продуктов гидролитического расщепления жира муки (жирных кислот) минеральных кислых фосфорсодержащих веществ (дигидрофосфатов) и органических кислот (молочной, уксусной, щавелевой и др.).
В нормальных условиях кислотность муки достигает 2,5—5,5 °Т. В процессе хранения кислотность муки увеличивается. Это связано главным образом с расщеплением жира муки под влиянием тканевых и микробных ферментов до свободных жирных кислот, с образованием окси- и кетокислот. Так как поверхностные слои зерна характеризуются большим содержанием жира, то
· мука грубого помола имеет более высокую кислотность,
· мука высших сортов – кислотность ниже, чем у муки грубого помола.
· мука низких сортов имеет большую кислотность (т.к. больше жира, фосфора и ферментов)
· мука высших сортов ниже, а потому
· кислотность ее больше, чем муки высших сортов.
Повышение кислотности муки расценивается как признак изменения ее свежести. Нарастание титруемой кислотности муки особенно интенсивно происходит в первые 15—20 дней после помола. При дальнейшем хранении муки кислотность ее возрастает незначительно и очень медленно. Такая мука хранению не подлежит и должна быть срочно реализована.
Анализ качества муки также проводится в специализированных лабораториях качества пищевых продуктов и сырья. Затем проводится анализ соответствия ГОСТам и только после этого делается заключение о качестве этого сырья.
Мукомольная промышленность нашей страны выпускает пять сортовпшеничной муки и три сорта ржаной хлебопекарной муки.
Крупчатка – 10% Сеяная – 63%
Высший сорт – 30% Обдирная – 87%
Первый сорт – 72% Обойная – 95%
Второй сорт – 85%
Обойная – 96%
Оборудование и реактивы: разные сорта (1, 2, 3) и/или виды (пшеничная, ржаная, кукурузная) муки, 0,1 М раствор гидроксида натрия, бюретка, воронка, колбы для титрованиия, фенолфталеин, цифровая лаборатория «Архимед», насадка – рН-метр, мешалка.
А) Ход опыта: В колбу для титрования помещают 5 г муки, затем прибавляют 40 мл воды, 5-6 капель фенолфталеина. Затем начинают приливать (по каплям) 0,1 М раствор едкого натра до появления розового окрашивания.
Б) Настройка параметров измерения:
1) частота измерений – каждую секунду;
2) число замеров – 1000
Ход опыта : В колбу для титрования помещают 5 г муки, затем прибавляют 40 мл воды, 5-6 капель фенолфталеина. Затем опускают датчик рН, начинают регистрацию данных и приливание (по каплям) 0,1 М раствор едкого натра при включённой мешалки до рН 8,2. Опыт повторяют 3 раза. Полученные данные занести в таблицу №3.
Таблица № 3 - Кислотность муки
| Образец муки | Масса муки в образце, г | Объём, прилитого раствора NaOH, мл | Среднее значение объёма, прилитого раствора NaOH, мл | Кислотность муки, град |
| Мука пшеничная | ||||
| Образец 1 |
|
| ||
| Образец 2 | ||||
| Образец 3 | ||||
| Мука ржаная | ||||
| Образец 1 |
|
| ||
| Образец 2 | ||||
| Образец 3 | ||||
| Мука кукурузная | ||||
| Образец 1 |
|
| ||
| Образец 2 | ||||
| Образец 3 | ||||
Результаты измерений: вычислить кислотность образцов муки по формуле:
Кислотность муки = V ( NaOH ) · 20 / 10
Задание:
Сделать вывод о различии в кислотности муки разного вида (пшеничной, ржаной, кукурузной)
Кислотность творога, прежде всего, свидетельствует о принадлежности к тому или иному сорту.
Так известно, что (запись на доске):
· Высший сорт творога имеет кислотность не более 200
· 1-й творога имеет кислотность не более 220,
· 2-й сорт творога имеет кислотность не выше 240 градусов.
Оборудование и реактивы: разные виды творога, 0,1 М раствор гидроксида натрия, бюретка, воронка, колбы для титрованиия, фенолфталеин, цифровая лаборатория «Архимед», насадка – рН-метр, мешалка.
А) Ход опыта: В колбу для титрования помещают 10 г творога (очистить от изюма и др. включений) и небольшими порциями приливают 20 мл воды, нагретой до 30-40 0С. Творог тщательно перемешивают стеклянной палочкой. Прибавляют 5 капель спиртового раствора фенолфталеина. Начинают титрование 0,1 М раствором едкого натра до появления розовой окраски.
Б) Настройка параметров измерения:
1) частота измерений – каждую секунду;
2) число замеров – 1000
Ход опыта : В колбу для титрования помещают 10 г творога (очистить от изюма и др. включений) и небольшими порциями приливают 20 мл воды, нагретой до 30-40 0С. Творог тщательно перемешивают стеклянной палочкой. Прибавляют 5 капель спиртового раствора фенолфталеина. Помещают в раствор датчик рН, начинают регистрацию данных, одновременно прибавляя 0,1 н. раствор гидроксида натрия до рН 8,2 (появления розовой окраски). Опыт повторяют 3 раза.
Полученные данные занести в таблицу №4.
Таблица № 4. Кислотность творога
| Образец творога | Масса творога в образце, г | Объём, прилитого раствора NaOH, мл | Среднее значение объёма, прилитого раствора NaOH, мл | Кислотность творога, град |
| Образец творога 1 | ||||
| 1 | ||||
| 2 | ||||
| 3 | ||||
| Образец творога 2 | ||||
| 1 | ||||
| 2 | ||||
| 3 | ||||
Результаты измерений: вычислить кислотность образцов творога по формуле:
Кислотность творога = V ( NaOH ) · 20
Задание.
1. Сделать вывод о принадлежности исследованного творога к определённому сорту, по записи, приведённой выше
o Какой метод мы использовали для определения качества продуктов питания? (Метод кислотно-основного титрования)
Оформить работу
· Заполнить таблицы
· Выполнить задания
Приложение 7. Анкета для учащихся перед выполнением эксперимента
1. Часто ли с Вами на уроках проводят химический эксперимент?
1) Да
2) Нет
2. Испытываете ли Вы сложности при выполнение практических, лабораторных работ?
1) Да
2) Нет
3. Знаете ли, Вы, какие реакции относятся к реакциям нейтрализации?
1) Да
2) Нет
4. Знаете ли Вы, что такое водородный показатель?
1) Да
2) Нет
5. Знакома ли Вам методика титрования растворов?
1) Да
2) Нет
6. Знаете ли Вы что такое индикаторы? Работали ли Вы с ними на уроках химии?
1) Да
2) Нет
7. Имеете ли Вы опыт работы с цифровыми лабораториями?
1) Да
2) Нет
Благодарим за участие в исследовании!
Приложение 8. Анкета для учащихся после выполнения работы
1. Задумывались ли Вы о качестве продуктов, которые употребляете?
1) Да
2) Нет
2. Считаете ли Вы что правильно и рационально питаетесь?
1) Да
2) Нет
3. Получили ли Вы новые знания по химии на сегодняшнем факультативе?
1) Да
2) Нет
4. Насколько полезными эти знания оказались для Вас?
1) Полезные
2) Очень полезные
3) Вовсе не полезные
5. Знаете ли Вы, какие реакции относятся к реакциям нейтрализации?
1) Да, это знание я получил на уроках химии
2) Да, но сегодняшняя работа позволила закрепить теоретический материал на практике
3) Нет
6. Знаете ли, Вы, что такое водородный показатель?
1) Да, это знание я получил на уроках химии
2) Да, но сегодняшняя работа позволила закрепить теорию на практике
3) Да, я узнал это при проведении работы сегодня
4) Нет
7. Знаете ли Вы, что такое титрование?
1) Да
2) Нет
8. Понравилась ли Вам работа с цифровой лабораторией «Архимед»? Почему?
1) Да, так как ______________________________________________
2) Нет, так как ____________________________________________
9. Помогает ли предварительно проведённая презентация о цифровой лаборатории «Архимед» для использования её на элективном курсе
1) Да, презентация даёт полную информацию для работы с цифровой лаборатории «Архимед»
2) Да, но по моему мнению ________________________________
3) Нет
10. Доступна ли для Вас техника работы с цифровой лабораторией «Архимед»?
1) Да, я смогу использовать цифровую лабораторию «Архимед» в самостоятельной исследовательской деятельности
2) Да, я смогу использовать цифровую лабораторию «Архимед», но только при руководстве учителя
3) Нет
11. Позволяет ли использование цифровой лаборатории «Архимед» получать данные, недоступные в традиционных учебных экспериментах
1) Да
2) Нет
12. Какой эксперимент был наиболее наглядным для понимания Вами учебного материала?
1) С цифровой лабораторией «Архимед»
2) Без неё
13. Хотели бы Вы, чтобы на занятиях элективного курса использовалась цифровая лаборатория «Архимед»? Почему?
1) Да, так как _______________________________________________
2) Нет, так как ______________________________________________
Благодарим за участие в исследовании!
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ
Пензенский государственный педагогический университет им. В.Г. Белинского
Факультет естественно-географический
Кафедра химии и теории и методики обучения химии
ДИПЛОМНАЯ РАБОТА
Использование цифровой лаборатории «Архимед» в школьном химическом эксперименте
Студент Макарова О.Е.
Руководитель Фирстова Н.В.
К защите допустить.
Протокол № от «___» ____2009 г.
Зав. Кафедрой Керимов Э.Ю.
Пенза, 2009
Содержание
Введение
Глава 1. Обзор литературы
1.1 Информатизация системы образования
1.2 Информатизация химического образования
1.3 Цифровая лаборатория «Архимед» – новое поколение школьных естественно-научных лабораторий
Дата: 2019-07-24, просмотров: 413.