Наприклад, треба встановити чутливість реакції
Fe3+ + 3SCN ↔ Fe(SCN)3.
Для цього готують розчин, в 500 мл якого міститься 1г-іон заліза. Відомо, що при розведенні в 20 разів в 1 краплі об’ємом 0,02 мл ще можна виявити іони заліза (ІІІ). Граничне розведення суть
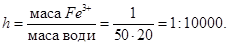
Знаходимо відкриваний мінімум: 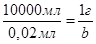 , звідси
, звідси
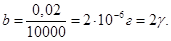 |
Селективність реакції – її вибірковість до тих чи інших речовин або іонів. Існують реакції, проведенню яких не заважають сторонні іони. Так, іони амонію можна виявити лугом.
Ця реакція, та їй подібні називаються специфічними. Високоспецифічних реакцій відомо надзвичайно мало.
№ 13
Умови виконання аналітичних реакцій. Приклади реакцій, що проходять на холоді і при нагріванні розчину
Реакції проводять при нагріванні чи охолодженні лише в тих випадках, коли нагрівання чи охолодження сприяє проходженню прямої реакції до кінця, прискорює її.
ІІ група – аніони, солі срібла яких важкорозчинні у воді і у розведеній азотній кислоті;
ІІІ група – не утворюють важкорозчинних солей з іонами барію і срібла.
Аніони SO42–, PO43–, CO32– належать до І групи;
″Cl‾, Br‾, I‾ ″ до ІІ групи;
″NO2‾, NO3‾ ″ до ІІІ групи.
Рівняння реакцій:
1) Na2SO4 + BaCl2 ↔ BaSO4↓ + 2NaCl
SO42– + Ba2+ ↔ BaSO4↓
Білий кристалічний осад, практично нерозчинний у воді і кислотах.
2) KI + AgNO3 ↔ KNO3 + AgI↓
I‾ + Ag+ ↔ AgI↓
Осад жовтого кольору, розчинний в тіосульфаті натрію і ціаніді калію, але нерозчинний в гідроксиді амонію.
3) На аніон NO2‾ груповий реактив відсутній через належність вказаного аніона до ІІІ аналітичної групи.
№ 62
Принцип аналітичної класифікації аніонів. До яких аналітичних груп належать аніони SO42–, PO43–, CO32–,Cl‾, Br‾, I‾, NO2‾, NO3‾ ? Написати молекулярні та іонні рівняння реакцій дії групових реактивів, якщо в розчині присутні такі аніони: PO43–, Cl‾, NO3‾. Зазначити колір осадів, розчинність
Поділ аніонів на аналітичні групи оснований на різній розчинності солей барію і солей срібла:
І група – аніони, солі барію яких важкорозчинні у воді;
Зазначити колір осадів, розчинність
Поділ аніонів на аналітичні групи оснований на різній розчинності солей барію і солей срібла:
І група – аніони, солі барію яких важкорозчинні у воді;
Титрування (рТ)
метиловий фіолетовий (І перехід) 1
тимоловий синій (І перехід) 2
метиловий фіолетовий (ІІ перехід) 2,5
метилоранж 4
бромфенол синій 4
метиловий червоний 5
лакмус 7
нейтральний червоний 7
феноловий червоний 8
тимоловий синій (ІІ перехід) 9
фенолфталеїн 9
тимолфталеїн 10
Інтервал рН, в межах якого відбувається помітна для людського ока зміна забарвлення індикатора, називають інтервалом переходу індикатора.
У межах інтервалу переходу індикатора є значення рН, при якому спостерігається найбільш помітна для людського ока зміна кольору індикатора. Це значення рН називають показникомтитрування індикатора (позначають рТ).
№ 129
Дати мотивовану відповідь, для чого застосовують індикатори та як їх вибирають
Індикатори в титрометричному аналізі і в його підрозділі – методі нейтралізації використовують для встановлення точки еквівалентності за різкою зміною кольору індикатора, яка повинна спостерігатись поблизу точки еквівалентності і в самій цій точці. Однак, таким методом встановити точку еквівалентності можна лише з певною точністю, так як, по-перше, показник титрування рТ вибраного індикатора і рН розчину в точці еквівалентності можуть суттєво відрізнятись; по-друге, не всякий індикатор різко змінює колір у вказаній точці.
Умовою правильного вибору індикатора, а значить, і умовою найбільш точного визначення точки еквівалентності, є те, щоб різниця значень рТ індикатора і рН розчину в точці еквівалентності була якнайменшою. При цьому показник титрування індикатора знаходять з довідників, а рН розчину в точці еквівалентності обчислюють за рівнянням реакції.
№ 130
За допомогою кривих титрування дати обґрунтовану відповідь, де точність титрування буде найвищою:
а) при титруванні сильної кислоти лугом;
б) при титруванні слабкої кислоти лугом?
Чи можна титрувати слабку кислоту слабкою основою?
а) поглянемо на криву титрування сильної кислоти лугом
(0,1 н розчин HCl 0,1 н розчином NaOH):
 | |||
 | |||
 рН 14
рН 14
 7
7

 0
0
0 40 80 120 160 200
об’єм NaOH, мл
З малюнка видно, що при титруванні сильної кислоти лугом біля точки еквівалентності спостерігається різка зміна рН розчину. Помилка титрування в даному випадку становить 0,1%.
б) тепер поглянемо на криву титрування слабкої кислоти лугом
(0,1 н розчину оцтової кислоти 0,1 н розчином NaOH):


 рН 14
рН 14
 7
7
 0
0
Об’єм NaOH , мл
Характер кривої показує, що при титруванні слабкої кислоти лугом немає різкої зміни рН біля точки еквівалентності. У цьому випадку помилка титрування може сягати 10%.
Таким чином, точність титрування буде найвищою у випадку титрування сильної кислоти сильною основою.
Титрувати слабку кислоту слабкою основою практично неможливо тому що при зміні рН на ± 1 кислота буде недотитрована приблизно на 10%, потім приблизно на стільки ж буде перетитрована.
№ 131
Дати загальну характеристику методу перманганатометрії
Перманганатометрія – один з методів об’ємного аналізу (підгрупа методів окислення-відновлення), в якому речовину визначають титруванням розчином перманганату калію.
У кислому середовищі основна реакція методу йде за рівнянням:
MnO4‾ + 8H+ + 5e‾ → Mn2+ + 4H2O.
У слабокислих або лужних розчинах перманганат відновлюється до Mn4+, який випадає у вигляді нерозчинного осаду двоокису марганцю:
MnO4‾ + 4H+ + 3e‾ → MnO2↓ + 2H2O
Метод застосовують для визначення багатьох відновників, серед них
Fe2+, Sn2+, Mn2+, V4+, U4+.
При титруванні розчином перманганату калію звичайно не застосовують ніяких спеціальних індикаторів. Точку еквівалентності встановлюють за рожевим забарвленням, яке виникає від невеликого надлишку добавленого розчину перманганату. Отже, індикатором є сам робочий розчин.
Оскільки препарат KMnO4 не має властивостей вихідної речовини через значну кількість домішок двоокису марганцю, нормальність розчину перманганату калію встановлюють за щавлевою кислотою.
№ 132
Титровані розчини методу перманганатометрії. У чому полягає різниця приготування робочого титрованого розчину КMnO4 та стандартного розчину щавлевої кислоти?
Робочим розчином методу перманганатометрії є розчин перманганату калію. Після встановлення нормальності цього розчину за щавлевою кислотою він має назву титрований робочий розчин. Різниця приготування титрованого робочого розчину КMnO4 та стандартного розчину щавлевої кислоти полягає в тому, що, по-перше, препарат перманганату калію, на відміну від препарату щавлевої кислоти, не містить кристалізаційної води (яку останній з часом втрачає), отже його не треба перекристалізовувати перед розчиненням; по-друге, приготувавши стандартний розчин щавлевої кислоти, ми будемо знати його нормальність з достатньою точністю, тоді як нормальність приготовленого робочого розчину КMnO4 відома лише приблизно і встановити її буде необхідно за тим же розчином щавлевої кислоти.
№ 133
Дати мотивовану відповідь, чи можна приготувати титрований розчин KMnO4, виходячи з точної наважки, без встановлення його концентрації за вихідною речовиною
НЕ МОЖНА. Тому, що KMnO4 не має властивостей вихідної речовини. Препарат завжди має більшу або меншу кількість домішок двоокису марганцю, позбутися яких важко. Крім того, концентрація розчину KMnO4 з часом змінюється внаслідок відновлення під впливом світла, невеликих кількостей органічних речовин, які потрапляють у розчин з пилом, тощо.
Точну концентрацію розчину KMnO4 можна встановити за щавелевою кислотою.
№ 134
Розрахувати наважку КMnO4, необхідну для приготування 1,0 л 0,05 н розчину. Зазначити основні етапи приготування розчину КMnO4
Зрівняння реакції
MnO4‾ + 8Н+ + 5е– → Mn2+ + 4H2O
бачимо, що еквівалент КMnO4 рівний 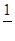 його молярної маси. Отже, для того, щоб приготувати 1 л 0,05 н розчину, треба відважити на технічних терезах
його молярної маси. Отже, для того, щоб приготувати 1 л 0,05 н розчину, треба відважити на технічних терезах
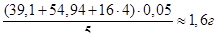 препарату КMnO4.
препарату КMnO4.
Наважку переносять у вимірювальну колбу і заливають приблизно на ½ дистильованою водою, старанно перемішують до повного розчинення кристалів. Слідкують, щоб кристали КMnO4 розчинились повністю, оскільки процес дуже повільний. Потім доводять об’єм розчину до 1 л. Не раніше, як через 10–12 діб нормальність отриманого розчину встановлюють за щавлевою кислотою.
№ 135
Скласти рівняння реакції, яка відбувається при встановленні нормальності робочого розчину КMnO4 за вихідною речовиною. Зазначити хід та умови цього визначення
Рівняння реакції:
2КMnO4 + 5H2С2O4 + 3H2SO4 → К2SO4 + 2MnSO4 + 10CO2↑ + 8H2O
2 MnO4‾ + 8H+ + 5е– → Mn2+ + 4H2O
5  C2O42– → 2е– + 2CO2↑
C2O42– → 2е– + 2CO2↑
2MnO4‾ + 5C2O42– + 16H+ → 2Mn2+ + 10CO2↑ + 8H2O
Хід визначення: піпеткою відбирають 20 або 25 мл 0,1 н розчину щавлевої кислоти і переносять у конічну колбу ємністю 200 мл. Добавляють 15–20 мл розчину сірчаної кислоти (1:4) і нагрівають до температури 80–90°С. При цьому стежать, щоб стінки колби вище рівня рідини не перегрівались, оскільки це може призвести до термічного розкладу щавлевої кислоти:
t°
H2С2O4 → CO2↑ + CO↑ + H2O
До гарячого розчину щавлевої кислоти з бюретки добавляють кілька крапель розчину перманганату калію і чекають, доки зникне рожеве забарвлення. Потім додають наступні порції розчину перманганату, щоразу чекаючи зникнення рожевого забарвлення. Після додавання 2–3 мл розчину перманганату титрування йде швидше і робочий розчин можна добавляти більшими порціями. Ознакою кінця титрування є забарвлення розчину в рожевий колір, який не зникає тривалий час. Визначення треба повторити з новими порціями розчину щавлевої кислоти ще 2–3 рази, при цьому розходження в об’ємах між окремими паралельними пробами не має перевищувати 0,02–0,03 мл. Відлічувати об’єм розчину перманганату, витраченого на титрування, зручно за верхнім меніском на бюретці. Нормальність розчину перманганату обчислюють за формулою:
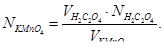
№ 136
Як прискорити реакцію, що є основою визначення концентрації розчину KMnO4? Що є каталізатором?
Реакція між KMnO4 і щавлевою кислотою безпосередньо не йде або йде дуже повільно. Навпаки, швидкість реакції між KMnO4 і іонами марганцю(ІІ), в результаті якої утворюється двоокис марганцю, досить велика. Найшвидше взаємодіють MnO2 та H2C2O4.
Досліди показують, що каталізатором в даній реакції є іони марганцю(ІІ). Збільшення їх концентрації значно прискорює реакцію.
№ 137
Чому не потрібен індикатор при перманганатометричних визначеннях? Як встановлюють точку еквівалентності при титруванні розчином перманганату калію?
Тому що в даному випадку індикатором є сам робочийрозчин KMnO 4. Точку еквівалентності встановлюють за рожевим забарвленням, яке виникає від невеликого надлишку добавленого розчину KMnO4. Помилку титрування при такому способі визначення точки еквівалентності легко встановити за допомогою сліпої проби.
№ 138
Література
1) І.В. П’ятницький “Аналітична хімія”, Київ, Вища школа, 1969;
2) И. Шапиро, В. Шапиро “Аналитическая химия”, М.,Наука, 1978
Наприклад, треба встановити чутливість реакції
Fe3+ + 3SCN ↔ Fe(SCN)3.
Для цього готують розчин, в 500 мл якого міститься 1г-іон заліза. Відомо, що при розведенні в 20 разів в 1 краплі об’ємом 0,02 мл ще можна виявити іони заліза (ІІІ). Граничне розведення суть
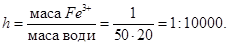
Знаходимо відкриваний мінімум: 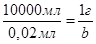 , звідси
, звідси
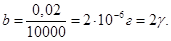 |
Селективність реакції – її вибірковість до тих чи інших речовин або іонів. Існують реакції, проведенню яких не заважають сторонні іони. Так, іони амонію можна виявити лугом.
Ця реакція, та їй подібні називаються специфічними. Високоспецифічних реакцій відомо надзвичайно мало.
№ 13
Умови виконання аналітичних реакцій. Приклади реакцій, що проходять на холоді і при нагріванні розчину
Реакції проводять при нагріванні чи охолодженні лише в тих випадках, коли нагрівання чи охолодження сприяє проходженню прямої реакції до кінця, прискорює її.
Дата: 2019-05-29, просмотров: 347.