Министерство здравоохранения Российской Федерации
САНКТ-ПЕТЕРБУРГСКИЙ ФАРМАЦЕВТИЧЕСКИЙ техникум
МЕТОДИЧЕСКОЕ ПОСОБИЕ
К практическим занятиям по фармацевтической химии
Часть III
Методическое пособие предназначено для студентов, изучающих фармацевтическую химию по программе, составленной по специальности 33.0201 «Фармация» базового уровня среднего профессионального образования.
В практикум включены внутриаптечный контроль преимущественно асептически приготовленных лекарственных средств.
К каждому занятию приведены цели и задачи работы, вопросы для самоподготовки, материальное обеспечение, содержание работы, общие указания и образцы составления алгоритмов внутриаптечного контроля различных видов ап течной продукции, а также справочный материал для самостоятельной работы студентов.
ГЕТЕРОЦИКЛИЧЕСКИЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА
ЗАНЯТИЕ 1
Внутриаптечный контроль раствора фурацилина 0,02%- 100мл
Время занятия 90 минут
Вопросы для самоподготовки:
Студенты должны знать
• Русское, латинское и химическое название фурацилина, свойства, подлинность, доброкачественность препарата (испытание на чистоту) и методы количественного определения, применение и хранение фурацилина
• Внутриаптечный контроль раствора фурацилина
• Фотоколориметрический (ФЭК) метод анализа, методику определения, формулы расчета содержания вещества в анализируемом растворе.
Студенты должны выполнить
• Ответить на вопросы индивидуальных письменных заданий
• Провести ВАК раствора фурацилина, определить концентрацию методом ФЭК, по результатам определения сделать заключение о качестве предложенной лекарственной формы
• Резушльтаты анализа оформит в журнале провизора-аналитика
Анализ раствора фурацилина 0,02% - 100мл
Rp Sol Nitrofurali 0,02% 100ml
D.S. для полоскания горла
Свойства.
Прозрачная зеленовато-желтого цвета жидкость без запаха. Без механических включений.
Подлинность
1. К исследуемому раствору прибавляют раствор щелочи, появляется оранжевое окрашивание.
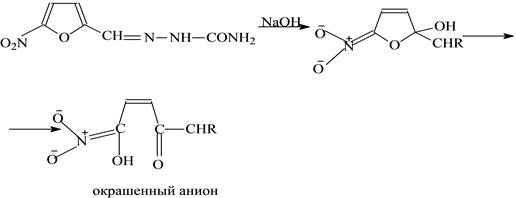
Количественное определение.
Метод фотоколориметрии
Этот метод основан на определении степени поглощения света окрашенными растворами. Для выполнения определения этим методом используют фотоэлектроколориметры (ФЭК), которые позволяют провести анализ с точностью 1-2 отн.%%.
Основными частями ФЭК являются : источник излучения, светофильтр, фотоэлемент, кюветы.
В качестве источника излучения испроьзуют лампы накаливания, обеспечивающие работу в видимой области спектра.
Для увеличения чувствительности и точности фотометрического определения используют поглощение не смешанного излучения (белый свет), а лишь тех лучей, которые максимально поглощаются окрашенным раствором. Для того, чтобы из смешанного излучения выделить лучи определенных длин волн, на пути световых потоков перед поглощающим раствором помещают избирательные поглотители света – светофильтры.
Для измерения оптической плотности определяемый раствор выливают в специальную стеклянную посуду – кюветы. Выбор кювет зависит от интенсивности окраски раствора: чем интенсивнее окраска раствора, тем тоньше кювета.
Фотоэлемент преобразует световую энергию, прошедшую через определяемый раствор, в электрическую.
Отношение интенсивности потока излучения, прошедшего через исследуемый раствор, к интенсивности первоначального потока излучения называется пропусканием (Т)
I0 I , где
I0 - интенсивность падающего монохроматческого излучения
I - интенсивность прошедшего через исследуемый раствор монохроматического излучения
Оптическая плотность (А) – логарифм обратной величины пропускания
А =lg 1
Т
Шкала прибора (ФЭК) проградуирована в единицах оптической плотности (А) (нижняя часть) и в единицах пропускания (Т) (верхняя часть). Жанная работа основана на определении оптической плотности (А) и будет использоваться нижняя часть шкалы.
Зависимость интенсивности светового потока, который проходит через раствор, от толщины слоя исследуемого раствора и концентрации растворенного вещества выражается объединенным законом Бугера- Ламберта- Бера: оптическая плотность раствора (А) прямо пропорциональна концентрации окрашенного раствора (с) и толщи не слоя этого раствора (l):
A = ἑ×l×c
ἑ - коэффициент поглощения света (постоянная величина для каждого окрашенного вещества, зависит от его природы).
Концентрацию исследуемых веществ можно определить различными способами:
• Путем сравнения оптических плотностей стандартного и исследуемого раствора
В этом случае в две пробирки вносят одинаковые объёмы стандартного и исследуемого растворов, добавляют одинаковое количество реактивов. Измеряют оптическую плотность при одинаковой толщине слоя. Концентрацию исследуемого раствора вычисляют по формуле:
Сан. = Аан.×Сст , где
Аст
Сст концентрация стандартного раствора
Сан концентрация исследуемого раствора
Аан оптическая плотность исследуемого раствора
Аст оптическая плоьность стандартного раствора
• Путем определения концентрации окрашенного вещества по калибровочному графику
Готовят серию окрашенных стандартных растворов с известной концентрацией (5-10 образцов), измеряют величины их оптических плотностей и строят график зависимости концентоасии от оптической плотности.
А
С
С исследуемым раствором проводят операции, аналогичные стандартным растворам. Определяют оптическую плотность исследуемого раствора и по графику определяют концентрацию. Калибровочную прямую периодически проверяют.
Методика количественного определения фурацилина в растворе.
К 0,5мл исследуемого раствора фурацилина прибавляют 7,5 мл воды и 2 мл 0,1 моль/л раствора гидроксида натрия. Перемешивают.
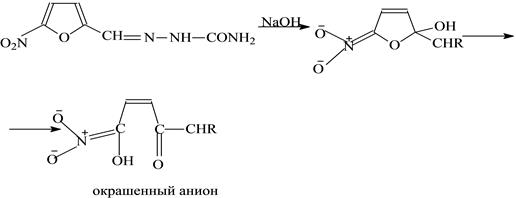
Максимальная величина оптической плотности реакционной смеси устанавливается через 15 минут и не изменяется в течение часа. Поэтому через 15-20 минут исследуемый раствор выливают в кювету с толщиной слоя 0,5 см и измеряют оптическую плотность со светофильтром 450нм (А1). Во вторую кювету такой же толщины помещают раствор сравнения – воду.
Далее определяют оптическую плотность эталонного раствора(А2). Раствор сравнения – вода. Для приготовления эталонного раствора берут 0,5мл раствора с точно известной концентрацией (0,02%), прибавляют 7,5 мл воды и 2 мл 0,1 моль/л раствора гидроксида натрия. Перемешивают. Проводят определение оптической плотности через 15-20 минут.
Содержание фурацилина в граммах вычисляют по формуле
m = 0,0002×V×A1
V1×A2 , где
A1 – оптическая плотность исследуемого раствора
A2 – оптическая плотность стандартного раствора
0,0002 – содержание фурацилина в граммах в 1 мл стандартного раствора
V – общий объём раствора
V1- объём раствора, взятый для анализа.
Доп. откл. -?
Сделайте заключение о качестве анализируемого раствора
Составьте самостоятельно алгоритм внутриаптечного контроля раствора фурацилина.
| АО «Петербургские аптеки» Аптека № 116 г. Санкт Петербург ул. Типанова д.3 Гр. Смирнову С.Т. 60лет рец. № 10291 |
| Н А Р У Ж Н О Е |
| Раствор нитрофурала (Фурацилина) 0,2% 100мл Для полоскания горла Дата приготовления…………. Годен до………. Цена…….. Хранить в прохладном темном месте Хранить в недоступном для детей месте |
ЗАНЯТИЕ 2
Производные пиразола
Фармакопейный анализ анальгина.
Исследовательская задача на производные пиразола
Задачи
1. Коррекция и систематизация знаний по теме "производные пиразола"
Продолжительность занятия
2 академических часа ( 90 минут )
Вопросы для самоподготовки
Материальное обеспечение
Реактивы и растворители
• разведенная кислота хлористоводородная
• 0,01 моль/л раствор кислоты хлористоводородной
• 0,1 моль/л раствор йодата калия
• раствор хлорида железа (III)
• спирт
Титрованные растворы и реактивы
• 0,1 моль/л раствор йода
Посуда, приборы,оборудование
• титровальная установка
• весы аналитические
• весы ручные и разновес
• колба для титрования
• мерные цилиндры на 10 мл
• пробирки
Analginum.
1 фенил 2,3диметил метиламинопиразолон- 5- N-метансульфат натрия
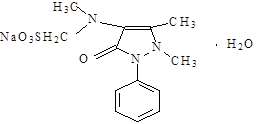
Свойства
Белый или белый с едва заметным желтоватым оттенком крупноигольчатый кристаллический порошок без запаха, горьковатого вкуса. В присутствии влаги быстро разлагается. Водные растворы при стоянии желтеют.
Растворимость
Подлинность
Задачи
Русские, латинские, химические названия; получение, свойства, подлинность, испытание на чистоту, количественное определение, применение и хранение барбитала, фенобарбитала, барбитала натрия, этаминала натрия, тиамина хлорида и тиамина бромида.
Материальное обеспечение
Реактивы
• - кислота хлористоводородная
• - 1% спиртовой раствор нитрата кобальта
• - резорцин ( кристаллический )
• - раствор гидроксида аммония
• - спирт этиловый
Титрованные растворы и индикаторы
• 0,1 моль/л раствор натрия гидроксида;
• фенолфталеин.
Посуди, приборы, оборудование:
• титровальная установка;
• микробюрстка;
• ручные вссочки и разновес;
• колба для титрования;
• пробирки.
Rp: Phenobarbitali 0,05
Sacchari 0,2 M.f.pulv.
D.t.d. № 6
Свойства
Подлинность
• На фенобарбитал
• К 0,05 г порошка прибавляют 10 капель 95% спирта, 5 капель 1 °/1 спиртового раствора нитрата кобальта и 1-2 капли водно-спиртового раствора гидроксида аммония. Появляется фиолетовое окрашивание.
• реакция с сульфатом меди в присутствии карбонатного буфера. Образуется осадок бледно-сиреневого цвета.
• На сахар
• К 0,02 г порошка прибавляют 1-2 мл хлористоводородной кислоты несколько кристаллов резорцина и кипятят 1 минуту. Появляется красное окрашивание.
Количественное определение
Хранение: под замком
ВРД 0,2
ВСД 0,5
| АО «Петербургские аптеки» Аптека № 116 г. Санкт Петербург ул. Типанова д.3
Гр. Сорокиной Н.И. 65лет рец. № 4191
| |
| В Н У Т Р Е Н Н Е Е | |
| порошки | Фенобарбитала 0,05 Сахара 0,2 Дата……………. Годен до………. Цена……….. Хранить в недоступном для детей месте Хранить в прохладном темном месте |
ЗАНЯТИЕ 7
ПРОИЗВОДНЫЕ ТРОПАНА.
Материальное обеспечение
Реактивы и растворители:
• кислота азотная;
• раствор бария хлорида;
• раствор серебра нитрата;
• кислота уксусная;
• спирт;
• хлороформ.
Титрованные растворы и индикаторы:
• 0,05 моль/л раствор натрия гидроксида;
• 0,05 моль/л раствор серебра нитрата;
• фенолфталеин;
• бромфеноловый синий.
Посуда, приборы, оборудование:
• титровальная установка;
• микробюретка;
• пипетка 1 мл;
• склянка для титрования;
• глазные пипетки;
• пробирки.
Кр: Solutionis Atropini sulfatis 1%— 10ml
Slerilisetur!
Состав
Атропина сульфата 0,1 г
Натрия хлорида 0,08г
Воды очищенной 10 мл
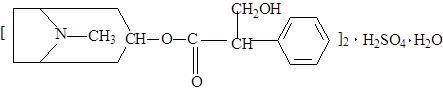
Свойства
Бесцветная прозрачная жидкость
Подлинность
1. На основание атропина.
Реакция Витали-Морена
К 5 каплям расчтвора прибавляют несколько капель конц. азотной кислоты и выпаривают на водяной бане досуха. К желтоватому остатку после охлаждения прибавляют по 3 капли спиртового раствора едкого калия и ацетона. Появляется фиолетовое окрашивание, исчезающее при стоянии.
Под влиянием нагревания с азотной кислотой происходит гидролиз основания атропина, а затем нитрования троповой кислоты. При добавлении едкого калия появляется фиолетовое окрашивание вследствие образования хиноидной структуры.
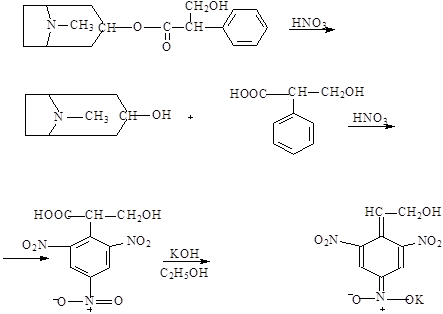
• для доказательсва серной кислоты к 2 каплям раствора прибавляют 2 капля раствора хлорида бария. Образуется белый кристаллический осадок, нерастворимый в кислотах и щелочах.
H2SO4 + BaCl2 = BaSO4 + 2HCl
• На СГ
K 5 каплям раствора прибавляют по 1 капле азотной кислоты и раствоpa нитрата серебра. Наблюдают выделение белого творожистого осадка, не растворимого в азотной кислоте.
СГ + AgN03 —» AgCl + NO3-
Количественное определение
/. Количественное определение атропина сульфата
Моль/л
mNaCl = V*K*T* A
навеска
ДОП.ОТКЛ = ? Vор = ?
| АО «Петербургские аптеки» Аптека № 116 г. Санкт Петербург ул. Типанова д.3 Гр. Рыжовой Н.Т. 25лет рец. № 4191 |
| Г Л А З Н Ы Е К А П Л И |
| Раствор атропина сульфата 1% 10 мл По 2 ткапли в оба глаза на ночь Дата приготовления……….годен до……. Цена…………. Хранить в прохладном темном месте Хранить в недоступном для детей месте |
ЗАНЯТИЕ 8
Задачи
Продолжительность занятия
2 академических часа (90 минут).
Вопросы для самоподготовки
• Составьте алгоритм внутриаптечного контроля внутриаптечной заготовки порошков с папаверином гидрохлоридом.
• Приказ М3 РФ № 751 об анализе внутриаптечной заготовок
• Химический контроль папаверина гидрохлорида. Расчеты. Оформление результатов контроля.
Материальное обеспечение
а) Реактивы и растворители:
• кислота азотная концентрированная; кислота азотная;
• кислота серная концентрированная;
• раствор гидроксида натрия;
• кислота хлористоводородная;
• раствор гидроксида аммония;
• реактив Марки;
• раствор серебра нитрата;
• резорцин (кристаллический);
• раствор кобальта нитрата;
• спирт этиловый.
б)Титрованные растворы и индикаторы:
• 0,1 моль/л раствор натрия гидроксида;
• фенолфталеин.
в)Посуда, приборы, оборудование:
• титровальная установка;
• микробюретка;
• ручные весочки и разновес;
• склянка для титрования;
• фарфоровая чашка или часовое стекло;
• водяная баня
Свойства
ПОДЛИННОСТЬ
На основание папаверина
На сахар
Моль/л
Папаверина гидрохлорида 2,0
Сахара 20.0
_____________________________________
0,22x100 m общ =22,0
№ анализа:
Дозы не превышены.
• Органолептический контроль
Микстура
ЗАНЯТИЯ 11
ПРОИЗВОДНЫЕ ИЗОАЛЛОКСАЗИНА.
ВНУТРИАПТЕЧНЫЙ КОНТРОЛЬ ВНУТРИАПТЕЧНОЙ ЗАГОТОВКИ» ВИТАМИННЫХ ГЛАЗНЫХ КАПЕЛЬ № 10
Задачи
• Коррекция и совершенствование знаний по теме «Производные изо- аллоксазина».
• Освоить внутриаптечный контроль внутриаптечной заготовки вита- минных глазных капель.
• Освоить химический контроль многокомпонентных глазных капель с учетом их взаимного влияния на анализ друг друга.
Продолжительность занятия
2 академических часа (90 минут).
Вопросы для самоподготовки.
• Составьте алгоритм внутриаптечного контроля внутриаптечной заготовки витаминных глазных капель.
• Химический контроль многокомпонеитых глазных капель. Влияние компонентов смеси на анализ друг друга. Расчеты. Оформление результата контроля.
Материальное обеспечение
реактивы и растворители:
• кислота концентрированная серная;
• paствор ацетата свинца;
• кислота разведенная уксусная;
• раствор гидроксида аммония;
• раствор серебра нитрата;
• 0,2 моль/л раствор иода;
• раствор крахмала;
• раствор перекиси водорода;
• реактив Фслинга;
• тимол (кристаллический).
титрованные растворы и индикаторы:
• 0,I моль/л раствор натрия гидроксида;
• 0,I моль/л раствор серебра нитрата;
• фенолфталеин;
• эозинат натрия.
‘Посуда , приборы, оборудование:
• титровальная установка;
• рефрактометр;
• микробюретка;
• мерные пинетки на 1 и 5 мл;
• склянка для титрования
• глазные пипетки;
• пробирки;
• вата;
• выпарительная чашка.
Riboflavini 0,001
Kalii iodidi 0,3
Acidi ascorbinici 0,02
Solutionis Glucosi 3%— 10ml
MDS Глазные капли.
Внутриаптечная заготовка № 10.
СВОЙСТВА
Прозрачная жидкость желтого цвета
Подлинность
• На аскорбиновую кислоту и калия иодид с помощью одного реактива - раствора нитрата серебра
К 3 каплям раствора прибавляют 1-2 капли раствора нитрата серебра. Образуется желтый творожистый осадок (доказательство йодида)
KJ + AgNO3 -» AgJ + KNO3
Калия иодид вступает в реакцию первым, так как ионные реакции идут практически моментально, значительно быстрее, чем окислительно-восстановительные реакции. Затем вступает в реакцию аскорбиновая кислота и появляется темный осадок.
С -- ОН C = O
|| +2Ag NO3 = | + 2HNO3 + 2 Ag+
С -- ОН C = O
| |
• На аскорбиновую кислоту
(Присутствие KJ не мешает)
К 4-5 каплям раствора прибавляют 1-2 капли раствора крахмала| и 4-5 капель 0,02 моль/л раствора иода. Наблюдается обесцвечивание раствора иода (буро-синее окрашивание не появляется).
| |
C-OH C=O
|| + I2 = | + 2HI
C-OH C=O
| |
• На калия иодид
(Присутствие аскорбиновой кислоты не мешает)
К 4—5 каплям раствора прибавляют по 1-2 капли раствора ацетата евши ца. Образуется желтый осадок.
2KJ + (СН3СОО)2РЬ -> РЫ2 + 2СН3СООН
• На глюкозу с реактивом Фелинга
Доказать глюкозу с реактивом Фелинга в присутствии аскорбиновой кислоты не удается, так как аскорбиновая кислота является более сильным восстановителем и первой вступает в реакцию этим реактивом. Поэтому необходимо окислить аскорбиновую кислоту, чтобы она не мешала определению глюкозы. Для этого к 0,5 мл раствора прибавляют по 3 капли пергидроля и раствора аммиака и кипятят 3 минуты. В этих условиях енольная форма аскорбиновой кислоты окисляется до кетоформы.
| "о" |
С -- ОН = C = О
|| | + 2Н+
С -- ОН С = О
| |
енольная кетонная
(в-ль) (ок-ль)
(! выделяющаяся кислота нейтрализуется раствором аммиака).
Затем проводят качественную реакцию на глюкозу с реактивом Фелинга при нагревании. Образуется кирпично-красный осадок.
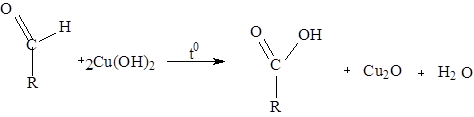
На глюкозу с тимолом в концентрированной серной кислоте
( Присутствие аскорбиновой кислоты не мешает)
0,5 мл раствора помещают в выпарительную чашку и выпаривают на водяной бане. После охлаждения к сухому остатку прибавляют 0,01г тимола, 5-6 капель концентрированной серной кислоты и 1-2 капли воды. Появляется красно-фиолетовое окрашивание.
На рибофлавин
6,7-диметил-9-( D-1-рибитил) - изоаллоксазин
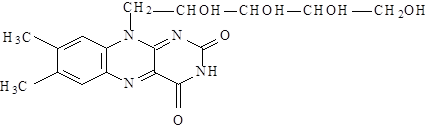
а) Раствор рибофлавина имеет зеленовато-жёлтую окраску и зеленую флюоресценцию в ультрафиолетовом свете. При добавлении соляной кислоты или щелочи зеленая флюоресценция исчезает, а при добавлении гидросульфита натрия ( восстановитель) исчезает и окраска и флюоресценция
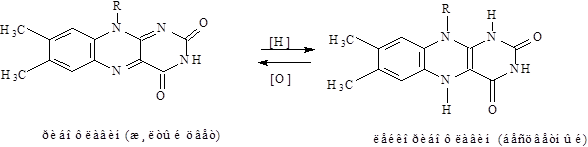
.
б) К 0,5 мл раствора прибавляют 2-3 капли концентрированной серии кислоты. Появляется красное окрашивание, переходящее в желтое при добавлении 1 капли воды.
Количественное определение
• Количественное определение аскорбиновой кислоты.
Метод нейтрализации.
К 5 мл раствора прибавляют 3-4 капли фенолфталеина и титруют О,1 моль/л раствором натрия гидроксида до розового окрашивания (V,).
| |
C-OH C-OH
|| + NaOH = || + H2O
C-OH C-ONa
| Fаскорбиновой кислоты=1 |
T = 176,13 *1 *0,1 =0,0176 г/мл
1000
m аскорбиновая к-та = V * K * T * A
навеска
А- весь объём внутриаптечной заготовки
доп.откл = ±?
б) Метод иодометрии
5 мл раствора помещают в склянку с притертой пробкой и титруют
0,1 моль/л раствором иода до синего окрашивания. Индикатор — 8 капель
раствора крахмала (V )
| |
C-OH C=O
|| + I2 = | + 2HI
C-OH C=O
| |
f=1|2
T = 176.13 *1|2*0,1 = 0,0088г/мл
1000
m аскорбиновая к-та = V * K * T * A
навеска
А - весь объём внутриаптечной заготовки
доп.откл = ±?
• Количественное определение калия иодида
аргентометрия с адсорбционным индикатором. Метод Фаянса
К 1 мл раствора прибавляют 5 капель уксусной кислоты, 3-5 капель эозината натрия и титруют 0,1 моль/л раствором нитрата серебра до розового окрашивания и коагуляции осадка(V).
KI + AgNO3 = AgI + KNO3
1 мл 0,1 моль/л раствора нитрата серебра соответствует 0,0166 г калия йодида
mKI = V*K*T*A =
навеска
доп.отклонения = ? Vориент =?
Количественное определение глюкозы
В многокомпонентных смесях один компонент можно определить рефрактометрически при условии, что все другие компоненты определены титриметрическими методами ( их содержание указывают в процентах )
С% глюкозы = nгл кап - n0 - C%аск. к-ты*Fаск к-та -C%KI*FKI =
Fглюкоза
Fглюкоза = 0,00142
Fаскорбин. к-та = 0,0016
FKI = 0,0013
показатель преломления рибофлавина так мал, что им пренебрегают.
доп.откл = ±?
Содержание рибофлавина можно определить методом фотоколориметрии.
АЛГОРИТМ ВНУТРИАПТЕЧНОГО КОНТРОЛЯ ВНУТРИАПТЕЧНОЙ ЗАГОТОВКИ ВИТАМИННЫХ ГЛАЗНЫХ КАПЕЛЬ
• Письменный контроль Проверяется запись в книге учета лабораторных и фасовочных работ.
Воды очищенной стерильной 96 мл
Рибофлавина 0,01
Кислоты аскорбиновой 0,2
Глюкозы (безводной) 3,0 (в пересчете на водную глюкозу - 3,3)
Калия иодид______ З,0____
Vобщ = 100 мл
№ анализа:
Подпись провизора-аналитика:
Глазные капли готовятся в асептических условиях*.
Паспорт письменного контроля витаминных глазных капель, выполненных по индивидуальному рецепту, с учетом особенностей приготовления лекарственных формы, выглядит следующим образом:
Гл
Дата ППК номер рецепта
Взято: Aquae purificatae sterilisatae q.s.
Acidi ascorbinici 0,02
Glucosi 0,33 (перерасчет на водн. глюкозу)
Aquae purificatae sterilisatae 5 ml
Vобщ = 5 ml
Kalii iodidi 0,3
Solutionis Riboflavini 1:5000- 5 ml
Vобщ = 10 ml
Приготовил № анализа
Проверил: Подпись провизора-аналитика
• Органолептический контроль
Прозрачная желтого цвета жидкость без видимых механических включений
• Физический контроль
Количество флаконов 10. V = 10 мл доп.отк = ± 10%
От каждой серии внутриаптечной заготовки физическому контролю подлежат не менее 3-х флаконов.
Проверяется герметичность укупорки.
• Химический контроль
По приказу М3 РФ № 751 внутриаптечная заготовка (каждая серия) подлежит полному химическому контролю обязательно.
Качественный контроль: проверка наличия всех компонентов прописи . Количественное определение компонентов прописи.
mаск к-та = 0,2г доп.отк = ± 10%
mKJ= 3,0г доп.отк = ±4%
m глкж= 3,0 доп.отк = ±4%
• Оформление результатов контроля:
заполнить «Журнал регистрации результатов органолептическою, физического и химического контроля внутриаптечной заголовки, лекарственных форм, изготовленных по индивидуальным рецептам (требованиям лечебно-профилактических учреждений), концентратов, полуфабрикатов, тритураций и спирта при разведении в аптеке"
в книге учета лабораторных и фасовочных работ поставить номер м и подпись провизора-аналитика.
• Оформление к отпуску
Основная этикетка: «Глазные капли», «Приготовлено асептически».
Предупредительные надписи: «Хранить в прохладном и защищенном от света месте" «Хранить в недоступном для детей месте». На этикетке приведены наименование и местонахождение аптеки, состав лекарственного средства на русском языке, способ применения, серия, дата, цена, срок годности.
| АО «Петербургские аптеки» Аптека № 116 г. Санкт Петербург ул. Типанова д.3 серия №………… анализ №………………. |
| Г Л А З Н Ы Е К А П Л И |
| Рибофлавина 0,001 Калия йодида 0,3 Кислоты аскорбиновой 0,02 Раствора декстрозы(глюкозы) 3% 10 мл Дата приготовления……….годен до……. Цена…………. Хранить в прохладном темном месте Хранить в недоступном для детей месте |
ЗАНЯТИЕ 12
Внутриаптечный контроль клазных капель 0,25% раствора левомицетина
ЗАДАЧИ.
1. Освоить внутриаптечный контроль лекарственного средства с антибиотиком.
2. Изучить химический контроль левомицетина.
Продолжительность занятия
2 академических часа (90 минут)
Вопросы для самоподготовки
1. Алгоритм внутриаптечного контроля глазных капель 0,25% раствора левомицетина, выписанных по индивидуальному рецепту.
2. Химический контроль девомицетина. Обзор возможных методов качественного и количественного анализа. Расчеты. Оформление результатов контроля.
Материальное обеспечение.
а) реактивы и растворители
• кислота серная
• кислота азотная
• кислота хлористоводородная
• раствор натрия гидроксида
• раствор гидроксида аммония
• раствор серебра нитрата
• раствор калия йодида
• раствор пероксида водорода
• раствор натрия нитрита
• раствор меди сульфата
• цинковая пыль
• раствор нафтола
• спирт
б)титрованные растворы и индикаторы
• 0,01 моль/л раствор натрия тиосульфата
• 0,01моль/л раствор серебра нитрата
• 0,01моль/л раствор натрия нитрита
• 0,01моль/л раствор аммония тиоцианата (роданида)
• 0,02моль/л раствор натрия нитрита
• 0,1 моль/л раствор серебра нитрата
• крахмал
• метиленовый синий
• железо-аммонийные квасцы
• тропеолин ОО
• бромфеноловый синий
в) посуда, приборы, оборудование
• титровальная установка
• рефрактометр
• микробюретка
• склянки для титрования
• пробирки
• воронка
• вата
• глазные пипетки
• водяная баня
Rp: Sol. Laevomycetini 0,25% - 10 ml
Sterilisetur!
D.S. глазные капли. По 2 капли 3 раза в день в больной глаз.
расчет изотоничности глазных капель
Эквивалент левомицетина по натрию хлориду равен 0,1
0,025 *0,1 = 0,0025
0,09 - 0,0025 = 0,0875 ≈0,09
Состав
Левомицетина 0,025
натрия хлорида 0,09
Воды очищенной стерильной 10 мл
ПРИМЕЧАНИЕ!! Для точности изготовления готовят 2 порции
ПОДЛИННОСТЬ
1. на левомицетин
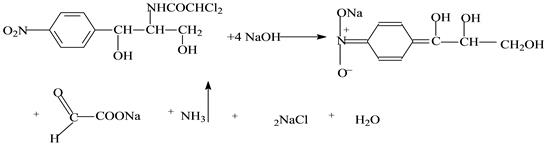
а) реакции, основанные на щелочном гидролизе
К 0,5 мл раствора прибавляют 4-5 мл 10% раствора гидроксида натрия и нагревают. Появляется жёлтое окрашивание, переходящее при дальнейшем нагревании в оранжево-красное. Ощущается запах аммиака.
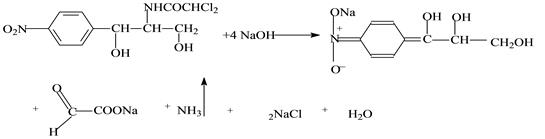
При этом происходит минерализация органически связанного хлора. Хлорид-ион можно обнаружить реакцией с нитратом серебра.
NaCl + AgNO3 = AgCl + NaNO3
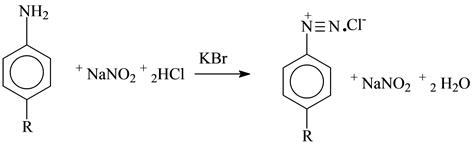
б) Реакция азосочетния после восстановления нитрогруппы.
К 0,5 мл раствора прибавляют 2 мл соляной кислоты, 0,1г цинковой пыли и нагревают на водяной бане 2 минуты для восстановления нитрогруппы. После охлаждения раствор фильтруют и проводят реакцию диазотирования и азосочетания
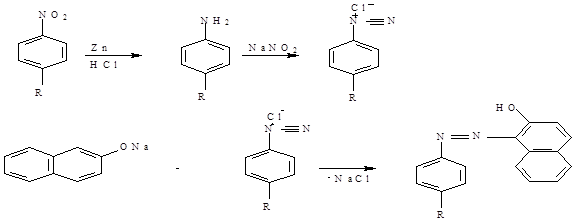
2. на хлорид натрия- методику и химизм привести самостоятельно.
Количественное определение
1. Количественное определение левомицетина
а) метод йодометрии - косвенное титрование.
Метод основан на образовании растворимого комплексного соединения левомицетина с сульфатом меди в щелочной среде.
К 5 мл раствора левомицетина прибавляют 5 мл воды точно пипеткой 0,5 мл 10% раствора гидроксида натрия и 0,5 мл 5% раствора сульфата меди. Появляется сине - фиолетовое окрашивание в результате образрвания растворимого комплекса. Смесь взбалтывают 2 минуты, фильтруют через ватный тампон( входящий на 1-1,5 см в трубочку воронки) и промывают водой 3 раза по 5 мл.
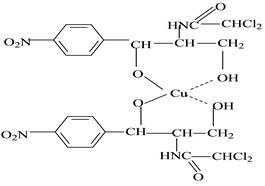
К фильтрату прибавляют по каплям разведенную серную кислоту до обесцвечивания. При этом комплекс разлагается. Для определения выделившегося сульфата меди прибавляют 0,5г калия йодида. Выделившийся йод оттитровывают растворм тиосульфата натрия.
2CuSO4 + 4KI = Cu2I2 + I2 + 2K2SO4 I2 + 2Na2S2O3 =2 NaI + Na2S4O6
1 мл 0,01 моль/л раствора тиосульфата натрия соответствует 0,006463 г левомицетина
mлевомицетин = VKT10
5
доп. отклонения? ориентиров. объём ?
б) метод нитритометрии после восстановления нитрогруппы
К 3 мл раствора прибавляют 1 мл концентрированной соляной кислоты и постепенно 0,25 г цинковой пыли. Затем еще добавляют 1 мл концентрированной соляной кислоты , оставляют на 15 минут и жидкость фильтруют. Колбу и фильтр промывают 40 мл воды. Промывные воды присоединяют к основному фильтрату, добавляют 1г бромида калия, 2 капли тропеолинаОО и 1 каплю метиленового синего и титруют 0,02 моль/л растворм нитрита натрия, добавляя его по8-10 капель в начале титрования , в конце титрования - 1-2 капли.
1 мл 0,02 моль/л раствора нитрита натрия соответствует 0,006463 г левомицетина.
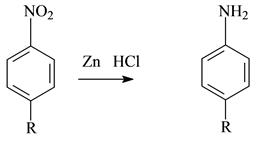
mлевомицетин = V•K•T•10
3
доп. отклонения? ориентиров. объём ?
в) Аргентометрия по Фольгарду. Обратное титрование.
К 1 мл раствора прибавляют по 5 мл раствора гидроксида натрия (8%) и раствора пероксида водорода. Колбу прикрывают воронкой и кипятят на электроплитке около 10 минут ( жидкость упаривается до 2-2,5 мл). После охлаждения воронку промывают 5 мл воды ( прибавляют к основному раствору), затем добавляют разведенную азотную кислоту до кислой реакции среды.
К раствору прибавляют 5 мл (избыток)0,01 моль/л раствора нитрата серебра, 2-3 мл железо-аммонийных квасцов, взбалтывают и оттитровывают 0,01 моль/л раствором роданида аммония до красноватого окрашивания раствора.
NaCl + AgNO3 = AgCl + NaNO3
AgNO3 + NH4CNS = AgCNS + NH4NO3
в точке эквивалентности: 3NH4CNS + FeNH4(SO4)2 = Fe(CNS)3 + 2(NH4)2SO4
красн. р-р
mлевомицетин = (5 - V)•T•10
1
доп. отклонения? ориентиров. объём ?
1 мл 0,01 моль/л раствора нитрата серебра соответствует0,001615 г левомицетина
2. Количественное определение натрия хлорида.
Аргентометрия с ПДИ по методу Фаянса.
К 1 мл раствора прибавляют 1 мл воды, 1-2 капли раствора бромфенолового синего, по каплям уксусную кислоту до зеленовато-желтого окрашивания и титруют 0,1 моль/л раствором нитрата серебра до образования фиолетового осадка
NaCl + AgNO3 = AgCl + NaNO3
! мл 0,1 моль/л раствора нитрата серебра соответствует 0,005844 г натрия хлорида
mлевомицетин = VKT10
1
доп. отклонения? ориентиров. объём ?
Составьте алгоритм внутриаптечного контроля.
| АО «Петербургские аптеки» Аптека № 116 г. Санкт Петербург ул. Типанова д.3 Гр. Сорокиной Н.И. 65лет рец. № 4191 |
| Г Л А З Н Ы Е К А П Л И |
| Раствор левомицетина 0,25% 10 мл По 2 капли в больной глаз 3 раза в день Дата приготовления……….годен до……. Цена…………. Хранить в прохладном темном месте Хранить в недоступном для детей месте |
ЗАНЯТИЯ 13
КОНТРОЛЬНАЯ РАБОТА№ 3
на тему"ВНУТРИАПТЕЧНЫЙ КОНТРОЛЬ ЛЕКАРСТВЕННЫХ ЛЕКАРСТВЕННЫХ СРЕДСТВ ГЕТЕРОЦИКЛИЧЕСКОЙ СТРУКТУРЫ "
Задачи
• Обобщить и систематизировать знания по теме "Гетероциклические средства"
• Обобщить и систематизировать знания по внутриаптечному контролю жидких, твёрдых и асептически проиготовленных лекарственных средств.
• Совершенствовать профессиональные знания, умения и навыки по внутриаптечному контролю различной аптечной продукции.
Продолжительность занятия
академических часа ( 90 минут)
Задание и для самоподготовки
• 1Повторить виды внутриаптечного контроля, специфические показатели качества жидких, твердых и асептически приготовленных лекарственных средств, расчеты содержания действующего вещества, отклонений (и сравнение с допустимой нормой), титра, ориентировочного объема титранта.
• Знать отличительные особенности внутриаптечного контроля лекарственных средств, выписанных по индивидуальному рецепту или требованию лечебного учреждения, приготовленных в виде внутриаптечной заготовки или при заполнении штангласа.
• Повторить химический контроль всех лекарственных средств, выносимых на контрольную работу № 3.
Материальное обеспечение
См. методические рекомендации к соответствующим практическим занятиям.
Алгоритм ответа
• По развернутым тестам цифрами набрать внутриаптечный контроль лекарственного средства, предложенного на анализ, и сдать преподавателю на проверку.
• В контрольной работе описать все виды внутриаптечного контроля лекарственного средства. В химическом контроле привести химизм происходящих процессов, расчеты содержания действующего вещества, допустимые нормы отклонения. При титриметрическом определении рассчитать ориентировочный объем титранта. Предъявить работу для проверки преподавателю.
• Выполнить практически внутриаптечный контроль. Сделать заключение. Оформить отчетную документацию. Сдать работу на проверку преподавателю.
• Убрать рабочее место.
"Слепые" методики анализа лекарственных средств
ОГЛАВЛЕНИЕ
| № п/п | Название лекарственного средства | Номер методики |
| 1. | Дибазол | 1 |
| 2. | Пилокарпина гидрохлорид | 2 |
| 3. | Никотиновая кислота | 3 |
| 4. | Пиридоксина гидрохлорид | 4 |
| 5. | Фенобарбитал | 5 |
| в. | Атропина сульфат | 6 |
| 7. | Кофеин бензоат натрия | 7 |
| 8 | Папаверина гидрохлорид | 8 |
| 9 | Эуфиллин | 9 |
• К 5 мл раствора прибавляют 3 мл....... и титруют 0,1 моль/л.......при взбалтывании до ......окрашивании Индикатор............... (3капли) 1 мл 0,1 моль/л раствора ........... соответствует 0,02447г дибазола.
• К 1 мл раствора прибавляют 3 мл............ и титруют 0,05 моль/л.......при взбалтывании до ......окрашивания водного слоя. Индикатор............... (2-3 капли) 1 мл 0,05 моль/л раствора ........... соответствует 0,012235г пилокарпина гидрохлорида.
• 0,1 г порошка растворяют в 2-3 мл воды, прибавляют 2-4 капли индикатора...........Титруют0,1моль/л раствором.............до ..........окрашивания 1 мл 0,1 моль/л раствора ........... соответствует 0,01231г никотиновой кислоты
• 0,2 г порошка растворяют в 2 мл воды, прибавляют 2-3 капли индикатора...........Титруют 0,02моль/л раствором.............до ..........окрашивания 1 мл 0,02 моль/л раствора ........... соответствует 0,00413г пиридоксина гидрохлорида
• 0,1 г порошка растворяют в 3 мл.....,нейтрализованного по ........прибавляют 3 капли индикатора...........Титруют 0,1моль/л раствором.............до ..........окрашивания 1 мл 0,1 моль/л раствора ........... соответствует 0,02322г фенобарбитала
• К 1 мл раствора прибавляют 2 мл............ и титруют 0,05 моль/л.......при взбалтывании до ......окрашивания водного слоя. Индикатор............... (2-3 капли) 1 мл 0,05 моль/л раствора ........... соответствует 0,01737г атропина сульфата
• К 1 мл раствора прибавляют 1 мл............ и титруют 0,02 моль/л.......при взбалтывании до ......окрашивания водного слоя. Индикатор............... (1-2 капли) 1 мл 0,02 моль/л раствора ........... соответствует 0,00464г кофеина бензоата натрия (титр условный)
• 0,22 г порошка растворяют в 2 мл...... прибавляют 3-5 капель) индикатора...........Титруют0,1моль/л раствором.............до ..........окрашивания 1 мл 0,1 моль/л раствора ........... соответствует 0,03759г папаверина гидрохлорида
• 0,05 г порошка растворяют в 5 мл...... , прибавляют 1-2 капли индикатора...........Титруют 0,02моль/л раствором.............до ..........окрашивания 1 мл 0,02 моль/л раствора ........... соответствует 0,004293г эуфиллина (титр условный)
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ПРИКАЗ
от 26 октября 2015 г. N 751н
ОБ УТВЕРЖДЕНИИ ПРАВИЛ
ИЗГОТОВЛЕНИЯ И ОТПУСКА ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ
ДЛЯ МЕДИЦИНСКОГО ПРИМЕНЕНИЯ АПТЕЧНЫМИ ОРГАНИЗАЦИЯМИ.
| №№ п\п | Аптечная продукция | Обязательные виды контроля |
| 1. 2. 3. 4. | Жидкие лекарственные формы для внутреннего и наружного применения, изготовленные по индивидуальным рецептам и требованиям ЛПУ. Порошки для внутреннего и наружного применения, изготовленные по индивидуальным рецептам и требованиям ЛПУ. Мази. Глазные капли, не содержащие наркотические, психотроптные и сильнодействующие вещества | Письменный, органолептический, контроль при отпуске |
| 5. 6. 7. 8. | Растворы для инъекций Стерильные растворы для наружного применения. Глазные капли, содержащие наркотические, психотроптные и сильнодействующие вещества. Все лекарственные формы для новорожденных и детей до 1 года. | Письменный, органолептический, физический, полный химический, контроль при отпуске |
| 9. | Растворы атропина сульфата, растворы кислоты хлористоводородной (для внутреннего применения) и растворы серебра нитрата | Письменный, органолептический, полный химический, контроль при отпуске |
| 10. | Концентрированные растворы, тритурации | Письменный, органолептический, полный химический, контроль при отпуске |
| 11. 12. | Лекарственные препараты в виде внутриаптечной заготовки (каждая серия). Спирт этиловый при разведении в аптеке | Письменный, органолептический, полный химический, контроль при отпуске |
| 13. 14. 15. | Лекарственные средства, концентрированные растворы при перемещении из помещений хранения в ассистентскую. Расфасованные лекарственные средства, в т.ч. промышленного производства Жидкие растворы в бюреточной установке | Письменный, органолептический, качественный химический, контроль при отпуске |
Другие виды контроля (физический, опросный, химический) проводятся выборочно в течение рабочего дня у каждого фармацевта.
Контроль поступающих в аптеку рецептов и требований лечебных учреждений.
Проверить:
• правильность выписывания;
• совместимость ингредиентов;
• соответствие доз (списки А, Б) возрасту больного;
• наличие указаний о способе применения лекарственного средства.
АЛГОРИТМ ОПРОСНОГО КОНТРОЛЯ
• Назвать первый входящий ингредиент (для сложных лекарственных форм), а для сложных лекарственных форм — и его количество.
• Выслушать информацию фармацевта, который продолжает называть взятые ингредиенты и их количества.
• Сравнить данную информацию с ППК.
• Сделать вывод.
Таблица N 1
Таблица N 1.1
Таблица N 2
Таблица N 3
Допустимые отклонения в общем объеме жидких лекарственных форм при изготовлении массо-объемным методом <*>
| Прописанный объем, мл | Отклонения, % |
| До 10 | ± 10 |
| Свыше 10 до 20 | ± 8 |
| Свыше 20 до 50 | ± 4 |
| Свыше 50 до 150 | ± 3 |
| Свыше 150 до 200 | ± 2 |
| Свыше 200 | ± 1 |
Таблица N 4
Допустимые отклонения в массе навески отдельных лекарственных средств в жидких лекарственных формах при изготовлении массо-объемным методом <*>
| Прописанная масса, г | Отклонения, % |
| До 0,02 | ± 20 |
| Свыше 0,02 до 0,2 | ± 15 |
| Свыше 0,1 до 0,2 | ± 10 |
| Свыше 0,2 до 0,5 | ± 8 |
| Свыше 0,5 до 0,8 | ±7 |
| Свыше 0,8 до 1 | ± 6 |
| Свыше 1 до 2 | ± 5 |
| Свыше 2 до 5 | ± 4 |
| Свыше 5 | ± 3 |
Таблица N 5
Допустимые отклонения в общей массе жидких лекарственных форм при изготовлении методом по массе <*>
| До 10 | ± 10 |
| Свыше 10 до 20 | ± 8 |
| Свыше 20 до 50 | ± 5 |
| Свыше 50 до 150 | ± 3 |
| Свыше 150 до 200 | ± 2 |
| Свыше 200 | ± 1 |
Таблица N 6
Допустимые отклонения в массе навески отдельных лекарственных средств в жидких лекарственных формах при изготовлении методом по массе и в мазях <*>
| Прописанная масса, г | Отклонения, % |
| До 0,1 | ± 20 |
| Свыше 0,1 до 0,2 | ± 15 |
| Свыше 0,2 до 0,3 | ± 12 |
| Свыше 0,3 до 0,5 | ± 10 |
| Свыше 0,5 до 0,8 | ± 8 |
| Свыше 0,8 до 1 | ±7 |
| Свыше 1 до 2 | ± 6 |
| Свыше 2 до 10 | ± 5 |
| Свыше 10 | ± 3 |
Примечание:
<*> Отклонения, допустимые в массе навески отдельных лекарственных средств в жидких лекарственных формах при изготовлении способом по массе или массо-объемным способом, а также в мазях, определяются не на концентрацию в процентах, а на массу навески каждого лекарственного средства, входящего в эти лекарственные формы.
Например, при изготовлении 10 мл 2% раствора пилокарпина гидрохлорида масса навески должна составлять 0,2 г, для которой допускается отклонение ± 10%. При анализе достаточно установить, что было взято не менее 0,18 г и не более 0,22 г пилокарпина гидрохлорида.
Таблица N 7
Таблица N 7.1
В тубах
| Прописанная масса, г | Отклонения, % |
| Свыше 50 до 100 | ± 4 |
Таблица N 8
РЕФРАКТОМЕТРИЧЕСКИЕ ТАБЛИЦЫ
| Кон | Показатели преломления | Факторы | ||
| цент | растворов | показате | ||
| Наименование растворов | рация. | данной | допустимые | лей |
| % | концен | отклонения | преломле | |
| трации | ния | |||
КОНЦЕНТРАТЫ (до 20 % + 2 %. свыше 20 % ± 1 %)
| АМИДОПИРИН | 5 | 1,3442 | 1,3440-1,3444 | 0,00225 |
| АММОНИЯ ХЛОРИД | 20 | 1,3690 | 1,3683-1,3697 | 0,0018 |
| БАРБИТАЛ НАТРИЯ | 10 | 1,3512 | 1,3508-1,3516 | 0,00182 |
| ГЕКСАМЕТИЛЕН ТЕТРАМИН | 20 | 1,3670 | 1,3663-1,3677 | 0,0017 |
| ГЛЮКОЗА (безводная) | 50 | 1,4040 | 1,4033-1,4047 | 0,00142 |
| КАЛИЯ БРОМИД | 20 | 1,3562 | 1,3557-1,3567 | 0,001 16 |
| КАЛИЯ ИОДИД | 20 | 1,3590 | 1,3585-1,3595 | 0,0013 |
| КАЛЬЦИЯ ХЛОРИД | 20 | 1.3558 | 1,3553-1,3563 | 0,00114 |
| КАЛЬЦИЯ ХЛОРИД | 50 | 1,3870 | 1,3865-1,3875 | 0,00108 |
| КИСЛОТА АСКОРБИНОВАЯ | 2 | 1.3360 | 1,3359-1,3361 | 0,0015 |
| КИСЛОТА АСКОРБИНОВАЯ | 10 | 1,3482 | 1,3479-1,3485 | 0,0152 |
| КИСЛОТА БОРНАЯ | 4 | 1,3357 | 1,3356-1,3358 | 0,00067 |
| КОФЕИН-БЕНЗОАТ НАТРИЯ | 5 | 1,3426 | 1,3424-1,3428 | 0,00192 |
| КОФЕИН-БЕНЗОАТ НАТРИЯ | 20 | 1,3714 | 1,3706-1,3722 | 0,00192 |
| МАГНИЯ СУЛЬФАТ | 50 | 1,3740 | 1.3736-1,3744 | 0,00082 |
| НАТРИЯ БЕНЗОАТ | 10 | 1,3544 | 1,3540-1,3548 | 0,00214 |
| НАТРИЯ БРОМИД | 20 | 1,3590 | 1,3585-1,3595 | 0,0013 |
| НАТРИЯ ГИДРОКАРБОНАТ | 5 | 1,3392 | 1.3391-1,3394 | 0,00125 |
| НАТРИЯ САЛИЦИЛАТ | 10 | 1,3530 | 1,3526-1,3534 | 0,002 |
| ХЛОРАЛГИДРАТ | 20 | 1,3554 | 1,3550-1,3558 | 0.00112 |
ЛЕК. ФОРМЫ ДЛЯ ИНЪЕКЦИЙ (± 3 %)
| АМИДОПИРИН | 4 | 1,3420 | 1,3417-1,3423 | 0,00225 |
| АНАЛЬГИН | 25 | 1,381 | 1,3796-1,3824 | 0,00192 |
| АНАЛЬГИН | 50 | 1,4275 | 1,4247-1,4303 | 0,00189 |
| БАРБАМИЛ | 4 | 1,3402 | 1,3400-1,3404 | 0,0018 |
| БАРБАМИЛ | 5 | 1,342 | 1,3417-1,3423 | 0,0018 |
| ГЕКСАМЕТИЛЕНТЕТРАМИН | 40 | 1,4019 | 0,00172 | |
| ГЛЮКОЗА (безводная) | 5 | 1,3401 | 1,3399-1,3403 | 0,00142 |
| ГЛЮКОЗА (безводная) | 10 | 1,3472 | 1,3468-1,3476 | 0,00142 |
| ГЛЮКОЗА (безводная) | 20 | 1,3614 | 1,3606-1,3623 | 0,00142 |
| Г ЛЮКОЗА (безводная) | 25 | 1,3685 | 1,3674-1,3696 | 0,00142 |
| ГЛЮКОЗА (безводная) | 40 | 1,3898 | 1,3881-1,3915 | 0,00142 |
| КАЛИЯ ХЛОРИД | 3 | 1,3368 | 1,3367-1,3369 | 0,001269 |
| КАЛИЯ ХЛОРИД | 5 | 1,3394 | 1,3392-1,3396 | 0,001269 |
| КАЛИЯ ХЛОРИД | 7,5 | 1,3425 | 1,3422-1,3428 | 0,001269 |
| КАЛИЯ ХЛОРИД | 10 | 1,3457 | 1,3453-1,3461 | 0,001269 |
| КИСЛОТА АМИНОКАПРОНОВАЯ | 1 | 1,3349 | 1,3348-1,3350 | 0,00185 |
| КИСЛОТА АМИНОКАПРОНОВАЯ | 2 | 1,3367 | 1,3366-1,3368 | 0,00185 |
| КИСЛОТА АМИНОКАПРОНОВАЯ | 5 | 1,3423 | 1,3420-1,3425 | 0,00185 |
| КИСЛОТА АМИНОКАПРОНОВАЯ на физиологическом р-ре | 5 | 1,3438 | ||
| КОФЕИН-БЕНЗОАТ НАТРИЯ | 10 | 1,3522 | 1,3519-1,3526 | 0,00192 |
| НАТРИЯ ГИДРОКАРБОНАТ | 3 | 1,3368 | 1,3366-1,3369 | 0,00125 |
| НАТРИЯ ГИДРОКАРБОНАТ | 5 | 1,3393 | 1,3391-1,3394 | 0,00125 |
| НАТРИЯ НУКЛЕИНАТ | 1 | 1,3348 | 1.3347-1,3348 | 0,00176 |
| НАТРИЯ НУКЛЕИНАТ | 2 | 1,3365 | 1,3364-1,3366 | 0.00175 |
| НАТРИЯ НУКЛЕИНАТ | 5 | 1,3416 | 1.3413-1,3418 | 0,00171 |
| НАТРИЯ ХЛОРИД | 10 | 1.3494 | 1,3489-1,3499 | 0,00164 |
| НАТРИЯ ЦИТРАТ | 1 | 1.3341 | ||
| НАТРИЯ ЦИТРАТ | 2 | 1,3355 | ||
| НАТРИЯ ЦИТРАТ | 5 | 1,3393 | 1,391-1,3395 | 0,00126 |
| НОВОКАИН | 4 | 1,3418 | 1,3415-1,3421 | 0,0022 |
| НОВОКАИН | 5 | 1,344 | 1,3437-1,3443 | 0,0022 |
| НОВОКАИН | 10 | 1,355 | 1,3543-1,3557 | 0,0022 |
| НОРСУЛЬФАЗОЛ-НАТРИИ | 10 | 1.3502 | 1,3498-1,3506 | 0,00172 |
ВНУТРИАПТЕЧНАЯ ЗАГОТОВКА (не менее 200 мл + 3 %)
| АММОНИЯ ХЛОРИД | 5 | 1,343 | 1,3427-1,3433 | 0,002 |
| АММОНИЯ ХЛОРИД | 10 | 1,352 | 1,3514-1,3526 | 0,0019 |
| КАЛИЯ ИОДИД | 3 | 1,3369 | 1,3368-1,337 | 0,0013 |
| КАЛЬЦИЯ ХЛОРИД | 2 | 1,3354 | 1,3353-1,3354 | 0,00118 |
| КАЛЬЦИЯ ХЛОРИД | 3 | 1,3365 | 1,3364-1,3367 | 0,00118 |
| КАЛЬЦИЯ ХЛОРИД | 5 | 1,3389 | 1,3387-1,3391 | 0,00118 |
| КАЛЬЦИЯ ХЛОРИД | 10 | 1,3446 | 1,3443-1,3449 | 0,00116 |
| КАЛЬЦИЯ ГЛКЖОНАТ | 5 | 1,341 | 1.3408-1,3412 | 0,0016 |
| КИСЛОТА ГЛЮТАМИНОВАЯ | 1 | 1,3348 | 1,3347-1,3349 | 0,00182 |
| МАГНИЯ СУЛЬФАТ | 10 | 1,3423 | 1,3420-1,3426 | 0,00093 |
| МАГНИЯ СУЛЬФАТ | 15 | 1.3468 | 1,3464-1.3472 | 0,00092 |
| МАГНИЯ СУЛЬФАТ | 20 | 1,3510 | 1,3505-1,3515 | 0.00090 |
| МАГНИЯ СУЛЬФАТ | 25 | 1,3553 | 1,3546-1,3559 | 0,00089 |
| МАГНИЯ СУЛЬФАТ | 33 | 1,3617 | 1,3609-1,3626 | 0,00087 |
| МЕДИ СУЛЬФАТ | 5 | 1,3387 | 1,3385-1,3389 | 0,00114 |
| МЕДИ СУЛЬФАТ | 10 | 1,3442 | 1,3440-1,3445 | 0,00112 |
| МЕДИ СУЛЬФАТ | 20 | 1,3554 | 1,3547-1,3561 | 0,00112 |
| НАТРИЯ ИОДИД | 3 | 1,3373 | 1,3372-1,3374 | 0,00143 |
| НАТРИЯ ТИОСУЛЬФАТ | 10 | 1,345 | 1,3446-1,3454 | 0,0012 |
| НАТРИЯ ТИОСУЛЬФАТ | 60 | 1,399 | 1,3970-1,4010 | 0,0011 |
| НАТРИЯ ФОСФАТ 3-х ЗАМ. | 2 | 1,3342 | ||
| НАТРИЯ ФОСФАТ 3-х ЗАМ. | 3 | 1,335 | ||
| НАТРИЯ ФОСФАТ 3-х ЗАМ. | 5 | 1,3362 | ||
| НАТРИЯ ХЛОРИД | 20 | 1,3644 | 1,3635-1,3653 | 0,00157 |
| СИРОП | 64 | 1,4510-1,4540 | ||
| СУЛЬФАЦИЛ-НАТРИИ | 10 | 1,3529 | 1.3523-1,3535 | 0,00199 |
| СУЛЬФАЦИЛ-НАТРИИ | 15 | 1,3629 | 1,3620-1,3638 | 0,00199 |
| СУЛЬФ АЦИЛ-НАТРИИ | 20 | 1.3728 | 1.3716-1,374 | 0,00199 |
| СУЛЬФАЦИЛ-НАТРИИ | 30 | 1,3927 | 1.3909-1,3945 | 0,00199 |
| ФОРМАЛЬДЕГИД | 36,5 | 1,3753 | 1,3741-1,3765 | 0,001159 |
| ФОРМАЛЬДЕГИД | 37,5 | 1,3765 | 1,3762-1,3768 | 0,00116 |
| ЭУФИЛЛИН | 1 | 1,3348 | 1,3347-1,3349 | 0,0018 |
Показатели преломления спирто-водных растворов, концентрация которых выражена в об. %
| Концентрация спирта | Показатели преломления при 20 ° С | Поправка показателя преломления на 1% спирта | Тем ператур ны й коэффициент |
| 0 | 1,33300 | 10-4 | |
| 1 | 1,33345 | 4,5.1 0-4 | 1.104 |
| 2 | 1.33400 | 5,5.10-4 | 1.104 |
| 3 | 1,33444 | 4,4.10-4 | 1,1.10-4 |
| 4 | 1.33493 | 4.9.10-4 | 1,1. 10-4 |
| 5 | 1,33535 | 4,2.10-4 | 1,2.10-4 |
| 6 | 1.33587 | 5.2.10-4 | 1,2.10-4 |
| 7 | 1.33641 | 5,4.10-4 | 1,3.10-4 |
| 8 | 1.33700 | 5.0.10-4 | 1,3.10-4 |
| 9 | 1.33760 | 6.0.10-4 | 1.3.I0-4 |
| 10 | 1.33808 | 4,8.10-4 | 1,4.10-4 |
| 11 | 1,33870 | 6,2.10-4 | 1,4.10-4 |
| 12 | 1.33924 | 5.4.10-4 | 1.4.10-4 |
| 13 | 1.33977 | 5,З.10-4 | 1.4.10-4 |
| 14 | 1,34043 | 6,6. 10-4 | 1,4.10-4 |
| 15 | 1.34096 | 5,3.10-4 | 1,5.10-4 |
| 16 | 1,34158 | 6,2.1 O-4 | 1,5.10-4 |
| 17 | 1,34209 | 5,1.10-4 | 1,5.10-4 |
| 18 | 1.34270 | 6,1. ю-4 | 1,5.10-4 |
| 19 | 1.34330 | 6.0.10-4 | 1,5.10-4 |
| 20 | 1,34390 | 6,0.10-4 | 1,6.10-4 |
| 21 | 1,34452 | 6,2.10-4 | 1,6.10-4 |
| 22 | 1,34512 | 6,0.1 0-4 | 1,7.10-4 |
| 23 | 1,34573 | 6,1.10-4 | 1.8.10-4 |
| 24 | 1,34635 | 6,2.10-4 | 1.9.10-4 |
| 25 | 1,34697 | 6,2.10'4 | 2.0.10-4 |
| 30 | 1.35000 | 6.0.10 -4 | 2,0.10-4 |
| 35 | 1,35320 | 6,4.10-4 | 2.1.10-4 |
| 40 | 1,35500 | 4,0.10-4 | 2.4.10-4 |
| 45 | 1,35700 | 4,0.10-4 | 2.4.10-4 |
| 50 | 1,35900 | 4.0.10-4 | 2.6.10-4 |
| 55 | 1,36060 | 3,2.10-4 | 2,6.10-4 |
| 60 | 1,36180 | 2,4.10-4 | 3,4.10-4 |
| 65 | 1,36300 | 2,4.10-4 | 3,6.10-4 |
| 70 | 1,36380 | 1,6.10-4 | 3,8.10-4 |
| 75 | 1,36450 | 1,4.10-4 | 4,0.10-4 |
Таблица коэффициентов увеличения объема водною раствора при растворении лекарственных веществ
| Наименование | КУО мл/г | Наименование | КУО мл/г |
| Аммония хлорид | 0,72 | Кофеин-бензоат натрия | 0,65 |
| Анальгин | 0,90 | Магния сульфат | 0,50 |
| Антипирин | 0,85 | Натрия бензоат | 0,60 |
| Барбамил | 0,76 | Натрия бромид | 0,29 |
| Барбитал-натрий | 0.64 | Натрия гидрокарбонат | 0,30 |
| Г ексаметилентетрамин | 0.78 | Натрия йодид | 0,38 |
| Г лтокоза безводная | 0,64 | Натрия салицилат | 0,59 |
| Глюкоза (влажность 10 %) | 0,69 | Н атр ия пара-ам и носал и цил ат | 0,64 |
| Иод (в растворе калия иодида) | 0,23 | Натрия тетраборат | 0,47 |
| Калия бромид | 0,27 | Натрия тиосульфат | 0,51 |
| Калия иодид | 0,25 | Натрия хлорид | 0,33 |
| Кальция глюконат | 0,50 | Новокаин | 0,81 |
| Кальция лактат | 0.67 | Папаверина гидрохлорид | 0.77 |
| Кальция хлорид | 0.58 | Сульфацил-натрий | 0,62 |
| Кислота аскорбиновая | 0.61 | Эфедрина гидрохлорид | 0,84 |
| Кислота борная | 0.68 | Эуфиллин | 0,70 |
Таблица сроков хранения некоторых концентрированных растворов
В условиях аптеки
| Наименование | Концентрация, | Срок годности (сутки) | |
| % | при t° X | ранения | |
| не выше 25 °С | 3-5 °С | ||
| Аммония хлорид | 20 | 15 | |
| Барбитал натрия | 10 | 10 | |
| Гексаметилентетрамин * | 10, 20,40 | 20 | |
| Глюкоза (безводная) | 10,20,40, 50 | 4 | 10 |
| Калия бромид * | 20 | 20 | |
| Калия иодид * | 20 | 15 | |
| Кальция хлорид | 50 | 30 | |
| Кальция хлорид | 5, 10, 20 | 10 | |
| Кислота аскорбиновая * | 5 | 5 | |
| Кислота хлористоводородная | 10 | 30 | |
| Кофеин-бензоат натрия | 5 | 7 | 15 |
| Кофеин-бензоат натрия | 20 | 20' | |
| Магния сульфат | 10, 25. 50 | 15 | |
| Натрия бензоат | 10 | 20 | |
| Натрия бромид * | 20 | 20 | |
| Натрия гидрокарбонат | 5 | 4 | 10 |
| Натрия салицилат * | 40 | 20 | |
| Хлоралгидрат | 10 | 5 | |
| Хлоралгидрат | 20 | 15 | |
Примечание: *) - хранить в защищенном от света месте
Таблица изотонических эквивалентов некоторых лекарственных веществ по натрию хлориду
| Наименование препарата | Эквивалент по натрию хлориду |
| Атропина сульфат | 0,1 |
| Бензилпенициллина качисвая соль | 0.16 |
| Бензилпенициллина натриевая соль | 0.15 |
| Глюкоза (безводная) | 0.18 |
| Гоматропина гидробромид | 0.16 |
| Дикаин | 0.18 |
| Димедрол | 0.2 |
| Калия иодид | 0.35 |
| Кальция глюконат | 0.16 |
| Кальция лактат | 0.2 |
| Кальция хлорид | 0.36 |
| Кислота аскорбиновая | 0.18 |
| Кислота борная | 0.53 |
| Кофеин-бен юат натрия | 0.23 |
| Левомицетин | 0.097 |
| Магния сульфат | 0.14 |
| Морфина гидрохлорид | 0.15 |
| Натрия бромид | 0.62 |
| Натрия гидрокарбонат | 0,65 |
| Натрия хлорид | 1.0 |
| Новокаин | 0.18 |
| Папаверина гидрохлорид | 0,1 |
| Пилокарпина гидрохлорид | 0.22 |
| Пиридоксина гидрохлорид | 0,28 |
| Цинка сульфат | 0.12 |
| Этилморфина гидрохлорид | 0,15 |
Министерство здравоохранения Российской Федерации
САНКТ-ПЕТЕРБУРГСКИЙ ФАРМАЦЕВТИЧЕСКИЙ техникум
МЕТОДИЧЕСКОЕ ПОСОБИЕ
к практическим занятиям по фармацевтической химии
Часть III
Методическое пособие предназначено для студентов, изучающих фармацевтическую химию по программе, составленной по специальности 33.0201 «Фармация» базового уровня среднего профессионального образования.
В практикум включены внутриаптечный контроль преимущественно асептически приготовленных лекарственных средств.
К каждому занятию приведены цели и задачи работы, вопросы для самоподготовки, материальное обеспечение, содержание работы, общие указания и образцы составления алгоритмов внутриаптечного контроля различных видов ап течной продукции, а также справочный материал для самостоятельной работы студентов.
ГЕТЕРОЦИКЛИЧЕСКИЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА
ЗАНЯТИЕ 1
Внутриаптечный контроль раствора фурацилина 0,02%- 100мл
Время занятия 90 минут
Вопросы для самоподготовки:
Студенты должны знать
• Русское, латинское и химическое название фурацилина, свойства, подлинность, доброкачественность препарата (испытание на чистоту) и методы количественного определения, применение и хранение фурацилина
• Внутриаптечный контроль раствора фурацилина
• Фотоколориметрический (ФЭК) метод анализа, методику определения, формулы расчета содержания вещества в анализируемом растворе.
Студенты должны выполнить
• Ответить на вопросы индивидуальных письменных заданий
• Провести ВАК раствора фурацилина, определить концентрацию методом ФЭК, по результатам определения сделать заключение о качестве предложенной лекарственной формы
• Резушльтаты анализа оформит в журнале провизора-аналитика
Анализ раствора фурацилина 0,02% - 100мл
Rp Sol Nitrofurali 0,02% 100ml
D.S. для полоскания горла
Свойства.
Прозрачная зеленовато-желтого цвета жидкость без запаха. Без механических включений.
Подлинность
1. К исследуемому раствору прибавляют раствор щелочи, появляется оранжевое окрашивание.

Количественное определение.
Метод фотоколориметрии
Этот метод основан на определении степени поглощения света окрашенными растворами. Для выполнения определения этим методом используют фотоэлектроколориметры (ФЭК), которые позволяют провести анализ с точностью 1-2 отн.%%.
Основными частями ФЭК являются : источник излучения, светофильтр, фотоэлемент, кюветы.
В качестве источника излучения испроьзуют лампы накаливания, обеспечивающие работу в видимой области спектра.
Для увеличения чувствительности и точности фотометрического определения используют поглощение не смешанного излучения (белый свет), а лишь тех лучей, которые максимально поглощаются окрашенным раствором. Для того, чтобы из смешанного излучения выделить лучи определенных длин волн, на пути световых потоков перед поглощающим раствором помещают избирательные поглотители света – светофильтры.
Для измерения оптической плотности определяемый раствор выливают в специальную стеклянную посуду – кюветы. Выбор кювет зависит от интенсивности окраски раствора: чем интенсивнее окраска раствора, тем тоньше кювета.
Фотоэлемент преобразует световую энергию, прошедшую через определяемый раствор, в электрическую.
Отношение интенсивности потока излучения, прошедшего через исследуемый раствор, к интенсивности первоначального потока излучения называется пропусканием (Т)
I0 I , где
I0 - интенсивность падающего монохроматческого излучения
I - интенсивность прошедшего через исследуемый раствор монохроматического излучения
Оптическая плотность (А) – логарифм обратной величины пропускания
А =lg 1
Т
Шкала прибора (ФЭК) проградуирована в единицах оптической плотности (А) (нижняя часть) и в единицах пропускания (Т) (верхняя часть). Жанная работа основана на определении оптической плотности (А) и будет использоваться нижняя часть шкалы.
Зависимость интенсивности светового потока, который проходит через раствор, от толщины слоя исследуемого раствора и концентрации растворенного вещества выражается объединенным законом Бугера- Ламберта- Бера: оптическая плотность раствора (А) прямо пропорциональна концентрации окрашенного раствора (с) и толщи не слоя этого раствора (l):
A = ἑ×l×c
ἑ - коэффициент поглощения света (постоянная величина для каждого окрашенного вещества, зависит от его природы).
Концентрацию исследуемых веществ можно определить различными способами:
• Путем сравнения оптических плотностей стандартного и исследуемого раствора
В этом случае в две пробирки вносят одинаковые объёмы стандартного и исследуемого растворов, добавляют одинаковое количество реактивов. Измеряют оптическую плотность при одинаковой толщине слоя. Концентрацию исследуемого раствора вычисляют по формуле:
Сан. = Аан.×Сст , где
Аст
Сст концентрация стандартного раствора
Сан концентрация исследуемого раствора
Аан оптическая плотность исследуемого раствора
Аст оптическая плоьность стандартного раствора
• Путем определения концентрации окрашенного вещества по калибровочному графику
Готовят серию окрашенных стандартных растворов с известной концентрацией (5-10 образцов), измеряют величины их оптических плотностей и строят график зависимости концентоасии от оптической плотности.
А
С
С исследуемым раствором проводят операции, аналогичные стандартным растворам. Определяют оптическую плотность исследуемого раствора и по графику определяют концентрацию. Калибровочную прямую периодически проверяют.
Методика количественного определения фурацилина в растворе.
К 0,5мл исследуемого раствора фурацилина прибавляют 7,5 мл воды и 2 мл 0,1 моль/л раствора гидроксида натрия. Перемешивают.

Максимальная величина оптической плотности реакционной смеси устанавливается через 15 минут и не изменяется в течение часа. Поэтому через 15-20 минут исследуемый раствор выливают в кювету с толщиной слоя 0,5 см и измеряют оптическую плотность со светофильтром 450нм (А1). Во вторую кювету такой же толщины помещают раствор сравнения – воду.
Далее определяют оптическую плотность эталонного раствора(А2). Раствор сравнения – вода. Для приготовления эталонного раствора берут 0,5мл раствора с точно известной концентрацией (0,02%), прибавляют 7,5 мл воды и 2 мл 0,1 моль/л раствора гидроксида натрия. Перемешивают. Проводят определение оптической плотности через 15-20 минут.
Содержание фурацилина в граммах вычисляют по формуле
m = 0,0002×V×A1
V1×A2 , где
A1 – оптическая плотность исследуемого раствора
A2 – оптическая плотность стандартного раствора
0,0002 – содержание фурацилина в граммах в 1 мл стандартного раствора
V – общий объём раствора
V1- объём раствора, взятый для анализа.
Доп. откл. -?
Сделайте заключение о качестве анализируемого раствора
Составьте самостоятельно алгоритм внутриаптечного контроля раствора фурацилина.
| АО «Петербургские аптеки» Аптека № 116 г. Санкт Петербург ул. Типанова д.3 Гр. Смирнову С.Т. 60лет рец. № 10291 |
| Н А Р У Ж Н О Е |
| Раствор нитрофурала (Фурацилина) 0,2% 100мл Для полоскания горла Дата приготовления…………. Годен до………. Цена…….. Хранить в прохладном темном месте Хранить в недоступном для детей месте |
ЗАНЯТИЕ 2
Производные пиразола
Фармакопейный анализ анальгина.
Исследовательская задача на производные пиразола
Задачи
1. Коррекция и систематизация знаний по теме "производные пиразола"
Дата: 2019-04-23, просмотров: 1232.