Литературный обзор
Сорбция меди на различных сорбентах
Сравнение сорбируемости меди на синтетических катионитах и анионитах
Содержание меди в промышленных стоках даже после проведения реагентной очистки превышает предельно допустимую концентрацию на 2-5 порядков. В связи с этим остро стоит проблема доочистки этих стоков до санитарных норм, традиционно решаемая с использованием ионитов.
В реальных растворах, полученных на установке реагентной очистки Ефремовского завода СК после проведения реагентной очистки натриевой щелочью присутствуют ионы меди (10 - 2000 мг/дм3), натрия (7 - 24 г/дм3), ацетат-ионы (0,5-3,5 моль/дм3) и аммиак (1-10 г/дм3). Для оптимизации процесса доочистки стоков до санитарных норм была исследована сорбируемость меди в динамическом и статическом режимах на синтетических сульфокатионитах КУ-1, КУ-2-8, КУ-2-20 (в Н- и Na-форме) и анионитах АВ-16Г, АВ-17-8, ЭДЭ-10П (в ОН- и Сl-форме).
Сравнение сорбируемости меди на катионитах в динамических условиях показало, что максимальные ее значения 2-4 мэкв/г (при концентрации меди в исходном растворе 2 г/дм3), сохраняющиеся при регенерации, имеют сильнокислотные катиониты КУ-2-8 и КУ-1 в Н-форме. Они проявляют высокую селективность к ионам меди даже в присутствии значительных концентраций катионов - натрия, вступающих в конкурирующее равновесие ионного обмена наряду с катионами меди (при мольных отношениях Na/Cu не превышающих 25). Показано, что при увеличении степени сшивки при переходе от КУ-2-8 к КУ-2-20, а также переходе от Н-формы к Na-форме катионитов сорбируемость меди значительно уменьшается.
Сорбируемость меди в динамических условиях на анионитах увеличивается по ряду : АВ-17-8< ЭДЭ-10П <АВ-16Г и для АВ –16Г достигает величин 3 и 4 мэкв/г (для солевой и ОН- форм соответственно), сопоставимых с сорбируемостью меди на катионитах КУ-2-8 и КУ-1. Исследование регенерации отработанных анионитов при обработке их раствором щелочи показали, что медь десорбируется лишь в незначительной степени, что объясняется образования прочных комплексов меди с функциональными группами, в частности этилендиаминными, входящими в состав анионитов. Величины сорбируемости меди из реальных стоков для всех ионитов оказываются значительно ниже значений приводимых в литературе для модельных растворов, содержащих только ионы меди, за счет протекания конкурирующего ионого обмена с катионами натрия или ацетат-ионами, а также процессов комплексообразования меди с аммиаком и ацетат-ионами.
Результаты сорбируемости меди, свинца и кадмия Таблица1
| Сорбируемый Металл | Количество сорбированных ионов,А, мг/мл | |
| Немодиф. | Модиф. | |
| Медь | 10,4 | 14,2 |
| Свинец | 32,6 | 45,5 |
| Кадмий | 17,94 | 19,95 |
По мнению авторов, изученные сорбенты (модифицированная и немодифицированная) порода обладают значительной сорбционной емкостью, что позволяет использовать эти материалы в технологии для доочистки воды. [6].
Гуминовые кислоты
Методы извлечения и структура гуминовых кислот
Дитизоновый метод
В кислой среде и в присутствии избытка дитизона ионы меди образуют фиолетовый первичный дитизонат Cu(HDz)2 — устойчивое соединение, растворимое в неполярных растворителях (СС14, СНС13). Эта реакция положена в основу чувствительных фотометрических методов определения меди. В щелочной среде образуется менее интенсивно окрашенный желто-коричневый вторичный дитизонат CuDz, также растворимый в СС14 и СНС13. Вторичный дитизонат меди(П) может образоваться и в нейтральной или кислой среде при недостатке дитизона.
Молярный коэффициент поглощения раствора первичного дитизоната меди Cu(HDz)2 в четыреххлорпстом углероде равен 4,52*104 при 550 нм, удельное поглощение 0,71.
Реакция образования дитизоната меди протекает довольно медленно, поэтому при экстракции необходимо продолжительное встряхивание и рекомендуется применять механическую качалку. На скорость экстракции благоприятное действие оказывает увеличение концентрации дитизона в органической фазе и низкая кислотность водной среды.
Оптимальная скорость экстракции наблюдается в том случае, когда кислотность анализируемого раствора соответствует рН 1. При этой кислотности и применении 0,001—0,002.%-ного раствора дитизона еще не экстрагируются висмут и другие металлы, реагирующие с дитизоном. Вместе с медью дитизоном экстрагируются благородные металлы Pt, Pd, Au, Ag и Hg, реагирующие с дитизоном. Обычно содержание этих металлов (это чаще всего ртуть и серебро) в исследуемых растворах очень мало, намного меньше, чем содержание меди, и их можно удалить из экстракта в четыреххлористом углероде путем промывания раствором иодида кадия (например, 1%-ного), который дает с ними прочные иодидные комплексы. При наличии хлоридов в исследуемом растворе серебро не экстрагируется. Присутствие в растворе цитратов или тартратов несколько мешает экстракции меди дитизоном.
Удалить благородные металлы, мешающие определению меди, можно предварительной экстракцией их дитизоном из 1 н. раствора минеральной кислоты. Все благородные металлы, кроме палладия, образуют дитизонаты желто-оранжевого цвета, причем скорость экстракции их намного выше скорости экстракции меди. Исследуемый раствор извлекают небольшими порциями раствора дитизона в четыреххлористом углероде до тех пор, пока органический слой перестанет быстро приобретать желтый оттенок и после продолжительного встряхивания станет фиолетовым.
Для фотометрического определения меди можно использовать одноцветные или двуцветные дитизоновые методы. Вымывание свободного дитизона из экстракта при одноцветном методе следует проводить сильно разбавленным раствором аммиака и встряхивать недолго, чтобы избежать частичного превращения первичного дитизоната Cu(HDz)2 , во вторичный CuDz.
Дитизоновый метод применяют для определения меди в различных материалах, в частности в олове, титане и его сплавах, соединениях урана, биологических материалах.
Дитиокарбаматный метод
При добавлении к раствору (при рН 4 — 11), содержащему небольшое количество ионов меди(П), водного раствора диэтилдитиокарбамата натрия (Na-ДДТК, купраль, карбамат) раствор окрашивается в желто- коричневый цвет вследствие образования коллоидного раствора труднорастворимого комплекса меди. В этом комплексе соотношение Си : ДДТК равно 1:2. Медь соединяется с молекулами реагента посредством двух атомов серы, образуя редко встречающееся внутрикомплексное соединение с четырехчленными циклами. Добавка к раствору защитного коллоида (например, гуммиарабика) делает псевдораствор более устойчивым и позволяет фотометрически определять медь в водной фазе.
В более точном и более чувствительном, чаще используемом экстракционном варианте метода используется растворимость комплекса в органических растворителях, например четыреххлористом углероде, хлороформе, трихлор-этилене, амилацетате, изоамиловом спирте. Экстракция карбамата меди протекает легко, и полученные растворы довольно устойчивы.
Молярный коэффициент погашения раствора комплекса в четыреххлористом углероде при макс = 436 нм составляет 1,4*104 (удельное поглощение 0,22).
Определению меди при помощи диэтилдитиокарбамата натрия мешают металлы, образующие окрашенные карбаматные комплексы, главным образом Fe, Bi, Mn, Ni, Co, Cr, Mo, U. Эффективным маскирующим веществом, значительно повышающим селективность метода, является комплексон III. В тартратной или цитратной среде при рН 8—9 этот реагент маскирует Fe, Mn, Ni, Со, а также Cd, Pb, Zn и РЗЭ, образующие с диэтилдитиокарбаматом бесцветные комплексы. Среди тех металлов, которые дают окрашенные соединения с карбаматом, не маскируются, кроме меди, только висмут и таллий (Ш). После восстановления таллия до Т1(1) он уже не мешает определению меди. Из экстракта, содержащего карбамат меди и висмута, 5 н. раствором соляной кислоты можно извлечь висмут (встряхивать в течение 30 сек). Цианиды разлагают карбамат меди, а комплекс висмута остается неизмененным.
Определению меди, кроме цианидов, мешают также гипосульфиты, окислители и восстановители, которые могут восстановить Cu(ll) до Cu(I) или окислить диэтилдитиокарбамат натрия.
Определение меди усложняется также в связи с тем, что диэтилдитиокарбамат натрия нерастворим в органических растворителях. Кроме того, этот реагент довольно легко разлагается в кислых растворах на диэтиламин и сероуглерод.
Иногда вместо диэтилдитиокарбамата натрия используют диэтилдитио-карбамат диэтиламмония, который растворяется в хлороформе и устойчив к действию кислот.
Исследуемый раствор, содержащий Си(П), осаждают хлороформным раствором реагента.
Шедивец и Вашак избежали мешающего действия некоторых металлов (например, железа, марганца, цинка) на определение меди путем замены диэтилдитиокарбамата натрия карбаматом свинца. При встряхивании раствора этого реагента в хлороформе с водным раствором, содержащим медь, происходит реакция замещения. Этой реакции могут мешать металлы, комплексы которых более прочны, чем комплекс свинца; к числу таких металлов относятся Hg, Ag, Tl(III) и частично Bi. Креймер и Ломехов исследовали кинетику этой реакции.
Дибензилдитиокарбамат цинка менее селективен, чем диэтилдитиокарбамат свинца, но более устойчив в сильно кислой среде, он растворяется в четыреххлористом углероде и хлороформе. С помощью этого реагента можно экстрагировать медь из 1—2 н. соляной или серной кислоты.
Кроме указанных дитиокарбаматов для фотометрического определения меди рекомендуют также пирролидиндитиокарбамат натрия, пиперазин-бис-(дитиокарбамат) натрия и диэтанолдитиокарбамат калия.
Диэтилдитиокарбамат натрия используют для определения меди в цинке, кадмии, свинце, сурьме, титане и цирконии и других металлах, графите, органических соединениях, нефти, сточных водах, воде, почве и растительных материалах.
Метод с применением диэтилдитиокарбамата свинца используют для определения меди в различных металлах, растворах никеля и кобальта и воде.
Дибензилдитиокарбамат цинка нашел применение при определении меди в органических соединениях, пищевых продуктах, растительных материалах, воде и фосфатах.
Экспериментальная часть
Пробоотбор
Сапропель
Объект исследования – сапропель (Белгородская область. Красногвардейский район река Тихая Сосна.) Отбор пробы производился по гостовской методике с поверхности залежи сапропеля по 5 л после спуска озера в 10 точках. Река Тихая Сосна берет начало на южных склонах Среднерусской возвышенности (Волоконский район) и несет свои воды по Красногвардейскому, Красненскому и Алексеевскому районам, впадая в Дон. Общая длина реки 161 км, в пределах Белгородской области - 105 км, ширина от 10 до 50 м, пойма большей частью луговая, частично заболоченная. В пойме и по берегам преобладают лиственные леса из дуба - черешчатого, березы, сосны обыкновенной. По левому берегу распространена луговая растительность, основу которой составляют злаковые, бобовые, осоки, подмарейник настоящий, тысячелистник, клевер горный. На реке Тихая Сосна в Красногвардейском районе, находится пойменное озеро-старица. Прибрежная зона озера покрыта тростником, кувшинками, рдестом, элодеей, а на поверхности в большом количестве растет ряска. Данное озеро относится к дистрофным озерам из-за ежегодного накопления в ложе органических остатков.
Подготовка сорбентов к работе
Бурый уголь
Бурый уголь, измельчали в шаровой мельнице, просеивали через сита c определенным размером отверстий и высушивали до постоянной массы. Для экспериментов брали фракцию с размером частиц 0,5-2 мм.
Сапропель
Пробы усреднялись. Сушка сапропеля производилась на воздухе при комнатной температуре. Измельчали сапропель в мельнице.
Выделение гуминовых кислот
Гуминовые кислоты (ГК) выделяли из деминерализованного сапропеля обработкой 2- и 12%- ными растворами HCl и 0,1 н водным раствором NaOH: одна порция (ГК 1) при комнатной температуре, другая (ГК 2) – при температуре кипения водяной бани; продолжительность выделения в обоих случаях составляла 2 часа. Данную операцию повторяли многократно (6 – 8 раз) до полного выщелачивания ГК. Раствор гуматов затем разлагали 5 %-ным раствором HCl. Выпавший осадок ГК отфильтровывали через взвешенный фильтр «синяя лента», тщательно отмывали дистиллированной водой, ставили на 24 часа на диализ, сушили в сушильном шкафу при t=40 0С и взвешивали.
Характеристика сорбентов
Элементный анализ
Элементный анализ выполнялся на автоматическом анализаторе (фирмы «Карло Эрба», модель 1100, Италия).
Условия: температура в реакторе сжигания 1100С; наполнитель – Cr2O3/CuO; газ-носитель – He. Температура в восстановительном реакторе 650С; наполнитель – Cu - стружка. Температура хроматографической колонки - 127С; стационарная твердая фаза – хромосорб-12; детектор – катарометр по теплопроводности. Окислитель – AgMnO4; стандарт – 9-нитроантрацен.
Технически характеристики
3.3.2.1 Методика определения зольности
Предварительно взвешенные тигли прокаливали в муфельной печи при 800 0С в течение 1,5 часов. Затем охлаждали в эксикаторе, взвешивали и снова прокаливали в муфельной печи в течение 30 минут, охлаждали и взвешивали. Далее брали навеску образца (1,5г краснодарского сапропеля и бурого угля), вносили в тигель и помещали в муфельную печь на 1,5 часа при температуре 800 0С, охлаждали и взвешивали. Затем в течение 30 минут снова прокаливали, доводили до постоянной массы и взвешивали.
3.3.2.2 Методика определения влажности
Предварительно взвешенные тигли прокаливали в муфельной печи при 800 0С в течение 1,5 часов. Затем охлаждали в эксикаторе, взвешивали и снова прокаливали в муфельной печи в течение 30 минут, охлаждали и взвешивали. Далее брали навеску образца (1,5г краснодарского сапропеля и бурого угля), вносили в тигель и помещали в сушильный шкаф на 1,5 часа при температуре 110 0С, охлаждали и взвешивали. Затем в течение 30 минут снова прокаливали, доводили до постоянной массы и взвешивали.
3.3 Методика определения содержания меди спектрофотометрически
Фотометрическое определение меди проводили на фотоэлектрокалориметре КФК-3.
Для построения градуировочного графика готовили 14 стандартных растворов, содержащих 0,5, 1,5, 2,5, 3,5, 5,5, 6,5, 8,5, 9,5, 10,5, 12,5, 13,5, 16,5, 17,5, 18,5 мг меди в 25 см3 раствора. Для этого в мерные колбы вместимостью 25 см3 вносили расчетный объем рабочего раствора с концентрацией 1 мг/мл, добавляли в каждую колбу 5 см3 5% -ного раствора аммиака и доводили объёмы колб до метки дистиллированной водой. Для приготовления раствора сравнения в колбу на 25 см3 приливали 5 см3 5% - ного раствора аммиака и доводили до метки дистиллированной водой. Все приготовленные стандартные растворы фотометрировали при 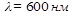 относительно раствора сравнения. На основании полученных результатов строили градуировочный график в координатах: оптическая плотность от концентрации меди (рис. 1). Для выбора оптимальной длины волны строили спектральную характеристику самого концентрированного стандартного раствора определяя оптическую плотность при разных длинах волн.
относительно раствора сравнения. На основании полученных результатов строили градуировочный график в координатах: оптическая плотность от концентрации меди (рис. 1). Для выбора оптимальной длины волны строили спектральную характеристику самого концентрированного стандартного раствора определяя оптическую плотность при разных длинах волн.
Для выбора оптимальной длины волны строили спектральную характеристику самого концентрированного стандартного раствора определяя оптическую плотность при разных длинах волн.
К анализируемому раствору приливали 1 см 3 раствора HNO3 (1:1), доводили pH до 8-9 растворами натриевой щелочи или серной кислоты, приливали 10 см3 раствора аммиака и доводили объём до 50 см3 дистиллированной водой. Подготовленную пробу фотометрировали относительно раствора сравнения, пользуясь градуировочным графиком, находили содержание меди в анализируемом растворе.
Оптическая плотность

Рисунок 1 Градуировачный график для определения концентрации меди
Технические характеристики
Были доведены до постоянной массы бурой уголь и сапропели (белгородский и краснодарский). По методике, проведенной в соответствии с ГОСТами: ГОСТ 11022-90, ГОСТ 11306-83, была определена зольность бурого угля и сапропелей и влажность (определена в соответствии с ГОСТом 11305-83. Данные представлены в таблице 6.
Зольность и влажность бурого угля и сапропелей Таблица 6
| Влажность, % | Зольность, % | Органическое вещество, % | |
| Бурый уголь | 6,9±0,2 | 0,1793±0,0009 | 99,8±0,2 |
| Сапропель (Белгород) | 3,9±0,1 | 82,8±0,0 | 13,2±0,1 |
| Сапропель (Краснодар) | 0,023±0,004 | 84,0±0,2 | 16,0±0,2 |
Элементный анализ
Проводили анализ исходных образцов (бурого угля и сапропелей) на содержание углерода, азота и водорода по методу органического анализа. Результаты анализа представлены в таблице 7.
Элементный анализ образцов Таблица 7
| Сорбент | Исходная навеска, масс. % daf | ОМ, масс. % | ||||||
| С | Н | N | С | H | N | O+S | H/C | |
| Бурый уголь | 50,0 | 4,0 | 1,4 | 66,4 | 0,6 | 1,9 | 31,1 | 0,01 |
| Сапропель (Белгород) | 4,6 | 5,1 | 4,0 | 64,7 | 5,1 | 4,0 | 26,2 | 0,08 |
| Сапропель (Краснодар) | 3,9 | 0,7 | 0,3 | 28,5 | 0,6 | 1,8 | 69,1 | 0,02 |
Выделение гуминовых кислот
Методика выделение гуминовых кислот описана в экспериментальной части в пункте [2.3.]. Выход ГК представлен в таблице 9:
Выход гуминовых кислот Таблица 9
| Название образца | Выход, мас.% ОМ |
| Гуминовые кислоты выделенные из сапропеля (Белгород) | 11,2 |
| Гуминовые кислоты выделенные из бурого угля | 54,9 |
Элементный анализ
По гостовским условиям был произведен элементный анализ на определение содержания углерода, азота и водорода гуминовых кислот, выделенных из сапропеля и бурого угля.
Элементный анализ образцов Таблиуа 9.1
| Сорбент | Исходная навеска, масс. % daf | ОМ, масс. % | ||||||
| С | H | N | С | H | N | O+S | H/C | |
| ГК из бурого угля | 38,4 | 3,4 | 1,0 | - | - | - | - | - |
| ГК из сапропеля (белг.) | 42,7 | 3,4 | 2,6 | 64,7 | 5,1 | 4,0 | 26,2 | 0,08 |
Исходя из результатов гуминовые кислоты, выделенные из бурого угля и белгородского сапропеля близки по элементному анализу.
ИК-спектры ГК
Проведен анализ снятия данных по ИК-спектроскопии гуминовых кислот, выделенных из бурого угля и белгородского сапропеля.
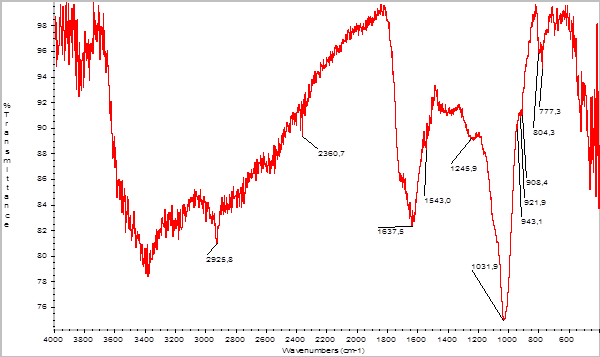
Рисунок 2.ИК-спектр гуминовых кислот, выделенных их сапропеля
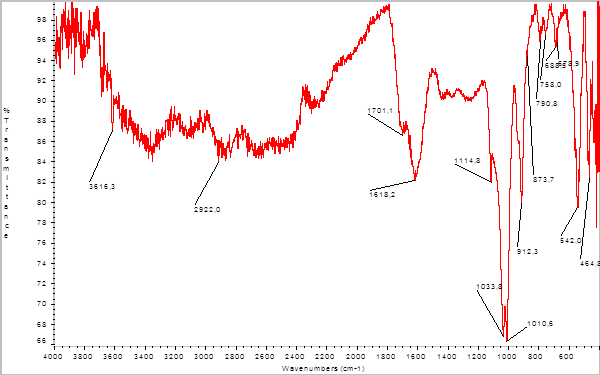
Рисунок 3.ИК-спектр гуминовых кислот, выделенных из бурого угля
Соотношение интенсивностей полос для гуминовых кислот Таблица 10
| Образец | ICOOH (1700) | IOH (3400) | ICOOH/ IOH |
| Гуминовые кислоты из сапропеля (Белгород) | 85,297 | 78,142 | 1,0916 |
| Гуминовые кислоты из бурых углей | 86,584 | 85,444 | 1,0133 |
Из приведенных результатов видно, что отношение интенсивностей карбоксильных и гидроксильных групп гуминовых кислот, выделенных из белгородского сапропеля и бурого угля имеют близкие значения.
Выводы
8. Бурый уголь, сапропели, а также гуминовые кислоты охарактеризованы методами элементного анализа и ИК-спектроксопией.
9. Показано, что ГК, выделенные из бурого угля и сапропелей имеют близкие элементный состав и соотношение карбоксильных и гидроксильных групп и могут быть выделены: из бурого угля выход составляет 54,9%; из белгородского сапропеля выход составляет 11,2%.
10. Изучение кинетических кривых рН(t) и Г(t) показало, что равновесие сорбции устанавливается за 20 – 30 минут.
11. Изучение изотерм сорбции позволяет распределить сорбенты в ряд по увеличению сорбируемости:
ГК (выделенные из бурого угля)<минеральный сорбент<модифицированный минеральный сорбент<ГК (выделенные из белгородского сапропеля)<бурый уголь<остаток бурого угля после выделения ГК<остаток белгородского сапропеля после выделения ГК<белгородский сапропель<краснодарский сапропель.
Список литературы
[1]. Современные проблемы экологии и рационального природопользования в тульской области: Доклады 5-й региональной научно-практической конференции./Под редакцией Э.М. Соклова. – Тула: Изд-во ТулГУ, 2006. – 194с.
[2]. Аширов А. Ионообменная очистка сточных вод, растворов и газов. – Л.: Химия, 1983. – 296с.
[3]. Мелехова Н.И. Внутренние сырьевые ресурсы в агропромышленном комплексе. Демидовские чтения. Второй юбилейный выпуск. – Тула, 1996. – с.33-39.
[4]. Жуков А.И., Монгайт И.И., Родзиллер И.Д. Методы очистки производственных сточных вод. – М.: Стройиздат, 1977. С.84-85.
[5]. Вишнякова Л.Г., Мелехова Н.И. Применение медно – аммиачного раствора в качестве комплексного микроудобрения. Информационный листок. – Тула: ЦНИТИ, №84-89. – с.2-3.
[6]. М.И. Гельфман, Ю.В. Тарасова, Т.В. Шевченко. Химическая промышленность, 2002, №2 – с.20-26.
[7]. Орлов Д.С. Гумусовые кислоты почв и общая теория гумификации. М. Изд-во МГУ 1990г. – 325с.
[8]. Пунтус Ф.А., Бамбалов Н.Н., Смычкин Т.П. Исследование перефирической части гуминовых кислот, торфа и сапропелей.//Проблемы использования сапропелей в народном хозяйстве. – Минск: Наука и техника. 1976г. – с.115-122.
[9]. З. Марченко. Фотометрическое определение элементов. Изд-во «Мир» М.1971.
[10]. Вязова Н.Г., Крюкова В.Н., Латыше В.П. Сорбционные свойства гуминовых кислот. Химия твердого топлива №6 – 1999.
Литературный обзор
Сорбция меди на различных сорбентах
Дата: 2019-05-28, просмотров: 365.