Опыты с капроном. Капрон 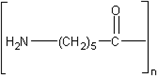 рассматривается в курсе химии в связи с изучением аминокислот. Синтез капрона пока не разработан в качестве школьного опыта, хотя принципиально он вполне доступен. С капроном (в виде волокон, кусочков ткани, технических деталей) могут быть проведены следующие опыты.
рассматривается в курсе химии в связи с изучением аминокислот. Синтез капрона пока не разработан в качестве школьного опыта, хотя принципиально он вполне доступен. С капроном (в виде волокон, кусочков ткани, технических деталей) могут быть проведены следующие опыты.
а) В три пробирки с концентрированной серной кислотой, 10-процентным раствором щелочи и ацетоном помещают образцы капрона. Замечают, что растворение капрона происходит только в кислоте.
б) Нагревают капрон в пробирке на пламени горелки. Сначала он размягчается, затем плавится (216°С), при дальнейшем нагревании разлагается, выделяя летучие продукты с неприятным запахом.
в) Поджигают капроновое волокно. Оно горит с трудом, плавясь и образуя твердый, янтарного цвета шарик.
г) Кусочек капроновой смолы или свернутые в комочек обрывки трикотажного изделия нагревают в щипцах над пламенем горелки. Когда капрон начнет размягчаться и сделается вязким, прикасаются к нему лучинкой или стеклянной палочкой и, отводя затем ее быстро в сторону, вытягивают тонкие нити капрона, которые оказываются при этом довольно прочными.
Распознавание пластмасс. К окончанию курса органической химии у учащихся накопились уже достаточно сведений о пластмассах как теоретического, так и практического характера. Это позволяет поставить работы по распознаванию некоторых видов пластмасс.
Изделия из полиэтилена легче воды, жирные на ощупь, при нагревании быстро размягчаются, горят голубоватым пламенем, при этом ощущается слабый запах расплавленного парафина. В термостате при температуре 100—120°С они размягчаются. Для опыта могут быть использованы полиэтиленовая электроизоляция, пленочные материалы, флаконы, пробки от бутылок и т.д.
Полихлорвиниловые материалы распознаются по отщеплению хлороводорода при нагревании исследуемого образца в пробирке (обрезки клеенки, накидки, электроизоляции и т.п.). Хлороводо-род определяется по запаху, с помощью влажной лакмусовой бу-
мажки или по образованию дымка хлорида аммония при поднесении к пробирке палочки, смоченной раствором аммиака. Полихлорвинил горит в пламени с обильным выделением копоти. Размягчается при температуре около 60—66°С.
Изделия из политетрафторэтилена жирные на ощупь, матового цвета, напоминают по внешнему виду воск, не горят, плавятся лишь в сильном пламени.
Полистирол бывает прозрачный и непрозрачный, легко размягчается при нагревании, горит коптящим пламенем, выделяя при этом запах мономера. Изделия из полистирола хрупки, при постукивании звенят. Размягчается полистирол при 80°С. В качестве образцов для исследования могут быть использованы вазочки, розетки, обломки шкатулки, детские игрушки и т.п.
Полиметилметакрилат (листовое органическое стекло, письменные приборы, линейки, ручки, зубные щетки и т.д.) внешне очень похож на прозрачный полистирол. Отличить от последнего его можно по отсутствию звонкости и хрупкости, горит голубоватым пламенем без копоти, при этом слышится характерное потрескивание и выделяется эфирный запах.
Фенолформальдегидные пластмассы используются при изготовлении различных электродеталей черного и темно-коричневого цвета (штепсельные розетки, выключатели, телефонные трубки и другие изделия). При нагревании они не размягчаются и не плавятся, а разлагаются, при этом обнаруживается запах фенола и формальдегида. Фенол можно обнаружить, если порошкообразную пластмассу прокипятить в течение 20—30 мин с водой и затем на профильтрованный раствор подействовать бромной водой или раствором хлорида железа. Горят фенопласты только в пламени.
БЕЛКИ
Несмотря на большое значение белков, школьный эксперимент по этой теме сравнительно беден. Он сводится обычно к опыту свертывания белка при нагревании и 1—2 цветным реакциям. В дополнение к этим работам следует считать весьма целесообразными опыты по обнаружению отдельных элементов в белках и опыты, иллюстрирующие коллоидное состояние белков в растворах.
Открытие к белках азота. Если понятие об определении углерода, водорода и галогенов было дано в первых темах курса органической химии, то здесь, прежде всего, следует ознакомить учащихся с открытием в белках азота и серы.
В пробирку помещают немного сваренного вкрутую или жидкого яичного белка, прибавляют двойное количество измельченной натронной извести и нагревают. В присутствии щелочи азот выделяется из белка в виде аммиака, который обнаруживают по запаху, по посинению поднесенной к отверстию пробирки влажной лакмусовой бумажки или при помощи стеклянной палочки, смоченной концентрированной соляной кислотой.
Открытие в белках серы. Сущность опыта состоит в том, что органическое вещество разрушают нагреванием со щелочью или сплавлением с металлическим натрием. Сера при этом выделяется в виде сульфида натрия Na2S, после чего се нетрудно открыть по образованию характерного осадка сульфида свинца PbS.
Осторожно нагревают в пробирке яичный белок или кусочек белой шерсти с концентрированным раствором щелочи до полного растворения белка. Образующийся сульфид натрия переходит в раствор. К полученному раствору приливают ацетат свинца. Выпадает черный осадок сульфида свинца.
Примечание. Открытие азота и серы можно провести в одном опыте. Белок кипятят с крепким раствором щелочи. Обнаруживают выделяющийся аммиак. После растворения белка разбавляют раствор водой и прибавляют раствор свинцовой соли.
Дата: 2019-05-28, просмотров: 337.