При изучении углеводородов учащиеся узнали, как строение углеродного скелета влияет на свойства вещества. При изучении спиртов расширяется круг их структурно-химических представле-
ний: они начинают знакомиться с функциональными группами атомов в молекулах органических соединений. Поэтому в данной теме имеют большое значение опыты, иллюстрирующие химические свойства, обусловленные функциональной группой.
Кроме того, экспериментальное ознакомление с получением и свойствами спиртов важно для понимания широкого использования их в технических целях.
ЭТАНОЛ (ЭТИЛОВЫЙ СПИРТ)
Этиловый спирт, как наиболее важный и распространенный представитель класса предельных одноатомных спиртов, изучается наиболее подробно. На нем выясняется и характерное строение спиртов.
В связи с доступностью исходного вещества представляется возможным изучение вести в строго логическом плане — рассмотреть вначале физические свойства, затем химические свойства вещества и т.д., не перемешивая со способами получения, как было в предыдущих темах.
Удельный вес спирта и изменение объема при смешении с водой. В цилиндр наливают 20 мл воды и вливают осторожно по стенке 20 мл подкрашенного спирта. Спирт располагается слоем сверху.
Стеклографом отмечают верхний уровень жидкости. Цилиндр закрывают и взбалтывают жидкость. Отмечают верхний уровень жидкости после смешения спирта с водой. Учащиеся видят, что произошло уменьшение объема. Нескольким учащимся можно дать цилиндр со смесью в руки; они убеждаются, что при смешении произошло разогревание, следовательно, растворение не было чисто физическим процессом.
Обнаружение воды в спирте. Безводный спирт, ректификат и спирт, разбавленный водой, наливают в демонстрационные пробирки или стаканы и прибавляют небольшие количества обезвоженного медного купороса (CuSO4). Содержимое пробирок взбалтывают. В первой пробирке соль не синеет (нет воды для образования кристаллогидрата CuSO4 • 5Н2О), во второй синеет постепенно, в третьей происходит быстрое посинение соли.
Обнаружение высших спиртов (сивушного масла) в спирте. Для обнаружения высших спиртов используют их нерастворимость в воде.
В два сосуда наливают спирт-сырец и ректификат. К тому и другому приливают двойное количество воды. После перемешивания палочкой раствор спирта, содержащий сивушное масло, мутится вследствие образования эмульсии нерастворимых гомологов.
При этом запах «сивухи» значительно усиливается. Раствор ректификата остается прозрачным.
Концентрированна раствора спирта. Пользуясь свойством некоторых солей давать кристаллогидраты с водой и нерастворимостью их в спирте (например, поташа К2СО3), можно в значительной степени выделить спирт из раствора. К водному раствору, содержащему примерно поровну спирта и воды, прибавляют сухой карбонат калия до тех пор, пока он не перестанет растворяться и жидкость не расслоится. Внизу образуется слой водного раствора поташа, сверху — крепкий раствор спирта. Берут пипеткой немного спирта из верхнего слоя и поджигают в фарфоровой чашке. В отличие от исходного раствора спирт после высаливания легко загорается. Концентрированный спирт может быть использован в дальнейшем для опытов.
Получение абсолютного спирта. Безводный этиловый спирт требуется для некоторых демонстрационных опытов по органической химии. В качестве исходного вещества берут спирт, содержащий наименьшее количество воды, например спирт-ректификат, содержащий 96% С2Н5ОН.
Так как остающиеся в ректификате 4% воды не могут быть отделены перегонкой (спирт и вода в этом соотношении образуют азеотропную смесь с постоянной точкой кипения и перегоняются одновременно как индивидуальное вещество), то для окончательного удаления воды пользуются химическим способом. Спирт обрабатывают веществами, реагирующими с водой, но не действующими на спирт. Образующиеся при этом продукты реакции должны легко отделяться от спирта. Чаще всего пользуются для этой цели водоотнимающимися средствами. Очевидно, Что применение концентрированной серной кислоты для этой цели исключено, так как она взаимодействует не только с водой, но и со спиртом. Непригоден и гранулированный хлорид кальция, так как он реагирует со спиртом, давая нелетучее соединение ЗСаСI2 • С2Н5ОН. Для обезвоживания спирта применяют свежеприготовленную негашеную известь СаО.
В колбу со спиртом насыпают извести столько, чтобы она касалась поверхности жидкости. Закрывают колбу резиновой пробкой, встряхивают смесь в течение нескольких минут и оставляют до следующего дня. После этого из смеси отгоняют спирт в приемник, предохраняемый от атмосферной влаги хлоркальциевой трубкой.
Обезвоживание можно провести быстрее, если на один объем спирта взять примерно 1/5 объема извести, смесь прокипятить в течение 2 ч в колбе с обратным холодильником и после этого сразу произвести отгонку.
Почти безводный спирт можно получить, настаивая его с прокаленным медным купоросом. Через несколько дней спирт декантируют с сульфата меди и обрабатывают второй порцией этой же соли. Если после этого сульфат меди не синеет, спирт отгоняют. Образовавшийся продукт оказывается пригодным для школьных опытов, требующих безводного спирта.
Спирт — растворитель.
а).Приготовление лака. Наливают в пробирку 1/4 ее объема спирта и растворяют в нем 2—3 г какой-либо смолы. Для быстрого растворения пробирку можно подогреть в стаканчике с горячей водой. Получившийся лак можно подкрасить какой-нибудь краской. С помощью ватки слой лака наносят на гладкую поверхность дерева.
б). Приготовление йодной тинкстуры. В две пробирки помещают равные количества измельченного иода; в одну пробирку приливают воду, а в другую столько же спирта.
Наблюдается быстрое растворение иода в спирте и плохая растворимость его в воде. Полученный спиртовой раствор иода может быть использован в школьной аптечке.
В пробирку с иодом и водой бросают несколько кристалликов иодида калия и смесь встряхивают. Наблюдается растворение иода.
Горение спирта. Спирт воспламеняется не только при поджигании, но и при действии ряда энергичных окислителей. Горение спирта выражается уравнением:
С2Н5ОН + ЗО2 à 2СО2 + ЗН2O
Приводимые ниже опыты свидетельствуют одновременно о сравнительно легкой окисляемости спирта.
а) Спирт, налитый в фарфоровую чашку, поджигают лучинкой; он горит бледно-голубым пламенем. Тушат пламя, покрывая чашку стеклом.
б) На металлическую пластинку помещают кристаллы оксида хрома (VI) СгО3 и с небольшой высоты опускают на них из пипетки несколько капель спирта. Спирт вспыхивает. При этом оксид хрома(VI) превращается в зеленый оксид хрома (III).
в) На фарфоровой пластинке к небольшому количеству измельченного перманганата калия добавляют концентрированной серной кислоты столько, чтобы получилась густая кашица. На образовавшийся оксид марганца (VII) капают несколько капель спирта. Спирт вспыхивает.
Обнаружение спирта в вине или пиве. В круглодонную колбу наливают 50—100 мл пива или вина, колбу закрывают пробкой с вертикальной стеклянной трубкой. Нагревают колбу до кипения и
через некоторое время поджигают пары спирта у верхнего конца трубки. Пиво предварительно должно быть хорошо взболтано для удаления углекислого газа, иначе при нагревании будет происходить сильное вспенивание.
Взаимодействие спирта с натрием. Реакция спирта с натрием — это первый опыт, показывающий резкое отличие химических свойств спирта от свойств предельных углеводородов. Назначение опыта: ознакомить учащихся с характерной для спиртов реакцией и продуктами, получающимися при этом.
В маленькую пробирку с 1—2 мл абсолютного спирта бросают 2-3 маленьких кусочка натрия. Наблюдают выделение газа. Пробирку закрывают пробкой с маленькой стеклянной трубочкой, конец которой оттянут. Выждав некоторое время, пока будет вытеснен из пробирки воздух, поджигают выделяющийся газ — водород.
После того как весь натрий прореагирует, пробирку охлаждают в стакане с водой. При охлаждении выпадает осадок алкоголята натрия. Если алкоголят не выделяется, раствор выливают в фарфоровую чашечку и осторожно выпаривают над пламенем спиртовки непрореагировавший спирт. Если, наоборот, натрий прореагировал не полностью, избыток его удаляют или заставляют прореагировать, добавляя немного спирта.
К алкоголяту натрия добавляют немного воды и 1—2 капли раствора фенолфталеина. Индикатор показывает щелочную реакцию. Обращают внимание учащихся на то, что для правильных выводов спирт должен быть безводным и что натрий должен прореагировать со спиртом полностью.
Если опыт ставится в большем масштабе, то выделение водорода дополнительно доказывается появлением паров воды при горении его под сухим стаканом.
Дегидратация этанола. Структурная формула этанола может быть подтверждена при изучении его дегидратации, идущей с образованием этилена.
В качестве катализатора для реакции лучше взять оксид алюминия, так как серная кислота, поглощая воду, не даст возможности ее обнаружить.
Собирают прибор, как показано на рис. 21. В фарфоровую или железную трубку насыпают оксид алюминия АI2О3, в делительную воронку наливают абсолютный спирт, в маленькую колбочку с отводной трубкой помещают обезвоженный сульфат меди. Нагревания до необходимой температуры можно достичь с помощью нескольких горелок.
Когда трубка с катализатором будет нагрета, пускают спирт по
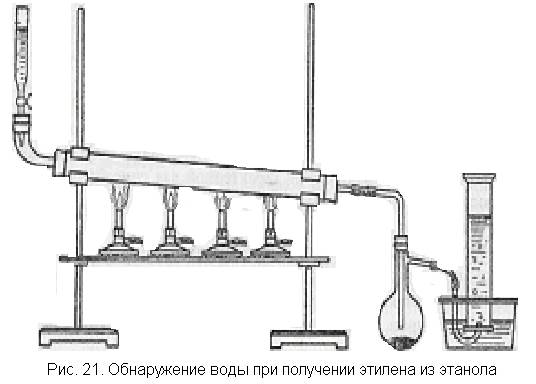
1 капле в секунду. Образующаяся вода не может остаться в нагретой трубке и в виде паров поступает в колбу, где конденсируется и образует с сульфатом меди синие кристаллики медного купороса. В цилиндре после вытеснения из прибора воздуха собирают этилен и затем проводят с ним одну из характерных реакций.
Для подтверждения структурной формулы спирта важно установить, что образование молекулы воды происходит за счет одной, а не двух молекул спирта. Можно было бы предположить, что вода отщепляется по схеме:
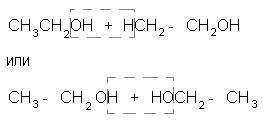
и образуются вещества без двойных связей в молекулах. Однако изучение собранного газа не оставляет сомнений, что он представляет собой непредельное соединение, т.е. что молекула воды отщепилась от одной молекулы спирта:
СН3 - СН2ОН à СН2 = СН2 + Н2О
Взаимодействие спирта с бромоводородом. Бромистоводородной кислотой школьные лаборатории обычно не располагают, поэтому в данном опыте получают бромоводород непосредственно в том сосуде, где должна пройти его реакция со спиртом. Исходными веществами являются: спирт, бромид калия и концентрированная серная кислота.
Учителю, однако, следует иметь в виду, что всякий раз, когда в
смеси содержатся спирт и серная кислота, прежде всего идет реакция между ними с образованием этилсерной кислоты:
С2Н5ОН + НО - SO2OH à Н2О + С2Н5 - О - SO2OH
которая и вступает в дальнейшие реакции. В данном случае она реагирует с бромидом калия:
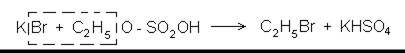
Собирают типовой прибор для перегонки жидкостей и в колбу помещают смесь, состоящую из 10 мл концентрированной серной кислоты и 10 мл этанола, происходит образование этилсерной кислоты. Охладив колбу, добавляют 10 мл воды и 5-7 г бромида калия. Колбу закрывают пробкой и нагревают на сильном пламени через асбестовую сетку. Для большего выхода продукта необходимо применение водяного холодильника (температура кипения С2Н5Вг 38,4°С). С этой же целью в приемник наливают холодную воду и даже помещают несколько кусочков льда и ставят приемник в сосуд с водой и льдом.
Капли тяжелого бромэтана при перегонке падают на дно. Внизу образуется слой маслянистой жидкости. Опыт прекращают, когда отогнано необходимое количество вещества, для чего вначале убирают приемник, а затем тушат горелку. Бромэтан может быть показан классу под водой. Параллельно демонстрируется чистый образец. Извлечение и очистка продукта производятся на внеклассных занятиях; полученный бромэтан демонстрируют при опросе на следующем уроке.
Для извлечения чистого вещества бромэтан отделяют с помощью делительной воронки, затем добавляют к нему двойное количество воды, взбалтывают, чтобы в ней растворились перегнавшиеся спирт, кислоты и различные продукты разложения, снова отделяют водный слой и сушат от остатков воды несколькими кусочками хлорида кальция. После этого бромэтан становится совершенно прозрачным и бесцветным.
В химическом кружке чистый бромэтан может быть получен в значительно большем количестве для демонстрационной коллекции и целого ряда опытов с ним (например, для синтеза углеводородов).
Получение иодэтана. Иодэтан легко образуется при непосредственном воздействии иодоводорода на спирт. Для этого не требуется даже присутствия водоотнимающего средства. Достаточно прокипятить в колбе с обратным холодильником смесь спирта с концентрированной иодистоводородной кислотой в отношении примерно 1: 3 и затем разбавить водой, чтобы внизу выделился слой иодэтана.
Можно получить иодэтан и насыщением спирта газообразным иодоводородом .
Отсутствие иодистоводородной кислоты в школе прежде всего наводит на мысль получать иодэтан методом, аналогичным получению бромэтана. Однако, как известно, при взаимодействии иодида калия или натрия с концентрированной серной кислотой образующийся иодоводород легко окисляется, что делает этот способ практически неприемлемым.
Иодэтан чаще всего получают взаимодействием спирта с иодидом фосфора (III). В качестве исходных веществ для реакции берут спирт, иод и фосфор. Два последних вещества реагируют, образуя Р13, который сразу же взаимодействует со спиртом.
З С2Н5ОН + PI3 à 3 С2Н5I + Н3РO3
В круглодонную колбу наливают 15 мл этанола и помещают 2 г красного фосфора, высушенного в эксикаторе над концентрированной серной кислотой. Затем частями добавляют 18—20 г йода, закрывая после каждого прибавления колбу пробкой с вертикальной трубкой-холодильником и тщательно взбалтывая. Иод вносят частями для того, чтобы реакция не шла слишком бурно. Если смесь сильно разогревается, колбу охлаждают в холодной воде. Чтобы смесь имела жидкую консистенцию и хорошо перемешивалась при встряхивании, берется избыток спирта по отношению к теоретическому.
После того как весь иод внесен, колбу закрывают пробкой с вертикальной трубкой и нагревают в течение 20-30 мин на водяной бане. Затем, присоединив вместо трубки обычный нисходящий холодильник, отгоняют иодэтан.
Собирающийся в приемнике иодэтан оказывается окрашенным йодом, частично улетучивающимся при перегонке, и содержит примесь спирта. Очищают дистиллят от примеси йода, добавляя по каплям раствор едкого натра до исчезновения бурой окраски. Гидроксид натрия реагирует с йодом:
2 NaOH + I2 à Nal + NalO + Н2О
Водный слой удаляют с помощью делительной воронки. Для окончательного удаления продуктов реакции йода со щелочью и спиртом иодэтан промывают еще раз водой и наконец сушат гранулированным хлоридом кальция.
Собранный продукт может быть взвешен и таким образом определен выход вещества.
Качественная реакция на спирт. Чувствительной реакцией на этиловый спирт (хотя и недостаточно специфичной) является так называемая иодоформная проба: образование характерного желтого осадка йодоформа при действии на спирт йода и щелочи. При этом последовательно протекают следующие реакции:
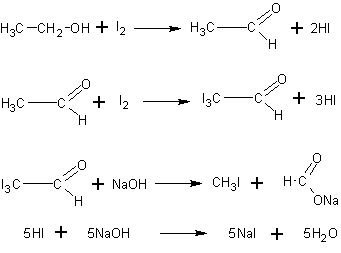
или суммарно:
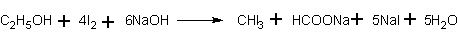
Таким способом удается установить наличие спирта в воде даже при концентрации 0,05%.
Знание иодоформной реакции (хотя бы по внешним проявлениям, без химизма процесса) помогает при изучении спирта и дает возможность поставить целый ряд интересных опытов с ним (например, получение спирта гидратацией этилена по А.М.Бутлерову).
1. В пробирку с исследуемой жидкостью бросают очень немного (1-2 кристаллика) истолченного йода или приливают 1—2 мл раствора его в иодиде калия. Смесь нагревают и приливают понемногу раствор едкого натра до обесцвечивания избытка йода. При охлаждении выпадают кристаллы йодоформа.
При малой концентрации спирта ясно ощущается лишь запах йодоформа, а кристаллы образуются после более или менее длительного стояния (например, на следующий день).
2. Когда подобный опыт нужно поставить не с целью качественного определения спирта, а для получения значительных количеств йодоформа, то его видоизменяют следующим образом. В колбу наливают 20 мл спирта, 80 мл воды, добавляют 15 г поташа и столько же растертого йода. Смесь взбалтывают и нагревают на водяной бане до исчезновения окраски йода. После того как начнут выпадать кристаллы, колбу оставляют стоять до охлаждения, после чего отделяют кристаллы и промывают их декантацией, стараясь быстрее закончить работу вследствие неприятного запаха йодоформа.
Получение этилового спирта из бромэтана. Демонстрация этого опыта показывает генетическую связь между различными классами органических соединений, именно переход от предельных уг-лсиодородов через галогенопроизводные к спиртам. К сожалению, опыт, который давал бы возможность непосредственно обнаружить появление спирта, требует много времени и поэтому, начатый на уроке, он может быть закончен лишь на следующем занятии. Опыт может быть также поставлен в кружке; в таком случае доступно будет выделение полученного продукта.
В небольшую колбу помешают 4—5 мл бромэтана и 20 мл водного раствора гидроксида калия. Колбу закрывают пробкой с обратным водяным холодильником и смесь кипятят на масляной бане в течение нескольких часов, пока жидкость не станет совершенно однородной. Это будет означать, что бромэтан (нерастворимый в воде) полностью прореагировал.
Из реакционной смеси отгоняют часть жидкости и производят иодоформную реакцию.
Получение этилового спита брожением сахара. В данной теме учащиеся знакомятся с брожением, как способом получения этанола. В дальнейшем, при изучении углеводов, они узнают, что брожение — это лишь одно из звеньев в процессе получения спирта из полисахаридов — крахмала и клетчатки.
 В плоскодонную колбу (рис. 22) наливают раствор 20 г обычного сахара или глюкозы в 100 г воды. Туда же вносят 3-4 г растертых с водой дрожжей (хорошо взять пивные дрожжи). Колбу закрывают пробкой с отводной трубкой, соединенной в свою очередь с U-образной трубкой, содержащей прозрачную (свежепрофильтрованную) известковую или баритовую воду. Ко второму колену U-образной трубки присоединяют хлоркальциевую трубку с натронной известью.
В плоскодонную колбу (рис. 22) наливают раствор 20 г обычного сахара или глюкозы в 100 г воды. Туда же вносят 3-4 г растертых с водой дрожжей (хорошо взять пивные дрожжи). Колбу закрывают пробкой с отводной трубкой, соединенной в свою очередь с U-образной трубкой, содержащей прозрачную (свежепрофильтрованную) известковую или баритовую воду. Ко второму колену U-образной трубки присоединяют хлоркальциевую трубку с натронной известью.
Колбу подогревают на водяной бане до 30—35аС. Начинается процесс брожения, о котором судят по выделению пузырьков газа и помутнению раствора в U-образной трубке.
На уроке может быть констатировано лишь образование углекислого газа при брожении. Чтобы в растворе образовалось заметное количество спирта, прибор
оставляют до следующего занятия в теплом месте (например, вблизи батареи отопления или печки), учащиеся ведут за ним наблюдение. Перегрев отрицательно сказывается на процессе брожения, поэтому не следует допускать повышения температуры выше указанной.
На следующем уроке к колбе присоединяют холодильник и отгоняют небольшое количество жидкости. В дистилляте доказывают наличие спирта иодоформной реакцией.
U-образную трубку промывают раствором соляной кислоты от осадка карбоната.
Получение этанола из этилена в присутствии серной кислоты. Получение этилового спирта из этилена было подробно изучено A.M. Бутлеровым. Он получал этанод гидратацией этилена в присутствии того же катализатора — концентрированной серной кислоты, который применяется и для обратной реакции — получения этилена из спирта. А.М.Бутлеров показал, что эта реакция является общей для получения спиртов из непредельных углеводородов, и предсказал ее промышленное значение.
Сейчас реакция гидратации непредельных углеводородов широко используется в промышленности для получения различных
спиртов.
В связи с необходимостью замены пищевого сырья и утилизации газов крекинга нефти этанол в больших количествах получают из этилена.
Демонстрация этого способа в классе важна, таким образом, с трех точек зрения: учащиеся знакомятся с одной из важных экспериментальных работ нашего гениального соотечественника, получают частичное представление о путях развития современной промышленности органической химии и знакомятся с влиянием условий на направление реакции в ту или иную сторону.
Можно считать демонстрацию этого способа получения спирта в данной части курса более целесообразной, чем демонстрацию получения спирта брожением крахмала. В химизме процессов гидролиза и брожения, даже в элементарной форме, разобраться учащимся до изучения углеводов чрезвычайно трудно, химизм же гидратации этилена довольно прост. Кроме того, предлагаемый опыт способствует установлению связи с ранее изученным материалом и закреплению знаний о химических свойствах непредельных углеводородов.
Единственная методическая трудность при постановке опыта состоит в том, что при кратковременности демонстрации не удается получить значительного количества этилового спирта и доказывать образование его приходится только иодоформной реакцией.
В промышленности этиловый спирт получают из этилена без применения серной кислоты путем прямой гидратации этилена водяным паром в присутствии ортофосфорной кислоты как катализатора.
Опыт сернокислотной гидратации, в соответствии с промышленным его осуществлением, состоит из двух частей. Сначала растворяют этилен в концентрированной серной кислоте, при этом образуется моноэтиловый эфир серной кислоты.
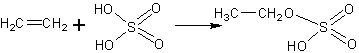
Затем растров разбавляют водой, при этом образуется этанол и освобождается серная кислота:
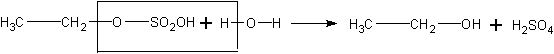
Понятно, что при изучении этого процесса в классе дается лишь суммарное уравнение реакции:
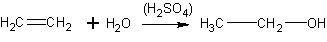
Серная кислота рассматривается как растворитель этилена и катализатор реакции (без указания механизма каталитического действия).
Лабораторная установка для проведения опыта чрезвычайно проста (рис. 23). Основную часть ее составляет прибор для получения этилена. Этилен следует пропустить через промывные склянки, чтобы спирт из колбы не попал в серную кислоту, где будет получаться спирт из этилена.
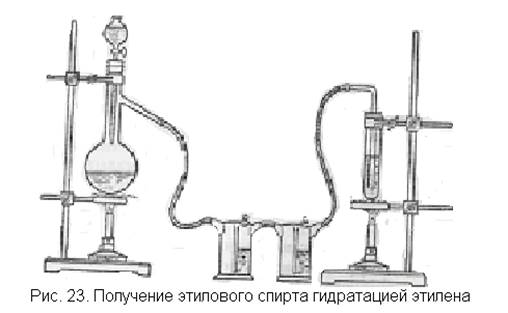
В колбу наливают смесь этанола с концентрированной серной кислотой и насыпают немного фарфоровой крошки (см. получение этилена, с. 46). Капельную воронку заполняют такой же смесью на случай, если выделение этилена в колбе быстро прекратится. К колбе присоединяют одну или две промывалки с серной кислотой для удержания паров спирта и пробирку или небольшую колбочку с концентрированной серной кислотой для поглощения этилена.
В промышленности этилен пропускают в серную кислоту под давлением в 10 ат и при нагревании до 70°С. В школьных условиях, преследуя чисто качественные, а не количественные цели опыт удается провести без применения давления.
Когда прибор собран и проверен, начинают нагревать колбу со спиртом и серной кислотой, чтобы установился равномерный ток газа. Одновременно нагревают пробирку с кислотой для поглощения этилена (примерно до 70—80"С). Во время опыта надо следить, чтобы кислоту из пробирки не перебросило в промывалку. Поэтому, если будет замечено падение давления этилена, сразу же вынимают трубку из пробирки, после чего добавляют в колбу смесь из воронки и затем снова опускают трубку. Примерно через 10 мин пропускания газа опыт прекращают. При этом сперва вынимают трубку из пробирки и только после этого прекращают нагревание.
Полученный раствор этилена в кислоте выливают понемногу в перегонную колбу, содержащую около 100 мл воды, все время охлаждая колбу в токе холодной воды, чтобы избежать потери спирта. Когда весь раствор прилит, насыпают в колбу немного фарфоровой крошки, закрывают колбу пробкой, присоединяют холодильник и в приемник отгоняют несколько миллилитров жидкости, содержащей спирт, который обнаруживают иодоформной реакций (с. 81). Раствор кислоты годен для использования при других опытах.
Опыт удается только с очень концентрированной серной кислотой или олеумом.
МЕТАНОЛ
Ряд опытов с метанолом может быть поставлен по аналогии с вышеописанным, при этом нет необходимости воспроизводить опыты в том объеме, как они ставятся при изучении этанола.
Поэтому здесь описываются опыты, характеризующие лишь некоторые особенности самого метанола.
Взаимодействие метанола с хлороводородом. Очень ле1 ко и быстро можно получить хлорметан по реакции:
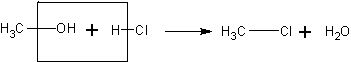
Демонстрация этого опыта подтверждает наличие гидроксильной группы в молекуле метанола. Хлорметан представляет собой газ и может быть обнаружен по цвету пламени.
1. В маленькую колбочку или пробирку с отводной трубкой наливают по 1-2 мл метанола, концентрированной соляной кислоты и концентрированной серной кислоты. При несильном нагревании смеси образуется газ, который после вытеснения воздуха собирают в цилиндр или пробирку над водой и поджигают. Хлорметан горит характерным зеленым пламенем, газ можно также поджечь у отводной трубки. Хлорметан не следует выпускать в лабораторию, так как он ядовит.
 2. В пробирку (рис. 24) наливают по 1 мл метанола и концентрированной серной кислоты и добавляют немного (на кончике ножа) прокаленной поваренной соли. Колбочку закрывают пробкой со стеклянной трубкой. При слабом нагревании образуется Хлорметан, который поджигают у отводной трубочки. При внесении в пламя стеклянного или фарфорового предмета образуется копоть, что свидетельствует о горении органического вещества.
2. В пробирку (рис. 24) наливают по 1 мл метанола и концентрированной серной кислоты и добавляют немного (на кончике ножа) прокаленной поваренной соли. Колбочку закрывают пробкой со стеклянной трубкой. При слабом нагревании образуется Хлорметан, который поджигают у отводной трубочки. При внесении в пламя стеклянного или фарфорового предмета образуется копоть, что свидетельствует о горении органического вещества.
По аналогии с образованием бромэтана уравнение реакции для простоты можно представить в следующем виде:
NaCI + H2SO4 à NaHSO4 + НСI
СН3ОН + НСI à СН3СI + H2O
На самом деле реакция идет через образование метилсерной кислоты СН3 — О — SO2OH, которая затем реагирует с хлоридом натрия, образуя Хлорметан и гидросульфат натрия:
CH3OSO2OH + NaCI à СН3СI + NaHSO4
Получение метанола при сухой перегонке дерева. Получение спирта по этому способу состоит из двух частей:
а) сухой перегонки дерева с целью получения дегтярной воды (наряду с углем, дегтем и газом) и б) выделения метанола из дегтярной воды.
Сухую перегонку дерева проводят в круглодонной термостойкой колбе с отводом (рис. 25). В колбу помещают сухие опилки и
стружку и нагревают сначала осторожно, а потом все сильнее и сильнее до тех пор, пока наблюдается обугливание дерева и образование жидких и газообразных продуктов. Приемник для дегтя и дегтярной воды ставят о ледяную воду, а выделяющиеся газы собирают путем вытеснения воды из пробирки.

Когда будет получено достаточное для демонстрации количество жидкости, опыт прекращают. При этом обращают внимание учащихся на расслоение жидкости (внизу — водный слой, сверху — деготь). С помощью делительной воронки отделяют водный слой и лакмусовой бумажкой обнаруживают присутствие кислоты.
Газообразные продукты сухой перегонки дерева собирают в два сосуда (цилиндры или пробирки). Затем в одном из них поджигают газ, который горит синеватым пламенем, а в другой приливают известковую воду для обнаружения углекислого газа в продуктах перегонки.
Для доказательства присутствия метанола в дегтярной воде уксусную кислоту нейтрализуют избытком гидроксида кальция (лакмус!) и, когда кислота будет связана, нагревают жидкость до кипения в пробирке с отводной трубкой. При поджигании пары метанола горят голубоватым пламенем.
Уксусную кислоту превращают в соль с той целью, чтобы она не улетучивалась с метанолом и не мешала распознаванию его по характеру пламени. Эта операция не усложняет понимания учащимися опыта, так как понятие о нейтрализации кислот они имеют. Присутствием ацетона в дегтярной воде при этом опыте можно пренебречь.
Для извлечения метанола берут по возможности большое количество дегтярной воды (например, 100 мл), нейтрализуют ее неболь-
шими порциями мела или известковым молоком, как было указано в предыдущем опыте, и фильтруют. Фильтрат помещают в перегонную колбу, закрывают колбу пробкой с термометром, присоединяют прямой водяной холодильник и отгоняют на водяной бане фракцию до 70—75'С. Метанол получается при этом с примесью воды и ацетона. Ацетон неизбежно летит со спиртом, так как точки кипения их близки (у метанола 65°С, у ацетона 56°С).
Сравнение свойств одноатомных спиртов. Обладая сходными химическими свойствами и составляя один гомологический ряд, предельные одноатомные спирты различаются по физическим свойствам и характеру горения. Это может быть легко показано на опытах.
а) В одинаковые цилиндры или демонстрационные пробирки наливают по 50 мл воды, подкрашенной перманганатом или бихроматом калия и добавляют по 10 мл спиртов, имеющихся в лаборатории, например, метанол, этанол, пропанол-1, пропанол-2, 2-метилпропанш1-2, бутанол, изобутанол и т.д. Энергично встряхивают содержимое цилиндров и дают жидкостям отстояться. Наблюдают, что первые гомологи растворились в воде полностью, бутанол растворяется частично, а другие не растворяются.
б) В небольшие тигли или фарфоровые чашечки наливают спирты в той же последовательности и поджигают. Наблюдают, что с увеличением молекулярного веса и содержания углерода в спиртах светимость пламени возрастает; высшие спирты горят коптящим пламенем. Тушат пламя, покрывая тигли крышками или стеклянными пластинками.
в) В пробирки или химические стаканчики наливают одинаковые количества различных спиртов и помещают небольшие кусочки металлического натрия. Сравнивают скорость выделения водорода в этих случаях.
ГЛИЦЕРИН
Цель опытов с глицерином — ознакомить учащихся с теми свойствами, которые обусловливают применение этого вещества в повседневной жизни, и показать, что глицерин является многоатомным спиртом (имеет как общие с одноатомными спиртами реакции, так и отличные от них).
Растворимость глицерина в воде. В демонстрационную пробирку (или небольшой цилиндр) наливают 5—7 мл глицерина и сверху по стенке прибавляют такой же объем подкрашенной (например, фуксином) воды. При встряхивании жидкость становится однородной и окрашивается равномерно.
Понижение точки замерзания водных растворов глицерина. Водные растворы глицерина (и этиленгликоля) применяются в качестве незамерзающих жидкостей для охлаждения моторов автомашин и самолетов.
а) Пробирку с полученным в предыдущем опыте водным раствором глицерина помещают в охладительную смесь (лед с поваренной солью). Одновременно в смесь помещают пробирку с водой. Через несколько минут убеждаются в том, что вода в пробирке замерзла, раствор же глицерина остался жидким.
б) Ученики могут провести исследование и определить: при каком процентном содержании глицерина в воде раствор перестает замерзать на улице в зимнее время.
Для этого готовят растворы следующих концентраций: 5%, 10%, 15%, 20% и т.д. — выставляют их на улицу в «мягкий» зимний день и затем в морозный. Отмечают температуру воздуха и устанавливают, начиная с какой концентрации растворы глицерина при данной температуре не замерзают.
Гигроскопичность глицерина. Свойство глицерина поглощать влагу и тем самым увлажнять предметы используется, например, для смягчения кожи.
На лист фильтровальной бумаги наносят несколько капель глицерина. На другой лист наносят столько же капель воды. К концу урока убеждаются, что бумага с водой высохла, а бумага с глицерином стала еще более влажной.
Горение глицерина. Демонстрация этого опыта важна тем, что позволяет устранить встречающееся иногда у учащихся неверное представление, будто с увеличением числа атомов углерода в молекуле органического вещества непременно возрастает светимость пламени. Это заключение у них появляется из сопоставления горения метана и этилена. Глицерин содержит три атома углерода в молекуле и тем не менее горит почти бесцветным пламенем, так как он богат кислородом и в процентном отношении содержит углерода меньше, чем этилен.
В небольшой пробирке или в тигельке нагревают до кипения 1 мл глицерина и поджигают выделяющиеся пары. Они горят почти бесцветным пламенем. Может оказаться, что глицерин сразу не загорается из-за присутствия в нем воды; в таком случае он должен быть предварительно обезвожен интенсивным нагреванием.
Реакция глицерина с натрием. Опыт демонстрирует общность свойств глицерина со спиртами.
В пробирку с 1—2 мл глицерина бросают очищенный кусочек натрия величиной с горошину. Пробирку слегка подогревают. Реакция идет вначале медленно, затем все более энергично.
Поджигают выделяющийся водород. Обычно под конец происходит обугливание глицерина.
Реакция с гидроксидом меди. С увеличением числа гидроксильных групп в молекуле вещества возрастает подвижность атомов водорода, т.е. увеличиваются кислотные свойства. Поэтому атомы водорода могут замещаться не только на активные щелочные металлы. Так, например, многоатомные спирты взаимодействуют с гидроксидом меди (уравнение приведено в упрощенном виде):
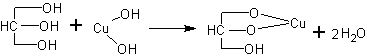
В демонстрационной пробирке (цилиндре, химическом стакане) получают гидроксид меди, добавляя к 4-5 мл раствора медного купороса раствор щелочи до полного осаждения гидроксида. Для успеха опыта щелочь должна быть непременно в избытке, поэтому, ставя опыт, учитель должен соотнести концентрации имеющихся растворов.
Осадок взбалтывают и половину его переносят в другую пробирку. К одной порции добавляют глицерин, пока при взбалтывании осадок гидроксида не исчезнет и Fie образуется темно-синий раствор. Сравнивают окраску раствора с окраской осадка гидроксида в другой пробирке.
Реакция с гидроксидом меди считается качественной реакцией на многоатомные спирты.
ФЕНОЛ
В данном разделе наиболее существенными являются опыты, показывающие растворимость фенола в щелочи, дезинфицирующее действие его и характер взаимного влияния атомов в молекуле фенола.
Растворимость фенола в воде и щелочах. В пробирку с несколькими кристалликами фенола приливают 2-3 мл воды. Пробирку закрывают пробкой и встряхивают. Убеждаются, что фенол не полностью растворился в воде и образовал непрозрачную эмульсию. Дают эмульсии отстояться, жидкость расслаивается: внизу образуется раствор воды в феноле, вверху — раствор фенола в воде.
Содержимое пробирки снова взбалтывают и к эмульсии фено-
ла прибавляют по каплям раствор щелочи. Раствор становится прозрачным, так как образующийся фенолят растворим в воде:
С6Н5ОН + NaOH à С6Н5ОNa + Н2О
В этой реакции фенол проявляет кислотные свойства. Это подтверждается и тем, что при действии кислот (добавляют по каплям соляную кислоту) фенол снова выделяется из раствора:
C6H5ONa + HCI à C6H5ONa + NaCl
Фенол — слабая кислота. Для приблизительного определения силы кислоты достаточно установить, какими кислотами она может вытесняться из солей. Фенол слабее угольной кислоты, поэтому при действии угольной кислоты на фенолят натрия образуется фенол:
С6Н5ОNa + (H2CO3) à С6Н5ОН + NaHCO3
Раствор фенолята натрия получают, прибавляя раствор щелочи к эмульсии фенола (избегать избытка щелочи!). Далее в него пропускают углекислый газ из аппарата Киппа. Образуется муть вследствие выделения свободного фенола.
Реакция фенола с бромной водой. Опыты, на которых можно развить идею о взаимном влиянии атомов в молекулах, имеют большое воспитательное значение. Взаимное влияние атомов можно рассмотреть на примере фенола после ознакомления с его кислотными свойствами.
Большая в сравнении со спиртами подвижность гидроксильного атома водорода в молекуле фенола (реакция со щелочью) обусловлена влиянием на гидроксильную группу соединенного с ней бензольного кольца. Гидроксильная группа в свою очередь влияет на бензольное ядро, ослабляя в орто- и пара-положениях связи атомов водорода с атомами углерода, вследствие чего атомы водорода значительно легче, чем в бензоле, замещаются атомами брома. Бензол, как известно, не реагирует с бромной водой (реагирует с чистым бромом в присутствии железа), фенол же легко реагирует с бромной водой, сразу замещая на бром три атома водорода в своей молекуле.
В демонстрационную пробирку берут немного (на кончике ножа) фенола и добавляют воды столько, чтобы при взбалтывании получился раствор (а не эмульсия) фенола. Далее прибавляют насыщенную бромную воду. Сначала образуется белая муть, а затем осадок трибромфенола:
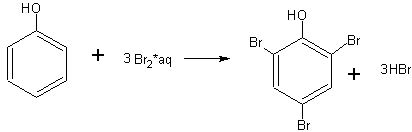
Трибромфенол обладает устойчивым неприятным запахом, поэтому надо остерегаться попадания его на руки и одежду.
Качественная реакция фенола. Характерной качественной реакцией на фенолы является взаимодействие с хлоридом железа(III). К разбавленному раствору (не эмульсии!) фенола добавляют несколько капель раствора хлорида железа FeCI3, Жидкость окрашивается в темно-фиолетовый цвет (белый экран!).
Дезинфицирующее действие фенола. Дезинфицирующее действие фенола основано на том, что он свертывает белок, чем прекращает жизнедеятельность бактерий.
Это действие наблюдают, прибавляя к небольшому количеству раствора куриного яйца в пробирке расплавленный фенол и взбалтывая смесь.
Следует указать учащимся, что этим же свойством фенола обусловливается появление белых пятен на коже рук при неосторожном обращении с ним.
Нитрование фенола. При нитровании фенола образуется тринитрофенол — пикриновая кислота:
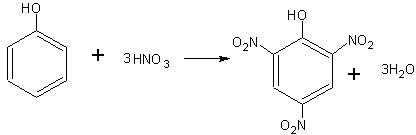
К 3 мл концентрированной азотной кислоты в пробирке приливают 1 мл (не больше) воды и в разбавленную, таким образом кислоту вносят по каплям 0,5 мл расплавленного фенола. Полученную смесь взбалтывают и нагревают до кипения. При последующем охлаждении образуются красивые желтые кристаллы пикриновой кислоты.
Получение фенола из салициловой кислоты. Способы получения фенола не рассматриваются в школьном курсе химии. На внеклассных занятиях (лучше после изучения кислот) можно поставить опыт получения фенола из салициловой кислоты. Существует большая аналогия между получением метана, бензола и фенола при
взаимодействии соответствующих кислот или их солей со щелочью. Везде происходит образование карбоната и соответствующего углеводорода или его производного:
CH3COONa + NaOH à CH4 + Na2CO3
C6H5COONa + NaOH à C6H6 + Na2CO3
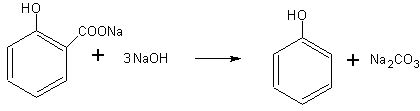
Для получения фенола можно воспользоваться салицилатом натрия или непосредственно салициловой кислотой. Эти вещества могут быть приобретены в аптеке.
В пробирку с отводной трубкой помещают смесь примерно одинаковых объемов салициловой кислоты, гидроксида натрия и оксида кальция. Смесь нагревают, опустив отводную трубку в известковую воду. Убеждаются в выделении углекислого газа. Затем отводную трубку опускают в сухую пробирку и отгоняют столько фенола, сколько позволяет исходное количество салициловой кислоты. Убеждаются в получении фенола по запаху и по реакции с раствором хлорида железа. Применять холодильник приэтом, разумеется, нет необходимости.
ПРОСТЫЕ ЭФИРЫ
Простые эфиры рассматриваются на уроках химии в общих чертах. Можно экспериментально ознакомить учащихся лишь с важнейшим представителем этого класса соединений — диэтиловым (серным) эфиром. Наибольшее значение здесь будут иметь опыты, иллюстрирующие некоторые физические свойства эфира и получение его из этанола. Лабораторные опыты с эфиром ставить не следует, так как пары его огнеопасны.
Низкая температура кипения эфира. Эфир является одной из жидкостей, обладающих низкой температурой кипения.
Нагревают в химическом стакане воду примерно до 50'С. В нагретую воду вносят пробирку с эфиром — эфир закипает. Одновременно можно внести пробирки с другими известными учащимся жидкостями (бензол, этанол) — кипение жидкостей не наступает.
Охлаждение при испарении эфира. Имея низкую температуру кипения, эфир оказывается чрезвычайно летучей жидкостью. На испарение его затрачивается много теплоты, вследствие чего происходит охлаждение окружающей среды. Испарение (и, следова-
тельно, охлаждение) может быть усилено при продувании воздуха через эфир.
а) На легкую деревянную пластинку ставят смоченный снизу водой тигелек, наливают 8 него 1 мл эфира и продувают через эфир воздух грушей. Тигелек примерзает к пластинке.
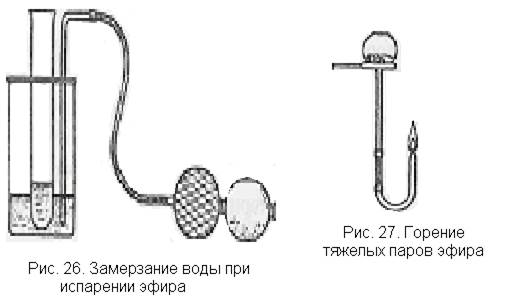
б) В пробирку (рис. 26) наливают 1—2 мл воды и помещают ее в стаканчик, где налит слой эфира в 1 см. Грушей продувают через эфир воздух. Вода в пробирке вскоре замерзает.
в) Продувают воздух через эфир, находящийся в пробирке, погруженной в воду. Вскоре пробирка снаружи покрывается ледяной корочкой.
Пары эфира тяжелее воздуха. По молекулярному весу эфира учащиеся находят, что пары эфира более чем в 2,5 раза тяжелее воздуха. Это свойство эфира, одновременно с его горючестью, может быть продемонстрировано рядом опытов.
а) К концу воронки без крана присоединяют загнутую вверх трубочку с оттянутым концом (рис. 27). В воронку кладут комочек ваты, смоченной эфиром. Через 2—3 сек поджигают пары эфира у отверстия трубки.
б) В стеклянную банку вводят несколько капель эфира и затем пускают туда табачный дым. Пары эфира, окрашенные дымом, можно переливать, как жидкость, из сосуда в сосуд и даже налить на поверхность стола, где они будут стелиться тяжелым облаком.
Взаимная растворимость эфира и воды. В демонстрационной пробирке к 10 мл воды добавляют понемногу эфир. При взбалтывании первые порции эфира частично растворяются в воде, затем на
поверхности собирается избыток эфира. Добавляют его еще немного, смесь взбалтывают и дают отстояться. Жидкость разделяется на два слоя: нижний слой — раствор эфира в воде, верхний слой — раствор воды в эфире.
Разделяют растворы с помощью делительной воронки и доказывают наличие воды в эфире и эфира в воде. Бросают в эфирный слой порошок безводного сульфата меди, наблюдают образование медного купороса. Нагревают в пробирке водный слой и поджигают выделяющиеся пары; наблюдают горение эфира.
Эфир как растворитель. Эфир — хороший растворитель многих веществ, в частности жиров. Применение его в качестве растворителя ограничивается лишь его огнеопасностью. Опыты по растворению веществ эфиром могут быть поставлены аналогично опытам с другими растворителями. Учащимся предлагается самостоятельно удалить при помощи эфира жирное пятно с ткани.
Получение эфира из спирта. Получение диэтилового эфира интересно тем, что очень убедительно показывает учащимся влияние условий реакции на образование разных продуктов из одних и тех же исходных веществ. Этиловый спирт и концентрированная серная кислота при нагревании выше 140— 150°С дают преимущественно этилен (с. 46), при температуре ниже 140°С дают диэтиловый эфир.
На результат реакции оказывают влияние и относительные количества взятых веществ.
При получении эфира относительное количество спирта должно быть больше, чем при получении этилена. Это объясняется тем, что эфир образуется при действии на этилсерную кислоту дополнительного количества спирта:
C2H5OSO2OH + НОС2Н5 à С2Н5— О — С2Н5 + H2SO4,
тогда как этилен получается при разложении этилсерной кислоты:
C2H5OSO2OH à С2Н4 + H2SO4.
Учащимся это может быть разъяснено так: при образовании молекулы этилена серная кислота отнимает воду от каждой молекулы спирта, а при образовании эфира она отнимает воду от каждых двух молекул спирта:
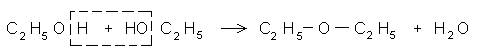
Опыт ведут так, чтобы вначале получить этилсерную кислоту, а затем к ней добавляют спирт и отгоняют эфир, нагревая жидкость не выше 140°С.
В небольшую колбу (рис. 28) наливают равные по объему ко-
личества спирта (ректификата) и концентрированной серной кислоты, что соответствует примерно эквимолекулярным соотношениям. В воронку наливают дополнительное количество спирта. В качестве приемника используют колбу Бунзена, которую ставят в сосуд со льдом и к боковой трубке его присоединяют длинную каучуковую трубку для отвода несконденсировавшихся паров эфира (под тягу или за окно).
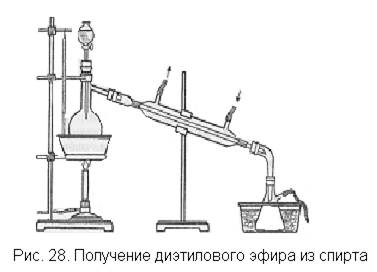
Нагревают колбу на песчаной бане (песок должен быть нагрет заранее) до температуры 140'С и, когда начнет перегоняться эфир, добавляют понемногу из воронки этанол. Через холодильник должна идти сильная струя холодной воды. Опыт ведут до получения необходимого для демонстрации количества эфира. С эфиром неизбежно отгоняется некоторое количество спирта и воды. Чтобы эфир отмыть от спирта, дистиллят переносят в делительную воронку, добавляют к нему равный объем воды, содержимое воронки взбалтывают, дают жидкости отстояться, сливают нижний водный слой, а эфир переносят в пробирку и демонстрируют классу.
После удаления спирта эфир промывают слабым раствором щелочи, освобождаясь от кислот, затем снова промывают водой и сушат хлоридом кальция. Эти операции выполняют уже не на уроке.
Проверка чистоты эфира. Большое значение имеет ознакомление учащихся, хотя бы в процессе кружковой работы, с методами проверки чистоты реактивов. Наиболее просто это можно осуществить с диэтиловым эфиром. Как видно из способа получения, недостаточно чистый эфир может содержать воду, кислоту, спирт.
Чтобы убедиться, содержит ли эфир воду, кислоту или спирт, в пробу его бросают маленький кусочек очищенного натрия. При наличии воды выделяется водород.
Наличие кислоты можно установить, если к пробе эфира добавить небольшое количество воды, жидкости взболтать, спустить из делительной воронки нижний водный слой и испытать его лакмусовой бумажкой.
Для открытия спирта проводят иодоформную реакцию. К пробе эфира добавляют немного воды, 2—3 капли раствора йода в иодиде калия или кристаллики йода и хорошо взбалтывают смесь. Затем обесцвечивают раствор незначительным количеством щелочи и подогревают. При наличии спирта после охлаждения образуется запах, а затем появляются желтые кристаллики йодоформа.
Сравнение свойств диэтилового эфира и бутанола. При изучении спиртов и простых эфиров впервые появляется возможность ознакомиться практически со свойствами изомерных веществ и убедиться, что при одинаковом составе между ними могут быть существенные различия. Наиболее доступным для опытов примером будет изомерия диэтилового эфира и бутанола (или изобутанола), так как оба эти вещества представляют собой жидкости и довольно распространены в лабораториях.
а) В одну пробирку наливают сухого диэтилового эфира, в другую пробирку — примерно столько же бутанола и помещают в жидкости по кусочку натрия. Замечают, что натрий с эфиром не взаимодействует, со спиртом же реакция идет, и выделяется водород.
б) В две пробирки наливают по одинаковому количеству диэтилового эфира и бутанола (например, по 1 мл). Помещают пробирки в заранее подготовленный стакан с горячей водой (50-60°С). Эфир при таком нагревании закипает, и пары его могут быть подожжены; спирт не кипит и не образует горючих паров.
ГЛАВА VI
АЛЬДЕГИДЫ И КЕТОНЫ
При изучении альдегидов учащиеся на опытах знакомятся со ступенчатым характером окисления органических веществ, с химизмом важных производственных процессов и с принципом получения синтетических смол.
Чтобы место альдегидов в ряду продуктов окисления углеводородов было понятно учащимся, при составлении химических уравнений не следует избегать пользования названиями и формулами кислот, в которые альдегиды превращаются. Формулы кислот могут быть даны предварительно догматически; в дальнейшем учащиеся получат для них экспериментальное обоснование.
При изучении альдегидов больше всего опытов ставится с формальдегидом как веществом, наиболее доступным для школы и имеющим большое промышленное значение. В соответствии с этим в настоящей главе формальдегиду отведено основное место. Для уксусного альдегида рассматриваются лишь реакции получения. Кетоны специально не изучаются в школе; поэтому из них здесь взят лишь один представитель — ацетон, и опыты с ним даны преимущественно для внеклассной работы учащихся.
ФОРМАЛЬДЕГИД (МЕТАНАЛЬ)
План изучения этого вещества целесообразно построить так, чтобы сразу после ознакомления с физическими свойствами альдегидов учащиеся изучили способы получения его, затем химические свойства и т.д. Несколько более раннее ознакомление со способами получения альдегида даст возможность далее, при изучении химических свойств (реакции окисления), рассматривать альдегиды как звено в цепи окисления углеводородов.
В качестве образца при ознакомлении со свойствами формальдегида можно пользоваться формалином. При этом следует сразу же добиться, чтобы учащиеся отчетливо понимали разницу между формалином и формальдегидом.
Запах формальдегида. Из физических свойств формальдегида наиболее доступно на практике ознакомление с запахом. Для этой цели на ученические столы раздаются пробирки с 0,5-1 мл формалина. После того как учащиеся ознакомятся с запахом, формалин может быть собран и использован для дальнейших опытов. Ознакомление с запахом формалина даст возможность учащимся обнаруживать это вещество в других опытах.
Горючесть формальдегида. Нагревают формалин в пробирке и поджигают выделяющиеся пары; они горят почти бесцветным пламенем. Пламя можно заметить, если в нем поджечь лучинку или бумажку. Опыт проводят в вытяжном шкафу.
Получение формальдегида. Так как до ознакомления с химическими свойствами формальдегид может быть обнаружен только по запаху, то первый опыт получения его следует поставить в виде лабораторной работы.
1. В пробирку наливают несколько капель метанола. В пламени горелки нагревают свернутый в трубочку небольшой кусочек медной сетки или спираль из медной проволоки и быстро опускают ее в метанол.
При прокаливании медь окисляется и покрывается черным налетом оксида меди, в спирте она снова восстанавливается и становится красной:
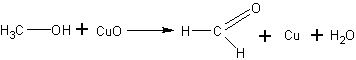
Обнаруживают резкий запах альдегида. Если процесс окисления повторить 2—3 раза, то можно получить значительную концентрацию формальдегида и раствор использовать для последующих опытов.
2. Кроме оксида меди для получения формальдегида могут быть использованы другие знакомые учащимся окислители.
К слабому раствору перманганата калия в демонстрационной пробирке добавляют 0,5 мл метанола и смесь нагревают до кипения. Появляется запах формальдегида, а фиолетовая окраска перманганата исчезает.
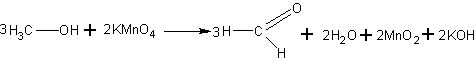
В пробирку наливают 2—3 мл насыщенного раствора бихромата калия К2Сг2О7 и такой же объем концентрированной серной кислоты. Добавляют по каплям метанол и очень осторожно подогревают смесь (отверстие пробирки направляют в сторону!). Далее реакция идет с выделением тепла. Желтая окраска хромовой смеси исчезает, и появляется зеленая окраска сульфата хрома
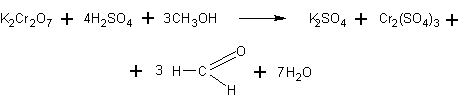
Уравнение реакции с учащимися можно не разбирать. Как и в предыдущем случае, им лишь сообщается, что бихромат калия окисляет метиловый спирт в альдегид, превращаясь при этом в соль трехвалентного хрома Cr2(SO4)3.
Взаимодействие формальдегида с оксидом серебра (реакция серебряного зеркала). Этот опыт должен быть продемонстрирован учащимся так, чтобы он одновременно явился и инструктажем к последующему практическому занятию.
Природа аммиачного раствора оксида серебра может быть подробно разъяснена учащимся, а можно лишь сообщить им, что образующийся при реакции гидроксид серебра — вещество непрочное и легко распадается на оксид серебра и воду:
AgNO3 + NH4OH à AgOH + NH4NO3
2AgOH à Ag2O + H2O
Оксид серебра обладает свойством растворяться в аммиаке.
Ag2O + 4NH4OH à 2[Ag(NH3)2]OH + Н2O
Окислительное действие оксида серебра объясняется тем, что это вещество является оксидом благородного металла, поэтому оксид неустойчив и при наличии восстановителя, т.е. вещества, легко окисляющегося, он легко отдает кислород, вследствие чего происходит выделение (восстановление) металлического серебра. Уравнение реакции можно дать в обычном виде:
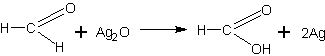
а можно представить полное уравнение реакции:
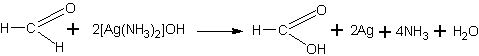
Серебряное зеркано образуется в том случае, если восстанавливающееся серебро осаждается на гладких стенках сосуда из не слишком концентрированных растворов. Малейшие загрязнения мешают восстанавливающемуся серебру «уцепиться» за стекло и заставляют его выделяться в виде рыхлого осадка. Значительно меньшее влияние на успех опыта оказывает характер нагревания. Если сосуд недостаточно чист, то даже самое осторожное нагревание не дает зеркала, и наоборот, если сосуд подготовлен тщательно, то даже нагревание смеси на открытом огне может дать желаемый результат.
Первый опыт получения серебряного зеркала следует провести в колбочке, а не в пробирке.
Колбу емкостью 50—100 мл до урока очищают от механических загрязнений, промывают ершиком с мыльной водой или нагревают в колбе раствор щелочи, затем споласкивают водой, промывают хромовой смесью и наконец начисто промывают дистиллированной водой.
В колбу наливают на четверть объема 2-процентный раствор нитрата серебра, затем добавляют постепенно раствор аммиака
(25-процентный аммиак следует разбавить в 8-10 раз) до тех пор, пока образующийся вначале осадок не растворится в его избытке. К образующемуся раствору добавляют осторожно по стенке 0,5-1 мл формалина и помещают колбу в стакан с горячей (лучше кипящей) водой. Вскоре в колбе образуется красивое серебряное зеркало.
Колбу можно нагревать без водяной бани, непосредственно на маленьком пламени, обнося пламя вокруг колбы и не встряхивая ее.
При демонстрации опыта вместо серебряного зеркала иногда образуется черный осадок. Учитель в таком случае обычно совершенно бракует опыт. Между тем при таком результате следует разъяснить учащимся, что здесь также произошло восстановление серебра только в виде рыхлого черного осадка.
Окисление формальдегида гидроксидом меди ( II ). В пробирку наливают 2 мл 5-процентного раствора формальдегида, 2 мл 10-процентного раствора гидроксида натрия и при встряхивании добавляют по каплям 2-процентный раствор сульфата меди (11) до появления неисчезающей взвеси. Содержимое пробирки нагревают до начала кипения и наблюдают изменение окраски реакционной смеси а именно: голубая окраска меняется на желтую (осадок), а затем на красную (осадок). Эта реакция, как и реакция серебряного зеркала, является качественной реакцией на альдегиды. Суммарное уравнение этой реакции следующее:
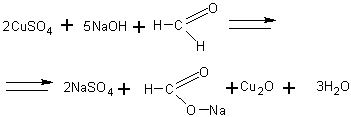
Однако с учащимися целесообразно рассматривать этот процесс поэтапно:
CuSO4 + 2NaOH = Си(ОН)2 + Na2SO4
Голубой
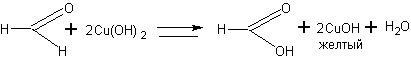
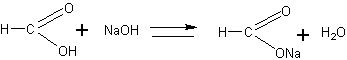
2CuOH à Cu2O + H2O
красный
Обращают внимание учащихся на то, что реакция протекает в
щелочной среде, поэтому образуется не муравьиная кислота, а соль как продукт нейтрализации. Изменяющаяся цветовая гамма продуктов является результатом превращений соединений меди, связанных с изменением степени ее окисления.
Дезинфицирующее действие формальдегида. Дезинфицирующее действие формальдегида объясняется его свойством свертывать белок.
К нескольким миллилитрам формалина в пробирке добавляют 1 мл куриного белка. Белок свертывается.
Полимеризация и деполимеризация альдегида. Формальдегид, как это впервые показал А.М.Бутлеров, легко уплотняется.
В продаже существует твердый полимер формальдегида — параформальдегид (СН2О)n или параформ.
а) Параформ может быть легко деполимеризован.
В сухую пробирку помещают несколько крупинок параформа и нагревают. Вещество разлагается, образуя газообразный формальдегид, который частично улетает (запах!), а частично на холодных стенках пробирки снова образуется полимер. Опыт объясняет применение параформа для дезинфекции помещений.
б) Полимеризацию формальдегида можно наблюдать при выпаривании его раствора.
Выпаривают осторожно на водяной бане в фарфоровой чашке 4—5 мл формалина. Образуется твердый остаток. Остаток нагревают на голом огне. Происходит деполимеризация и улетучивание продукта (вытяжной шкаф). Убедившись в этом, прекращают нагревание.
Взаимодействие формальдегида с аммиаком. Нагревая формальдегид с аммиаком, А.М.Бутлеров получил уротропин, широко известное антисептическое средство.
В фарфоровой чашке на водяной бане выпаривают смесь равных объемов формалина и концентрированного раствора аммиака. По мере улетучивания жидкости остаются бесцветные кристаллы уротропина (гексаметилентетрамина (CH2)6N4)N.
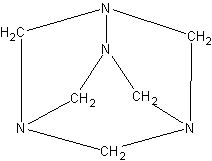
Знакомство учащихся со структурной формулой уротропина может быть лишь довольно поверхностным, так как класс аминов
еще не изучался. Однако структурная формула может быть ими осмыслена на основе знания валентности элементов.
С синтезированным или готовым уротропином можно выполнить следующие опыты. Нагревают уротропин в фарфоровой чашке, он улетучивается не плавясь. Раствор уротропина даст щелочную реакцию. При действии раствора щелочи уротропин разлагается, выделяющийся аммиак можно обнаружить обычными способами. При действии раствора серной кислоты на раствор уротропина (нагревание) также происходит разложение его, выделяющийся формальдегид может быть обнаружен по запаху.
Получение фенолформальдегидных смол. Основная масса получаемого в промышленности формальдегида идет на синтез фенолформальдегидных и других смол, необходимых для производства пластических масс. В основе получения фенолформальдегидных смол лежит реакция поликонденсации.
Наиболее доступен в школьных условиях синтез фенолформальдегидной смолы. Учащиеся к этому времени знакомы уже с обоими исходными веществами для получения смолы — фенолом и формальдегидом; опыт сравнительно несложен и идет безотказно; химизм процесса не представляет особой трудности для учащихся, если изобразить его следующим образом:
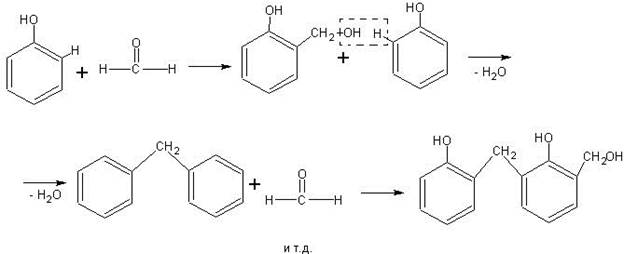
В зависимости от количественного соотношения фенола и формальдегида, а также от применяемого катализатора (кислотный или щелочной) может получаться новолачная или резольная смола. Первая из них термопластична и имеет линейную структуру, приведенную выше. Вторая — термореактивна, так как в ее линейных молекулах содержатся свободные спиртовые группы — СН2ОН, способные реагировать с подвижными водородными атомами других молекул, в результате чего образуется трехмерная структура.
В процессе классного изучения нет необходимости отдельно демонстрировать опыты получения новолачной и резольной смолы. Достаточно показать на одном опыте сам факт образования
высокомолекулярного соединения. В процессе внеклассных занятий можно получить смолы разного типа и даже формовать изделия из них. Опыты необходимо проводить под тягой вследствие летучести формальдегида.
а) Нагревают в пробирке на пламени спиртовки смесь 2,5 г кристаллического фенола и 5 мл формалина (40-процентного). Даже при кипении жидкости в ней не наблюдается химической реакции. Приливают к смеси 7-8 капель соляной кислоты (1 : 1). Вскоре происходит бурная реакция, и жидкость становится мутной. Охлаждают пробирку и дают смеси отстояться: внизу образуется смола, сверху — вода. Сливают водный слой и выливают смолу на лист картона или жести. Застывшая смола имеет светло-желтую окраску. Опыт убедительно показывает роль соляной кислоты как катализатора реакции.
б) Не ставя целью показать роль катализатора, опыт можно провести проще. Нагревают в пробирке смесь указанных выше количеств фенола, формальдегида и кислоты, пока не начнется бурная реакция. После того как образуется муть, дают смеси расслоиться и далее поступают как в предыдущем случае.
в) Действие аммиака в качестве катализатора можно проследить на следующем опыте, который можно поставить и в несколько укрупненном масштабе.
В большую пробирку насыпают 4—5 г фенола, приливают 10 мл 40-процентного формалина и 1—2 мл концентрированного раствора аммиака. Смесь нагревают в течение нескольких минут в пламени горелки. После того как смесь вскипит (бурная реакция) и затем сделается мутной вследствие образования смолы, охлаждают пробирку и дают жидкости расслоиться. Сливают верхний водный слой и демонстрируют в пробирке вязкую жидкость — фенолформальдегидную смолу. Затем смолу помещают в пробирке или в какой-нибудь формочке в сушильный шкаф, Через час-полтора (иногда раньше) смола превращается в твердую пластмассу. Так очень упрощенно может быть имитировано производство литых изделий из смолы.
г) Действие щелочного и кислотного катализатора на процесс поликонденсации можно показать одновременно. В две пробирки помешают по 2,5 г фенола и по 5 мл формалина. Затем в одну пробирку приливают 1 мл концентрированного раствора аммиака, а в другую — 7—8 капель соляной кислоты. Пробирки помешают в кипящую водяную баню. Через 5—10 мин в пробирках образуется смола. Сливают после отстаивания верхний водный слой и затем выливают смолу на листы картона или жести.
д) В химическом кружке учащиеся могут получить фенолфор-
мальдегидную смолу в большем количестве и с более тщательным соблюдением режима.
В круглодонную колбу с обратным холодильником помещают 25 г фенола, 50 мл формалина и 3 мл 40-процентного раствора едкого натра. Осторожно нагревают смесь через асбестированную сетку. Нагрев регулируют так, чтобы жидкость не кипела слишком бурно. По мере нагревания жидкость становится все более вязкой и примерно через час настолько густеет, что пузырьки газа с трудом вырываются на поверхность. Выливают жидкость в пробирку, При охлаждении она образует непрозрачную твердую массу. Чтобы довести процесс поликонденсации до образования трехмерной структуры, пробирку помещают в сушильный шкаф, где выдерживают продукт 1 ч при 50— 60°С и 3—4 ч при 70— 80°С. Образуется твердая нерастворимая смола ярко-розового цвета.
УКСУСНЫЙ АЛЬДЕГИД (ЭТАНАЛЬ)
После подробного ознакомления со свойствами формальдегида в данном разделе темы наибольшее значение приобретают опыты, связанные с получением уксусного альдегида. Эти опыты могут ставиться с целью: а) показать, что все альдегиды могут быть получены окислением соответствующих одноатомных спиртов, б) показать, как экспериментальным путем может быть обоснована структура альдегидов, в) познакомить с химизмом промышленного способа получения уксусного альдегида по Кучсрову.
Получение уксусного альдегида окислением этанола. В качестве окислителя спирта может быть взят оксид меди (II). Реакция идет аналогично окислению метанола:
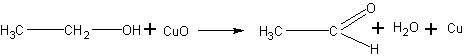
1. В пробирку наливают не более 0,5 мл этилового спирта и погружают раскаленную медную проволочку. Обнаруживают запах уксусного альдегида, напоминающий запах фруктов, и наблюдают восстановление меди. Если окисление спирта произвести 2-3 раза, всякий раз накаливая медь до образования оксида меди, то, собрав растворы, полученные учащимися в пробирках, можно будет использовать альдегид для опытов с ним.
2. В небольшую колбочку с отводной трубкой помещают 5 г измельченного бихромата калия К2Сг2О7, наливают 20 мл разбавленной серной кислоты (1:5) и затем 4 мл этилового спирта. К колбе присоединяют холодильник и нагревают ее на небольшом пламени через асбестированную сетку. Приемник для дистиллята ста-
вят в ледяную воду или снег. В приемник наливают немного воды и в воду опускают конец холодильника. Это делается для того, чтобы уменьшить улетучивание паров уксусного альдегида (темп. кип. 21 °С). Вместе с этаналем в приемник отгоняется некоторое количество воды, не прореагировавшего спирта, образующейся уксусной кислоты и других побочных продуктов реакции. Однако выделять чистый уксусный альдегид нет необходимости, так как полученный продукт хорошо дает обычные реакции альдегидов. Наличие альдегида устанавливают по запаху и по реакции серебряного зеркала.
Внимание учащихся обращают на изменение окраски в колбе. Зеленая окраска получившегося сульфата хрома (III) Cr2(SO4)3 становится особенно отчетливой, если содержимое колбы после опыта разбавить водой. Отмечают, что изменение окраски бихромата калия произошло вследствие окисления им спирта.
Получение уксусного альдегида гидратацией ацетилена. Замечательное открытие русского химика М.Г.Кучерова — присоединение воды к ацетилену в присутствии солей ртути легло в основу широко распространенного промышленного способа получения уксусного альдегида.
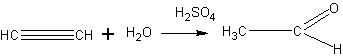
Несмотря на большое значение и доступность для школы, этот способ редко демонстрируется на уроках химии.
В промышленности процесс ведут, пропуская ацетилен в воду, содержащую соли двухвалентной ртути и серную кислоту, при температуре 70°С. Образующийся ацетальдегид при этих условиях отгоняется и конденсируется, после чего поступает в специальные башни для окисления в уксусную кислоту. Ацетилен получают из карбида кальция обычным путем и очищают его от примесей.
Необходимость очистки ацетилена и поддержания температуры в реакционном сосуде, с одной стороны, и неуверенность в получении нужного продукта — с другой, обычно снижают интерес к этому опыту. Между тем опыт можно достаточно просто и надежно провести как в упрощенном виде, так и в условиях, приближающихся к промышленным.
1. Опыт, в определенной степени отражающий условия проведения реакции на производстве и дающий возможность получить достаточно концентрированный раствор альдегида, можно провести в приборе, изображенном на рис. 29.
Первый этап — получение ацетилена. В колбу помещают кусочки карбида кальция и из капельной воронки медленно прибав-
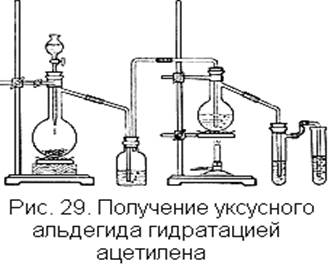
ляют воду или насыщенный раствор поваренной соли. Скорость прикалывания регулируют таким образом, чтобы установился ровный ток ацетилена приблизительно один пузырек в 1—2 с. Очистку ацетилена производят в промывалке с раствором сульфата меди:
CuSО4 + H2S àH2SO4
После очистки газ пропускают в колбу с раствором катализатора (15—20 мл воды, 6—7 мл конц. серной кислоты и около 0,5 г оксида ртути (II). Колбу, где проходит гидратация ацетилена, подогревают горелкой (спиртовкой), а образующийся уксусный альдегид в газообразном виде попадает в пробирки с водой, где и происходит его поглощение.
Минут через 5—7 в пробирке удается получить раствор этаналя значительной концентрации. Чтобы завершить опыт, сначала прекращают подачу воды к карбиду кальция, затем разъединяют прибор и без всякой дополнительной отгонки альдегида из реакционной колбы пользуются полученными растворами в пробирках для соответствующих опытов.
2. В самом упрощенном виде реакция М.Г.Кучерова может быть осуществлена следующим образом.
В небольшую круглодонную колбу наливают 30 мл воды и 15 мл конц. серной кислоты. Смесь охлаждают и вносят в нее немного (на кончике шпателя) оксида ртути (II). Нагревают смесь осторожно через асбестовую сетку до кипения, оксид ртути при этом превращается в сульфат ртути (II). Помещают в колбочку 4—5 кусоч-
ков карбида кальция, немедленно закрывают ее пробкой с газоотводной трубкой, конец которой опускают в пробирку с водой. Пробирку-приемник помещают в стакан со снегом или в охлаждающую смесь. Реакция карбида кальция с водой в присутствии серной кислоты протекает довольно спокойно. Продолжают слабое нагревание смеси в течение 10-12 мин. Уксусный альдегид перегоняется в пробирку-приемник и растворяется в воде. Присутствие альдегида в растворе можно обнаружить по запаху и по появлению розовой окраски фуксинсернистой кислоты. Реакции с аммиачным раствором оксида серебра и гидроксидом меди вследствие наличия примесей идут менее характерно.
БЕНЗОЙНЫЙ АЛЬДЕГИД
С бензальдегидом учащихся можно ознакомить кратко. Главная цель, которая преследуется здесь, — показать, что альдегиды существуют среди соединений не только жирного, но и ароматического ряда органических соединений.
Поэтому будет вполне достаточно ознакомить учащихся на опыте с характерным запахом а/тьдегида (что связано с практическим его использованием), с реакцией серебряного зеркала (что устанавливает принадлежность его к классу альдегидов) и с окислением кислородом воздуха (что наиболее убедительно показывает превращение альдегидов в кислоты).
Запах бензальдегида и окисление кислородом воздуха. Одновременно с тем, как учитель начинает излагать сведения о бензальдегиде, на ученические столы выдают часовые стекла или стеклянные пластинки, на которых нанесено по нескольку капель бензальдегида. Учащиеся знакомятся с запахом вещества. После того как объяснен дальнейший материал и продемонстрирована реакция серебряного зеркала с бензальдегидом (см. ниже), учитель сообщает, что бензойную кислоту, которую не пришлось наблюдать в проведенной реакции, .можно видеть на выданных пластинках с бензальдегидом. К этому времени на стеклах начинают появляться красивые кристаллы бензойной кислоты (для этого необходимо 10—15 мин). К следующему уроку весь альдегид превращается в кристаллы. Учащиеся составляют соответствующее уравнение реакции:
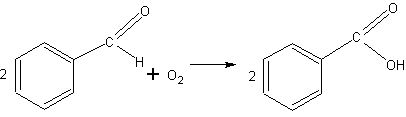
Реакция серебряного зеркала. Реакцию проводят совершенно так-
же, как с другими альдегидами. К 5—8 мл аммиачного раствора оксида серебра в чистой пробирке прибавляют 2—3 капли бензальдегида и нагревают смесь в горячей воде или осторожно над небольшим пламенем спиртовки. Образуются бензойная кислота и серебро.
АЦЕТОН (ДИМЕТИЛПРОПАНОН)
Школьной программой не предусматривается изучение кетонов. Однако некоторые учителя знакомят учащихся на уроках или в процессе внеклассной работы с окислением вторичных спиртов и практически наиболее важным представителем класса кетонов — ацетоном. Ниже приводятся опыты, которые могут быть использованы с этой целью.
Горение ацетона. Несколько капель ацетона наливают на крышку фарфорового тигля и поджигают. Ацетон горит слабо светящимся пламенем.
Растворимость ацетона в воде. К 2 мл воды добавляют равный объем ацетона. По встряхивании не удается установить расслоения жидкостей. Ацетон растворяется в воде.
Ацетон как растворитель смол и пластмасс. На этом свойстве ацетона основано его применение для изготовления лаков и для склеивания изделий из пластмасс.
а) В нескольких миллилитрах ацетона в пробирке растворяют при помешивании стеклянной палочкой столько целлулоида, чтобы раствор стал слегка вязким. Смачивают полученным лаком вату и натирают ею гладкий кусочек дерева — после улетучивания растворителя предмет оказывается «лакированным».
б) Два кусочка очищенной кинопленки или органического стекла (плексигласа) смачивают с концов ацетоном.
Через 1—2 мин накладывают концы пленки друг на друга и слегка сдавливают. После высыхания кусочки оказывают прочно склеенными ацетоном.
Отношение к аммиачному раствору оксида серебра. В две пробирки наливают одинаковые количества аммиачного раствора оксида серебра. В одну пробирку прибавляют раствор альдегида, в другую — такой же объем ацетона. Пробирки помещают одновременно в стакан с горячей водой. В пробирке с альдегидом появляется зеркало в пробирке с ацетоном восстановления серебра и, следовательно, окисления кетона не происходит.
Окисление ацетона. Ацетон не может быть окислен окисью серебра (см. предыдущий опыт), но он может быть окислен более энергичными окислителями.
Около 1 мл ацетона разбавляют в пробирке водой, приливают
серной кислоты, подогревают и вносят небольшими порциями измельченный перманганат калия, пока не перестанет исчезать его фиолетовая окраска. При нагревании раствора можно обнаружить по запаху пары уксусной кислоты.
При окислении происходит разрыв углеродной цепи и образование двух кислот — уксусной и муравьиной:
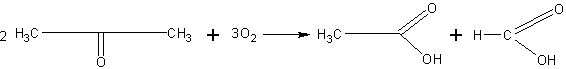
Получение бромацетона. Учащимся можно показать, что углеводородные радикалы кислородсодержащих органических веществ сохраняют в основном свойства углеводородов. Примером тому оказывается реакция бромирования ацетона:
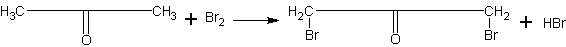
Реакция ацетона с бромом, кроме того, дает возможность довольно просто и в безопасной форме ознакомить учащихся с получением одного из слезоточивых веществ (лакриматоров). В настоящее время известны вещества, значительно превосходящие бромацетон по слезоточивому действию. Однако, принимая во внимание, что задача сводится к ознакомлению не с силой, а с характером действия вещества, целесообразно ограничиваться в указанных целях именно этим примером.
В вытяжном шкафу наливают в пробирку 1 мл ацетона и вносят несколько капель брома. Уже без подогрева обычно начинает ощущаться острый запах бромацетона. Если реакция не наступает, пробирку слегка подогревают (осторожно, беречь глаза!). Смачивают жидкостью из пробирки несколько полосок фильтровальной бумаги и раздают их на стеклышках учащимся или же помещают несколько капель жидкости на железную пластинку и нагревают ее над пламенем спиртовки.
Как только действие бромацетона на глаза обнаружено, хотя бы и в слабой форме, демонстрацию его прекращают и проветривают помещение.
Уравнение реакции учащиеся смогут составить сами, если им указать, что здесь в каждой молекуле ацетона замещается бромом один атом водорода.
В качестве наиболее сильного слезоточивого вещества указывается хлорацетофенон
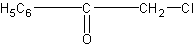
раздражающей концентрацией которого в воздухе считается 0,0003 мг/л.
Получение ацетона. В случае отсутствия в школьной лаборатории ацетон может быть получен для демонстрационных целей из солей уксусной кислоты, например, по реакции:
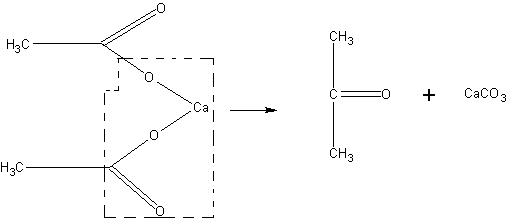
В наиболее простом виде опыт может быть проведен без выделения образующегося продукта.
В пробирке накаливают 2—3 г безводного ацетата натрия CH3COONa. Через 3—5 мин ощущается запах ацетона. Пары его при поджигании горят. По охлаждении пробирки с помощью соляной кислоты можно констатировать образование карбоната:
2CH3COONa à СН3 - СО - СН3 + Na2CO3
Na2CO3 + 2НС! à 2NaCl + Н2О + СО2
ГЛАВА VII
КАРБОНОВЫЕКИСЛОТЫ
Изучение предельных одноосновных кислот лучше всего начинать со второго члена гомологического ряда — с уксусной кислоты. Эта кислота частично уже известна учащимся, она доступна для школы, на ней более характерно проявляется структура карбоновых кислот. Муравьиная кислота как первый член ряда имеет некоторые особенности в строении и свойствах, а поэтому менее удобна для первоначального ознакомления с классом кислот.
В ряду одноосновных кислот вслед за уксусной и муравьиной рекомендуется рассмотреть также высшие гомологи кислот. Это позволит создать у учащихся более полную картину о гомологическом ряде и не возвращаться к этим кислотам в последующей теме при изучении жиров.
Химические свойства кислот в настоящей главе приводятся не полностью. С целью избежать повторения реакции кислот со спиртами описываются в следующей главе, где они являются специальным предметом рассмотрения.
УКСУСНАЯ КИСЛОТА
Учащимся знаком запах уксусной кислоты, они имеют представление о некоторых химических свойствах ее, поскольку эти свойства являются общими со свойствами неорганических кислот, знают структурную формулу кислоты. Поэтому не особенно существенно, какой порядок ознакомления с веществом будет принят. Если учитель сочтет необходимым уделить внимание обоснованию структурной формулы кислоты, то после рассмотрения физических свойств можно перейти к химическим свойствам, так как именно они дадут ответ на интересующий вопрос, и лишь затем рассмотреть способы получения.
Напротив, если учитель хочет подчеркнуть генетическую связь между органическими веществами различных классов, он предпочтет сначала рассмотреть способы получения кислот, особенно путем окисления спиртов и альдегидов, а затем перейдет к изучению химических свойств.
Кристаллизация уксусной кислоты. В демонстрационном опыте трудно показать, что чистая уксусная кислота кристаллизуется при + 16,7°С. Легче показать лишь сам факт «замерзания» ее при охлаждении. Наблюдение кристаллов объяснит учащимся, почему чистая уксусная кислота носит название ледяной.
1. В пробирку наливают несколько миллилитров уксусной кислоты (по возможности безводной) и помещают пробирку в ледяную воду. Вскоре при встряхивании наблюдают образование крупных блестящих кристаллов кислоты, напоминающих замерзшую воду. Если кислота не безводна, то она может не закристаллизоваться, в таком случае лучше пользоваться охладительной смесью снега с поваренной солью.
2. Вымораживанием кислоты из водного раствора легко получить чистую ледяную уксусную кислоту, которую можно хранить в качестве демонстрационного препарата. В небольшую колбочку наливают концентрированную уксусную кислоту и охлаждают в смеси снега с солью. Когда значительная часть жидкости закристаллизуется, выливают из колбы остаток жидкости — воду с некоторым количеством уксусной кислоты. Дают растаять замерзшей кислоте и снова помещают колбу в охладительную смесь. Когда часть жидкости снова закристаллизуется, опять сливают жидкость с кристаллов и повто-
ряют всю операцию еще раз. Так удается получить практически безводную уксусную кислоту, которую при понижении температуры очень легко переводить в кристаллическое состояние.
Горение уксусной кислоты. Проводя ряд аналогий между уксусной кислотой и минеральными кислотами, следует всякий раз подчеркивать особенность уксусной кислоты как кислоты органической, например ее горючесть.
Наливают в пробирку немного уксусной кислоты и нагревают в пламени горелки. При 118°С кислота кипит. Продолжая нагревание, поджигают пары лучинкой. Они горят слабо светящим пламенем. Учащиеся составляют уравнение реакции горения (в продуктах горения углекислый раз и вода) и дают объяснение слабой светимости пламени.
Отношение уксусной кислоты к окислителям. Легко показать, что, в отличие от спиртов и особенно альдегидов, уксусная кислота более устойчива по отношению к окислителям.
К разбавленному водному раствору чистой уксусной кислоты в химическом стакане прибавляют раствор перманганата калия и серной кислоты. Фиолетовая окраска раствора не исчезает.
Однако было бы неверным сделать заключение о неокисляемо-сти уксусной кислоты. Учащиеся уже знакомы с полным окислением кислоты при горении.
Действие уксусной кислоты на индикаторы. К растворам лакмуса и метилоранжа в демонстрационных пробирках или стаканчиках приливают немного раствора уксусной кислоты. Лакмус краснеет, метилоранж принимает розовую окраску (белый экран!).
Взаимодействие кислоты с металлами. В три пробирки наливают равные количества раствора уксусной кислоты. В одну пробирку помещают стружки магния, в другую — мелкие кусочки цинка, в третью — кусочки железной или медной проволоки. В первой пробирке наблюдают довольно энергичную реакцию. Убеждаются в том, что выделяющийся газ — водород, для чего пробирку закрывают пробкой с вертикальной трубочкой, собирают газ в перевернутую пробирку и поджигают его. Во второй пробирке реакция идет медленно и требует подогрев. Реакция с медью не идет даже при сильном нагревании.
Взаимодействие с основаниями. К очень разбавленному раствору щелочи, подкрашенному фенолфталеином, добавляют понемногу раствор уксусной кислоты, пока не обесцветится фенолфталеин. Составляют уравнение соответствующей реакции.
Аналогичный опыт может быть показан с гидроксидом кальция, взмученным в воде. При добавлении уксусной кислоты раствор становится прозрачным (ацетат кальция растворим в воде).
Взаимодействие с солями. Для опыта следует воспользоваться солью кислоты более слабой, чем уксусная, чтобы показать течение реакции до конца и образование соли уксусной кислоты. Наиболее удобны для этой цели карбонаты.
В маленькую колбу с отводной трубкой помещают 1—2 г поташа, соды или толченого мела и приливают 4—5 мл раствора уксусной кислоты. Колбочку закрывают пробкой и отводную трубку погружают в стакан с известковой водой. Известковая вода мутится от углекислого газа. Немного получившегося раствора можно выпарить на часовом стекле, чтобы наблюдать образование соли уксусной кислоты.
Уксусная кислота — кислота слабая. Чтобы показать учащимся, что уксусная кислота имеет небольшую степень диссоциации и является кислотой слабой, необходимо наряду с демонстрацией обычного опыта электропроводности ее поставить опыты, позволяющие провести хотя бы качественное сравнение скорости реакций уксусной кислоты и минеральных кислот.
а) В три пробирки помещают кусочки цинка и приливают равные количества соляной, серной и уксусной кислот (одинаковой концентрации). Замечают, что с уксусной кислотой реакция идет очень плохо или идет только при нагревании.
б) В три демонстрационные пробирки насыпают равные количества карбоната меди и прибавляют равные количества растворов соляной, серной и уксусной кислот одинаковой концентрации. Замечают, что в последнем случае скорость реакции наименьшая.
в) Если учащиеся знакомы с гидролизом солей, то можно показать гидролиз ацетата натрия и ацетата железа.
Последний опыт одновременно знакомит учащихся с характерной цветной реакцией уксусной кислоты.
К разбавленному раствору ацетата натрия приливают несколько капель фенолфталеина, и раствор разливают в две пробирки. Раствор в одной пробирке нагревают. Незначительное вначале порозовение фенолфталеина становится совершенно отчетливым при нагревании, так как гидролиз при этом усиливается:
CH3COONa + Н 2 O ó СН 3 СООН + NaOH
Поскольку водный раствор соли имеет щелочную реакцию, значит, уксусная кислота — кислота слабая.
Разбавленный раствор уксусной кислоты в стакане нейтрализуют постепенно щелочью в присутствии фенолфталеина или берут ранее полученный продукт нейтрализации. К раствору прибавляют несколько капель раствора хлорида железа FeCl3. Наблюдается характерное темно-красное окрашивание вследствие образования
ацетата железа Fe (III). При кипячении раствора образуется обильный красно-бурый осадок основного ацетата железа Fe(OH)2CH3COO. Гидролиз в этом случае проходит в значительной степени, так как соль образована слабым основанием и сравнительно слабой кислотой.
Основность уксусной кислоты. Хотя учащимся известны молекулярная и структурная формулы кислоты, можно экспериментально показать, что уксусная кислота одноосновна. Тогда станет совершенно очевидным различие в свойствах атомов водорода в молекуле кислоты.
Одноосновность кислоты легко показать, демонстрируя реакцию нейтрализации с применением молярных растворов.
Молярные растворы можно приготовить, например, из расчета 4 г едкого натра в 100 мл раствора и 6 г уксусной кислоты в 100 мл раствора. Отмеряют в коническую колбочку 10 мл молярного раствора кислоты, добавляют 2—3 капли фенолфталеина и прибавляют постепенно молярный раствор щелочи из другой бюретки до тех пор, пока появляющаяся розовая окраска не будет исчезать при взбалтывании жидкости, т.е. на каждую молекулу кислоты потребовалась одна, а не две и не три молекулы щелочи. Это значит, что уксусная кислота одноосновна.
Количественное получение метана из солей уксусной кислоты. Соли уксусной кислоты при нагревании со щелочью образуют метан (с. 27). Количественное проведение опыта дает возможность сделать заключение о структурной формуле кислоты.
Исследование продуктов реакции и сопоставление количества вступившей в реакцию соли с количеством образующегося метана позволяют сделают заключение о том, что реакция выражается уравнением:
CH3COONa + NaOH à СН 4 + Na2CO3
На основании этого ведутся рассуждения о возможной структуре соли и, следовательно, кислоты.
Собирают прибор, как показано на рис. 30. В небольшую колбу или пробирку (желательно из тугоплавкого стекла) помещают хорошо перемешанную смесь порошков свежеприготовленного безводного ацетата натрия и натронной извести в весовом отношении 1 : 4 (например, 2 и 8 г или 3 и 12 г). Избыток извести необходим, чтобы обеспечить полное использование соли. Двугорлую склянку-газометр заполняют насыщенным раствором поваренной соли. Прибор проверяют на герметичность.
Смесь нагревают на газовой горелке. Нагревание должно быть равномерным и достаточно интенсивным. После того как объем
метана перестанет увеличиваться, нагревание прекращают и дают пробирке остыть. Некоторое количество раствора хлорида натрия при этом переходит обратно в склянку. Установив уровни жидкости в стакане и склянке на одной линии, определяют объем газа в склянке или объем жидкости в стакане.
Отделив газометр от пробирки, можно вытеснить из него часть газа (поднимая стакан с водой) и подтвердить, что этот газ — метан. Вычислив количество вещества исходной соли и количество вещества образующегося метана (н.у.), делают вывод, что из одного моля ацетата натрия получается один моль метана. Получающиеся отклонения из-за неполноты протекания реакции и образования побочных продуктов незначительны и совершенно не дают повода сделать какое-либо другое заключение (например, о том, что из одного моля соли образуется два моля метана).
Чтобы установить природу твердого продукта реакции, в пробирку добавляют немного соляной кислоты, закрывают пробкой и отводную трубку погружают в известковую воду. По помутнению известковой воды устанавливают, что при реакции образовался карбонат. Очевидно, что это карбонат натрия.
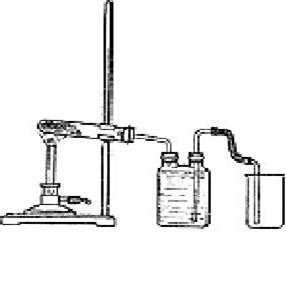
Рис. 30. Количественный опыт получения метана при взаимодействии ацетата натрия с натронной известью
Опыт дает надежные результаты в том случае, если исходные вещества будут тщательно подготовлены, хорошо перемешаны и будет обеспечено достаточное нагревание.
Получение кислоты окислением этанола. Альдегиды, как известно учащимся, легко окисляются в кислоты. Поэтому окисление спиртов в альдегиды можно поставить так, что образующийся альдегид, не успев удалиться из сферы реакции, тут же окислится далее в кислоту:
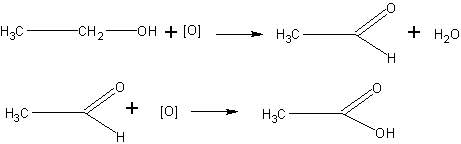
В качестве окислителя может быть использована хромовая смесь. Чтобы эта смесь могла окислить спирт в кислоту, реакцию проводят в условиях большей концентрации окислителя: берут больше бихромата, чем при получении альдегида, а спирт приливают к окислительной смеси постепенно, по мере отгонки образующейся кислоты.
Когда эти особенности получения кислоты обсуждены с учащимися, им становится понятным весь последующий опыт и одновременно закрепляются в памяти условия получения альдегидов из спиртов.
В колбочку с отводной трубкой (рис. 31) помещают 5 г измельченного бихромата калия К2Сг2О7 и 5 мл концентрированной серной кислоты. Из капельной воронки прибавляют по каплям водный раствор этанола (2 мл спирта на 8 мл воды) и отгоняют образующуюся уксусную кислоту. В приемнике собирается несколько миллилитров водного раствора уксусной кислоты с примесью альдегида и сложного эфира. Учащиеся должны дать объяснение изменению окраски раствора в колбе.

По запаху убеждаются в получении кислоты. Наблюдают образование водорода при действии на кислоту магния. Если учащиеся были знакомы также с цветной реакцией уксусной кислоты, то
нейтрализуют часть дистиллята содой (реакция не должна быть кислой) и добавляют несколько капель раствора хлорида железа (III). Темно-красное окрашивание раствора свидетельствует о наличии уксусной кислоты.
Запах уксусной кислоты иногда перебивается запахом альдегида. Чтобы освободиться от альдегида, кислоту нейтрализуют содой и раствор выпаривают. Альдегид при этом улетучивается. К остатку приливают минеральную кислоту и смесь слегка нагревают. Ощущается характерный запах уксусной кислоты.
Получение уксусной кислоты из ее солей. Данный эксперимент является повторением хорошо известного учащимся опыта из курса неорганической химии.
В колбочку с отводной трубкой насыпают 5 г обезвоженного ацетата натрия и добавляют 5 мл концентрированной серной кислоты. Сразу же начинается реакция. Подогревая колбу на горелке, отгоняют уксусную кислоту в пробирку через воздушный холодильник (стеклянную трубку). Если пробирку держать в ледяной воде, можно получить чистую уксусную кислоту в кристаллическом виде.
При необходимости уксусная кислота может быть получена таким способом' в значительных количествах.
Получение кислоты из продуктов сухой перегонки дерева. Ранее было показано (с. 86), что сухая перегонка дерева приводит к выделению дегтярной воды. Поэтому задача получения уксусной кислоты сводится к тому, чтобы удалить из дегтярной воды метанол и ацетон.
Предварительно с помощью лакмуса необходимо убедиться в присутствии кислоты в дегтярной воде.
Имеющееся в распоряжении количество дегтярной воды обрабатывают взмученной в воде известью до появления щелочной реакции на лакмус. При этом уксусная кислота образует ацетат кальция (СН3СОО)2Са. От раствора отгоняют метанол и ацетон или же раствор выпаривают до образования сухого остатка — так называемого древесного порошка, представляющего собой ацетат кальция с избытком извести. Порошок обрабатывают в колбе концентрированной серной кислотой и отгоняют уксусную кислоту, как в предыдущем опыте. В приемнике собирается концентрированная (60—80-процентная) уксусная кислота.
Получение уксусного ангидрида. Учащиеся должны иметь представление о том, что карбоновым кислотам, как и минеральным кислородсодержащим кислотам, соответствуют ангидриды.
При отсутствии в школьной лаборатории уксусного ангидрида (СН3СО)2О для демонстрационных целей он может быть приготовлен по реакции ацетата натрия с хлористым ацетилом:
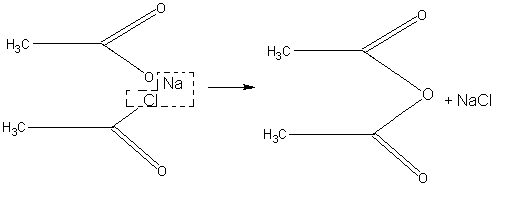
Чтобы жидкий хлористый ацетил по возможности нацело прореагировал и не улетучивался с ангидридом, пользуются избытком нелетучего вещества — ацетата натрия. Опыт проводят в вытяжном шкафу.
В колбу с отводной трубкой помещают 8 г обезвоженного ацетата натрия и приливают маленькими порциями 4—5 мл хлористого ацетила, встряхивая при этом колбу. Реакция образования ангидрида идет с выделением тепла.
К колбе присоединяют воздушный холодильник и отгоняют образующийся ангидрид на пламени горелки (темп. кип. 140°С). Сперва колбу нагревают осторожно, затем нагревание усиливают. Так как ангидрид обычно получается все же с примесью хлористого ацетила, к дистилляту прибавляют 0,5—1 г порошка ацетата натрия, чтобы полностью превратить хлористый ацетил в ангидрид, и снова перегоняют или же сохраняют его с примесью этой соли. Препарат обладает запахом уксусной кислоты. Хранят его в плотно закупоренной склянке. При действии воды на уксусный ангидрид образуется уксусная кислота:
(СН3СО)2 O + Н2О à 2СН3СООН
О наличии последней убедительно свидетельствует лакмусовая бумажка.
Получение хлористого ацетила. Хлористый ацетил может оказаться необходимым не только для получения ангидрида уксусной кислоты, но и для синтеза сложных эфиров.
Его получают действием треххлористого фосфора на уксусную
кислоту:
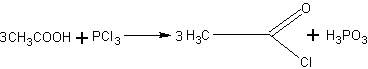
В колбу, соединенную с нисходящим водяным холодильником, помещают ледяную уксусную кислоту и при охлаждении небольшими порциями прибавляют треххлористый фосфор. Затем колбу закрывают пробкой и нагревают в вытяжном шкафу на водяной бане при 45— 50°С. Нагревание ведут до тех пор, пока не прекратится выделение хлороводорода (вследствие взаимодействия трех-
хлористого фосфора с протонсодержащими реагентами) и пока жидкость не разделится на два слоя. Сверху собирается хлористый ацетил, а внизу — фосфористая кислота. Хлористый ацетил отгоняют на водяной бане.
Так как хлористый ацетил чрезвычайно легко разлагается влагой воздуха, то приемник следует закрыть хлоркальциевой трубочкой.
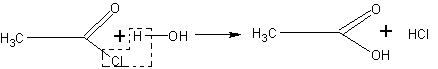
Хлористый ацетил можно отделить от фосфористой кислоты также с помощью делительной воронки.
Непременным условием успеха опыта является использование совершенно сухой посуды. Хранят хлористый ацетил в сухой склянке с плотной пробкой, залитой парафином.
Реакция хлористого ацетила с водой может служить наглядным примером взаимного влияния атомов в молекуле. Чрезвычайная подвижность атома хлора в группировке
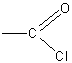
объясняется смещением электронной плотности в сторону кислорода карбонильной группы.
К 5—6 мл холодной воды в пробирке прибавляют несколько капель хлористого ацетила. Хлористый ацетил энергично реагирует с водой, образуя уксусную и соляную кислоты. В этом легко убедиться с помощью лакмуса и раствора нитрата серебра. Если вода для опыта взята недостаточно холодная, реакция происходит мгновенно. Разумеется, никакого подогрева смеси при этом не производится. Уксусный ангидрид реагирует с водой значительно слабее.
Исследование образца уксусной кислоты. Работа представляет интерес для внеклассных занятий по химии, так как знакомит учащихся с приемами контроля химической продукции.
Уксусная кислота может быть различной концентрации и может содержать примесь минеральных кислот, спирта и других органических веществ. Зная способ получения кислоты, учащиеся могут объяснить, как появляются эти примеси.
Концентрацию уксусной кислоты определяют титрованием ее щелочью известной концентрации. Для титрования столового уксуса может быть приготовлен 0,1 М раствор щелочи, для титрования эссенции — молярный раствор. С помощью бюретки берут по
5 мл исследуемого раствора в три конические колбочки, добавляют по 2—3 капли фенолфталеина и титруют из бюретки щелочью до появления остающейся при взбалтывании розовой окраски фенолфталеина. Из трех определений берут среднее арифметическое. Зная, что реакция выражается уравнением
СН3СООН + NaOH à CH3COONa + Н2О
вычисляют молярную, а затем и процентную концентрацию кислоты в исследуемом образце.
Примесь серной кислоты определяют, добавляя к образцу раствор хлорида бария. При отсутствии серной кислоты не должно получаться мути сульфата бария.
Примесь соляной кислоты устанавливают с помощью раствора нитрата серебра. В случае наличия хотя бы незначительного количества соляной кислоты при добавлении раствора нитрата серебра и подкислении азотной кислотой появляется муть или осадок.
Примесь органических соединений устанавливается с помощью слабого (0,1%) раствора перманганата калия. При наличии примесей перманганат обесцвечивается; уксусная кислота в этих условиях, как известно, не окисляется.
Таким способом могут быть исследованы образцы химически чистой уксусной кислоты, столового уксуса, уксусной эссенции и кислоты, полученной учащимися в лаборатории.
МУРАВЬИНАЯ КИСЛОТА
При изучении муравьиной кислоты необходимо поставить опыты, показывающие особенности ее строения и химических свойств.
Разложение муравьиной кислоты на оксид углерода ( II ) и воду. После того как учащиеся ознакомятся с физическими свойствами муравьиной кислоты (агрегатное состояние, запах, цвет) и вспомнят ее структурную формулу по реакциям окисления формальдегида, целесообразно поставить вопрос о том, как может быть подтверждена ее структурная формула. Учащиеся обращают внимание на то, что молекула муравьиной кислоты построена как бы из молекулы воды и молекулы оксида углерода (II):
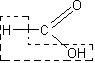
Естественно встает вопрос, нельзя ли получить кислоту реакцией оксида углерода (II) с водой. Учитель сообщает, что эта реак-
ция не идет так просто, как кажется: угарный газ не вступает в реакцию с водой. Но можно провести обратную реакцию: разложить кислоту на оксид углерода (II) и воду. В качестве водоотнимающего средства можно воспользоваться часто применяемой для этой цели серной кислотой. Оксид углерода (II) нетрудно будет обнаружить по его характерному пламени при горении.
В небольшую колбочку (или пробирку) с отводной трубкой наливают 1 мл муравьиной кислоты и 3-4 мл концентрированной серной кислоты. Колбу закрывают пробкой и нагревают в пламени горелки. Образующийся газ собирают в два цилиндра над водой. Во втором цилиндре газ поджигают (в первом — смесь газа с воздухом может дать взрыв). По синей окраске пламени учащиеся узнают оксид углерода (II). После этого поджигают оксид углерода (II) у отводной трубки. Опыт ведут до полного разложения муравьиной кислоты или останавливают его, прекращая нагревание. При проведении опыта необходимо следить, чтобы ядовитый газ не проникал в помещение. Опыт подтверждает формулу муравьиной кислоты.
Окисление муравьиной кислоты. Учащиеся легко устанавливают, что муравьиная кислота одновременно является альдегидом, так как имеет группировку атомов
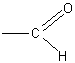
Это дает возможность предположить, что муравьиная кислота должна окисляться легче уксусной, и в частности давать реакцию серебряного зеркала.
До проведения опыта можно высказать предположение и о том, какие вещества будут получаться в результате реакции. Учащиеся составляют уравнение реакции, аналогичное уравнению для альдегидов, и замечают, что образуется угольная кислота:
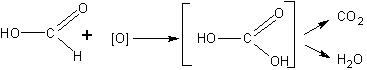
Поскольку угольная кислота, как известно, распадается с образованием углекислого газа, то для большей убедительности опыт, следовательно, надо поставить так, чтобы попытаться обнаружить углекислый газ.
а) Окисление перманганатом калия. В колбочке или пробирке с отводной трубкой к 1 мл муравьиной кислоты приливают 10 мл разбавленного раствора перманганата калия и немного серной кис-
лоты. Нагревают колбу через асбестовую сетку. Отводную трубку опускают в известковую воду. Перманганат калия при реакции обесцвечивается, содержимое колбы пенится от образующегося газа, и известковая вода мутится. Уксусная кислота, как известно, не обесцвечивает перманганат калия.
б). Окисление аммиачным раствором гидроксида серебра. Реакцию проводят как обычно, однако восстанавливающееся серебро при этом чаще всего выделяется не в виде зеркала, а в виде черного
осадка.
Получение муравьиной кислоты. Получение муравьиной кислоты из спирта и альдегида после всего изученного не представляет особого интереса. Значительно важнее было бы показать учащимся получение кислоты синтезом формиата натрия из оксида углерода(II) и едкого натра, что соответствует промышленному способу. Однако необходимость обращения со значительными количествами оксида углерода (II), даже при всей тщательности работы, делает опыт неприемлемым для школы.
При отсутствии в лаборатории муравьиной кислоты она может быть приготовлена нагреванием щавелевой кислоты с глицерином. Щавелевая кислота в этих условиях разлагается, образуя углекислый газ и муравьиную кислоту:
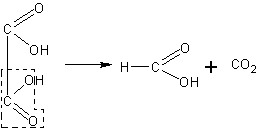
В колбу емкостью 200—250 мл с отводной трубкой помещают 30 г безводного глицерина и 30 г безводной щавелевой кислоты (кислоту обезвоживают осторожным нагреванием в сушильном шкафу при 95 - 100°С). Закрывают колбу пробкой с термометром, шарик которого погружают в смесь веществ. К колбе присоединяют нисходящий холодильник и приемник для дистиллята. Нагревают колбу через асбестированную сетку так, чтобы термометр показывал 110 — 115°С. Около 100°С начинается обильное выделение углекислого газа. При этом начинает отгоняться муравьиная кислота. Когда выделение углекислого газа станет слабым, добавляют вторую порцию (30 г) щавелевой кислоты и снова продолжают перегонку. При необходимости добавляют третью такую же порцию кислоты. После повторной дистилляции удается получить довольно крепкую муравьиную кислоту (темп. кип. кислоты 100°С).
Если почему-либо не удалось приготовить безводную щавелевую кислоту, можно воспользоваться кристаллической кислотой, беря ее всякий раз несколько большее количество. В этом случае будет получаться менее концентрированная кислота, так как одновременно перегоняется значительное количество воды.
Взаимодействие формиата натрия с натронной известью. Учащимся известно, что при нагревании солей карбоновых кислот с натронной известью (или едким натром) образуются соответствующие углеводороды.
Будет очень интересно предложить учащимся решить вопрос о том, какие продукты получатся при нагревании формиата натрия с натронной известью, а затем поставить соответствующий опыт и определить образующиеся вещества.
При реакции получаются водород и карбонат натрия:
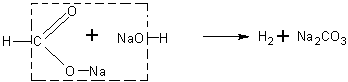
СТЕАРИНОВАЯ КИСЛОТА
При изучении высших кислот учащиеся подробно знакомятся со свойствами бытового химического продукта — мыла и впервые на практике встречаются с веществом, обладающим двойственной функцией, — олеиновой (непредельной) кислотой.
Свойства стеариновой кислоты. Стеариновая кислота в воде нерастворима, поэтому для опытов, иллюстрирующих ее кислотные свойства, нельзя, как обычно, воспользоваться водным раствором.
а) Расплавляют немного стеарина или стеариновой свечи в фарфоровой чашке и помещают в него небольшой кусочек натрия. Наблюдается выделение газа — водорода:
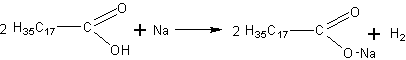
б) В пробирке растворяют кусочек стеарина в органическом растворителе (эфир, хлороформ, бензол) и к полученному раствору добавляют 2 капли спиртового раствора фенолфталеина. Затем вносят 1—2 капли разбавленного раствора гидроксида натрия и встряхивают пробирку. Розовой окраски раствора не наблюдается, так как стеариновая кислота нейтрализовала щелочь:
С17Н35СООН + NaOH à C17H35COONa + Н2О
При дальнейшем прибавлении щелочи к раствору кислоты розовая окраска появляется после того, как кислота будет нейтрализована.
Добавляя щелочь к эфиру с фенолфталеином без стеариновой кислоты, наблюдают моментальное появление окраски.
в) В пробирку со спиртом добавляют 2—3 капли щелочи и 1-2 капли фенолфталеина и к полученной смеси при перемешивании прибавляют эфирный раствор стеариновой кислоты или даже твердый стеарин. При этом происходит обесцвечивание раствора вследствие нейтрализации щелочи.
Стеариновая кислота — кислота слабая. О силе стеариновой кислоты можно судить по гидролизу ее солей, например стеарата натрия C17H35COONa.
а) Растворяют в воде тонкие стружки простого мыла и добавляют спиртовой раствор фенолфталеина. Появление розовой окраски говорит о том, что стеариновая кислота — кислота слабая. Параллельно может быть испытан фенолфталеином водный раствор ацетата натрия. В этом случае розовая окраска если и появляется, то очень слабая, так как уксусная кислота сильнее стеариновой.
б) В цилиндр до половины наливают воду, а затем по стенке осторожно прибавляют небольшое количество спиртового раствора мыла с фенолфталеином. В спиртовом растворе гидролиз соли не происходит и розовая окраска не наблюдается. На границе же соприкосновения спиртового раствора соли с водой появляется розовое кольцо.
Получение мыла (стеарата натрия) из стеарина. Один из современных способов получения мыла состоит в нейтрализации кислот, получаемых окислением синтетических углеводородов или же непосредственным синтезом из водяного газа.
Кусочек стеарина (стеариновой кислоты) нагревают в химическом стаканчике с водой, пока стеарин не расплавится (темп. пл. 69°С), и приливают к нему понемногу раствор гидроксида натрия до полного растворения (стеарат натрия растворяется в воде). К полученному раствору прибавляют поваренную соль до насыщения.
В насыщенном растворе поваренной соли стеарат натрия не растворяется и всплывает наверх в виде хлопьев.
Получение стеариновой кислоты из мыла. Стеариновая кислота, как кислота слабая, может быть получена действием минеральной кислоты на мыло:
2C17H35COONa + H2SO4 à 2C17H35COOH + Na2SO4
Как вещество не растворимое в воде, стеариновая кислота при этом выделяется из раствора.
В химическом стаканчике при нагревании готовят крепкий раствор мыла в воде. Для более быстрого растворения мыло должно быть предварительно нарезано в виде тонких стружек. Продолжая нагревать раствор мыла, прибавляют к нему раствор серной кислоты до выделения стеариновой кислоты. При охлаждении раствора 1 сверху образуется твердый слой стеариновой кислоты.
Таким способом в случае необходимости можно получить некоторое количество кислоты для классных занятий.
Моющее действие мыла. Мыло обладает свойством эмульгировать жиры и суспензировать твердые частички грязи.
а) Готовят, как было указано выше, раствор мыла в воде и прибавляют к нему 1 мл растительного масла. Смесь сильно взбалтывают до образования эмульсии, похожей на молоко. В другой пробирке подобным способом получают эмульсию из таких же количеств чистой воды и масла. Хотя во второй пробирке эмульсия была получена позднее, она быстро расслаивается на воду и масло. В первой же пробирке эмульсия оказывается устойчивой и не разделяется в течение всего урока.
б) В двух разных пробирках готовят суспензию сажи в воде и в мыльном растворе. Фильтруют растворы одновременно через бумажные фильтры. В первом случае фильтруется чистая вода, во втором случае мыльный раствор настолько сильно удерживает сажу, что суспензия, не разделяясь, проходит через фильтр.
Моющее действие мыла проявится еще более ярко, если фильтр с осадком сажи перевернуть на другую сторону, снова вложить в воронку и сперва пропустить через него воду, а затем мыльный раствор. Вода проходит прозрачной и не смывает сажу, мыльный же раствор совершенно очищает фильтр от сажи, становясь черным.
Действие жесткой воды на мыло. В жесткой воде мыло не дает пены и плохо мылит, так как превращается в нерастворимые в воде соли:
2C17H35COONa + СаСI2 à (C17H35COO)2Ca + 2NaCl
Хлопья нерастворимого мыла можно часто наблюдать при получении мыльного раствора в домашних условиях.
а) Раствор мыла в воде разливают в две пробирки. В одну из пробирок добавляют небольшое количество раствора хлорида кальция СаСI2. При встряхивании пробирок в одной из них наблюдают образование пены, в другой — отсутствие пены и образование осадка соли кальция.
б) В один цилиндр наливают около 50 мл дистиллированной воды, в другой такой же цилиндр — 50 мл водопроводной воды (если водопроводная вода очень «мягкая», в нее добавляют немного
раствора хлорида кальция). В оба цилиндра приливают по 1 мл спиртового раствора мыла и встряхивают. В первом случае образуется устойчивая пена. Во втором пены нет, но образуется осадок нерастворимой соли. Во второй цилиндр продолжают добавлять раствор мыла до тех пор, пока при встряхивании не будет получаться неисчезающая пена. По количеству затраченного раствора мыла можно приблизительно судить о степени жесткости воды.
Опыт показывает, что при пользовании жесткой водой большое количество мыла расходуется на осаждение кальциевых (и магниевых) солей и что только после их осаждения мыло, как поверхностно-активное вещество (ПАВ) начинает выполнять свою основную функцию — давать пену. Чтобы сделать воду «мягкой» и не расходовать мыло нерационально, соли кальция, как известно, осаждают предварительно кипячением или с помощью специальных добавок, например соды.
НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
Из класса непредельных одноосновных карбоновых кислот наибольший интерес для изучения представляют акриловая и олеиновая кислоты. Первая — как первый член гомологического ряда, производные которой имеют большое значение при получении синтетических материалов. Олеиновая кислота является представителем непредельных кислот, входящих в состав жиров.
Вместо акриловой кислоты СН2=СН—СООН можно воспользоваться ее ближайшим и более доступным гомологом — метакриловой кислотой, эфиры которой применяются для получения широко известных полимерных продуктов (органического стекла).
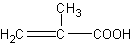
Получение метакриловой кислоты (по В.В.Некрасову). Метакриловая кислота может быть получена гидролизом сложного эфира — метилметакрилата. Метилметакрилат для этого опыта может быть в свою очередь получен деполимеризацией полиметилметакрилата (органического стекла), как это описано на с. 68. Гидролиз проводится в присутствии щелочи. Метакриловая кислота при этом образует соль, из которой она может быть выделена действием более сильной кислоты:
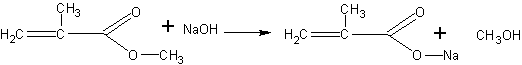
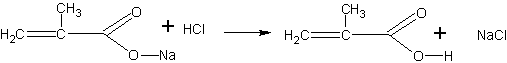
Помещают в пробирку 2 мл метилового эфира метакриловой кислоты (метилметакрилата) и 4 мл концентрированного раствора едкого натра. Чтобы смесь получилась гомогенной, добавляют 1 мл этанола и встряхивают. Через 15—20 мин переливают жидкость в фарфоровую чашку и выпаривают досуха на слабом пламени. Остаток представляет собой натриевую соль метакриловой кислоты с возможной примесью щелочи. Дальнейшая задача сводится к выделению кислоты из соли. Для этого сухой остаток переносят в пробирку и, охлаждая ее водой, добавляют несколько миллилитров концентрированной соляной кислоты (до кислой реакции на индикатор). После отстаивания смеси метакриловая кислота собирается сверху в виде маслянистой жидкости с характерным запахом. Кислоту переносят при помощи пипетки в другую пробирку.
Свойства метакриловой кислоты. Метакриловая кислота, будучи соединением непредельным, реагирует с бромной водой, перманганатом калия и легко полимеризуется.
а) К небольшому количеству (нескольким каплям) метакриловой кислоты приливают бромную воду и смесь встряхивают. Бромная вода обесцвечивается вследствие присоединения брома по месту двойной связи. Учащиеся составляют уравнение реакции.
Подобным образом проводится опыт с водным раствором пер-манганата калия.
б) К небольшому количеству метакриловой кислоты добавляют несколько крупинок перекиси бензоила в качестве инициатора реакции и нагревают до начала кипения. Кислота быстро полимеризуется.
Непредельность олеиновой кислоты. Олеиновая кислота является единственным представителем класса непредельных кислот, входящих в состав жиров и изучаемых в школьном курсе химии. Непредельность ее может быть проиллюстрирована действием обычных реактивов на двойную связь: бромной воды и раствора перманганата калия.
К 5—8 мл олеиновой кислоты в пробирке или колбочке приливают равный объем бромной воды или раствора перманганата калия и встряхивают. Окраска брома и перманганата калия исчезает вследствие присоединения по месту двойной связи.
ЩАВЕЛЕВАЯ КИСЛОТА
Наибольшее значение в этом разделе имеют опыты, связанные со строением щавелевой кислоты и ее двухосновностью.
Получение щавелевой кислоты из муравьиной. Первым подтверждением структурной формулы щавелевой кислоты может служить получение ее солей из солей муравьиной кислоты.
Формиат натрия при нагревании выделяет водород; одновременно образуется оксалат натрия
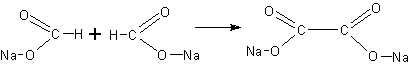
Очевидно, что из молекулы соли при этом уходит единственный атом водорода. А так как радикалы неспособны к сколько-нибудь длительному существованию, то они рекомбинируются, образуя молекулы новой соли, которой отвечает кислота
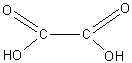
В пробирке, закрытой пробкой с вертикальной трубкой, нагревают в пламени горелки сухой формиат натрия.
Соль плавится и затем (при сильном нагревании) разлагается. Устанавливают выделение водорода, собирая его в пробирку или поджигая через некоторое время у отводной трубки.
Разложение щавелевой кислоты при нагревании с серной кислотой. Если щавелевая кислота имеет формулу
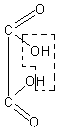
то можно предположить, что при отнятии от нее элементов воды должны выделяться углекислый газ и оксид углерода (II). Этот факт послужил бы подтверждением структурной формулы кислоты.
Учащимся можно предложить самим придумать прибор, в котором следовало бы провести эту реакцию так, чтобы обнаружить оба образующихся газа.
Опыт может быть осуществлен, например, в приборе, изображенном на рис. 32.
В небольшую колбочку помещают 2—3 г щавелевой кислоты и двойной объем концентрированной серной кислоты. В пробирку с отводной трубкой наливают известковую воду. При нагревании смеси кислот на горелке известковая вода мутится. Когда можно будет предположить, что воздух вытеснен из прибора, поджигают у отводной трубки пробирки оксид углерода (II), который горит характерным синим пламенем.
 Учащимся можно предложить разработать количественное проведение этого опыта, и в частности определить объемное соотношение образующихся газов. Некоторые указания к конструированию прибора им даст описание опыта разложения уксусной кислоты на углекислый газ и метан (с. 115). При этом в качестве обязательного требования необходимо поставить достижение максимальной простоты прибора.
Учащимся можно предложить разработать количественное проведение этого опыта, и в частности определить объемное соотношение образующихся газов. Некоторые указания к конструированию прибора им даст описание опыта разложения уксусной кислоты на углекислый газ и метан (с. 115). При этом в качестве обязательного требования необходимо поставить достижение максимальной простоты прибора.
Окисление щавелевой кислоты. Щавелевая кислота окисляется легче уксусной. Распадаясь на воду, углекислый газ и оксид углерода (II), она, очевидно, нуждается в незначительном количестве кислорода, чтобы дать конечные продукты окисления — углекислый газ и воду. Для простоты можно считать, что действие окислителя сводится к превращению угарного газа в углекислый.
В качестве окислителя может быть взят не раз применявшийся в подобных случаях перманганат калия с серной кислотой.
В небольшую колбочку с отводной трубкой наливают 5 мл концентрированного раствора щавелевой кислоты и равный объем разбавленной серной кислоты (1 : 5).
Из капельной воронки в колбу приливают постепенно 10 мл не слишком слабого раствора перманганата калия. При нагревании колбы фиолетовая окраска быстро исчезает и наблюдается энергичное выделение углекислого газа. Его пропускают в известковую или баритовую воду или же собирают в цилиндр и затем испытывают соответствующим способом. Уравнение реакции можно представить следующим образом:
5Н2С2O4 + 2KMnO4 + 3H2SO4 à 10СО2 + K2SO4 + 2MnSO4 + 8Н2O
Образование кислых и средних солей щавелевой кислоты. В молекуле щавелевой кислоты имеются две карбоксильные группы, следовательно, щавелевая кислота двухосновная.
Как кислота двухосновная, щавелевая кислота может давать соли кислые и средние. Это может быть показано на реакции нейтрализации.
Растворяют 12 г щавелевой кислоты примерно в 20 мл воды и делят раствор пополам. К одной части раствора приливают понемногу концентрированный раствор гидроксида калия. Наблюдают, что сначала образуется осадок, который при дальнейшем прибавлении щелочи растворяется. Очевидно, что сначала получается кислая соль (гидрооксалат калия), нерастворимая в воде. В дальнейшем, при добавлении щелочи, эта соль превратилась в среднюю, растворимую в воде:
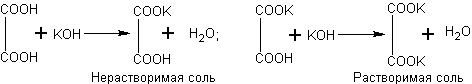
Если теперь к раствору средней соли прилить вторую порцию щавелевой кислоты, то снова образуется обильный осадок гидрооксалата калия:
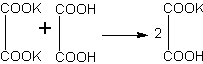
БЕНЗОЙНАЯ КИСЛОТА
Изучение бензойной кислоты на уроке не входит в программу по химии. Учителя иногда посвящают несколько минут ознакомлению с нею лишь для того, чтобы показать, как образуются кислоты в ароматическом ряду и что они собой представляют. Если ранее ставился опыт окисления бензальдегида в бензойную кислоту, здесь можно познакомить учащихся лишь с физическими свойствами ее.
Растворимость бензойной кислоты в воде. Встряхивая в пробирке очень небольшое количество кристаллов бензойной кислоты с водой, убеждаются, что заметного растворения не происходит. При нагревании пробирки происходит растворение кислоты, а при охлаждении она вновь кристаллизуется. Убеждаются, что водный раствор бензойной кислоты окрашивает лакмус в красный цвет.
Растворимость бензойной кислоты в щелочах. К небольшому количеству бензойной кислоты в пробирке прибавляют воду. Убедившись, что кислота не растворяется, добавляют по каплям крепкий раствор щелочи, пока кислота не растворится. После этого подкисляют раствор соляной кислотой. Выделяются мелкие кристаллы бензойной кислоты:
С6Н5СООН + NaOH à C6H5COONa + НСI+ H2O
C6H5COONa + НСI à С6Н5СООН + NaCl

Возгонка бензойной кислоты. Собирают прибор из двух пробирок разной величины, как показано на рис. 33. В большую пробирку на дно насыпают бензойную кислоту, а маленькая пробирка наполнена холодной водой. При нагревании прибора на пламени горелки бензойная кислота возгоняется и осаждается в виде белых кристаллов на пробирке-холодильнике.
С помощью бензойной кислоты учащимися может быть осуществлена имитация «зимнего пейзажа».
На картоне (с отверстиями) или на листе пористой (фильтровальной) бумаги монтируют небольшой макет сада. Под картоном (бумагой) нагревают в фарфоровой или железной чашке бензойную кислоту, накрыв всю установку стеклянным колпаком. Возгоняющаяся кислота, проходя через отверстия в картоне или поры в бумаге, осаждается на «деревьях» в виде красивого инея. Следует остерегаться попадания паров бензойной кислоты в атмосферу.
Получение бензойной кислоты окислением бензальдегида. Бензальдегид легко окисляется в бензойную кислоту кислородом воздуха.
На стеклянную пластинку, часовое стекло или в фарфоровую чашку помещают несколько капель бензальдегида. Через несколько минут начинают появляться кристаллы. К концу урока весь альдегид превращается в кислоту.
Взяв для опыта несколько миллилитров альдегида, таким способом можно получить бензойную кислоту в количестве, необходимом для демонстрации опытов с ней.
Получение бензола из бензойной кислоты (см. опыт на с. 63).
Дата: 2019-05-28, просмотров: 444.