Процесът на газификация (частично окисление с кислород) на газо-образни и течни горива се осъществява във факел при температура 1300 – 1600 0С и налягане 3,0 – 10,2 MРa в стоманени реактори, футировани с огнеопорни материали. Газообразни и течни горива, кислород и пара се подават в реактора през горелка, където става разпрашаване на течното гориво на малки капчици и смесването им с окислителя. Капките гориво се изпаряват в атмосферата на горещия газ и взаимодействат с кислорода, образувайки факел. При частично окисление на пари и газове се изключва само стадия на разпрашаване и изпарение.
Процесът на газификация се осъществява при недостиг на кислород с образуване на горещ газ. В качество на окислител служи кислорода. Участието на другия окислител – водните пари – в процеса на газифика-ция на въглеводородите е малко. Сярата се превръща в сероводород в повече от 90%. Около 0,5 – 3% от въглеродното гориво се превръща в сажди.
Полученият газ на 90 – 95% се състои от СО и Н2. В него се съдържа също въглероден диоксид, метан, азот, сероводород, органични съедине-ния на сярата, а също и непрореагирали водни пари. Необходимата дъл-бочина на превръщане без използване на катализатор се достига за сметка на провеждането на процеса при висока температура. Процесът се води при автотермични условия; топлината се получава за сметка на екзо-термичните реакции на газификация с образуване на СО и СО2.
Състава и добива на газа в процеса на паро-кислородна газифика-ция на алифатните въглеводороди се определя от условията на равнове-сие на същите реакции на парова конверсия на метана и конверсия на СО, които определят състава и добива на газ от ПК. Разликата е в това, че в реактора заедно с пара се подава и кислород, в който, макар и в неголеми количества се съдържа и азот. Уравненията на материалния баланс са дадени в таблица 16.
Газифията на алифатни въглеводороди с паро-кислородно подаване в производство на водород се използва рядко, тъй като е икономически неефективно в сравнение с паро-каталитичната конверсия. Практически интерес за производство на водород представлява газификацията на неф-тените остатъци – мазут, гудрон и др.
В състава на нефтените остатъци влизат не само високомолекулни парафинови въглеводороди, но и ароматни, хетероциклени и други съеди-нения. За технологични пресмятания на процеса на газификация е доста-тъчно да се знае елементния състав на суровината. Технологичните прес-мятания се улесняват и от това, че процеса се води при високотемперату-рни условия, когато съдържанието на метан в газа според условията на ТД равновесие е ниско и се определя основно от емпирични данни и лежи в границите 0,3 – 0,5% от газа.
При въвеждане на 0,5 м3 водна пара и 1 м3 кислород и достигане на равновесие не става отлагане на въглерод, но в действителност при про-цеса на газификация се отлага въглерод във вид на сажди. Затова в тех-нологичните изчисления се взема предвид саждообразуването в размер на 2 – 3%. За опростяване на технологичните изчисления се пренебрегва уравнието за равновесие на ПК на метана, а се отчита само равновесната реакция на конверсия на СО с водна пара.
Съдържанието на сяра в нефтените остатъци може да достигне 6 – 7%. ТД изчисления за преобразуването на сяра в условията на паро-кислородна газификация на нефтените остатъци са показали, че 90% от сярата се превръща в сероводород, около 7% - в карбамил-сулфид и 2% - във СS и неголямо количество – около 1% става на сажди.
Кислородът, съдържащ се в нефтените остатъци в количества не повече от 0,5 – 0,7 %, в процеса на газификация се превръща в кислород-съдържащи компоненти – Н2О, СО2 и СО. Не е нужно да се отчита вли-яние на кислорода в техническите изчисления, тъй като неговото присъст-вие практически не влияе на разхода на техническия кислород, нито на добива на газовите компоненти. Същото се отнася и за азота в суровината, съдържанието на който може да достигне до 1%. Азотът от суровината преминава основно в газа, но при газификация се образуват също в малки количества амоняк, азотни оксиди и цианиди. Трудно е да се определи за-висимостта на добива на тези съединения от съдържанието на азота в суровината. Технологичните изчисления, определящи разхода на кисло-род за газификация, добива и състава на газа за 1 кг суровина, се свежда до следното. Да обозначим елементния състав на 1 кг от суровината:
Въглерод............................. С Азот + кислород............ N
Водород.............................. Н Влага.............................. W
Сяра.................................... S Зола................................ А
Разходът на пара – „а” кг/кг от суровината, концентрацията на кисло-род в техническия кислород СО2, м3/м3, а концентрацията на азот, аргон и други благородни газове в техническия кислород тогава е 1 - СО2. Обема на кислорода в м3, изразходван за изгаряне на водорода – δ, а степента на ПК на СО с образуване на Н2 и СО2 – β.
За отределяне на въглерода, участващ в процеса на газификация с О2 и Н2О с образуване на СО + СО2, трябва от въглеродното гориво за извадим въглерода, превръщащ се в сажди (0,02 кг), и въглерод, израз-ходван за получаване на метан. Приемайки съдържанието на метана в га-за 0,5% и добива на газ – 3 м3 за 1 кг суровина, получаваме разхода на въглерод за образуване на метан равно на 0,008 кг. Количеството на гази-фицирания въглерод С` е равно на:
С` = С – (0,02 + 0,008)
Количеството на водорода в суровината, участващ в процеса на га-зификация се определя по уравнението:
Н` = Н – 0,00134 – 0,056. S
,където 0,00134 и 0,056.S е количеството водород, превръщащо се в СН4 и Н2S съответно.
Добива на отделните газови компоненти се определя по уравнения, приведени в таблица 16
Табл. 16 Материален баланс за пресмятане на паро-кислородната газификация на нефтените остатъци
| Компоненти | Обем, м3 за 1 кг суровина | |
| Изходни компоненти | Конвертиран газ | |
| Н2О О2 N2 CO CO2 H2 CH4 H2S COS + CS2 | 1,243.(a + W) 0,935.C` + δ (0,935.C` + δ)(1 - СО2)/ СО2 - - - - - - | 1,243.(a+W)–1,867.C`.β+2.δ - (0,935.C`+δ).(1-СО2)/СО2+0,8N 1,867.C`(1 – β) 1,867.C`.β 11,2.H` + 1,867. C`.β - 2δ 0,015 0,63.S 100.S |
След заместване на обема на компонентите Н2, СО2, СО, Н2О от таблицата в уравнението на константата на равновесие за реакцията на конверсия на СО с водни пари ще получим:
K2 = CH2.CCO2
CCO.CH2O
K2 = β.(11,2.H` + 1,867.C`.β – 2.δ)
(1 – β ).[1,243.(a + W) – 1,867.C`. β + 2. δ ]
Топлинният баланс на процеса на газификация се описва с урав-нението:
Q н + q т + qH 2 O + qO 2 = 1,867. C `.(1 – β).(12600 + t 2 . cCO ) + (11,2. H ` +
1,867. C `.β – 2.δ).(11100 + t 2 .cH 2 ) + [1.243.( a + W ) + 2.δ]. t 2 cH 2 O +
1,867. C `.β. t 2 . cCO 2 + qc + q
,където Q н е топлината от изгаряне на суровината, kJ/kg; q т е количество топлина, въвеждано със суровината в реактора, kJ/kg; qH 2 O е количество топлина, което се въвежда с парата, kJ/kg; qO 2 е количеството топлина, което се въвежда с кислорода в реактора, kJ/kgl; t 2 e температурата на из-ход от реактора, 0С; cCO, cH 2, cH 2 O, cCO 2 са средни топлинни капацитети на компонентите при постоянно налягане и температура на изход от реактора, kJ/(m3.0C); q – загуба на топлина в околната среда, kJ; qc – топлината на изгаряне и енталпията на саждите, метана, сероводорода, серните окиси, въглеродния сулфид и азота, пресметнати по уравнението:
qc = 1347 + 0,005.Q н + 18200 .S
Решавайки съвместно уравнението на равновесие на реакцията на конверсия на СО с водни пари и топлинния баланс ще намерим β и δ.
Szargan, P. е изучавал процеса на паро-кислородна газификация на течно гориво в промишлен реактор. Реакционните зони в газгенератора, според неговите изследвания, са показани на фигура 10.
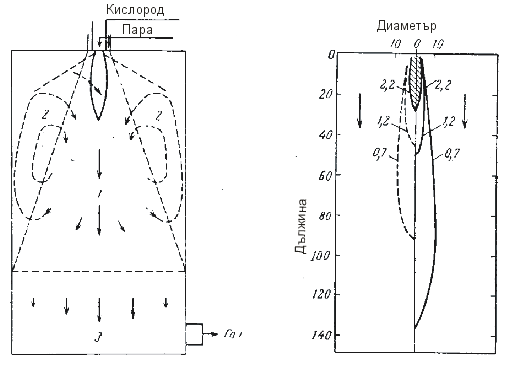
а б
Фиг. 10 а) Реакционни зони на факелния процес на газификация на течно гориво: 1 – зона на факела; 2 – зона на циркулация; 3 – зона на завършване на реакцията.
б) Изменение концентрацията на кислорода във факела при газификация на течни горива (прекъсната линия – екпериментални данни, непрекъсната линия – теоретични данни)
В горните зони течното гориво се разпръсква механично с форсун-ки и пневматично от паро-кислородната смес в горелката. Малките капки се изпаряват в атмосфера на горещ газ в зона 1 и 2. Потокът на окислителя засмуква изпареното гориво и газ от зона 2 в зона 1. В пламъка част от парите на горивото и газа изгарят, при което се достига температура по-висока от 2500 0С.
В противоположност на типичното направление на пламъка, този пламък е преобърнат, тъй като свободният кислород се намира отвътре, а горещият газ се засмуква отвън.
На фиг. 10 - б) е показано изменението на концентрацията на кисло-рода във факела за газификация на течни горива с отдалечаване от усти-ето. В пламъка, при концентрация на кислорода 2,2 м3 на 1 кг гориво, тем-пературата достига до 3000 0С. Заедно с продуктите от пълното горене СО2 и Н2О се образуват и продукти от дисоциация: СО, Н2, О2, а също и атомен кислород, водород и хидрооксиден радикал. Свободен и атомен кислород има не само на границите на пламъка, но и на разстояние, пре-вишаващо 1,6 пъти дължината на пламъка (концентрация на О2 > 1,2 м3/кг), а атомният водород и радикалът –ОН – на разстояние 2,2 (концентрация на О2 > 0,9 м3/кг). Дължината на пламъка се определя основно от сечение-то на изходната дюза на форсунката. Налягането в реактора не влияе на дължината на пламъка.
Обяснявайки химизма на процеса на газификация на течни горива и сравняването му с механизма на частично окисление на газообразно го-риво, авторите считат, че процесът протича в два стадия. Първо протича пълно изгаряне на въглеводородите, при което се изразходва всичкия кис-лород. Във втория стадий става конверсия на останалите въглеводороди с пара и въглероден диоксид. Предложен и механизъм на частично окисление на метана във факела с отчитане образуването на ацетилен в качеството му на междинен продукт. Съобразно с този механизъм проце-сът протича на три стадия: на първия става верижна реакция на окисле-ние на метана и се образуват предимно въглеводороди С2 и вода, на вто-рият стадии има окисление на ацитилена и водорода, а на третия – пълно окисление на всички междинни продукти до въглероден оксид и водород.
Л.Н. Алейнова и колектив експериментално определят основните стадии на непълно горене на метана. Авторите считат, че процесът се състои от три стадия. Първият се характеризира с пълно отреагиране на кислорода и натрупване на СО, водород, СО2, вода и малки количества ацетилен; на вторият стадий се натрупва ацетилен и спира натрупването на водни пари и СО2; на третият стадий става конверсия на въглеводоро-ди, разграждане на ацетилена до отделните елементи и газификация на саждите.
Отличителна особеност на газификацията на течни горива е отделя-не на сажди. Газификацията се води при условия, водещи до образуване на сажди, въпреки че при достигане на ТД равновесие, въглеродът в продуктите на реакцията трябва да отсъства. Получаването на сажди зависи от относителния разход на кислород и водна пара, температурата и налягането на процеса, качеството на разпръскане на горивото и смес-ването му с окислителя. Получаването на сажди намаля с увеличаване от-носителния разход на кислород и водна пара. Установено е, че при отно-сителен разход на кислород, равен на 0,6 м3 на 1 кг мазут, се отделя 7% (масови) сажди (изчислено по мазута), при относителен разход 0,8 м3/кг – 0,5% (масови).
Образуването на дисперсен въглерод се обяснява с това, че заедно с процесите на непълно и пълно изгаряне при газификация протичат процеси на разцепване на въглеводородите. В съответствие с основните положения в теорията на П. А. Теснер, образуването на сажди се предшества от образуването на радикал, от който се образува зародиша на саждената частица. От съотношението кислород:гориво зависи не само добива на сажди, но и тяхната относителна повърхност.
Електронно-микроскопски изследвания на сажди, получени от паро-кислородна газификация на мазут, показали, че първичните частици имат сферична форма и диаметър 20 - 50ηm. Има и по-големи частици, които, както предполагат авторите, се образуват от механично съединяване на първичните. От това изследване се прави извод, че саждите в процеса на газификация на течни горива се образуват от паровата фаза, а не от теч-на при коксуване на капки от гориво, както се е предполагало по-рано.
Електронно-микроскопските изследвания показали също, че първич-ните частици изгарят отвън и с повишение на температурата стават силно пористи. Някои частици се окисляват до търкостенни черупки, защото окислението при тях протича първо във вътрешността на частицата.
Изборът на режим на газификация на течните и газообразни въгле-водороди се определя не само от условията на ТД равновесие, отколкото от техническите възможности за водене на процеса. Давлението се под-бира в зависимост от технико-икономическите разчети. Широко разпрост-ранение са получили инсталации за газификация при налягане 2,0 – 4,2 MРa; максималното налягане на процеса може да достигне 10 Mрa.
В зависимост от условията на ТД равновисие, ниска концентрация на метан в газа може да се достигне при температура по-висока от 1000 0С. Но скоростта на реакция при такава температура без катализатор е малка, а при това се наблюдава значително саждообразуване. Затова процесът се провежда при температура по-ниска от 1300 0С. С повишава-не на налягането трябва да се повиши и температурата на процеса, например по следния начин:
Налягане, МРа............................ 3 6 10
Температура, 0............................ 1300 1350 1400
Отношението пара:суровина се приема също от емпиричните данни от 0,3 до 0,5, при което колкото по-тежка е суровината, толкова по-висок е разхода на пара. Подгряването на изходните компоненти позволява малко да се намали разхода на кислород и да се подобрят условията на проце-са.
Температурата на подгряване на суровината се колебае в широки граници от 80 до 300 0С. Минималната температура е ограничена от вис-козността на суровината: суровината трябва да бъде подгрята минимум до 20 – 30 0С, като при тази температура визкозитета става достатъчен за по-даване и разпръскване във форсунките. В тях суровината се разпръсква добре при вискозитет 3 – 4 условни градуса. Максимално допустима тем-пература на нагряване на суровината се ограничава от условията на отде-ляне на кокс по стените на подгревателя на суровината. Суровината ряд-ко се подгрява в подгреватели с пряк огън, а с водна пара с ниско наляга-не и температура 110 – 120 0С.
Най-сложно се явява подгряването на кислорода във връзка с ръста на неговата реакционна активност по отношение на металите. Температу-рата на кислорода, подаван в реоктора, се избира в границите от 20 – 300 0С. Безопасното подгряване на кислород до 300 0С може да се обезпечи при използване на прегрята водна пара.
Разходът на кислород зависи също и от загубите на топлина в реак-ционната зона, а последните зависят от производителността и конструк-тивното оформление на газгенератора и е в границите 0,1 – 4% от топли-ната на изгаряне на изходната суровина. В съвремените високопроизводи-телни промишлени газгенератори загубата на топлина в реакционната зона не превишава 0,3 – 0,5%.
В таблица 17 са приведени показатели на процеса паро-кислородна газификация на природен газ, бензинови пари и тежко котелно гориво при налягане около 3 МРа, а в талица 18 – газификация на различни суровини про налягане 6 МРа по данни на фирма Shell. В таблица 19 е даден мате-риален баланс от газификацията на мазут.
Табл. 17 Показатели на процеса паро-кислородна газификация на въглеводороди при налягане 3 МРа
| Показатели | Приро-ден газ | Бен-зин | Тежко котелно гори-во |
| Разход за 1 кг от суровината кислород (95%-ен)............... водна пара (с температура на насищане 246 0С)........... Температура на подгряване, 0С суровина.............................. кислород.............................. водна пара.......................... Добив на газ, м3 за 1 кг суровина Състав на газа, % СО2 ………………………….. СО …………………………… Н2 ……………………………. СН4 ………………………….. N2 + Ar ………………………. H2S + COS …………………. | 0,98 0,05 236 236 246 3,73 2,8 34,5 61,0 0,3 1,4 - | 0,83 0,35 300 300 300 3,29 3,9 41,7 52,7 0,3 1,4 7.10-3 | 0,75 0,40 236 236 246 2,95 4,3 46,9 46,2 0,3 1,4 0,9 |
Табл. 18 Показатели за процеса паро-кислородна газификация на Различни суровини при налягане 6 МРа
| Показатели | Природен газ | Лек бензин от пър-вична дестилация | Мазут | Крекинг-остатък | Вакуум остатък | Остатък от деас-фалтизация | Мазут | Крекинг-остатък |
|
Температура, 0С, на вход в реактора суровина............... кислород............... пара....................... Разход на кислород за 1 кг суровина (95%) м3/кг....................... пара, кг.................. газ (сух), м3........... Състав на газа, % СО2........................ СО......................... Н2.......................... СН4....................... N2.......................... Ar.......................... H2S....................... COS..................... Производство на пара в котел-утилизатора, кг/кг............................ Налягане на насите- ната пара, МРа........ Добив на сажди, % (тегл.) | Без циркулация на сажди | С циркула- ция на саж- ди | ||||||
| 300 245 313 0,983 0,20 3,63 3,88 33,82 60,13 0,60 0,72 0,85 - - 3,54 10,5 0,02 | 250 245 313 0,879 0,40 3,21 5,21 41,29 51,45 0,60 0,58 0,86 0,01 - 3,06 10,5 3,0 | 245 245 313 0,750 0,45 2,94 4,91 46,19 46,02 0,60 0,65 0,80 0,80 0,03 2,72 10,5 3,0 | 245 245 313 0,763 0,45 2,98 4,86 46,89 45,81 0,60 0,63 0,81 0,38 0,02 2,81 10,5 3,0 | 245 245 313 0,745 0,50 2,90 5,55 46,54 45,03 0,60 0,68 0,81 0,76 0,03 2,80 10,5 3,0 | 300 245 313 0,771 0,55 2,80 6,09 46,99 43,26 0,60 0,62 0,80 1,57 0,07 2,80 10,5 3,0 | 245 245 313 0,776 0,45 3,01 5,10 46,61 45,42 0,60 0,65 0,81 0,78 0,03 2,85 10,5 3,0 | 245 245 313 0,786 0,47 3,06 5,15 47,01 45,41 0,60 0,63 0,81 0,37 0,02 2,90 10,5 3,0 | |
Табл. 19 Материален баланс на паро-кислородната газификация на мазута
| Компоненти | Коли- чество | Тук се включват елементите | ||||
| С | Н | О | N | S | ||
| Приход, кг | ||||||
| Мазут........................... Водна пара................. Кислород..................... | 100,0 46,0 100,9 | 87,3 - - | 9,8 5,1 - | 0,8 40,9 100,9 | 0,7 - - | 1,4 - - |
| Общо...... | 246,9 | 87,3 | 14,9 | 142,6 | 0,7 | 104 |
| Н2................................. СО……………………… СО2 ……………………. Н2О ……………………. Н2S.............................. COS............................. N2................................. CH4.............................. Сажди.......................... | 12,0 178,0 26,9 24,1 1,4 0,1 0,7 0,4 3,3 | - 76,4 73 - - 0,02 - 0,3 3,3 | 12,0 - - 2,7 0,1 - - 0,1 - | - 101,6 19,6 21,4 - 0,02 - - - | - - - - - - 0,7 - - | - - - - 1,3 0,1 - - - |
| Общо....... | 246,9 | 87,3 | 14,9 | 142,6 | 0,7 | 1,4 |
Дата: 2019-05-28, просмотров: 334.