Барбитуровая кислота – 2,4,6-тригидроксипиримидин – таутомерное соединение. Молекулы барбитуровой кислоты претерпевают лактим- лактамную и кето-енольную таутомерию.
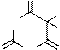
Схема таутомерии барбитуровой кислоты.
 OH
OH
 |
лактим-
O H O
 H
H

 N лактим- N
N лактим- N
O
 H H N H
H H N H
 кето- H
кето- H
H OH

лактамная O
N OH H
лактамная O N H
O H енольная O N O
 H
H

 лактим-енольная лактам-енольная лактам-кетонная
лактим-енольная лактам-енольная лактам-кетонная
форма форма форма
Лактам-кетонная форма барбитуровой кислоты не имеет ароматического строения. Наиболее устойчивой таутомерной формой является, вероятно, лактам-енольная. Считается, что эту форму барбитуровая кислота может иметь в твердом состоянии.
Барбитуровая кислота является довольно слабой кислотой (рКа ~ 4), но она сильнее уксусной кислоты (рКа 4.75). Малорастворима в холодной воде, растворяется в щелочах с образованием растворимой в воде соли. Барбитуровая кислота образует соли с одним эквивалентом основания (показывает свойства одноосновной кислоты). С учетом того, что более сильные кислотные свойства должен иметь гидроксил у второго атома углерода (между двумя электроноакцепторными атомами азота) и лучшую делокализацию отрицательного заряда в анионе обеспечивает лактим- енольная форма, схему реакции нейтрализации барбитуровой кислоты можно записать так:
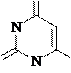
 O O O
O O O
 H
H


 O OH
O OH
H
HN
HO N OH
NaOH
-HOH
HN

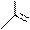 ONa OH
ONa OH
более сильный натриевая соль барбитуровой кислоты
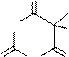
Барбитураты – это производные барбитуровой кислоты, в структуре которых у пятого атома углерода присутствуют один или два углеводородных заместителя:
 O
O
 H 3 4
H 3 4
N
2
 O 1N H
O 1N H
R'
5 R''
6 O
R'=R''=C2H5 5,5-диэтилбарбитуровая кислота
(барбитал, веронал);
R'=C2H5 5-фенил-5-этилбарбитуровая кислота
R''=C6H5 (фенобарбитал);
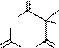
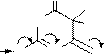
Для барбитуратов возможна только лактим-лактамная таутомерия. Их кислотные свойства выражены существенно меньше, чем у барбитуровой кислоты (невозможно образование у аниона ароматического строения и меньше возможности делокализации заряда). Например, для барбитала рКа ~ 7-8. Натриевые соли барбитуратов хорошо растворимы в воде:
 O O
O O
 H C H
H C H

O
 H C H
H C H
 |
2 5 H
N
C2H5 2 5
 N
N
 C2H5 N
C2H5 N

 O N O H O N H
O N O H O N H
C2H5 O
NaOH
 -H2O
-H2O
ONa
C2H5
N O
барбитал барбитал-натрий
 Синтез барбитуровой кислоты и барбитуратов может быть осуществлен из малонового эфира (алкил- и диалкилмалонового эфира) и мочевины:
Синтез барбитуровой кислоты и барбитуратов может быть осуществлен из малонового эфира (алкил- и диалкилмалонового эфира) и мочевины:

 NH H5C2O
NH H5C2O
O
 C R'
C R'

O
 H R'
H R'

2 +d C SN
N
R''
 C +dC
C +dC

R''

-2HOC H
 O NH
O NH
H C O O
2 5 O N O

2 5 2 H
Таким образом одна из таутомерных форм барбитуровой кислоты и барбитуратов может рассматриваться как циклический уреид малоновой кислоты.
Барбитуровая кислота и барбитураты способны не только как кислоты образовывать соли. Для них известны и другие типы реакций, возможность которых определяют все таутомерные формы каждого соединения.
Схемы реакций таутомеров барбитуровой кислоты.
 O OH-
O OH-
 |
H 4NaOH, to
O
 (SN) C
(SN) C

N 2NH3 + Na2CO3 + ONa CH2


 O N O H
O N O H
субстрат
 OH
OH
щелочной гидролиз
(S )
C
 ONa O
ONa O

 O H H C O
O H H C O

 |
 +d N
+d N
H3C N 3 N

 HO N
HO N
CH3 OSO3CH3

 OH HO N
OH HO N

 Cl
Cl
 N
N
OH
 6HI
6HI
-H+
HO OH
+d восстановление
Cl N Cl -3I2, -3HCl N

+2NH3
N
-NH4Cl
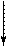
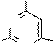 Cl
Cl

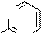 4HI N
4HI N
H2N N
Cl -2I2, 2HCl
H2N N
Дата: 2019-05-28, просмотров: 458.