Термодинамический процесс представляет собой непрерывное изменение состояния системы, происходящее в результате взаимодействия её с окружающей средой.
Одним из примеров термодинамического процесса является работа газа.
Работа газа
F = pS, Н – сила, действующая на поршень при подводе тепла;
L = pSΔh, Дж – работа, совершаемая газом;
SΔh = ∆V – изменение объёма; L = p∆V, Дж
Законы термодинамики
Первый закон термодинамики (закон сохранение энергии): Энергия не исчезает и не возникает из ничего, а лишь переходит из одного состояния в другое в эквивалентных количествах.
Q = ∆U + p∆V ,Дж
∆U – изменение внутренней энергии, Дж
∆U = Mcv(T2 – T1)
Второй закон термодинамики (определяет условия, при которых возможно преобразование одного вида энергии в другой) – формулировка по Клаузису: «Теплота не может переходить сама собой от более холодного тела к более тёплому».
Удельная энтальпия – количество теплоты, необходимой для нагревания в изобарном процессе 1 кг газа от 0 до t0С:
h =cpmt, Дж/кг
Энтальпия: H = Mcp(t2 – t1), Дж
Энтропия – величина, изменение которой dS в элементарном процессе равно отношению бесконечно малого количества теплоты Q, сообщённой 1 кг газа, к термодинамической температуре Т:
dS = 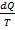 , Дж/кг.К
, Дж/кг.К
Круговые циклы
Последовательный ряд процессов, во время которых тело, претерпев ряд изменений, возвращается в первоначальное состояние, называют круговым процессом или циклом.
Например, цикл преобразования теплоты в механическую работу в ДВС. Здесь подвод тепла осуществляется в процессе сгорания топлива, а процесс отвода тепла осуществляется выпуском отработавшего газа или пара
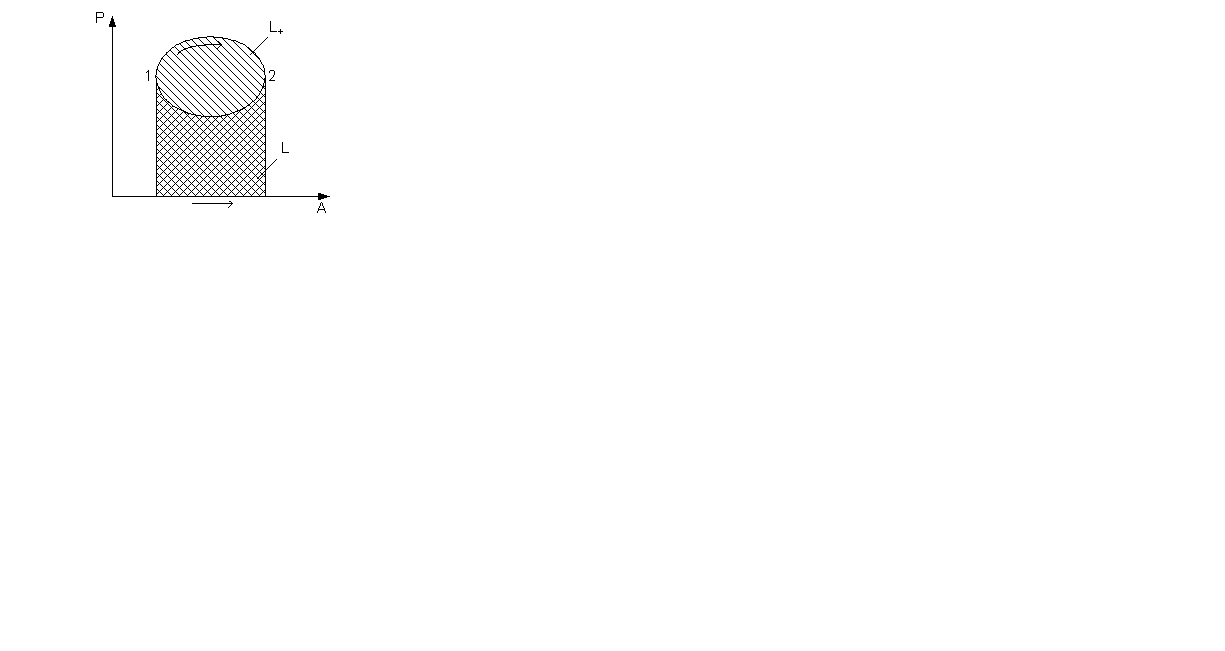
L0 = L1 – L2 –полезная работа
L1 – работа расширения
L2 – работа сжатия
Q 0 = L 0 =( Q 1 - Q 2 ) – полезно использованная теплота
ηt = 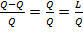
Проанализируем цикл: т.к. в круговом процессе рабочее тело возвращается в первоначальное состояние, то его внутренняя энергич не изменяется. Если в процессе расширения тело получает тепло Q1, а при сжатии отдаст Q2, то в виде тепла в цикле исчезает (Q1-Q2). При неизменной внутренней энергии согласно первого закона термодинамики теплота может быть преобразована только в работу.
Экономичность теплового двигателя оценивают с помощью термического КПД.
КПД зависит от количества подведённой и отведённой теплоты, которые в свою очередь определяются процессами, образующими цикл. Из этого следует, сто подбором процессов можно влиять на экономичность двигателя.
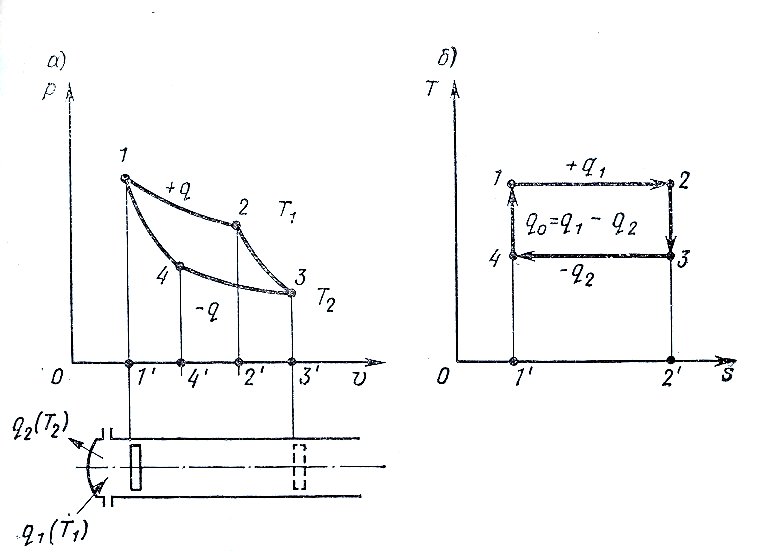
Самым экономичным является цикл Карно, состоящий из двух изотерм и двух адиабат.
Количество подведенного тепла 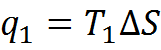
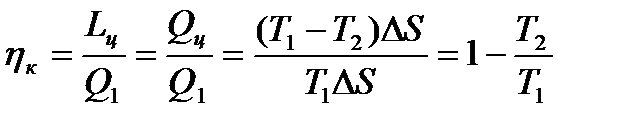 Теплота цикла
Теплота цикла 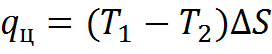
К.п.д. цикла Карно
Изотермический процесс, т.к. максимально возможное количество теплоты преобразуется в работу.
Адиабатный процесс, т.к. работа совершается за счёт внутренней энергии и отсюда максимальный КПД.
1-2 - расширение по изотерме за счёт подвода тепла
2-3 - расширение по адиабате за счёт изменения внутренней энергии
3-4 - сжатие по изотерме (минимальное количество затраченной работы)
4-1 - сжатие по адиабате
Работа, совершаемая газом – площадь 1-2-3-3|-1|-1
Полезная работа: Lпол = Lрасш – Lсж, площадь 1-2-3-4-1
Дата: 2019-02-19, просмотров: 399.