Типы связи в кристаллах
Тип связи, возникающий между частицами в кристалле, определяется электронным строением атомов, вступающих во взаимодействие.
Существую следующие типы связей в кристаллах:
1. Молекулярная
2. Металлическая
3. Ковалентная
4. Ионная
2.2 Молекулярный тип связи (силы Ван-дер-Ваальса)
· Осуществляется за счет слабых сил мгновенной поляризации (рис. 2.1).
· Возникает между электрически нейтральными частицами: N 2 , H 2 , Cl 2 , H 2 O , CO 2 , CH 4.
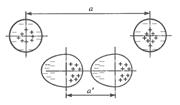 Электроны будут сосредоточены в одной части, ионы – в другой.
Электроны будут сосредоточены в одной части, ионы – в другой.
Возникает взаимное притяжение. Каждый атом стремится, притянуть как можно больше частиц, т.е. не определенное количество атомов, а произвольное и максимально возможное.
 Свойства:
Свойства:
· Ненаправленная связь;
· Слабые силы связи обусловливают низкие температуры плавления и испарения (у жидкости (Н2О) – при комнатной температуре;
· Низкий модуль упругости (Е) и высокий коэффициент линейного расширения;
· Связь характерна для диэлектриков.
Металлический тип связи
Возникает между атомами металла и структурными составляющими металлов и сплавов – фазами. При (сближении) взаимодействии происходит перекрытие валентных энергетических зон, образуются свободные электроны, которые принадлежат всем атомам (т.е. «электронный газ»). Перекрытие оболочек происходит из-за незаполненных внутренних уровней.
Свойства:
· Металлическая связь - ненаправленная;
· Кристаллическая решетка: ОЦК, ГЦК и ГПУ: Ni , Ag , Cu , Au , Fe , Pt , Al , Pb ;
· Возможен полиморфизм;
· Наличие электронных зон обеспечивает очень хорошую теплопроводность и электропроводность (характерная для проводников);
· Электронная эмиссия (испускание электронов) даже при комнатной температуре;
· Положительный коэффициент электропроводности (при нагреве коэффициент увеличивается);
Механические свойства: хорошая пластичность (пластическая деформация остается после снятия нагрузки).
Ковалентный тип связи
Осуществляется за счет обобществления валентных электронов соседними атомами. Характерна для элементов Ш, IV , V группы таблицы Менделеева: C (алмаз), Si , Ge , Sn, и соединениями SiC , AlN, рис. 2.2.
Количество атомов, с которыми данный атом объединяет свои электроны n=8. Связь очень прочная, для превращения электрона в электрон проводимости нужна дополнительная энергия E (энергетический барьер) в виде тепла либо света. Поэтому при нагреве проводимость увеличивается, а электросопротивление – уменьшается.
Свойства:
· Связь направленная;
· Кристаллы с ковалентной связью обладают высокой твердостью;
· Низкая плотность упаковки;
· Высокие температуры плавления и испарения (t пл алмаза=5000 ºС);
· Высокий модуль упругости;
· Низкий коэффициент линейного расширения;
· 
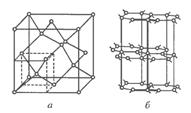 Ковалентные кристаллы – полупроводники или диэлектрики.
Ковалентные кристаллы – полупроводники или диэлектрики.
Алмаз: не элементарная ячейка (1/8 часть решетки): a=b = c, К=4.
Графит: слоистая решетка ГП в которой 1 из 4-х атомов находится на значительном удалении. В плоскости – ковалентные связи, а между основаниями – слабые молекулярные силы Ван-дер-Ваальса. При деформации в первую очередь разрушаются слабые силы, поэтому у графита низкая твердость. А также большой коэффициент линейного расширения. Алмазом можно резать стекло, а графитом писать!
В графите два типа связей: молекулярная и ковалентная.
Ионный тип связи
Возникает за счет электростатических сил притяжения. Образуется между металлами (малой валентности) и неметаллами (высокой валентности). Металлы отдают свои валентные электроны при сближении, становясь положительно заряженными ионами. Неметалл, принимая электрон, заряжается отрицательно. В результате возникает электростатическое взаимодействие. Na + Cl - , Mg 4+ Si 4- , Fe 2+ O 2- .
Свойства:
· Связь сильная, ненаправленная;
· Связь характерна для диэлектриков и полупроводников;
· Высокая твердость, повышенная хрупкость;
· Высокая температура плавления и испарения;
· Высокий модуль упругости.
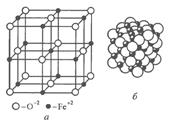 Для ионных кристаллов координационное число определяется соотношением радиусов металлических и неметаллических ионов, т.к. каждый ион стремится, притянуть к себе как можно больше ионов противоположного знака. В решетке ионы укладываются как мячи разных диаметров.
Для ионных кристаллов координационное число определяется соотношением радиусов металлических и неметаллических ионов, т.к. каждый ион стремится, притянуть к себе как можно больше ионов противоположного знака. В решетке ионы укладываются как мячи разных диаметров.
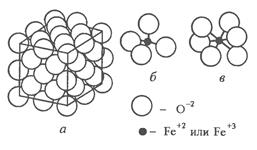
 R нм > R ме. Например, ионы кислорода образуют решетку ГЦК, а ионы железа помещаются в порах. Поэтому в ионных кристаллах нельзя выделить пару ионов, которые можно было бы считать молекулой. Примеры: NaCl , FeO. Решетка типа «шпинель» - неэлементарная (1/8 часть), а= b = c, K=6, определяет число ионов противоположного знака, которые окружают данный ион (рис. 2.3).
R нм > R ме. Например, ионы кислорода образуют решетку ГЦК, а ионы железа помещаются в порах. Поэтому в ионных кристаллах нельзя выделить пару ионов, которые можно было бы считать молекулой. Примеры: NaCl , FeO. Решетка типа «шпинель» - неэлементарная (1/8 часть), а= b = c, K=6, определяет число ионов противоположного знака, которые окружают данный ион (рис. 2.3).
При нагреве соотношение радиусов может изменяться, так как у неметалла он возрастает интенсивнее, чем у металла. Это приводит к изменению типа кристаллической структуры, т.е. к полиморфизму, (полиморфизм свойственен не только чистым элементам). Например, шпинельный FeO, превращается в Fe 2 O 3 с ромбоэдрической решеткой. От этого зависит коррозионная стойкость железа, которая резко снижается, с образованием Fe 2 O 3 при 500˚С. Большая плотность упаковки ионов в решетке FeO способствует высокому сопротивлению химической коррозии.
Полиморфизм
Способность менять кристаллическое строение при изменении температуры или давления, или и того и другого вместе, называется полиморфизмом. Переход от одной решетки к другой – полиморфное превращение. Модификации обозначают начальными буквами греческого алфавита: α, β, γ. Им обладают 32 элемента. Например: Fe , Co , Ti , Zr , Sn , U (имеет 3 модификации). (Показать на примере Fe).
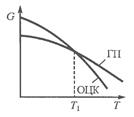 Значение полиморфизма (рис. 2.4): он лежит в основе изменения при термической обработке сплавов.
Значение полиморфизма (рис. 2.4): он лежит в основе изменения при термической обработке сплавов.
Например, у сплавов железа и титана можно значительно повысить твердость и прочность, если использовать полиморфные превращения. Благодаря полиморфизму у железа при быстром охлаждении (закалка) твердость повышается в 10 раз. А у алюминия, у которого нет полиморфных превращений, всего на 10%.
 Также в некоторых сплавах можно получить явление памяти формы.
Также в некоторых сплавах можно получить явление памяти формы.
Некоторые неметаллы также обладают полиморфизмом. К примеру, всем известный углерод графит – низкотемпературная модификация с гексагональной решеткой, и алмаз – с кубической кристаллической решеткой. Графит – мягкий, алмаз – очень твердый. Более стабильным является графит.
Полиморфное превращение бывает необратимым (алмаз – графит) и обратимым (железо).
Фазовый состав сплавов
Термин «сплав» в настоящее время имеет широкое значение. Сейчас этот термин используют не только при получении материалов, содержащих несколько компонентов путем сплавления, а и при использовании других технологических способов: порошковую металлургию (прессование твердых частиц и их последующее спекание при высоких температурах), диффузионный метод (проникновение одного вещества в другое твердое вещество при высоких температурах), плазменное напыление, кристаллизацию из паров в вакууме, электролиз и т.д. преимущественное использование в промышленности находят сплавы металлов с металлами или неметаллами. В сплавах элементы могут по-разному взаимодействовать между собой, образуя различные по химическому составу, типу связи и строению кристаллические фазы.
Фазой называется однородная, отделенная поверхностью раздела часть металла или сплава, имеющая одинаковые состав, строение и свойства. В зависимости от атомно-кристаллической структуры различают твердые растворы и промежуточные фазы.
Твердыми растворами называются кристаллы, в которых сохраняется тип кристаллической решетки, элемента-растворителя.
В промежуточных фазах образуется новый тип кристаллической решетки, отличающийся от решеток элементов, его образующих.
Твердые растворы
Твердые растворы являются кристаллическими фазами переменного состава. Атомы растворенного элемента В размещаются в кристаллической решетке растворителя – элемента А, замещая атомы в узлах решетки или внедряясь между узлами. В первом случае кристаллы называют твердыми растворами замещения, во втором – твердыми растворами внедрения (рис.2.5). Количество замещенных атомов, так же как и количество внедренных, может  изменяться в широких пределах, что и приводит к переменной растворимости твердых растворов.
изменяться в широких пределах, что и приводит к переменной растворимости твердых растворов.
Твердые растворы обозначаются буквами греческого алфавита: α, β, γ и т.д. или А(В), где А – растворитель, В – растворенный элемент.
 Твердые растворы замещения. Замещение атомов растворителя А атомами растворенного элемента В возможно, если атомные радиусы отличаются не более, чем на 15%. Это условие называют размерный фактор. В твердых растворах атомы растворенного вещества, как правило, распределяются в решетке растворителя статистически. Вокруг атома растворенного вещества возникают местные искажения пространственной решетки, которые приводят к изменению свойств и среднего периода решетки. Растворение элементов с меньшим атомным радиусом, чем атомный радиус растворителя, вызывает уменьшение среднего периода решетки, а с большим – его увеличение.
Твердые растворы замещения. Замещение атомов растворителя А атомами растворенного элемента В возможно, если атомные радиусы отличаются не более, чем на 15%. Это условие называют размерный фактор. В твердых растворах атомы растворенного вещества, как правило, распределяются в решетке растворителя статистически. Вокруг атома растворенного вещества возникают местные искажения пространственной решетки, которые приводят к изменению свойств и среднего периода решетки. Растворение элементов с меньшим атомным радиусом, чем атомный радиус растворителя, вызывает уменьшение среднего периода решетки, а с большим – его увеличение.
Образование твердых растворов всегда сопровождается увеличением электрического сопротивления и уменьшением температурного коэффициента электрического сопротивления; твердые растворы обычно менее пластичны (исключение составляют твердые растворы на основе меди) и всегда более твердые и прочные, чем чистые металлы.
Растворимость элементов в твердом состоянии уменьшается при увеличении различия в атомных радиусах сплавленных элементов и их валентности.
При образовании твердых растворов замещения возможна и неограниченная растворимость элементов в твердом состоянии, т.е. когда при любом количественном соотношении сплавляемых элементов все разнородные атомы размещаются в узлах общей пространственной решетки.
Неограниченная растворимость наблюдается при соблюдении размерного фактора и если элементы имеют одинаковый тип кристаллической решетки. Неограниченная растворимость в твердом состоянии наблюдается в сплавах Cu – Au , Cu – Ni , Ge – Si. В полиморфных металлах встречается неограниченная растворимость в пределах одной модификации пространственной решетки. Например, Feα дает неограниченный ряд твердых растворов с хромом (ОЦК решетки), а Feγ – неограниченный ряд твердых растворов с никелем (ГЦК решетки).
Многие твердые растворы замещения при относительно невысоких температурах способны находиться в упорядоченном состоянии, т.е. вместо статического распределения разносортных атомов в узлах пространственной решетки атомы одного и другого металла размещаются в совершенно определенном порядке. Такие твердые растворы называются упорядоченными (используется термин «сверхструктура»).
Переход из неупорядоченного в упорядоченное состояние происходит при определенной температуре или в определенном интервале температур. Температура, при которой твердый раствор полностью разупорядочивается, называется точкой Курнакова 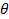 к. Упорядочение происходит обычно только при медленном охлаждении твердого раствора из температурной области выше
к. Упорядочение происходит обычно только при медленном охлаждении твердого раствора из температурной области выше 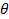 к.
к.
Упорядоченные твердые растворы встречаются в системах с значительной или неограниченной растворимостью в твердом состоянии; при этом полная упорядоченность возникает при концентрациях твердого раствора, соответствующих простым атомным соотношениям компонентов типа АВ или АВ3. Частичная упорядоченность наблюдается при составах, близких к указанным. Расположение атомов в упорядоченных твердых растворах двух сплавов меди с золотом, составов, соответствующих концентрациям AuCu 3 и AuCu, показано на рис. 2.6.
Возникновение и исчезновение порядка в расположении атомов твердых растворов сопровождается изменением свойств. При упорядочении возрастают электропроводность, температурный коэффициент электрического сопротивления, твердость и прочность; снижается пластичность сплава. У ферромагнитных сплавов изменяются магнитные свойства: например у 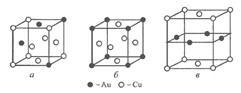 пермаллоев (магнитные сплавы железа с никелем) при упорядочении в несколько раз уменьшается магнитная проницаемость. Некоторые сплавы в неупорядоченном состоянии парамагнитны, а после упорядочения становятся ферромагнитными, например сплавы Гейслера
пермаллоев (магнитные сплавы железа с никелем) при упорядочении в несколько раз уменьшается магнитная проницаемость. Некоторые сплавы в неупорядоченном состоянии парамагнитны, а после упорядочения становятся ферромагнитными, например сплавы Гейслера  (Mn – Cu – Al).
(Mn – Cu – Al).
Твердые растворы внедрения. Такие твердые растворы возникают при сплавлении переходных металлов с неметаллами, имеющими малый атомный радиус – водородом, азотом, углеродом, бором.
Основным условием, определяющим возможность растворения путем внедрения, является размерный фактор. Размер межузельного атома должен быть несколько больше размера поры.
Твердые растворы внедрения всегда имеют ограниченную растворимость и встречаются преимущественно тогда, когда растворитель имеет ГП или ГЦК решетки, в которых имеются поры с радиусом 0,41R, где R – радиус атома растворителя. В ОЦК решетке растворимость путем внедрения мала, так как размер пор не превосходит 0,29R.
Примером твердых растворов внедрения, имеющих промышленное значение, являются твердые растворы углерода в Feγ и Feα. Так, Feγ с ГЦК решеткой растворяет до 2,14% (мас.) углерода, а Feα с ОЦК решеткой почти совсем его не растворяет (максимальная растворимость составляет около 0,02% (мас.)).
Искажения решетки при образовании твердых растворов внедрения больше, чем при образовании твердых раствором замещения, поэтому у них более резко изменяются и свойства. По мере увеличения концентрации растворенного элемента в твердом растворе заметно возрастают электрическое сопротивление, твердость и прочность, но значительно понижаются пластичность и вязкость.
В сплавах, содержащих более двух элементов, возможно растворение в одном и том же растворителе и путем замещения, и путем внедрения. Так, при сплавлении железа с марганцем и углеродом получится твердый раствор, в котором марганец растворяется путем замещения, а углерод – путем внедрения.
В заключение следует подчеркнуть, что твердые растворы – это кристаллы, наиболее близкие по свойствам к растворителю, так как сохраняют его кристаллическую решетку и тип связи. В частности, твердые растворы на основе металлов отличаются высокой технологической пластичностью: хорошо деформируются в горячем, а многие и в холодном состоянии.
Твердые растворы составляют основу большинства промышленных конструкционных сплавов и сплавов специального назначения.
Промежуточные фазы
Кристаллы, образованные различными элементами и имеющие собственный тип кристаллической решетки, отличающийся от решеток, составляющих элементов, называются промежуточной фазой.
В зависимости от природы элементов в промежуточных фазах может быть любой тип связи, который, в первую очередь, и определяет свойства кристаллов, в частности электрические.
Промежуточные фазы, как и твердые растворы, являются кристаллами, существующими в некотором интервале концентраций. Переменный состав объясняется либо наличием небольших межузельных «лишних» атомов (или ионов) в кристаллической решетке промежуточной фазы, либо недостатком атомов в узлах решетки.
Промежуточные фазы обозначают так же, как и твердые растворы, буквами греческого алфавита. Однако допускаются обозначения и химическими формулами, которые отражают состав (стехиометрический), при котором кристаллы не имеют дефектов – межузельных атомов и вакансий.
Замечено, что структура промежуточной фазы зависит от трех факторов: относительного размера атомов, их валентности и от положения в Периодической системе элементов, что определяет их электронную структуру.
Системы металл – неметалл
Фазы с ионным типом связи. К ним относятся оксиды металлов. Простой оксид железа FeO имеет ГЦК решетку (см. рис. 2.3). Все кислородные узлы решетки заполнены, тогда как часть металлических узлов свободна. Таким образом, оксид FeO имеет структуру с большим дефицитом металлических ионов, что определяет появление полупроводниковых свойств.
 Оксид железа Fe 3 O 4 – это двойной оксид FeO
Оксид железа Fe 3 O 4 – это двойной оксид FeO 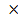 Fe 2 O 3
Fe 2 O 3  (рис. 2.6). его кристаллическая решетка – шпинель содержит двух- и трехвалентные ионы железа, расположенные в межузельных порах ионов кислорода. Два вида ионов железа и ионный тип связи обеспечивают оксиду особые магнитные свойства в высокочастотных полях. Большая плотность упаковки ионов в решетке, несмотря на небольшой дефицит ионов железа, способствует высокому сопротивлению химической коррозии.
(рис. 2.6). его кристаллическая решетка – шпинель содержит двух- и трехвалентные ионы железа, расположенные в межузельных порах ионов кислорода. Два вида ионов железа и ионный тип связи обеспечивают оксиду особые магнитные свойства в высокочастотных полях. Большая плотность упаковки ионов в решетке, несмотря на небольшой дефицит ионов железа, способствует высокому сопротивлению химической коррозии.
 Фазы с ионно-ковалентным типом связи. Такие фазы образуются при взаимодействии металлов I – Ш группы с неметаллами V – VI группы подгруппы В Периодической системы элементов (например, ZnS и AlP). Эти фазы обладают полупроводниковыми свойствами.
Фазы с ионно-ковалентным типом связи. Такие фазы образуются при взаимодействии металлов I – Ш группы с неметаллами V – VI группы подгруппы В Периодической системы элементов (например, ZnS и AlP). Эти фазы обладают полупроводниковыми свойствами.
Фазы с ковалентно-металлическим типом связи. Фазы, в которых преобладает металлический тип связи, образуются при взаимодействии переходных металлов с углеродом, азотом, бором и водородом и называются соответственно карбидами, нитридами, боридами, гидридами.
Кристаллическая структура этих соединений зависит от относительных размеров атомов неметалла R нм и металла R м. Если отношение R нм/ R м 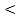 0,59, образуются промежуточные фазы с простыми пространственными решетками, в которых атомы неметалла располагаются в порах. Эти промежуточные фазы называют фазами внедрения. Если отношение R нм/ R м
0,59, образуются промежуточные фазы с простыми пространственными решетками, в которых атомы неметалла располагаются в порах. Эти промежуточные фазы называют фазами внедрения. Если отношение R нм/ R м 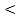 0,59, то атом неметалла не может разместиться в поре, тогда образуются сложные пространственные решетки с большим числом атомов в элементарной ячейке.
0,59, то атом неметалла не может разместиться в поре, тогда образуются сложные пространственные решетки с большим числом атомов в элементарной ячейке.
Фазы внедрения имеют кристаллические решетки (чаще всего плотноупакованные ГЦК и ГП); при этом тип решетки фазы внедрения не совпадает с типом решетки металла, образующего эту фазу (исключением являются некоторые гидриды). Атомы металла в фазах внедрения размещаются в узлах решетки, тогда как атомы неметалла закономерно распределяются в октаэдрических и тетраэдрических порах решетки.
Химический состав фаз внедрения указывается формулами: MeX, Me 2 X, Me 4 X, и MeX 4 , где Me – металл, X – неметалл; однако это фазы переменного состава, в которых число металлических атомов отличается от стехиометрического состава.
К фазам внедрения типа MeX относятся следующие карбиды: TiC , NbC , WC , MoC , VC. Вольфрам и молибден могут образовывать и фазы внедрения тип Me 2 X: Mo2C, и W 2 C. Примером фазы внедрения типа Me 4 X является нитрид железа Fe 4 N , а фазы типа MeX 4 - гидрид циркония ZrH 4.
В карбиде TiC фактическое содержание углерода, который располагается в межузельных порах, может колебаться в пределах 38…50% (ат.). Очевидно, что только при 50% (ат.) С состав карбида точно описывается формулой TiC.
В фазах внедрения преобладает металлическая связь, чем и определяются такие их свойства как высокая электрическая проводимость, положительный коэффициент электросопротивления (как у чистых металлов и твердых растворов на их основе); некоторые фазы внедрения обладают сверхпроводимостью. Однако есть свойства, которые указывают на значительную долю в фазах внедрения ковалентной связи. Большинство фаз внедрения чрезвычайно тугоплавки и имеют высокую твердость.
Карбиды и нитриды, относящиеся к фазам внедрения, присутствуют в структуре многих коррозионно-стойких, износостойких и жаропрочных конструкционных сталей. Карбиды TiC , TaC , WC , W 2 C служат основой порошковых твердых сплавов для режущих инструментов.
К карбидам с отношением R нм/ R м 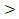 0,59 относятся Fe 3 C (в сталях его называют цементитом), Mn 3 C , Cr 23 C и Cr 23 C 3 (например, в Fe 3 C отношение R нм/ R м
0,59 относятся Fe 3 C (в сталях его называют цементитом), Mn 3 C , Cr 23 C и Cr 23 C 3 (например, в Fe 3 C отношение R нм/ R м 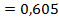 ). Карбиды Fe 3 C , Cr 23 C и Cr 23 C 3 – важнейшие промежуточные фазы в конструкционных и инструментальных сталях, во многом определяющие их свойства. В последних двух карбидах преобладает металлическая связь, хотя имеется и определенная доля ковалентной. Эти промежуточные фазы отличаются высокой твердостью и хрупкостью, они также достаточно тугоплавки, но уступают по этим свойствам карбидам, являющимися фазами внедрения.
). Карбиды Fe 3 C , Cr 23 C и Cr 23 C 3 – важнейшие промежуточные фазы в конструкционных и инструментальных сталях, во многом определяющие их свойства. В последних двух карбидах преобладает металлическая связь, хотя имеется и определенная доля ковалентной. Эти промежуточные фазы отличаются высокой твердостью и хрупкостью, они также достаточно тугоплавки, но уступают по этим свойствам карбидам, являющимися фазами внедрения.
Системы металл – металл
При сплавлении металлов могут образовываться промежуточные фазы с металлическим типом связи. К ним относятся электронные фазы, фазы Лавеса и σ-фазы.
Электронные фазы. Для максимального содержания металла более высокой валентности характерно совершенно определенное значение электронной концентрации[1]: 3/2, 21/13, 7/4. Фазы с указанными значениями электронной концентрации принято обозначать 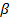 ,
, 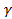 и
и 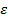 соответственно.
соответственно.
Указанным электронным концентрациям можно приписать соответствующие химические формулы. Например, в сплавах меди с цинком, в которых могут образовываться все фазы с указанными концентрациями, такими формулами будут соответственно CuZn , Cu 5 Zn 8 , CuZn 3.
В большинстве сплавов β-фазы имеют ОЦК решетку, 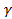 -фазы – сложную кубическую решетку с 52 атомами в элементарной ячейке и
-фазы – сложную кубическую решетку с 52 атомами в элементарной ячейке и 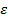 -фазы – ГП решетку.
-фазы – ГП решетку.
Свойства электронных соединений, в частности механические свойства, зависят в значительной мере от упорядоченности атомов компонентов в кристаллической решетке электронного соединения. Так, β-фазы с ОЦК решеткой почти во всех системах при высоких температурах неупорядочены, и в этом состоянии их свойства близки к свойствам твердых растворов, т.е. они не отличаются высокой твердостью и обладают хорошей пластичностью. При низких температурах неупорядоченные β-фазы неустойчивы: они либо распадаются на двухфазные смеси, либо упорядочиваются, как, например в системе Cu – Zn. Упорядоченные β-фазы значительно более тверды и хрупки. Почти всегда упорядочены, причем вплоть до температуры плавления, и во всех системах обладают хрупкостью γ-фазы, 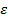 -фазы всегда имеют неупорядоченное строение.
-фазы всегда имеют неупорядоченное строение.
Электронные соединения присутствуют в структуре многих сплавов на медной основе: латунях (Cu – Zn ), бронзах (Cu – Al , Cu – Sn и др.); они являются упрочняющими фазами.
Фазы Лавеса. Эти промежуточные фазы практически постоянного состава АВ2 образуются при взаимодействии металлов самых различных групп Периодической системы элементов; при этом атомный радиус элемента В должен быть меньше, чем атомный радиус элемента А, на 20…30%.
Фазы Лавеса имеют упорядоченные сложные кубические или гексагональные решетки, в магнитном поле они ведут себя как диамагнетики. Фазы Лавеса, образованные переходными металлами (NbFe 2 , MoFe 2 , TiFe 2 , TiCr 2), присутствуют в структуре некоторых жаропрочных сплавов и способствуют их упрочнению.
Сигма фазы. Эти фазы переменного состава образуются при сплавлении переходных металлов, имеющих близкие размеры атомов. Сигма фазы имеют частично упорядоченную сложную решетку. В железных сплавах, содержащих более 20% (мас.) Cr (используются как коррозионно-стойкие конструкционные материалы), медленное охлаждение из области твердого раствора или изотермическая выдержка при 800…600  приводит к образованию кристаллов σ-фазы, которое сопровождается увеличением твердости и охрупчиванием сплавов.
приводит к образованию кристаллов σ-фазы, которое сопровождается увеличением твердости и охрупчиванием сплавов.
Дата: 2019-02-18, просмотров: 2962.