МОДУЛЬ 1. СТРУКТУРА И СВОЙСТВА МАТЕРИАЛОВ
Лекция. Кристаллические и аморфные вещества. Дефекты кристаллов
Кристаллические и аморфные вещества
В природе существуют две разновидности твердых тел, различающиеся по своим свойствам: кристаллические и аморфные.
 Кристаллическое состояние характеризуется наличием дальнего порядка, когда существует определенное расположение атомов вдоль любого направления в расположении частиц и симметрией кристаллической решетки.
Кристаллическое состояние характеризуется наличием дальнего порядка, когда существует определенное расположение атомов вдоль любого направления в расположении частиц и симметрией кристаллической решетки.
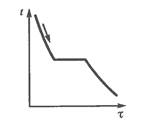
Кристаллические тела остаются твердыми до определенной температуры, при которой они переходят в жидкое состояние. При охлаждении процесс идет в обратном направлении (рис. 1.1).

 Строение вещества определяется не только взаимным расположением атомов, частиц, но и расположением этих частиц в пространстве. Наиболее упорядочено размещение атомов, молекул и ионов в кристаллах (от греческого «кристаллос» – лед), где частицы расположены в определенном порядке, образуя в пространстве кристаллическую решетку. При определенных условиях образования они могут иметь естественную форму правильных симметричных многогранников.
Строение вещества определяется не только взаимным расположением атомов, частиц, но и расположением этих частиц в пространстве. Наиболее упорядочено размещение атомов, молекул и ионов в кристаллах (от греческого «кристаллос» – лед), где частицы расположены в определенном порядке, образуя в пространстве кристаллическую решетку. При определенных условиях образования они могут иметь естественную форму правильных симметричных многогранников.
Для аморфного состояния характерно наличие только ближнего порядка. Структуры аморфных веществ напоминают жидкости, однако обладают гораздо меньшей текучестью. Аморфное состояние обычно неустойчиво. Под действием механических нагрузок или при изменении температуры аморфные тела могут закристаллизоваться. Реакционная способность веществ в аморфном состоянии значительно выше, чем в кристаллическом.
Главный признак аморфного (от греческого «аморфос» – бесформенный) состояния вещества – отсутствие трехмерной периодичности структуры, характерной для кристаллического состояния.
Аморфные тела изотропны, то есть их механические, оптические, электрические и другие свойства не зависят от направления. У аморфных тел нет фиксированной температуры плавления: плавление происходит в некотором температурном интервале. Переход твердого аморфного вещества в жидкое состояние не сопровождается скачкообразным изменением свойств.
При охлаждении жидкого вещества не всегда происходит его кристаллизация. при определенных условиях может образоваться неравновесное твердое аморфное (стеклообразное) состояние. В стеклообразном состоянии могут находиться простые вещества (углерод, фосфор мышьяк, сера, селен), оксиды (например, бора, кремния, фосфора), галогениды, халькогениды, многие органические полимеры.
Структура кристаллов
В кристаллических веществах свойства зависят от структуры. В понятие «структура» входят:
· электронное строение атомов и характер их взаимодействия в кристалле;
· пространственное расположение элементарных частиц;
· химический состав, размер и форма кристаллов.
В зависимости от размеров структурных составляющих и применяемых методов их выявления, существуют следующие виды структуры:
· тонкая структура (изучают с помощью электронного микроскопа);
·  микроструктура (изучают с помощью микроскопа);
микроструктура (изучают с помощью микроскопа);
· макроструктура (изучают визуально).
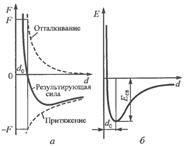
В кристалле атомы располагаются на определенном расстоянии друг от друга. Это расстояние определяется взаимодействием сил действующих в кристалле (рис. 1.2).
Виды взаимодействия атомов и электронов:
 1) притяжение между ядрами и электронами собственных атомов и электронами соседних атомов;
1) притяжение между ядрами и электронами собственных атомов и электронами соседних атомов;
2) отталкивание между ядрами соседних атомов.
Расстояние, соответствующее минимуму энергии (Есв) и обеспечивающее термодинамическую стабильность кристалла, называется параметром решетки.
Элементы кристаллографии
Кристаллическая решетка
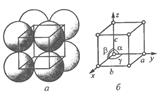 Для описания элементарной ячейки используют три линейных параметра: a , b , c – расстояние до ближайших атомов по трем осям координат; и три угловых параметра: α , β, γ – это углы между линейными параметрами (рис. 1.3).
Для описания элементарной ячейки используют три линейных параметра: a , b , c – расстояние до ближайших атомов по трем осям координат; и три угловых параметра: α , β, γ – это углы между линейными параметрами (рис. 1.3).
Места, занятые атомами – узлы, а пространство не занятое атомами – междоузлия.

 Теоретически доказано, что всего может существовать 230 различных пространственных кристаллических структур. Большинство из них (но не все) обнаружены в природе или созданы искусственно.
Теоретически доказано, что всего может существовать 230 различных пространственных кристаллических структур. Большинство из них (но не все) обнаружены в природе или созданы искусственно.
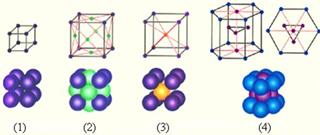
На рис. 1.4 приведены примеры простых кристаллических решеток: 1 – простая кубическая решетка; 2 – гранецентрированная кубическая решетка; 3 – объемноцентрированная кубическая решетка; 4 – гексагональная решетка.
 О степени сложности судят по числу частиц, приходящихся на одну элементарную ячейку: n = 1 – простая (n = 1/8×8); n> 1 – сложная. Число частиц определяется из условия, что элементарная ячейка находится в окружении таких же ячеек.
О степени сложности судят по числу частиц, приходящихся на одну элементарную ячейку: n = 1 – простая (n = 1/8×8); n> 1 – сложная. Число частиц определяется из условия, что элементарная ячейка находится в окружении таких же ячеек.
ОЦК (a=b=c, α, β, γ=90º); n=1/8×8+1=2.
ОЦК решетка у следующих металлов: Na , K , Feα , Tiβ , Zrβ , W , Nb , Mo.
ГЦК (a=b=c, α, β, γ=90º); n=1/8×8+1/2×6=4.
ГЦК решетка у следующих металлов: Al , Cu , Feγ , Au , Ag , Pt , Pb.
ГПУ состоит из 3-х элементарных ячеек(a = b = c, α, β=90º, γ=120º); n=1/6×12+1/2×2+3=6.
ГПУ решетка у следующих металлов: Mg , Be , Tiα , Zrα , Zn , Cd.
Точечные дефекты
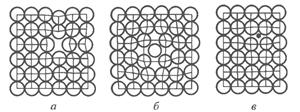 Виды точечных дефектов: к самым простым точечным дефектам относятся а) вакансии, б) межузельные атомы основного вещества, в) чужеродные атомы внедрения (рис. 1.7).
Виды точечных дефектов: к самым простым точечным дефектам относятся а) вакансии, б) межузельные атомы основного вещества, в) чужеродные атомы внедрения (рис. 1.7).
 Каждой температуре соответствует равновесная крнцентрация вакансий, а также межузельный атомов. Например в меди при 20 – 25 ºС содержится 10-13% (ат.) вакансий, а вблизи точки плавления – уже 10-2% (ат.) (одна вакансия приходится на 104 атомов).
Каждой температуре соответствует равновесная крнцентрация вакансий, а также межузельный атомов. Например в меди при 20 – 25 ºС содержится 10-13% (ат.) вакансий, а вблизи точки плавления – уже 10-2% (ат.) (одна вакансия приходится на 104 атомов).
Пересыщение точечными дефектами достигается при резком охлаждении после высокотемпературного нагрева, при пластическом деформировании и при облучении нейтронами.
С течением времени избыток вакансий сверх равновесной концентрации уничтожается на свободных поверхностях кристалла, порах, границах зерен и других дефектах решетки. Места, где исчезают вакансии, называются стоками вакансий. Вакансии являются самой важной разновидностью точечных дефектов; они ускоряют все процессы, связанные с перемещениями атомов (диффузия, спекание порошков и т.д.).
В ионных и ковалентных кристаллах вакансии и другие точечные фефекты электрически активны и могут быть как донорами, тк и акцепторами. Это создает в кристаллах преобладание определенного типа проводимости.
Все виды точечных дефектов искажают кристаллическую решетку и в определенной мере, влияют на физические свойства.
1.8 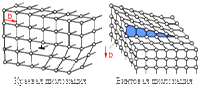 Линейные дефекты
Линейные дефекты
 Важнейшие виды линейных несовершенств – краевые и линейные дислокации (рис. 1.8). Краевая дислокация в сечении представляет собой край «лишней» полуплоскости в решетке. Вокруг дислокаций решетка упруго искажена. Мерой искажения служит так называемый вектор Бюргерса. Он определяет незавершенность контура вокруг дислокаций по сравнению с идеальной решеткой. Энергия, возникающая в области дислокации: E = Gb 2 /2.
Важнейшие виды линейных несовершенств – краевые и линейные дислокации (рис. 1.8). Краевая дислокация в сечении представляет собой край «лишней» полуплоскости в решетке. Вокруг дислокаций решетка упруго искажена. Мерой искажения служит так называемый вектор Бюргерса. Он определяет незавершенность контура вокруг дислокаций по сравнению с идеальной решеткой. Энергия, возникающая в области дислокации: E = Gb 2 /2.

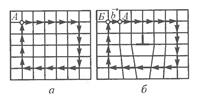 Он получается, если обойти замкнутый контур в идеальном кристалле (рис. 1.9, а), переходя от узла к узлу, а затем этот же путь повторить в реальном кристалле, заключив дислокацию внутрь контура. Как видно на рис 1.9, б, в реальном кристалле контур окажется незамкнутым. Вектор b, который нужен для замыкания контура, называется вектором Бюргерса. У краевой дислокации вектор Бюргерса равен межатомному расстоянию и перпендикулярен дислокационной линии, у винтовой дислокации – параллелен.
Он получается, если обойти замкнутый контур в идеальном кристалле (рис. 1.9, а), переходя от узла к узлу, а затем этот же путь повторить в реальном кристалле, заключив дислокацию внутрь контура. Как видно на рис 1.9, б, в реальном кристалле контур окажется незамкнутым. Вектор b, который нужен для замыкания контура, называется вектором Бюргерса. У краевой дислокации вектор Бюргерса равен межатомному расстоянию и перпендикулярен дислокационной линии, у винтовой дислокации – параллелен.
В кристаллах содержатся дислокации разных знаков, различающиеся ориентацией векторов Бюргерса. Дислокации одного знака, расположенные в одной плоскости, отталкиваются друг от друга, противоположных – знаков притягиваются.
 Плотность дислокаций – это суммарная длина всех линий дислокаций в единице объема. В полупроводниковых кристаллах она равна 104 – 105 см-2, у отожженных металлов – 106–108 см-2. При холодном пластическом деформировании плотность дислокаций возрастает до 1011–1012 см-2. Попытка увеличить плотность свыше 1012 см-2 приводит к появлению трещин и разрушению металла.
Плотность дислокаций – это суммарная длина всех линий дислокаций в единице объема. В полупроводниковых кристаллах она равна 104 – 105 см-2, у отожженных металлов – 106–108 см-2. При холодном пластическом деформировании плотность дислокаций возрастает до 1011–1012 см-2. Попытка увеличить плотность свыше 1012 см-2 приводит к появлению трещин и разрушению металла.
Свойства дислокаций:
1) способность к перемещению под действием напряжений и осуществлению пластическектах структуры.ой деформации;
2) способность к торможению на различных объектах структуры.
Причины возникновения дислокаций:
1)  неоднородность процесса кристаллизации (напряжения и примеси);
неоднородность процесса кристаллизации (напряжения и примеси);
2) механическое воздействие на кристалл.
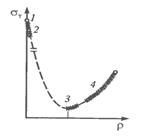
Дислокации значительно влияют на физические и на механические свойства металлов. Особенно велико влияние дислокаций на прочность кристаллов. Благодаря подвижным дислокациям экспериментально определенный предел текучести металлов в 1000 раз меньше теоретического значения. При значительном увеличении плотности дислокаций и уменьшении их подвижности прочность увеличивается в несколько раз по сравнению с отожженным состоянием. На рис. 1.10 показана зависимость прочности от количества дефектов – кривая Одинга.
Поверхностные дефекты
Поверхностными дефектами являются большеугловые и малоугловые границы, дефекты упаковки, границы двойников. Поликристаллические материалы содержат огромное число мелких зерен. В соседних зернах решетки ориентированы различно (рис.11), и граница между зернами представляет собой переходный слой шириной 1 – 5 нм. В нем нарушена правильность расположения атомов, имеются скопления дислокаций, повышена концентрация примесей. Границы между зернами называются большеугловыми, так как соответственные кристаллографические направления в соседних зернах образуют углы в десятки градусов.

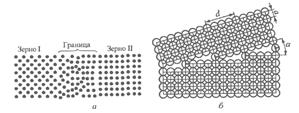 Каждое зерно, в свою очередь, состоит из субзерен (блоков). Субзерно представляет собой часть кристалла относительно правильного строения, а его границы – стенки дислокаций, разлеляют зерно на отдельные субзерна. Угол (α) взаимной разориентации между соседними субзернами составляет не более 5º. На этих малоугловых границах также скапливаются примеси.
Каждое зерно, в свою очередь, состоит из субзерен (блоков). Субзерно представляет собой часть кристалла относительно правильного строения, а его границы – стенки дислокаций, разлеляют зерно на отдельные субзерна. Угол (α) взаимной разориентации между соседними субзернами составляет не более 5º. На этих малоугловых границах также скапливаются примеси.
Поверхностные дефекты влияют на механические и физические свойства материалов. Особенно большое значение имеют границы зерен. Предел текучести σт связан с размером зерен d зависимостью
σт= σ0+ k / 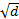 ,
,
где σт и k – постоянные для данного материала. Поэтому чем мельче зерно, тем выше предел текучести, вязкость и меньше опасность хрупкого разрушения. Аналогично, но более слабо влияет на механические свойства размер субзерен.
Вдоль границ зерен и субзерен быстрее протекает диффузия, чем сквозь кристалл, особенно при нагреве.
Объемные дефекты
Виды объемных дефектов:
1) трещины;
2) поры.
Причины возникновения объемных дефектов:
· в результате слияния вакансий;
· уменьшение объема материала при кристаллизации;
· в результате механических воздействий.
Влияние на свойства: объемные дефекты ухудшают все свойства материалов.
Выводы:
Практическое значение дислокаций:
1. Прочность реального кристалла и сплава в 1000 раз ниже теоретической прочности вследствие наличия дефектов структуры.
2. В результате становится возможным пластическое деформированеие металла (ковка, штамповка и др.).
3. Возможность упрочнять металлы и сплавы.
Типы связи в кристаллах
Тип связи, возникающий между частицами в кристалле, определяется электронным строением атомов, вступающих во взаимодействие.
Существую следующие типы связей в кристаллах:
1. Молекулярная
2. Металлическая
3. Ковалентная
4. Ионная
2.2 Молекулярный тип связи (силы Ван-дер-Ваальса)
· Осуществляется за счет слабых сил мгновенной поляризации (рис. 2.1).
· Возникает между электрически нейтральными частицами: N 2 , H 2 , Cl 2 , H 2 O , CO 2 , CH 4.
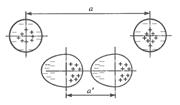 Электроны будут сосредоточены в одной части, ионы – в другой.
Электроны будут сосредоточены в одной части, ионы – в другой.
Возникает взаимное притяжение. Каждый атом стремится, притянуть как можно больше частиц, т.е. не определенное количество атомов, а произвольное и максимально возможное.
 Свойства:
Свойства:
· Ненаправленная связь;
· Слабые силы связи обусловливают низкие температуры плавления и испарения (у жидкости (Н2О) – при комнатной температуре;
· Низкий модуль упругости (Е) и высокий коэффициент линейного расширения;
· Связь характерна для диэлектриков.
Металлический тип связи
Возникает между атомами металла и структурными составляющими металлов и сплавов – фазами. При (сближении) взаимодействии происходит перекрытие валентных энергетических зон, образуются свободные электроны, которые принадлежат всем атомам (т.е. «электронный газ»). Перекрытие оболочек происходит из-за незаполненных внутренних уровней.
Свойства:
· Металлическая связь - ненаправленная;
· Кристаллическая решетка: ОЦК, ГЦК и ГПУ: Ni , Ag , Cu , Au , Fe , Pt , Al , Pb ;
· Возможен полиморфизм;
· Наличие электронных зон обеспечивает очень хорошую теплопроводность и электропроводность (характерная для проводников);
· Электронная эмиссия (испускание электронов) даже при комнатной температуре;
· Положительный коэффициент электропроводности (при нагреве коэффициент увеличивается);
Механические свойства: хорошая пластичность (пластическая деформация остается после снятия нагрузки).
Ковалентный тип связи
Осуществляется за счет обобществления валентных электронов соседними атомами. Характерна для элементов Ш, IV , V группы таблицы Менделеева: C (алмаз), Si , Ge , Sn, и соединениями SiC , AlN, рис. 2.2.
Количество атомов, с которыми данный атом объединяет свои электроны n=8. Связь очень прочная, для превращения электрона в электрон проводимости нужна дополнительная энергия E (энергетический барьер) в виде тепла либо света. Поэтому при нагреве проводимость увеличивается, а электросопротивление – уменьшается.
Свойства:
· Связь направленная;
· Кристаллы с ковалентной связью обладают высокой твердостью;
· Низкая плотность упаковки;
· Высокие температуры плавления и испарения (t пл алмаза=5000 ºС);
· Высокий модуль упругости;
· Низкий коэффициент линейного расширения;
· 
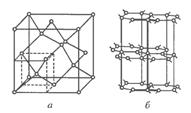 Ковалентные кристаллы – полупроводники или диэлектрики.
Ковалентные кристаллы – полупроводники или диэлектрики.
Алмаз: не элементарная ячейка (1/8 часть решетки): a=b = c, К=4.
Графит: слоистая решетка ГП в которой 1 из 4-х атомов находится на значительном удалении. В плоскости – ковалентные связи, а между основаниями – слабые молекулярные силы Ван-дер-Ваальса. При деформации в первую очередь разрушаются слабые силы, поэтому у графита низкая твердость. А также большой коэффициент линейного расширения. Алмазом можно резать стекло, а графитом писать!
В графите два типа связей: молекулярная и ковалентная.
Ионный тип связи
Возникает за счет электростатических сил притяжения. Образуется между металлами (малой валентности) и неметаллами (высокой валентности). Металлы отдают свои валентные электроны при сближении, становясь положительно заряженными ионами. Неметалл, принимая электрон, заряжается отрицательно. В результате возникает электростатическое взаимодействие. Na + Cl - , Mg 4+ Si 4- , Fe 2+ O 2- .
Свойства:
· Связь сильная, ненаправленная;
· Связь характерна для диэлектриков и полупроводников;
· Высокая твердость, повышенная хрупкость;
· Высокая температура плавления и испарения;
· Высокий модуль упругости.
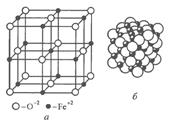 Для ионных кристаллов координационное число определяется соотношением радиусов металлических и неметаллических ионов, т.к. каждый ион стремится, притянуть к себе как можно больше ионов противоположного знака. В решетке ионы укладываются как мячи разных диаметров.
Для ионных кристаллов координационное число определяется соотношением радиусов металлических и неметаллических ионов, т.к. каждый ион стремится, притянуть к себе как можно больше ионов противоположного знака. В решетке ионы укладываются как мячи разных диаметров.
 R нм > R ме. Например, ионы кислорода образуют решетку ГЦК, а ионы железа помещаются в порах. Поэтому в ионных кристаллах нельзя выделить пару ионов, которые можно было бы считать молекулой. Примеры: NaCl , FeO. Решетка типа «шпинель» - неэлементарная (1/8 часть), а= b = c, K=6, определяет число ионов противоположного знака, которые окружают данный ион (рис. 2.3).
R нм > R ме. Например, ионы кислорода образуют решетку ГЦК, а ионы железа помещаются в порах. Поэтому в ионных кристаллах нельзя выделить пару ионов, которые можно было бы считать молекулой. Примеры: NaCl , FeO. Решетка типа «шпинель» - неэлементарная (1/8 часть), а= b = c, K=6, определяет число ионов противоположного знака, которые окружают данный ион (рис. 2.3).
При нагреве соотношение радиусов может изменяться, так как у неметалла он возрастает интенсивнее, чем у металла. Это приводит к изменению типа кристаллической структуры, т.е. к полиморфизму, (полиморфизм свойственен не только чистым элементам). Например, шпинельный FeO, превращается в Fe 2 O 3 с ромбоэдрической решеткой. От этого зависит коррозионная стойкость железа, которая резко снижается, с образованием Fe 2 O 3 при 500˚С. Большая плотность упаковки ионов в решетке FeO способствует высокому сопротивлению химической коррозии.
Полиморфизм
Способность менять кристаллическое строение при изменении температуры или давления, или и того и другого вместе, называется полиморфизмом. Переход от одной решетки к другой – полиморфное превращение. Модификации обозначают начальными буквами греческого алфавита: α, β, γ. Им обладают 32 элемента. Например: Fe , Co , Ti , Zr , Sn , U (имеет 3 модификации). (Показать на примере Fe).
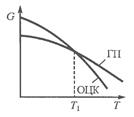 Значение полиморфизма (рис. 2.4): он лежит в основе изменения при термической обработке сплавов.
Значение полиморфизма (рис. 2.4): он лежит в основе изменения при термической обработке сплавов.
Например, у сплавов железа и титана можно значительно повысить твердость и прочность, если использовать полиморфные превращения. Благодаря полиморфизму у железа при быстром охлаждении (закалка) твердость повышается в 10 раз. А у алюминия, у которого нет полиморфных превращений, всего на 10%.
 Также в некоторых сплавах можно получить явление памяти формы.
Также в некоторых сплавах можно получить явление памяти формы.
Некоторые неметаллы также обладают полиморфизмом. К примеру, всем известный углерод графит – низкотемпературная модификация с гексагональной решеткой, и алмаз – с кубической кристаллической решеткой. Графит – мягкий, алмаз – очень твердый. Более стабильным является графит.
Полиморфное превращение бывает необратимым (алмаз – графит) и обратимым (железо).
Фазовый состав сплавов
Термин «сплав» в настоящее время имеет широкое значение. Сейчас этот термин используют не только при получении материалов, содержащих несколько компонентов путем сплавления, а и при использовании других технологических способов: порошковую металлургию (прессование твердых частиц и их последующее спекание при высоких температурах), диффузионный метод (проникновение одного вещества в другое твердое вещество при высоких температурах), плазменное напыление, кристаллизацию из паров в вакууме, электролиз и т.д. преимущественное использование в промышленности находят сплавы металлов с металлами или неметаллами. В сплавах элементы могут по-разному взаимодействовать между собой, образуя различные по химическому составу, типу связи и строению кристаллические фазы.
Фазой называется однородная, отделенная поверхностью раздела часть металла или сплава, имеющая одинаковые состав, строение и свойства. В зависимости от атомно-кристаллической структуры различают твердые растворы и промежуточные фазы.
Твердыми растворами называются кристаллы, в которых сохраняется тип кристаллической решетки, элемента-растворителя.
В промежуточных фазах образуется новый тип кристаллической решетки, отличающийся от решеток элементов, его образующих.
Твердые растворы
Твердые растворы являются кристаллическими фазами переменного состава. Атомы растворенного элемента В размещаются в кристаллической решетке растворителя – элемента А, замещая атомы в узлах решетки или внедряясь между узлами. В первом случае кристаллы называют твердыми растворами замещения, во втором – твердыми растворами внедрения (рис.2.5). Количество замещенных атомов, так же как и количество внедренных, может 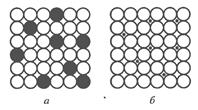 изменяться в широких пределах, что и приводит к переменной растворимости твердых растворов.
изменяться в широких пределах, что и приводит к переменной растворимости твердых растворов.
Твердые растворы обозначаются буквами греческого алфавита: α, β, γ и т.д. или А(В), где А – растворитель, В – растворенный элемент.
 Твердые растворы замещения. Замещение атомов растворителя А атомами растворенного элемента В возможно, если атомные радиусы отличаются не более, чем на 15%. Это условие называют размерный фактор. В твердых растворах атомы растворенного вещества, как правило, распределяются в решетке растворителя статистически. Вокруг атома растворенного вещества возникают местные искажения пространственной решетки, которые приводят к изменению свойств и среднего периода решетки. Растворение элементов с меньшим атомным радиусом, чем атомный радиус растворителя, вызывает уменьшение среднего периода решетки, а с большим – его увеличение.
Твердые растворы замещения. Замещение атомов растворителя А атомами растворенного элемента В возможно, если атомные радиусы отличаются не более, чем на 15%. Это условие называют размерный фактор. В твердых растворах атомы растворенного вещества, как правило, распределяются в решетке растворителя статистически. Вокруг атома растворенного вещества возникают местные искажения пространственной решетки, которые приводят к изменению свойств и среднего периода решетки. Растворение элементов с меньшим атомным радиусом, чем атомный радиус растворителя, вызывает уменьшение среднего периода решетки, а с большим – его увеличение.
Образование твердых растворов всегда сопровождается увеличением электрического сопротивления и уменьшением температурного коэффициента электрического сопротивления; твердые растворы обычно менее пластичны (исключение составляют твердые растворы на основе меди) и всегда более твердые и прочные, чем чистые металлы.
Растворимость элементов в твердом состоянии уменьшается при увеличении различия в атомных радиусах сплавленных элементов и их валентности.
При образовании твердых растворов замещения возможна и неограниченная растворимость элементов в твердом состоянии, т.е. когда при любом количественном соотношении сплавляемых элементов все разнородные атомы размещаются в узлах общей пространственной решетки.
Неограниченная растворимость наблюдается при соблюдении размерного фактора и если элементы имеют одинаковый тип кристаллической решетки. Неограниченная растворимость в твердом состоянии наблюдается в сплавах Cu – Au , Cu – Ni , Ge – Si. В полиморфных металлах встречается неограниченная растворимость в пределах одной модификации пространственной решетки. Например, Feα дает неограниченный ряд твердых растворов с хромом (ОЦК решетки), а Feγ – неограниченный ряд твердых растворов с никелем (ГЦК решетки).
Многие твердые растворы замещения при относительно невысоких температурах способны находиться в упорядоченном состоянии, т.е. вместо статического распределения разносортных атомов в узлах пространственной решетки атомы одного и другого металла размещаются в совершенно определенном порядке. Такие твердые растворы называются упорядоченными (используется термин «сверхструктура»).
Переход из неупорядоченного в упорядоченное состояние происходит при определенной температуре или в определенном интервале температур. Температура, при которой твердый раствор полностью разупорядочивается, называется точкой Курнакова 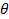 к. Упорядочение происходит обычно только при медленном охлаждении твердого раствора из температурной области выше
к. Упорядочение происходит обычно только при медленном охлаждении твердого раствора из температурной области выше 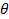 к.
к.
Упорядоченные твердые растворы встречаются в системах с значительной или неограниченной растворимостью в твердом состоянии; при этом полная упорядоченность возникает при концентрациях твердого раствора, соответствующих простым атомным соотношениям компонентов типа АВ или АВ3. Частичная упорядоченность наблюдается при составах, близких к указанным. Расположение атомов в упорядоченных твердых растворах двух сплавов меди с золотом, составов, соответствующих концентрациям AuCu 3 и AuCu, показано на рис. 2.6.
Возникновение и исчезновение порядка в расположении атомов твердых растворов сопровождается изменением свойств. При упорядочении возрастают электропроводность, температурный коэффициент электрического сопротивления, твердость и прочность; снижается пластичность сплава. У ферромагнитных сплавов изменяются магнитные свойства: например у 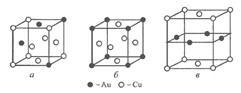 пермаллоев (магнитные сплавы железа с никелем) при упорядочении в несколько раз уменьшается магнитная проницаемость. Некоторые сплавы в неупорядоченном состоянии парамагнитны, а после упорядочения становятся ферромагнитными, например сплавы Гейслера
пермаллоев (магнитные сплавы железа с никелем) при упорядочении в несколько раз уменьшается магнитная проницаемость. Некоторые сплавы в неупорядоченном состоянии парамагнитны, а после упорядочения становятся ферромагнитными, например сплавы Гейслера  (Mn – Cu – Al).
(Mn – Cu – Al).
Твердые растворы внедрения. Такие твердые растворы возникают при сплавлении переходных металлов с неметаллами, имеющими малый атомный радиус – водородом, азотом, углеродом, бором.
Основным условием, определяющим возможность растворения путем внедрения, является размерный фактор. Размер межузельного атома должен быть несколько больше размера поры.
Твердые растворы внедрения всегда имеют ограниченную растворимость и встречаются преимущественно тогда, когда растворитель имеет ГП или ГЦК решетки, в которых имеются поры с радиусом 0,41R, где R – радиус атома растворителя. В ОЦК решетке растворимость путем внедрения мала, так как размер пор не превосходит 0,29R.
Примером твердых растворов внедрения, имеющих промышленное значение, являются твердые растворы углерода в Feγ и Feα. Так, Feγ с ГЦК решеткой растворяет до 2,14% (мас.) углерода, а Feα с ОЦК решеткой почти совсем его не растворяет (максимальная растворимость составляет около 0,02% (мас.)).
Искажения решетки при образовании твердых растворов внедрения больше, чем при образовании твердых раствором замещения, поэтому у них более резко изменяются и свойства. По мере увеличения концентрации растворенного элемента в твердом растворе заметно возрастают электрическое сопротивление, твердость и прочность, но значительно понижаются пластичность и вязкость.
В сплавах, содержащих более двух элементов, возможно растворение в одном и том же растворителе и путем замещения, и путем внедрения. Так, при сплавлении железа с марганцем и углеродом получится твердый раствор, в котором марганец растворяется путем замещения, а углерод – путем внедрения.
В заключение следует подчеркнуть, что твердые растворы – это кристаллы, наиболее близкие по свойствам к растворителю, так как сохраняют его кристаллическую решетку и тип связи. В частности, твердые растворы на основе металлов отличаются высокой технологической пластичностью: хорошо деформируются в горячем, а многие и в холодном состоянии.
Твердые растворы составляют основу большинства промышленных конструкционных сплавов и сплавов специального назначения.
Промежуточные фазы
Кристаллы, образованные различными элементами и имеющие собственный тип кристаллической решетки, отличающийся от решеток, составляющих элементов, называются промежуточной фазой.
В зависимости от природы элементов в промежуточных фазах может быть любой тип связи, который, в первую очередь, и определяет свойства кристаллов, в частности электрические.
Промежуточные фазы, как и твердые растворы, являются кристаллами, существующими в некотором интервале концентраций. Переменный состав объясняется либо наличием небольших межузельных «лишних» атомов (или ионов) в кристаллической решетке промежуточной фазы, либо недостатком атомов в узлах решетки.
Промежуточные фазы обозначают так же, как и твердые растворы, буквами греческого алфавита. Однако допускаются обозначения и химическими формулами, которые отражают состав (стехиометрический), при котором кристаллы не имеют дефектов – межузельных атомов и вакансий.
Замечено, что структура промежуточной фазы зависит от трех факторов: относительного размера атомов, их валентности и от положения в Периодической системе элементов, что определяет их электронную структуру.
Системы металл – неметалл
Фазы с ионным типом связи. К ним относятся оксиды металлов. Простой оксид железа FeO имеет ГЦК решетку (см. рис. 2.3). Все кислородные узлы решетки заполнены, тогда как часть металлических узлов свободна. Таким образом, оксид FeO имеет структуру с большим дефицитом металлических ионов, что определяет появление полупроводниковых свойств.
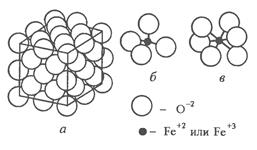 Оксид железа Fe 3 O 4 – это двойной оксид FeO
Оксид железа Fe 3 O 4 – это двойной оксид FeO 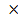 Fe 2 O 3
Fe 2 O 3  (рис. 2.6). его кристаллическая решетка – шпинель содержит двух- и трехвалентные ионы железа, расположенные в межузельных порах ионов кислорода. Два вида ионов железа и ионный тип связи обеспечивают оксиду особые магнитные свойства в высокочастотных полях. Большая плотность упаковки ионов в решетке, несмотря на небольшой дефицит ионов железа, способствует высокому сопротивлению химической коррозии.
(рис. 2.6). его кристаллическая решетка – шпинель содержит двух- и трехвалентные ионы железа, расположенные в межузельных порах ионов кислорода. Два вида ионов железа и ионный тип связи обеспечивают оксиду особые магнитные свойства в высокочастотных полях. Большая плотность упаковки ионов в решетке, несмотря на небольшой дефицит ионов железа, способствует высокому сопротивлению химической коррозии.
 Фазы с ионно-ковалентным типом связи. Такие фазы образуются при взаимодействии металлов I – Ш группы с неметаллами V – VI группы подгруппы В Периодической системы элементов (например, ZnS и AlP). Эти фазы обладают полупроводниковыми свойствами.
Фазы с ионно-ковалентным типом связи. Такие фазы образуются при взаимодействии металлов I – Ш группы с неметаллами V – VI группы подгруппы В Периодической системы элементов (например, ZnS и AlP). Эти фазы обладают полупроводниковыми свойствами.
Фазы с ковалентно-металлическим типом связи. Фазы, в которых преобладает металлический тип связи, образуются при взаимодействии переходных металлов с углеродом, азотом, бором и водородом и называются соответственно карбидами, нитридами, боридами, гидридами.
Кристаллическая структура этих соединений зависит от относительных размеров атомов неметалла R нм и металла R м. Если отношение R нм/ R м 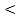 0,59, образуются промежуточные фазы с простыми пространственными решетками, в которых атомы неметалла располагаются в порах. Эти промежуточные фазы называют фазами внедрения. Если отношение R нм/ R м
0,59, образуются промежуточные фазы с простыми пространственными решетками, в которых атомы неметалла располагаются в порах. Эти промежуточные фазы называют фазами внедрения. Если отношение R нм/ R м 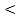 0,59, то атом неметалла не может разместиться в поре, тогда образуются сложные пространственные решетки с большим числом атомов в элементарной ячейке.
0,59, то атом неметалла не может разместиться в поре, тогда образуются сложные пространственные решетки с большим числом атомов в элементарной ячейке.
Фазы внедрения имеют кристаллические решетки (чаще всего плотноупакованные ГЦК и ГП); при этом тип решетки фазы внедрения не совпадает с типом решетки металла, образующего эту фазу (исключением являются некоторые гидриды). Атомы металла в фазах внедрения размещаются в узлах решетки, тогда как атомы неметалла закономерно распределяются в октаэдрических и тетраэдрических порах решетки.
Химический состав фаз внедрения указывается формулами: MeX, Me 2 X, Me 4 X, и MeX 4 , где Me – металл, X – неметалл; однако это фазы переменного состава, в которых число металлических атомов отличается от стехиометрического состава.
К фазам внедрения типа MeX относятся следующие карбиды: TiC , NbC , WC , MoC , VC. Вольфрам и молибден могут образовывать и фазы внедрения тип Me 2 X: Mo2C, и W 2 C. Примером фазы внедрения типа Me 4 X является нитрид железа Fe 4 N , а фазы типа MeX 4 - гидрид циркония ZrH 4.
В карбиде TiC фактическое содержание углерода, который располагается в межузельных порах, может колебаться в пределах 38…50% (ат.). Очевидно, что только при 50% (ат.) С состав карбида точно описывается формулой TiC.
В фазах внедрения преобладает металлическая связь, чем и определяются такие их свойства как высокая электрическая проводимость, положительный коэффициент электросопротивления (как у чистых металлов и твердых растворов на их основе); некоторые фазы внедрения обладают сверхпроводимостью. Однако есть свойства, которые указывают на значительную долю в фазах внедрения ковалентной связи. Большинство фаз внедрения чрезвычайно тугоплавки и имеют высокую твердость.
Карбиды и нитриды, относящиеся к фазам внедрения, присутствуют в структуре многих коррозионно-стойких, износостойких и жаропрочных конструкционных сталей. Карбиды TiC , TaC , WC , W 2 C служат основой порошковых твердых сплавов для режущих инструментов.
К карбидам с отношением R нм/ R м 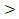 0,59 относятся Fe 3 C (в сталях его называют цементитом), Mn 3 C , Cr 23 C и Cr 23 C 3 (например, в Fe 3 C отношение R нм/ R м
0,59 относятся Fe 3 C (в сталях его называют цементитом), Mn 3 C , Cr 23 C и Cr 23 C 3 (например, в Fe 3 C отношение R нм/ R м 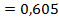 ). Карбиды Fe 3 C , Cr 23 C и Cr 23 C 3 – важнейшие промежуточные фазы в конструкционных и инструментальных сталях, во многом определяющие их свойства. В последних двух карбидах преобладает металлическая связь, хотя имеется и определенная доля ковалентной. Эти промежуточные фазы отличаются высокой твердостью и хрупкостью, они также достаточно тугоплавки, но уступают по этим свойствам карбидам, являющимися фазами внедрения.
). Карбиды Fe 3 C , Cr 23 C и Cr 23 C 3 – важнейшие промежуточные фазы в конструкционных и инструментальных сталях, во многом определяющие их свойства. В последних двух карбидах преобладает металлическая связь, хотя имеется и определенная доля ковалентной. Эти промежуточные фазы отличаются высокой твердостью и хрупкостью, они также достаточно тугоплавки, но уступают по этим свойствам карбидам, являющимися фазами внедрения.
Системы металл – металл
При сплавлении металлов могут образовываться промежуточные фазы с металлическим типом связи. К ним относятся электронные фазы, фазы Лавеса и σ-фазы.
Электронные фазы. Для максимального содержания металла более высокой валентности характерно совершенно определенное значение электронной концентрации[1]: 3/2, 21/13, 7/4. Фазы с указанными значениями электронной концентрации принято обозначать 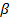 ,
, 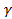 и
и 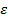 соответственно.
соответственно.
Указанным электронным концентрациям можно приписать соответствующие химические формулы. Например, в сплавах меди с цинком, в которых могут образовываться все фазы с указанными концентрациями, такими формулами будут соответственно CuZn , Cu 5 Zn 8 , CuZn 3.
В большинстве сплавов β-фазы имеют ОЦК решетку, 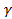 -фазы – сложную кубическую решетку с 52 атомами в элементарной ячейке и
-фазы – сложную кубическую решетку с 52 атомами в элементарной ячейке и 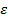 -фазы – ГП решетку.
-фазы – ГП решетку.
Свойства электронных соединений, в частности механические свойства, зависят в значительной мере от упорядоченности атомов компонентов в кристаллической решетке электронного соединения. Так, β-фазы с ОЦК решеткой почти во всех системах при высоких температурах неупорядочены, и в этом состоянии их свойства близки к свойствам твердых растворов, т.е. они не отличаются высокой твердостью и обладают хорошей пластичностью. При низких температурах неупорядоченные β-фазы неустойчивы: они либо распадаются на двухфазные смеси, либо упорядочиваются, как, например в системе Cu – Zn. Упорядоченные β-фазы значительно более тверды и хрупки. Почти всегда упорядочены, причем вплоть до температуры плавления, и во всех системах обладают хрупкостью γ-фазы, 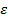 -фазы всегда имеют неупорядоченное строение.
-фазы всегда имеют неупорядоченное строение.
Электронные соединения присутствуют в структуре многих сплавов на медной основе: латунях (Cu – Zn ), бронзах (Cu – Al , Cu – Sn и др.); они являются упрочняющими фазами.
Фазы Лавеса. Эти промежуточные фазы практически постоянного состава АВ2 образуются при взаимодействии металлов самых различных групп Периодической системы элементов; при этом атомный радиус элемента В должен быть меньше, чем атомный радиус элемента А, на 20…30%.
Фазы Лавеса имеют упорядоченные сложные кубические или гексагональные решетки, в магнитном поле они ведут себя как диамагнетики. Фазы Лавеса, образованные переходными металлами (NbFe 2 , MoFe 2 , TiFe 2 , TiCr 2), присутствуют в структуре некоторых жаропрочных сплавов и способствуют их упрочнению.
Сигма фазы. Эти фазы переменного состава образуются при сплавлении переходных металлов, имеющих близкие размеры атомов. Сигма фазы имеют частично упорядоченную сложную решетку. В железных сплавах, содержащих более 20% (мас.) Cr (используются как коррозионно-стойкие конструкционные материалы), медленное охлаждение из области твердого раствора или изотермическая выдержка при 800…600  приводит к образованию кристаллов σ-фазы, которое сопровождается увеличением твердости и охрупчиванием сплавов.
приводит к образованию кристаллов σ-фазы, которое сопровождается увеличением твердости и охрупчиванием сплавов.
Получение монокристаллов
Большое научное и практическое значение имеют монокристаллы. Монокристаллы отличаются минимальными структурными несовершенствами. Получение монокристаллов позволяет изучать свойства металлов, исключив влияние зерен. Применение в монокристаллическом состоянии германия и кремния высокой чистоты дает возможность использовать их полупроводниковые свойства и свести к минимуму неконтролируемые 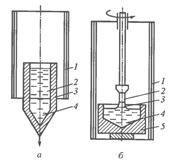 изменения электрических свойств.
изменения электрических свойств.
Монокристаллы можно получить, если создать условия для роста кристалла только из одного центра кристаллизации. Существует несколько методов, в которых использован этот принцип. Важнейшими из них являются методы Бриджмена и Чохральского.
 Метод Бриджмена (рис. 4.8, а) состоит в следующем: металл, помещенный в тигель с коническим дном 3, нагревается в вертикальной трубчатой печи 1 до температуры на 50 – 100 ºС выше температуры его плавления. Затем тигель с расплавленным металлом 2 медленно удаляется из печи. Охлаждение наступает в первую очередь в вершине конуса, где и появляются первые центры кристаллизации. Монокристалл 4 вырастает из того зародыша, у которого направление преимущественного роста совпадает с направлением перемещения тигля. При этом рост других зародышей подавляется. Для непрерывного роста монокристалла необходимо выдвигать тигель из печи со скоростью, не превышающей скорость кристаллизации данного металла.
Метод Бриджмена (рис. 4.8, а) состоит в следующем: металл, помещенный в тигель с коническим дном 3, нагревается в вертикальной трубчатой печи 1 до температуры на 50 – 100 ºС выше температуры его плавления. Затем тигель с расплавленным металлом 2 медленно удаляется из печи. Охлаждение наступает в первую очередь в вершине конуса, где и появляются первые центры кристаллизации. Монокристалл 4 вырастает из того зародыша, у которого направление преимущественного роста совпадает с направлением перемещения тигля. При этом рост других зародышей подавляется. Для непрерывного роста монокристалла необходимо выдвигать тигель из печи со скоростью, не превышающей скорость кристаллизации данного металла.
Метод Чохральского (рис. 4.8, б) состоит в вытягивании монокристалла из расплава, нагретого в печи 1. Для этого используется готовая затравка 2 – небольшой образец, вырезанный и монокристалла. Затравка вводится в поверхностные слой жидкого металла 4, имеющего температуру чуть выше температуры плавления. Плоскость затравки, соприкасающаяся с поверхностью расплава, должна иметь кристаллографическую ориентацию, которую желательно получить в растущем монокристалле 3. Затравку выдерживают в жидком металле для оплавления и установления равновесия в системе жидкость – кристалл. Затем затравку медленно, со скоростью, не превышающей скорости кристаллизации ( 1 – 2 мм/мин), удаляют из расплава. Тянущийся за затравкой жидкий металл в области более низких температур над поверхностью ванны кристаллизуется, наследуя структуру затравки. Для получения симметричной формы растущего монокристалла и равномерного распределения примесей в нем ванна 5 с расплавом вращается со скоростью 100 об/мин, в навстречу ей с меньшей скоростью вращается монокристалл.
Диаметр растущего монокристалла зависит от скорости выращивания и температуры расплава. Увеличение скорости выращивания ведет к выделению большей теплоты кристаллизации, перегреву расплава и уменьшению диаметра монокристалла.
Очень перспективно выращивание монокристаллов в практически недостижимый в земных условиях, способствует значительной очистке от примесей. Вследствие того, что в невесомости силы гравитации ничтожно малы, в расплавах практически не возникает конвекция, которая в земных условиях вызывает нестабильность роста кристаллов. Нестабильность роста, в свою очередь, служит причиной появления несовершенств кристаллического строения, неоднородности химического состава и свойств кристаллов. Отсутствие конвекции не исключает образования микронеоднородностей, вызванных другими причинами. Однако монокристаллы, выращенные в космосе, совершеннее по структуре, распределению легирующих добавок (примесей), лучше по свойствам и значительно больше по размерам.
Примером промышленного использования монокристаллической структуры является производство лопаток для газотурбинного двигателя из жаропрочного никелевого сплава.
Лопатки, изготовленные по традиционной технологии, имели поликристаллическую структуру и содержали мелкие литейные поры. Под действием статических переменных нагрузок, а также высоких температур, свойственных условиям эксплуатации лопаток, на границах зерен и пор возникали трещины и другие дефекты, вызывающие преждевременное разрушение изделия.
Новая технология, созданная под руководством академика РАН Е.Н. Каблова, обеспечивает получение монокристаллической практически беспористой структуры. Такая структура формируется благодаря направленной кристаллизации из одного центра, для чего используется монокристаллическая затравка с заданной кристаллографической ориентацией.
Литейная пористость уменьшается благодаря увеличению температурного градиента на фронте кристаллизации с 40ºС/мм до 200 ºС/мм при постоянной скорости кристаллизации. В этом случае объемная доля микропор уменьшается приблизительно в 10 раз.
Монокристаллическая структура лопаток, уменьшение количества и размера пор обеспечивают существенное повышение прочностных характеристик.
Временное сопротивление, предел текучести при 20ºС и сточасовая длительная прочность при 1100ºС увеличиваются приблизительно в 2 раза, достигая соответственно 1480, 654 и 110МПа. Предел усталости при 900ºС, определенный на базе 2∙107 циклов, повышается в 1,5 раза, достигая 360 МПа.
По сравнению с лопатками с поликристаллической структурой монокристаллические лопатки (при одинаковом химическом составе) имеют повышенную жаропрочность и сопротивление усталости.
Аморфные металлы
При сверхвысоких скоростях охлаждения из жидкого состояния (>106 ºС /с) диффузионные процессы настолько замедляются, что подавляется образование зародышей и рост кристаллов. В этом случае при затвердевании образуется аморфная структура. Материалы с такой структурой получили название аморфные металлические сплавы (АМС), или металлические стекла. Затвердевание с образованием аморфной структуры принципиально возможно практически для всех металлов. В настоящее время аморфная структура получена более чему 200 сплавов и полупроводниковых материалов. Это сплавы легкоплавких, редкоземельных (Sc, Y, La и др.) и переходных металлов. Для образования аморфной структуры переходных металлов к ним необходимо добавлять так называемые аморфизаторы (C, P, B, N, S и др.). При этом состав сплава должен отвечать формуле Me 80 X 20, где Me – один или несколько переходных металлов, %(ат.); X – элементы, добавляемые для образования и стабилизации аморфной структуры, %(ат.). Так, известны аморфные сплавы, состав которых отвечает формулам Fe80P13B7; Fe70Cr10P15B5; Ni80S20; Fe40Ni40S14B6 и др. У сплавов систем «металл–металл» эта зависимость не соблюдается.
Сверхвысокие скорости охлаждения жидкого металла (< 106 ºС/с) для получения аморфной структуры можно реализовать такими способами, как катапультирование капли на холодную пластину, центрифугирование капли или струи, газом или жидкостью с высокой охлаждающей способностью и др. наиболее эффективными способами получения лент, пригодных для практического применения, считают охлаждение жидкого металла на внешней или внутренней поверхностях вращающихся барабанов, изготовленных из материалов высокой теплопроводности, прокатку между холодными валками металла, подаваемого в виде струи.
Тонкий слой аморфного металла получают при расплавлении поверхности изделий лазерным лучем благодаря быстрому отводу теплоты при затвердевании массой основного металла.
АМС можно получить и путем сверхбыстрого охлаждения из газовой среды (парообразного или ионизированного состояния), электролизом и катодным распылением с высокими скоростями осаждения, химическим осаждение (сплавы Ni – P) и механическим легированием.
АМС значительно отличаются от своих кристаллических аналогов по строению и, следовательно, по свойствам. В их структуре отсутствует дальний порядок в размещении атомов и характерные особенности структуры поликристаллических сплавов: границы зерен, дислокации и другие дефекты. У АМС нет зональной ликвации и в целом они более однородны по структуре и химическому составу, чем их кристаллические аналоги. В тоже время АМС в зависимости от условий получения сохраняют геометрические и химические неоднородности ближнего порядка. В макромасштабе они проявляются в форме неоднородностей плотности по толщине и длине лент. Как следствие, в лентах возникают остаточные напряжения и изменение свойств.
Границей сохранения аморфного состояния является температура кристаллизации t к 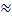 0,5t пл, определяемая при нагреве со скоростью 20ºС/мин.
0,5t пл, определяемая при нагреве со скоростью 20ºС/мин.
Для повышения стабильности свойств АМС применяют отжиг. По сравнению с кристаллическими аналогами АМС имеют более низкую плотность, на 20 – 40% ниже модуль упругости и 2…4 раза больше удельное электросопротивление.
АМС систем «металл – неметалл» имеют σв = 2000…4000 МПа, но при растяжении разрушаются с малым удлинением (δ 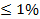 ). Твердость АМС достигает 1000 – 14000 HV в закаленном состоянии.
). Твердость АМС достигает 1000 – 14000 HV в закаленном состоянии.
В то же время АМС при сжатии деформируются на 40 – 50% без разрушения, а ленты изгибаются на 180ºС до параллельности сторон. Особенностью АМС является отсутствие наклепа при различных технологических операциях.
АМС на основе железа являются магнитно-мягкими материалами, в которых нет кристаллографической магнитной анизотропии и существенно снижены потери на перемагничивание. При этом магнитные свойства малочувствительны к механическим воздействиям. Получены магнитные материалы и с высокой магнитной энергией. Они представляют собой соединения редкоземельных и переходных материалов.
По сравнению с кристаллическими аналогами АМС сохраняют избыточную энергию, которая выделяется при кристаллизации. По этой причине АМС химически активны; коррозионно-стойкими являются лишь сплавы, у которых образуется пассивирующаяся защитная пленка. Это, в первую очередь, сплавы железа с хромом и достаточным количеством фосфора и углерода. По сравнению с коррозионно-стойкими требуется меньше хрома: 8 – 9% против 13% в сталях.
Большое практическое значение имеет возможность получения аморфных металлов виде ленты, проволоки диаметром несколько микрометров непосредственно при литье, минуя такие операции, как ковка, прокатка, волочение, промежуточные отжиги, зачистки, травление.
Возврат и рекристаллизация
Неравновесная структура, созданная холодным деформированием, у большинства металлов остается устойчивой при 25ºС. Переход металла в более стабильное состояние происходит при нагреве. При повышении температуры ускоряется перемещение точечных дефектов, и создаются условия для перераспределения дислокаций и уменьшения их количества.
Процессы, происходящие при нагреве, подразделяют на возврат и рекристаллизацию. В свою очередь, при возврате различают отдых и полигонизацию.
Возвратом называют все изменения тонкой структуры и свойств, которые не сопровождаются изменением микроструктуры деформированного металла, т.е. размер и форма зерен при возврате не изменяются.
Рекристаллизация – это процесс зарождения и роста новых зерен с меньшим количеством дефектов строения; в результате рекристаллизации образуются новые чаще всего равноосные зерна.
Отдыхом холоднодеформированного металла называют стадию возврата, при которой уменьшается количество точечных дефектов, в основном вакансий; в ряде металлов (Al , Fe) отдых включает также переползание дислокаций, которое сопровождается взаимодействием дислокаций разных знаков и приводит к заметному уменьшению их плотности. Перераспределение дислокаций сопровождается уменьшением остаточных напряжений. Отдых уменьшает удельное электросопротивление и повышает плотность металла. Твердость и прочность уменьшаются максимально на 10 – 15% первоначальных значений и настолько же соответственно увеличивается пластичность. После отдыха повышается сопротивление коррозионному растрескиванию.
Полигонизацией называют процесс формирования субзерен, разделенных малоугловыми границами. Каждое субзерно представляет собой многогранник, практически не содержащий дислокаций. Полигонизация является результатом нескольких элементарных процессов перемещения дислокаций: скольжения и переползания краевых дислокаций, поперечного скольжения винтовых дислокаций. Во время полигонизации несколько уменьшается плотность дислокаций благодаря взаимодействию и аннигиляции дислокаций противоположных знаков. Для начала полигонизации в наклепанных металлах технической чистоты необходим нагрев до 0,3…0,35 Тпл, в наклепанных сплавах – до более высоких температур.
 Различают предрекристаллизационную и стабилизирующую полигонизацию. Предрекристаллизационная полигонизация развивается в наклепанных металлах с ячеистой дислокационной структурой. Дислокационные стенки при нагреве уплотняются и ячейки превращаются в субзерна. Уплотненные стенки ячеек сохраняют значительную кривизну и настолько подвижны, что отдельные субзерна могут увеличиться и стать центрами первичной рекристаллизации. Предрекристаллизационная полигонизация является начальной стадией первичной рекристаллизации. Строение субзерен и их границ мало зависит от температуры. При повышении температуры нагрева наклепанного металла увеличивается скорость полигонизации: структуры полигонизации, образовавшиеся при разных температурах отжига, практически не отличаются.
Различают предрекристаллизационную и стабилизирующую полигонизацию. Предрекристаллизационная полигонизация развивается в наклепанных металлах с ячеистой дислокационной структурой. Дислокационные стенки при нагреве уплотняются и ячейки превращаются в субзерна. Уплотненные стенки ячеек сохраняют значительную кривизну и настолько подвижны, что отдельные субзерна могут увеличиться и стать центрами первичной рекристаллизации. Предрекристаллизационная полигонизация является начальной стадией первичной рекристаллизации. Строение субзерен и их границ мало зависит от температуры. При повышении температуры нагрева наклепанного металла увеличивается скорость полигонизации: структуры полигонизации, образовавшиеся при разных температурах отжига, практически не отличаются.
 Стабилизирующая полигонизация представляет собой формирование субзерен, разделенных плоскими дислокационными стенками (рис. 4.19). Стенки малоподвижны и весьма устойчивы, при дальнейшем нагреве они сохраняются почти до температур плавления металлов. После формирования субзеренной структуры рекристаллизации не происходит. Стабилизирующая полигонизация развивается лишь при определенных условиях: отсутствие ячеистой дислокационной структуры, избыток краевых дислокаций одного знака и др. такие условия выполняются в монокристаллах и крупнозернистых поликристаллах после небольших пластических деформаций. В подобных материалах результаты перераспределения дислокаций существенно зависят от температуры отжига. При сравнительно высоких температурах нагрева (выше 0,35Тпл) вместо полигонизации развивается первичная рекристаллизация. Если стабилизирующая полигонизация успешно завершилась после отжига (0,3 – 0,35)Тпл, то при дальнейшем нагреве даже при более высокой температуре рекристаллизация не развивается.
Стабилизирующая полигонизация представляет собой формирование субзерен, разделенных плоскими дислокационными стенками (рис. 4.19). Стенки малоподвижны и весьма устойчивы, при дальнейшем нагреве они сохраняются почти до температур плавления металлов. После формирования субзеренной структуры рекристаллизации не происходит. Стабилизирующая полигонизация развивается лишь при определенных условиях: отсутствие ячеистой дислокационной структуры, избыток краевых дислокаций одного знака и др. такие условия выполняются в монокристаллах и крупнозернистых поликристаллах после небольших пластических деформаций. В подобных материалах результаты перераспределения дислокаций существенно зависят от температуры отжига. При сравнительно высоких температурах нагрева (выше 0,35Тпл) вместо полигонизации развивается первичная рекристаллизация. Если стабилизирующая полигонизация успешно завершилась после отжига (0,3 – 0,35)Тпл, то при дальнейшем нагреве даже при более высокой температуре рекристаллизация не развивается.
Ограничение подвижности дислокаций затрудняет полигонизацию. Закрепление дислокаций атомами легирующих элементов и примесей, образование дефектов упаковки, уменьшение концентрации вакансий (затрудняется переползание дислокаций) – все это затрудняет полигонизацию. Чаще она наблюдается в металлах с высокой энергией дефектов упаковки (Al , Mo).
Практическое значение полигонизации проявляется в следующем:
1. Создание субзёренной структуры упрочняет металл по аналогии с формированием мелкозёренной структуры с высокоугловыми границами. Эффект упрочнения при полигонизации проявляется в меньшем масштабе, так как границы субзерен способны легче пропускать дислокации по сравнению с высокоугловыми границами.
2. Образование субзёренной структуры, сохраняя основную долю упрочнения наклепанного металла, снижает остаточные напряжения. Это повышает сопротивление коррозионному растрескиванию. В частности, назначают отжиг при ~300ºС для предупреждения растрескивания.
3. Границы субзерен являются препятствием для перемещения дислокаций. Это используют для повышения жаропрочности деталей.
4. Субзёренная структура, образовавшаяся при динамической полигонизации, т.е. в процессе деформирования обеспечивает при термомеханической обработке сталей оптимальное сочетание пластичности и высокой прочности.
В зависимости от температуры нагрева и выдержки различают три стадии рекристаллизации: первичная, собирательная и вторичная.
Первичная рекристаллизация начинается с образования зародышей новых зерен и заканчивается полным замещением наклепанного металла новой поликристаллической структурой (рис. 4.20, а – в). Для начала первичной рекристаллизации необходимы два условия:
1) предварительная деформация наклепанного металла должна быть больше критической;
2) температура нагрева должны превысить критическое значение, составляющее некоторую долю от температуры плавления металла:
Трек = αТпл.

Рис. 4.20. Схема изменения микроструктуры наклепанного металла при нагреве: а – наклепанный металл; б – начало первичной рекристаллизации; в – завершение первичной рекристаллизации; г – рост зерен; д – образование равновесной структуры
 Коэффициент α уменьшается при увеличении степени деформации, т.е. металл после холодного деформирования ε = 90% будет рекристаллизовываться при более низкой температуре, чем такой же металл после деформирования при ε = 20%. Так, для металлов технической чистоты α = 0,3…0,4. Уменьшение количества примесей может понизить его значение до 0,1 – 0,2. Для твердых растворов α = 0,5…0,6, а при растворении тугоплавких металлов его значение может достигать α = 0,7…0,8. Для алюминия, меди и железа технической чистоты температурный порог рекристаллизации равен соответственно 100, 270 и 450ºС. На стадии первичной рекристаллизации зарождение и рост новых зерен происходит одновременно. Зерна растут путем движения большеугловых границ через наклепанный металл. В таком зерне плотность дислокаций и других дефектов минимальна, в наклепанном металле – максимальна.
Коэффициент α уменьшается при увеличении степени деформации, т.е. металл после холодного деформирования ε = 90% будет рекристаллизовываться при более низкой температуре, чем такой же металл после деформирования при ε = 20%. Так, для металлов технической чистоты α = 0,3…0,4. Уменьшение количества примесей может понизить его значение до 0,1 – 0,2. Для твердых растворов α = 0,5…0,6, а при растворении тугоплавких металлов его значение может достигать α = 0,7…0,8. Для алюминия, меди и железа технической чистоты температурный порог рекристаллизации равен соответственно 100, 270 и 450ºС. На стадии первичной рекристаллизации зарождение и рост новых зерен происходит одновременно. Зерна растут путем движения большеугловых границ через наклепанный металл. В таком зерне плотность дислокаций и других дефектов минимальна, в наклепанном металле – максимальна.
 Первичная рекристаллизация заканчивается при полном замещении новыми зернами всего объема деформированного металла (см. рис. 4.20, в).
Первичная рекристаллизация заканчивается при полном замещении новыми зернами всего объема деформированного металла (см. рис. 4.20, в).
Первичная рекристаллизация полностью снимет наклеп, созданный при пластическом деформировании, металл приобретает равновесную структуру с минимальным количеством дефектов кристаллического строения. Свойства металла после рекристаллизации близки к свойствам отожженного металла (рис. 4.21).
Особое значение имеет рост зерен при нагреве деформированного металла, когда его деформация близка к критической. При критической деформации еще не формируется ячеистая дислокационная структура, способная создать зародыши рекристаллизации, что способствовало бы формированию мелкозернистой структуры. Неоднородность деформации зерен, различия энергии упругих искажений являются движущей силой укрупнения зерен за счет менее устойчивых мелких зерен.
Собирательная рекристаллизация представляет самопроизвольный процесс укрупнения зерен, образовавшихся на стадии первичной рекристаллизации. Чем крупнее зерна, тем меньше суммарная поверхность границ зерен и тем меньше запас избыточной поверхностной энергии (по сравнению с объемом зерен).
Рост зерен происходит в результате перехода атомов от одного зерна к соседнему через границу раздела; одни зерна при этом постепенно уменьшаются в размерах и затем совсем исчезают, другие – становятся более крупными, поглощая соседние зерна (рис. 4.20, г). С повышением температуры рост зерен ускоряется.
Собирательная рекристаллизация тормозится, когда зерна становятся многогранниками с плоскими гранями, а углы между соседними гранями составляют 120º (рис. 4.20, д).
Вторичная рекристаллизация представляет собой стадию неравномерного роста одних зерен по сравнению с другими. В результате формируется конгломерат зерен-гигантов, соседствующих с зернами-карликами. Механические свойства подобной разнозернистой структуры хуже, чем однородной структуры рекристаллизованного металла. Вторичной рекристаллизации соответствуют высокие температуры нагрева наклепанного металла.
Описанный процесс рекристаллизации типичен для скоростей нагрева в обычных термических печах, и для завершения той или иной стадии рекристаллизации требуются выдержки порядка нескольких часов.
Первичная рекристаллизация ускоряется при высоких температурах (~ 1000 ºС/с) скоростях нагрева, где она развивается при высоких температурах и заканчивается формированием мелкозернистой структуры за секунды вместо часов. Для реализации скоростной рекристаллизации используют индукционный нагрев или непосредственное пропускание электрического тока через наклепанный металл.
 Пластичность и вязкость металлов, образующихся в результате рекристаллизации, зависит в основном от степени пластической деформации (рис. 5.15, а), а также от температуры, при которой происходила рекристаллизация. Увеличение выдержки при нагреве способствует росту зерен, но эффект значительно меньше, чем при повышении температуры нагрева.
Пластичность и вязкость металлов, образующихся в результате рекристаллизации, зависит в основном от степени пластической деформации (рис. 5.15, а), а также от температуры, при которой происходила рекристаллизация. Увеличение выдержки при нагреве способствует росту зерен, но эффект значительно меньше, чем при повышении температуры нагрева.
Зависимость размера зерен от степени деформации и температуры демонстрируют при помощи диаграмм рекристаллизации (рис. 5.15, б).
 Для конструкционных материалов общего назначения анизотропия свойств нежелательна. Рекристаллизованные сплавы, как правило, однородны по свойствам и анизотропии не обнаруживают. Однако при известных условиях в рекристаллизованном металле проявляется предпочтительная кристаллографическая ориентация зерен, которую называют текстурой рекристаллизации. Ее вид зависит от химического состава сплава, характера деформирования, природы и количества примесей, технологических факторов.
Для конструкционных материалов общего назначения анизотропия свойств нежелательна. Рекристаллизованные сплавы, как правило, однородны по свойствам и анизотропии не обнаруживают. Однако при известных условиях в рекристаллизованном металле проявляется предпочтительная кристаллографическая ориентация зерен, которую называют текстурой рекристаллизации. Ее вид зависит от химического состава сплава, характера деформирования, природы и количества примесей, технологических факторов.
Нередко она является копией текстуры деформации наклепанного металла. Образование текстуры рекристаллизации имеет практическое значение для сплавов с особыми физическими свойствами, когда требуется улучшить свойства в определенном направлении изделия. Например, в листах трансформаторной стали образование текстуры дает возможность уменьшить потери на перемагничивание по определенным направлениям листа.
Рекристаллизация многофазных сплавов представляет более сложный процесс, в котором на зарождении и росте новых рекристаллизованных зерен сказываются различия свойств каждой фазы, характер структуры и объемные соотношения между фазами. Особое значение имеют размер частиц второй фазы и среднее расстояние между частицами. Чем ближе друг к другу расположены частицы второй фазы, тем труднее перемещаться границе нового зерна и тем сильнее тормозится рекристаллизация. Это проявляется в повышении температуры рекристаллизации и увеличении времени для завершения первичной рекристаллизации многофазного сплава по сравнению с однофазным. Близость частиц второй фазы обеспечивается при достаточно высоком их содержании в сплаве. Когда частиц мало и они далеко друг от друга, их роль в рекристаллизации незначительна. Мелкие частицы (0,1 мкм и меньше) тормозят рекристаллизацию. Более крупные частицы (свыше 0,1 – 0,5 мкм) тормозят рекристаллизацию, когда располагаются близко одна от другой, и ускоряют ее, когда расстояние между ними возрастает. В последнем случае сказывается влияние межфазной границы, на которой преимущественно зарождаются новые зерна.
Тормозящее влияние дисперсных частиц второй фазы на рекристаллизацию успешно используют в промышленных сплавах для повышения рабочих температур.
При горячем деформировании материалов с ультрамелким зерном (0,5 – 10 мкм) проявляется сверхпластичное состояние металла. При низких скоростях деформирования (10-5 – 10-4 с-1) металл течет равномерно, не упрочняясь: относительные удлинения достигают 100 – 1000%.
Огромные деформации в сверхпластичном состоянии складываются из зернограничного скольжения, дополненного направленным (под действием напряжений) диффузионным переносом атомов и обычным скольжением внутри зерен. Для того чтобы реализовать сверхпластичное состояние, требуется сохранить ультрамелкие зерна в течение всего периода деформирования (порядка десятков минут) при температуре выше 0,5Тпл. промышленные сверхпластичные сплавы имеют двухфазную структуру (лучшее сочетание объемов обеих фаз 1:1, так как при этом максимальна поверхность межфазных границ) и поэтому сохраняют исходную мелкозернистость в течение всего срока изготовления изделий. К числу таких сплавов принадлежат различные эвтектические и эвтектоидные смеси, двухфазные сплавы титана и т.п.
Сверхпластичное состояние используют на практике для производства изделий весьма сложной формы при помощи пневматического формования листов или объемного прессования. Несмотря на медленность самого процесса формования и сравнительно высокие рабочие температуры, процесс выгоден, а в ряде случаев является единственным способом получения изделий, когда металл нужно без разрушения деформировать на 200 – 300% и выше.
Процессы, основанные на использовании мелкозернистой структуры, широко применяются в промышленности. Сверхпластичность наблюдается при горячем деформировании сплавов в непосредственной близости к температурам полиморфного превращения или плавления. В этих случаях микроструктура сохраняется, но кристаллическая решетка основы сплава оказывается неустойчивой: например, модуль упругости уменьшается в 2 – 3 раза. При малых скоростях деформирования металл способен деформироваться без разрушения на десятки процентов.
Кристаллизация сталей
Кристаллизация чистого железа протекает изотермически при 1539 ºС, а сплавов железа с углеродом – в интервале температур, рассмотрим вначале верхний участок диаграммы состояния(рис. 5.2), где происходит перитектическое превращение.
 Сплав I, содержащий менее 0,1%С, не испытывает перитектического превращения. Он кристаллизуется в интервал е температур точек 1 – 2. При этом составы жидкой фазы и феррита изменяются по обычным законам кристаллизации твердых растворов. Образуется зернистая структура, состоящая из кристаллов феррита. В интервале температур точек 3 – 4 происходит перекристаллизация феррита в аустенит, вызванная полиморфизмом железа.
Сплав I, содержащий менее 0,1%С, не испытывает перитектического превращения. Он кристаллизуется в интервал е температур точек 1 – 2. При этом составы жидкой фазы и феррита изменяются по обычным законам кристаллизации твердых растворов. Образуется зернистая структура, состоящая из кристаллов феррита. В интервале температур точек 3 – 4 происходит перекристаллизация феррита в аустенит, вызванная полиморфизмом железа.
 Сплав Ш, содержащий 0,16%С, при кристаллизации из жидкой фазы в интервале температур точек 8 – 9 образует кристаллы феррита, которые при температуре точки 9 имеют состав точки H, а оставшаяся жидкость – состав точки B. При 1499ºС протекает перитектическая реакция кристаллы феррита взаимодействуют с жидкой фазой состава точки J. Согласно правилу фаз перитектический процесс идет изотермически и при постоянной концентрации фаз, так как число степеней свободы при этом процессе равно нулю.
Сплав Ш, содержащий 0,16%С, при кристаллизации из жидкой фазы в интервале температур точек 8 – 9 образует кристаллы феррита, которые при температуре точки 9 имеют состав точки H, а оставшаяся жидкость – состав точки B. При 1499ºС протекает перитектическая реакция кристаллы феррита взаимодействуют с жидкой фазой состава точки J. Согласно правилу фаз перитектический процесс идет изотермически и при постоянной концентрации фаз, так как число степеней свободы при этом процессе равно нулю.
Сплавы типа II имеют содержание углерода от 0,1 до 0,16%С. В интервале температур точек 5 – 6 выделяется феррит. При температуре точки 6 в сплаве II содержится избыточный феррит. В результате перитектический процесс заканчивается образованием новой фазы аустенита при сохранении некоторого количества феррита:
Ф H + Ж B 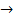 AJ + Ф H (ост) .
AJ + Ф H (ост) .
При дальнейшем охлаждении этот остаток феррита перекристаллизуется в аустенит с тем содержанием углерода, которое имеет сплав.
Сплавы типа IV содержат от 0,16 до 0,51%С. При температуре точки 11 они имеют избыток жидкой фазы по сравнению со сплавом III. В результате перитектический процесс заканчивается образованием аустенита при сохранении некоторого количества жидкой фазы:
Ф H + Ж B 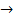 AJ + Ж В (ост) .
AJ + Ж В (ост) .
При дальнейшем охлаждении в интервале температур точек 11 – 12 оставшаяся жидкая фаза затвердевает, образуя аустенит. Концентрация углерода в аустените ниже температуры точки 11 изменяется по линии JE.
Таким образом, все рассмотренные сплавы, лежащие ниже линий NJ и JE, находятся в твердом состоянии и имеют аустенитную структуру.
Превращения чугунов
 В сплавах с содержанием углерода более 2,14% при кристаллизации происходит эвтектическое превращение. Такие сплавы называют белыми чугунами.
В сплавах с содержанием углерода более 2,14% при кристаллизации происходит эвтектическое превращение. Такие сплавы называют белыми чугунами.
 Сплав II (рис. 5.6) – эвтектический белый чугун (4,3%С) кристаллизуется при эвтектической температуре изотермически с одновременным выделением двух фаз: аустенита состава точки E и цементита. Образующаяся смесь этих фаз, как известно, названа ледебуритом. Фазовый состав ледебурита, как и любой эвтектики, постоянен и определяется отношением отрезков Ц/АЕ = EC / CF.
Сплав II (рис. 5.6) – эвтектический белый чугун (4,3%С) кристаллизуется при эвтектической температуре изотермически с одновременным выделением двух фаз: аустенита состава точки E и цементита. Образующаяся смесь этих фаз, как известно, названа ледебуритом. Фазовый состав ледебурита, как и любой эвтектики, постоянен и определяется отношением отрезков Ц/АЕ = EC / CF.
При дальнейшем охлаждении концентрация углерода в аустените изменяется по линии ES вследствие выделения вторичного цементита и к температуре эвтектоидного превращения принимает значение 0,8%С. При температуре линии PSK аустенит в ледебурите претерпевает эвтектоидное превращение в перлит.
В доэвтектических белых чугунах (< 4,3%С) кристаллизация сплава начинается с выделения аустенита из жидкого раствора. В сплаве I (см. рис. 5.6) этот процесс идет в интервале температур точек 1 – 2. При температуре точки 2 образуется эвтектика (ледебурит) по реакции
ЖС + АЕ 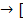 AE + Ц ] + АЕ.
AE + Ц ] + АЕ.
При последующем охлаждении из аустенита, структурно свободного и входящего в ледебурит, выделяется вторичный цементит. Обедненный вследствие этого аустенит при 727ºС превращается в перлит.
Структура доэвтектического белого чугуна показана на рис. 4.17, а. крупные темные поля на фоне ледебурита – перлит, образовавшийся из структурно свободного аустенита.

 Сплав III (см. рис. 5.6) – заэвтектический белый чугун ( > 4,3%С). В заэвтектических чугунах кристаллизация начинается с выделения из жидкого раствора кристаллов первичного цементита и в интервале температур точек 5 – 6; при этом состав жидкой фазы изменяется согласно линии DC. Первичная кристаллизация заканчивается эвтектическим превращением, с образованием ледебурита. При дальнейшем охлаждении происходят превращения в твердом состоянии, такие же, как в сплаве II.
Сплав III (см. рис. 5.6) – заэвтектический белый чугун ( > 4,3%С). В заэвтектических чугунах кристаллизация начинается с выделения из жидкого раствора кристаллов первичного цементита и в интервале температур точек 5 – 6; при этом состав жидкой фазы изменяется согласно линии DC. Первичная кристаллизация заканчивается эвтектическим превращением, с образованием ледебурита. При дальнейшем охлаждении происходят превращения в твердом состоянии, такие же, как в сплаве II.
Конечная структура заэвтектического чугуна при 20 – 25ºС показана на рис. 5.7, б. В ледебурите видны темные участки перлита; резко выделяются крупные пластинки первичного цементита.
Виды термической обработки
Термической обработкой называют технологические процессы, состоящие из нагрева и охлаждения металлических изделий с целью изменения их структуры и свойств.
Термической обработке подвергают слитки, отливки, полуфабрикаты, сварные соединения, детали машин, инструменты.
Основные виды термической обработки – отжиг, закалка, отпуск и старение. Каждый из указанных видов имеет несколько разновидностей.
Отжиг – термическая обработка, в результате которой металлы или сплавы приобретают структуру, близкую к равновесной: отжиг вызывает разупрочнение металлов и сплавов, сопровождающийся повышением пластичности и снятием остаточных напряжений.
Температура нагрева при отжиге зависит от состава сплава и конкретной разновидности отжига; скорость охлаждения с температуры отжига обычно невелика, она лежит в пределах 30 – 200ºС/ч.
Закалка – термическая обработка, в результате которой в сплавах образуется неравновесная структура. Неравновесные структуры при термической обработке можно получить только в том случае, когда в сплавах имеются превращения в твердом состоянии: переменная растворимость, полиморфные превращения твердых растворов, распад высокотемпературного твердого раствора по эвтектоидной реакции и др. Для получения неравновесной структуры сплав нагревают выше температуры фазового превращения в твердом состоянии, после чего быстро охлаждают, чтобы предотвратить равновесное превращение при охлаждении. Конструкционные и инструментальные сплавы закаливают для упрочнения. Сильно упрочняются при закалке сплавы, претерпевающие в равновесных условиях эвтектоидное превращение. Прочность возрастает либо вследствие мартенситного фазового перехода, либо из-за понижения температуры эвтектоидной реакции, приводящей к измельчению зерен, образующих эвтектоидную смесь. Если в результате закалки при 20 – 25ºС фиксируется состояние высокотемпературного твердого раствора, значительного упрочнения сплава непосредственно после закалки не происходит; основное упрочнение создается при повторном низкотемпературном нагреве или во время выдержки при 20 – 25ºС.
В сплавах с особыми свойствами закалка позволяет изменить структурно-чувствительные физические или химические свойства: увеличить удельное электрическое сопротивление или коэрцитивную силу, повысить коррозионную стойкость и др.
Отпуск и старение – термические обработки, в результате которых в предварительно закаленных сплавах происходят фазовые превращения, приближающие их структуру к равновесной.
Сочетание закалки с отпуском или старением практически всегда предполагает получение более высокого уровня свойств (твердости, характеристик прочности, коэрцитивной силы, удельного электросопротивления и др.) по сравнению с отожженным состоянием.
В большинстве сплавов после закалки получают пересыщенный твердый раствор (или смесь, твердых растворов); в этом случае основной процесс, происходящий при отпуске или старении, – распад пересыщенного твердого раствора.
Температуру и выдержку выбирают таким образом, чтобы равновесное состояние сплава при обработке не достигалось, как это происходит при отжиге. Скорость охлаждения с температуры отпуска или старения за редким исключением не влияет на структуру и свойства сплавов.
Термин «отпуск» используют обычно применительно к сталям и другим сплавам, испытывающим при закалке полиморфное превращение (двухфазные алюминиевые бронзы, некоторые сплавы на основе титана); термин «старение» применительно к сплавам, не претерпевающим при закалке полиморфного превращения (сплавы на основе алюминия, аустенитные стали, никелевые сплавы и др.).
Принципиальная возможность применения того или другого вида термической обработки может быть определена на основании диаграмм состояния фазового равновесия. В связи с этим выделяют следующие основные группы сплавов:
1. Сплавы, не имеющие фазовых превращений в твердом состоянии (см. рис. 3.3, 3.10);
2. Сплавы с переменной растворимостью компонентов в твердом состоянии (см. рис. 3.4);
3. Сплавы с эвтектоидным превращением (см. рис. 3.9).
Любой технологический процесс термической обработки состоит из трех основных этапов: нагрев, изотермическая выдержка и охлаждение. Нагрев, а иногда и весь процесс термической обработки (отжиг) проводят в термических печах.
Рекристаллизационный отжиг
Нагрев деформированных полуфабрикатов или деталей выше температуры рекристаллизации называют рекристаллизационным отжигом; в процессе выдержки происходит главным образом рекристаллизация. Скорость охлаждения при этой разновидности отжига не имеет решающего значения; обычно охлаждение после окончания выдержки проводят на воздухе. Цель отжига – понижение прочности и восстановление пластичности деформированного металла, получение определенной кристаллографической текстуры, создающей анизотропию свойств; и заданного размера зерна.
Рекристаллизационный отжиг часто используют в качестве межоперационной смягчающей обработки при холодной прокатке, волочении и других операциях холодного деформирования. Температуру отжига обычно выбирают на 100 – 200ºС выше температуры рекристаллизации.
Рекристаллизационный отжиг может быть использован в качестве окончательной обработки полуфабрикатов.
В некоторых металлах и твердых растворах рекристаллизация сопровождается образованием текстуры (преимущественной ориентации кристаллов в объеме детали), которая создает анизотропия свойств. Это позволяет улучшить те или иные свойства вдоль определенных направлений в деталях (магнитные свойства в трансформаторной стали и пермаллоях, модуль упругости в некоторых пружинных сплавах и т.п.).
В машино- и приборостроении широкое применение находят металлы и сплавы – твердые растворы, не имеющие фазовых превращений в твердом состоянии (алюминий, медь, никель, ферритные и аустенитные стали, однофазные латуни и бронзы).
В таких материалах единственной возможностью регулирования размера зерен является сочетание холодной пластической деформации с последующим рекристаллизационным отжигом.
Перлитное превращение
 Влияние степени переохлаждения на устойчивость аустенита и скорость превращения представляют графически в виде диаграмм. Эти диаграммы строят в координатах температура превращения – время; обычно время откладывают на логарифмической шкале (Рис. 7.2).
Влияние степени переохлаждения на устойчивость аустенита и скорость превращения представляют графически в виде диаграмм. Эти диаграммы строят в координатах температура превращения – время; обычно время откладывают на логарифмической шкале (Рис. 7.2).
 Диаграммы строят на основе экспериментальных данных. Образцы сталей, нагретые до аустенитного состояния, быстро переносят в ванну с жидкой средой, имеющей температуру ниже равновесной температуры превращения, и выдерживают до завершения превращения. При этом фиксируют изменение какого-либо свойства, чтобы определить время начала и конца превращения. При температурах, меньших точки Кюри, следят за изменением магнитных свойств стали, так как они изменяются наиболее резко (аустенит парамагнитен, а продукты превращения аустенита ферромагнитны).
Диаграммы строят на основе экспериментальных данных. Образцы сталей, нагретые до аустенитного состояния, быстро переносят в ванну с жидкой средой, имеющей температуру ниже равновесной температуры превращения, и выдерживают до завершения превращения. При этом фиксируют изменение какого-либо свойства, чтобы определить время начала и конца превращения. При температурах, меньших точки Кюри, следят за изменением магнитных свойств стали, так как они изменяются наиболее резко (аустенит парамагнитен, а продукты превращения аустенита ферромагнитны).
Основные закономерности перлитного превращения рассмотрим на примере эвтектоидной стали. Изотермический распад аустенита этой стали происходит в интервале температур от А r 1 (720ºС) до M н (250ºС), где M н – температура начала мартенситного превращения. Мартенситное превращение в эвтектоидной стали при постоянной температуре ниже точки M н не происходит.

 На диаграмме (см. рис. 7.2) нанесены С-образные кривые, указывающие время начала и конца превращения переохлажденного аустенита. В области диаграммы, расположенной левее линии 1, существует переохлажденный аустенит; между линиями 1 и 2 находится область, в которой происходит превращение; правее линии 2 лежит область, в которой существуют продукты превращения аустенита. Устойчивость аустенита зависит от степени переохлаждения. Наименьшей устойчивостью аустенит обладает при температурах, близких к 550ºС. Для эвтектоидной стали время устойчивости аустенита при 550 –- 560ºС составляет около 1 с. При повышении или понижении температуры относительно 550ºС устойчивость аустенита возрастает. Так, при 700ºС это время составляет около 10 с, а при 300ºС – около 60 с.
На диаграмме (см. рис. 7.2) нанесены С-образные кривые, указывающие время начала и конца превращения переохлажденного аустенита. В области диаграммы, расположенной левее линии 1, существует переохлажденный аустенит; между линиями 1 и 2 находится область, в которой происходит превращение; правее линии 2 лежит область, в которой существуют продукты превращения аустенита. Устойчивость аустенита зависит от степени переохлаждения. Наименьшей устойчивостью аустенит обладает при температурах, близких к 550ºС. Для эвтектоидной стали время устойчивости аустенита при 550 –- 560ºС составляет около 1 с. При повышении или понижении температуры относительно 550ºС устойчивость аустенита возрастает. Так, при 700ºС это время составляет около 10 с, а при 300ºС – около 60 с.
Превращения аустенита при температурах в интервале А r 1 – 550ºС называют перлитным, а превращение при температурах в интервале 550 – M н – промежуточным.
В интервале температур перлитного превращения в результате распада аустенита образуются пластинчатые структуры перлитного типа, т.е. структуры, образованные из кристаллов феррита и цементита. Перлитное превращение (рис. 7.3, а) вначале протекает медленно, затем скорость его увеличивается до постоянной величины; в конце превращения скорость постепенно убывает.
Строение перлитной структуры зависит от температуры превращения. С увеличением степени переохлаждения, в соответствии с общими законами кристаллизации, уменьшается размер образующихся кристаллов, т.е. возрастает дисперсность феррито-цементитной смеси.

 Дисперсность перлитных структур принято оценивать межпластиночным расстоянием, за которое принимают среднюю суммарную толщину соседних пластинок феррита (Ф) и цементита (Ц) (рис 7.4). если превращение происходит при температурах более высоких, чем 650 – 670ºС, образуется сравнительно грубая смесь кристаллов феррита и цементита с межпластиночным расстоянием (5…7)∙10-7 м; такую смесь называют собственно перлитом. Превращение при 640 – 590ºС дает межпластиночное расстояние (3…4)∙10-7 м; такую перлитную структуру называют сорбитом. При температуре превращения 580 – 550ºС межпластиночное расстояние уменьшается до (1…2) 10-7 м; такую структуру называют трооститом.
Дисперсность перлитных структур принято оценивать межпластиночным расстоянием, за которое принимают среднюю суммарную толщину соседних пластинок феррита (Ф) и цементита (Ц) (рис 7.4). если превращение происходит при температурах более высоких, чем 650 – 670ºС, образуется сравнительно грубая смесь кристаллов феррита и цементита с межпластиночным расстоянием (5…7)∙10-7 м; такую смесь называют собственно перлитом. Превращение при 640 – 590ºС дает межпластиночное расстояние (3…4)∙10-7 м; такую перлитную структуру называют сорбитом. При температуре превращения 580 – 550ºС межпластиночное расстояние уменьшается до (1…2) 10-7 м; такую структуру называют трооститом.
Указанное деление перлитных структур условно, так как дисперсность смесей монотонно увеличивается с понижением температуры превращения.
Центры кристаллизации перлитных колоний возникают преимущественно на границах зерен аустенита; при этом перлитные колонии растут во все стороны.
При перлитном превращении полиморфный переход γ 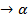 сопровождается перераспределением углерода. Для образования цементита, содержащего 6,69% С, необходимо перемещение атомов углерода на расстояния, значительно большие межатомных расстояний, так как среднее содержание углерода в твердом растворе до превращения гораздо меньше, чем в цементите.
сопровождается перераспределением углерода. Для образования цементита, содержащего 6,69% С, необходимо перемещение атомов углерода на расстояния, значительно большие межатомных расстояний, так как среднее содержание углерода в твердом растворе до превращения гораздо меньше, чем в цементите.
Несмотря на то, что подвижность атомов железа и углерода с понижением температуры от точки А r 1 уменьшается, скорость перлитного превращения возрастает, вплоть до 550ºС. Это объясняется тем, что с увеличением степени переохлаждения, быстро, возрастает число центров кристаллизации и соответственно уменьшаются расстояния, на которые должны переместиться атомы в процессе превращения.
С увеличением дисперсности структур перлитного типа возрастают прочность, и твердость стали; лучшую пластичность и вязкость имеет структура сорбита.
Отжиг сталей
Существует несколько разновидностей отжига. Для конструкционных сталей наибольшее применение находят перекристаллизационный отжиг, а для инструментальных – сфероидизирующий отжиг.
Нормализация сталей
Нормализации чаще всего подвергают конструкционные стали после горячей обработки давлением и фасонного литья. Нормализация отличается от отжига в основном условиями охлаждения; после нагрева до температуры на 50 – 70ºС выше АС3 сталь охлаждают на спокойном воздухе. Нормализация приводит к получению более высокой прочности стали, так как при ускорении охлаждения распад аустенита происходит при более низких температурах.
Легированные конструкционные стали с повышенной устойчивостью переохлажденного аустенита после нормализации приобретают высокую твердость, затрудняющую последующую обработку резанием. В связи с этим после нормализации проводят отпуск при температурах, обеспечивающих получение требуемой твердости (650 - 750ºС в зависимости от состава стали).
После нормализации углеродистых и низколегированных сталей, как и после отжига, образуется феррито-перлитная структура, однако имеются и существенные структурные отличия (рис. 7.17). При ускоренном охлаждении доэвтектоидный феррит при прохождении температурного интервала А r 3- А r 1 выделяется на границах зерен аустенита; поэтому кристаллы  феррита образуют сплошные или разорванные оболочки вокруг зерен аустенита – ферритную сетку.
феррита образуют сплошные или разорванные оболочки вокруг зерен аустенита – ферритную сетку.
 Нормализация позволяет несколько уменьшить анизотропию свойств, вызванную наличием в горячедеформированной стали вытянутых неметаллических включений. При ускоренном охлаждении (по сравнению с отжигом) возникает больше самопроизвольно образующихся центров кристаллизации, поэтому строчечность структуры менее резко выражена. Это дополнительное преимущество данного вида обработки.
Нормализация позволяет несколько уменьшить анизотропию свойств, вызванную наличием в горячедеформированной стали вытянутых неметаллических включений. При ускоренном охлаждении (по сравнению с отжигом) возникает больше самопроизвольно образующихся центров кристаллизации, поэтому строчечность структуры менее резко выражена. Это дополнительное преимущество данного вида обработки.
Свойства нормализованных горячекатаных полуфабрикатов существенно зависят от сечения: чем меньше сечение, тем быстрее произойдет охлаждение на спокойном воздухе и тем выше будет прочность стали.
Особенности закалки сталей
В большинстве случаев при закалке желательно получить структуру наивысшей твердости, т.е. мартенсит, при последующем отпуске которого можно понизить твердость и повысить пластичность стали. При равной твердости структуры, полученные при отпуске мартенсита, имеют лучшие механические свойства, чес структуры, полученные непосредственно в результате распада аустенита, за исключением нижнего бейнита.

 В зависимости от температуры нагрева под закалку называют полной и неполной. При полной закалке сталь переводят в однофазное аустенитное состояние, т.е. нагревают выше критических температур АС3 или АС cm, при неполной – до межкритических температур – между АС1 и АС3 (АС cm) (рис. 7.18 а).
В зависимости от температуры нагрева под закалку называют полной и неполной. При полной закалке сталь переводят в однофазное аустенитное состояние, т.е. нагревают выше критических температур АС3 или АС cm, при неполной – до межкритических температур – между АС1 и АС3 (АС cm) (рис. 7.18 а).
Доэвтектоидные стали, как правило, подвергают полной закалке, при этом оптимальной температурой нагрева является температура АС3 + (30…50  ). Такая температура обеспечивает получение при нагреве мелкозернистого аустенита и соответственно после охлаждения – мелкокристаллического мартенсита. Недогрев до температуры АС3 приводит к сохранению в структуре кристаллов доэвтектоидного феррита, что при некотором уменьшении прочности обеспечивает повышенную пластичность закаленной стали.
). Такая температура обеспечивает получение при нагреве мелкозернистого аустенита и соответственно после охлаждения – мелкокристаллического мартенсита. Недогрев до температуры АС3 приводит к сохранению в структуре кристаллов доэвтектоидного феррита, что при некотором уменьшении прочности обеспечивает повышенную пластичность закаленной стали.
Заэвтектоидные стали подвергают неполной закалке. Оптимальная температура нагрева углеродистых и низколегированных сталей при этом – температура АС1 + (30…50  ).
).
После закалки заэвтектоидная сталь приобретает структуру, состоящую из мартенсита и цементита. Кристаллы цементита тверже кристаллов мартенсита, поэтому при неполной закалке заэвтектоидные стали имеют более высокую твердость, чем при полной. Так как сталь предварительно подвергалась сфероидизирующему отжигу, избыточные карбиды округлой формы не вызывают снижения вязкости. Высоколегированные инструментальные стали ледебуритного класса (рис. 7.18, б) для повышения теплостойкости[5] нагревают при закалке до очень высоких температур (область 1), близких к эвтектической. При этом происходит распад всех вторичных карбидов, аустенит обогащается не только углеродом, но и легирующими элементами, содержащимися в карбидах. В результате получается высоколегированный, а следовательно, и теплостойкий мартенсит.
Если высоколегированные инструментальные стали используют не как теплостойкие, а только как износостойкие, температуру закалки понижают (см. рис. 7.18, область 2). Сохраняя некоторое количество вторичных карбидов нерастворенными. При такой закалке температура нагрева достаточно высокая (900 – 1000  ). Это связано с влиянием легирующих элементов на критические температуры стали и с малой скоростью диффузии легирующих элементов в твердом растворе.
). Это связано с влиянием легирующих элементов на критические температуры стали и с малой скоростью диффузии легирующих элементов в твердом растворе.
Для получения мартенситной структуры необходимо переохладить аустенит до температуры мартенситного превращения; следовательно, скорость охлаждения должна превышать критическую скорость (см. рис. 7.18).
Для углеродистых сталей 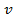 кр составляет 400 – 1400
кр составляет 400 – 1400 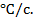 Для того чтобы переохладить аустенит таких сталей до температуры мартенситного превращения, необходимо прибегать к очень резкому охлаждению, которое достигается погружением закаливаемых деталей в холодную воду либо воду с добавками соли или едкого натра (табл. 6.2).
Для того чтобы переохладить аустенит таких сталей до температуры мартенситного превращения, необходимо прибегать к очень резкому охлаждению, которое достигается погружением закаливаемых деталей в холодную воду либо воду с добавками соли или едкого натра (табл. 6.2).
При охлаждении на поверхности стальной детали не должна образоваться паровая пленка, препятствующая теплообмену с закалочной средой.
Лучшей является стадия пузырькового кипения охлаждающей жидкости. Чем больше температурный интервал этой стадии, тем интенсивнее охлаждает закалочная среда.
 |
Лучше пользоваться добавками едкого натра, так как щелочная среда не вызывает последующей коррозии стальных деталей. Многие легированные стали приобретают мартенситную структуру при охлаждении в холодных или подогретых маслах, а высоколегированные стали закаливаются на мартенсит даже при охлаждении на воздухе.
|
 . Однако в некоторых случаях для уменьшения деформации (коробления) деталей или для предотвращения образования трещин условия охлаждения усложняют.
. Однако в некоторых случаях для уменьшения деформации (коробления) деталей или для предотвращения образования трещин условия охлаждения усложняют.
Коробление и растрескивание вызываются значительными остаточными напряжениями, возникающими при закалке. Основной источник напряжений – увеличение объема при превращении аустенита в мартенсит. Модуль упругости в температурном интервале мартенситного превращения достаточно велик, поэтому возникающие из-за объемных изменений напряжения релаксируют с малой скоростью. Значительные макроскопические напряжения возникают из-за неодновременности превращения по сечению, а также в закаливаемых деталях сложной формы. Остаточные напряжения уменьшаются при условии одновременного превращения по сечению и понижения скорости охлаждения в интервале температур M н – M к.
В практике термической обработки сталей широкое использование нашли следующие способы охлаждения, позволяющие значительно уменьшить величину остаточных напряжений: закалка в двух средах и ступенчатая закалка.

 Закалка в двух средах. Схема обработки показана на рис. 7.19. после нагрева под закалку деталь погружают на определенное время в воду, в результате чего достигается быстрое прохождение температурного интервала минимальной устойчивости аустенита, а затем переносят в более мягкую охлаждающую среду, обычно в масло.
Закалка в двух средах. Схема обработки показана на рис. 7.19. после нагрева под закалку деталь погружают на определенное время в воду, в результате чего достигается быстрое прохождение температурного интервала минимальной устойчивости аустенита, а затем переносят в более мягкую охлаждающую среду, обычно в масло.
Ступенчатая закалка. При ступенчатой закалке деталь, нагретую до температуры закалки, переносят в жидкую среду, имеющую температуру на 50 – 100  выше мартенситной точки M н закаливаемой стали, и выдерживают небольшое время, необходимое для выравнивания температуры по сечению, а затем окончательно охлаждают на спокойном воздухе. (см. рис. 7.19).
выше мартенситной точки M н закаливаемой стали, и выдерживают небольшое время, необходимое для выравнивания температуры по сечению, а затем окончательно охлаждают на спокойном воздухе. (см. рис. 7.19).
Получение мартенсита при таком способе охлаждения возможно только в легированных сталях с достаточно высокой устойчивостью переохлажденного аустенита в интервале температур перлитного превращения.
К ступенчатой закалке прибегают обычно при термической обработке инструментов небольшого сечения из низко- и среднелегированных сталей. Достоинство указанного способа охлаждения состоит в также в возможности правки инструментов в специальных приспособлениях при охлаждении после изотермической выдержки.
Изотермическая закалка. В некоторых случаях после закаоки на мартенсит и последующего отпуска не удается получить достаточной прочности и вязкости, тогда применяют изотермическую закалку на нижний бейнит, обладающий высокой вязкостью и прочностью.
При изотермической закалке нагретую деьаль переносят в ванну с расплавленными солями, имеющие температуру на 50 – 100  выше мартенситной точки M н, выдерживают при этой температуре до завершения превращения аустенита в бейнит и затем охлаждают на воздухе (см. рис 7.19).
выше мартенситной точки M н, выдерживают при этой температуре до завершения превращения аустенита в бейнит и затем охлаждают на воздухе (см. рис 7.19).
Изотермическая закалка, так же как и ступенчатая, применяется только к сталям с достаточной устойчивостью переохлажденного аустенита.
Для предотвращения коробления изделий, таких, как ножовки, пилы, бритвы, их охлаждают заневоленными, например, в массивных медных или стальных плитах; скорость охлаждения в этих условиях оказывается меньшей, чем в маслах.
Обработка холодом[6]. Охлаждение закаленных деталей до температуры, меньшей 20 – 25  , называют обработкой холодом.
, называют обработкой холодом.
Обработке холодом подвергают закаленные легированные стали, для которых температура конца мартенситного превращения M к значительно ниже 20 – 25  . Вследствие этого, после охлаждения до этой температуры, наряду с мартенситом в структуре оказывается значительное количество остаточного аустенита. Остаточный аустенит понижает твердость закаленной стали и может вызвать нестабильность размеров готовых деталей, так как, являясь нестабильной фазой, способен к распаду при низкой температуре с малой скоростью. Для стабилизации размеров закаленных изделий и повышения их твердости проводится охлаждение до температуры M к, в процессе которого аустенит превращается в мартенсит. Температура M к легированных сталей изменяется в широких пределах, поэтому при обработке холодом их охлаждают до температур от -40 до -196
. Вследствие этого, после охлаждения до этой температуры, наряду с мартенситом в структуре оказывается значительное количество остаточного аустенита. Остаточный аустенит понижает твердость закаленной стали и может вызвать нестабильность размеров готовых деталей, так как, являясь нестабильной фазой, способен к распаду при низкой температуре с малой скоростью. Для стабилизации размеров закаленных изделий и повышения их твердости проводится охлаждение до температуры M к, в процессе которого аустенит превращается в мартенсит. Температура M к легированных сталей изменяется в широких пределах, поэтому при обработке холодом их охлаждают до температур от -40 до -196 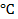 (температуры жидкого азота).
(температуры жидкого азота).
Остаточный аустенит в процессе выдержки при 20 – 25  несколько стабилизируется, поэтому обработку холодом следует проводить сразу после закалки.
несколько стабилизируется, поэтому обработку холодом следует проводить сразу после закалки.
Обработке холодом подвергают измерительные инструменты, детали подшипников качения, цементированные детали из легированных сталей и ряд других изделий.
Отпуск закаленных сталей
Нагрев закаленных сталей до температур, не превышающих А1, называют отпуском.
В результате закалки чаще всего получают структуру мартенсита с некоторым количеством остаточного аустенита. Иногда – структуру сорбита, троостита или бейнита.
Свойства отпущенной стали
Твердость отпущенной стали определяется нескольким факторами: уменьшение тетрагональности решетки, степени фазового наклепа и укрупнение карбидных частиц вызывают снижение твердости; выделение когерентных кристаллов ε-карбида и дисперсных кристаллов специальных карбидов, а также распад остаточного аустенита способствуют ее повышению.
В конструкционных сталях, в которых количество углерода обычно не превышает 0,7%, твердость уменьшается непрерывно, однако ее снижение невелико до 100 – 120  . В инструментальных сталях с более высоким содержанием углерода эффект твердения вследствие выделения ε-карбида преобладает, поэтому твердость при отпуске до 100 – 120
. В инструментальных сталях с более высоким содержанием углерода эффект твердения вследствие выделения ε-карбида преобладает, поэтому твердость при отпуске до 100 – 120  несколько увеличивается. Изменение твердости углеродистых сталей в интервале температур превращения 200 – 260
несколько увеличивается. Изменение твердости углеродистых сталей в интервале температур превращения 200 – 260  в большой степени зависят от количества остаточного аустенита; например, в
в большой степени зависят от количества остаточного аустенита; например, в 
 стали с содержание 1,2%C в интервале 200 – 300
стали с содержание 1,2%C в интервале 200 – 300  интенсивность снижения твердости уменьшается (рис. 7.23, а).
интенсивность снижения твердости уменьшается (рис. 7.23, а).
Аналогично изменяется твердость при отпуске низколегированных и среднелегированных сталей, не содержащих карбидообразующих легирующих элементов. Сильные карбидообразователи задерживают выделение карбидов железа, поэтому при температуре отпуска до 200 – 300 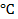 твердость снижается незначительно (рис. 7.23, б). При температурах выделения дисперсных специальных карбидов в сложнолегированных сталях (Cr. W, V; Mo, V и др.) происходит повышение твердости несмотря на уменьшение содержания углерода в мартенсите. Увеличение твердости у сталей с хромом, вольфрамом (молибденом) и ванадием наблюдается при температуре 500 – 600
твердость снижается незначительно (рис. 7.23, б). При температурах выделения дисперсных специальных карбидов в сложнолегированных сталях (Cr. W, V; Mo, V и др.) происходит повышение твердости несмотря на уменьшение содержания углерода в мартенсите. Увеличение твердости у сталей с хромом, вольфрамом (молибденом) и ванадием наблюдается при температуре 500 – 600  .
.
 Для закаленной и неотпущенной сталей характерно довольно низкие значения временного сопротивления, предела упругости и предела текучести; при отпуске до 300
Для закаленной и неотпущенной сталей характерно довольно низкие значения временного сопротивления, предела упругости и предела текучести; при отпуске до 300  эти характеристики прочности возрастают, а при дальнейшем ее повышении монотонно снижаются. Наиболее высокое отношение σ0,2/σв в конструкционных сталях достигается после отпуска при 450 – 650
эти характеристики прочности возрастают, а при дальнейшем ее повышении монотонно снижаются. Наиболее высокое отношение σ0,2/σв в конструкционных сталях достигается после отпуска при 450 – 650  (рис. 7.24).
(рис. 7.24).
 Характеристики пластичности δ и ψ возрастают по мере повышения температуры отпуска (см. рис. 7.24). ударная вязкость непосредственно после закалки низкая. С повышением температуры отпуска ударная вязкость увеличивается, однако есть два температурных интервала, при которых у конструкционных сталей она заметно снижается: 250 – 350
Характеристики пластичности δ и ψ возрастают по мере повышения температуры отпуска (см. рис. 7.24). ударная вязкость непосредственно после закалки низкая. С повышением температуры отпуска ударная вязкость увеличивается, однако есть два температурных интервала, при которых у конструкционных сталей она заметно снижается: 250 – 350 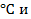 500 – 600
500 – 600  . Понижение вязкости соответственно называют отпускной хрупкостью I и II рода (рис. 7.25). Природа охрупчивания сталей после отпуска при указанных температурах недостаточно ясна.
. Понижение вязкости соответственно называют отпускной хрупкостью I и II рода (рис. 7.25). Природа охрупчивания сталей после отпуска при указанных температурах недостаточно ясна.

 Понижение ударной вязкости после отпуска при 250 – 350
Понижение ударной вязкости после отпуска при 250 – 350  наблюдается у всех конструкционных сталей независимо от степени легирования. Заметное падение ударной вязкости после отпуска при 500 – 600
наблюдается у всех конструкционных сталей независимо от степени легирования. Заметное падение ударной вязкости после отпуска при 500 – 600  наблюдается только у легированных конструкционных сталей – хромистых, марганцевых, хромоникелевых, хромомарганцевых и т.д. снижения вязкости почти не происходит в случае быстрого охлаждения от температуры отпуска (в воде или масле). Отпускная хрупкость II рода заметно подавляется даже при медленном охлаждении от температуры отпуска дополнительным легированием сталей молибденом или вольфрамом в количестве 0,3 и 1% соответственно.
наблюдается только у легированных конструкционных сталей – хромистых, марганцевых, хромоникелевых, хромомарганцевых и т.д. снижения вязкости почти не происходит в случае быстрого охлаждения от температуры отпуска (в воде или масле). Отпускная хрупкость II рода заметно подавляется даже при медленном охлаждении от температуры отпуска дополнительным легированием сталей молибденом или вольфрамом в количестве 0,3 и 1% соответственно.
Комплексную термическую обработку, состоящую из полной закалки и высокого отпуска конструкционных сталей, называют улучшением.
Общие закономерности
Химико-термической обработкой называют технологические процессы, приводящие к диффузионному насыщению поверхностного слоя деталей различными элементами.
Химико-термическую обработку применяют для повышения твердости, износостойкости, сопротивления усталости и контактной выносливости, а также для защиты от электрохимической и газовой коррозии.
Различают три стадии процесса химико-термической обработки.
На первой стадии протекают химические реакции в исходной (окружающей) среде, в результате которых образуются активные диффундирующие элементы, по-видимому, в ионизированном состоянии.
На второй стадии процесса они усваиваются насыщаемой поверхностью металла – происходит адсорбция или хемосорбция диффундирующих элементов, в результате чего тончайший поверхностный слой насыщается диффундирующим элементом (адсорбция), возникает градиент концентрации – движущая сила для следующей стадии процесса.
Третья стадия – диффузионное проникновение элемента вглубь насыщаемого металла, которое сопровождается образованием твердых растворов или фазовой перекристаллизацией.
 Первая и вторая стадии процесса химико-термической обработки протекают значительно быстрее третьей – диффузионной стадии, где формируются структура и свойства диффузионной зоны. Третья стадия определяет скорость процесса химико-термической обработки.
Первая и вторая стадии процесса химико-термической обработки протекают значительно быстрее третьей – диффузионной стадии, где формируются структура и свойства диффузионной зоны. Третья стадия определяет скорость процесса химико-термической обработки.
 Фазовые и структурные изменения, происходящие на состояния, если в диффузионном взаимодействии участвуют всего два элемента диффузионной стадии процесса, можно предсказать с помощью двойных диаграмм. При этом предполагается, что диффузионный процесс не интенсифицируется и образующаяся диффузионная зона находится в равновесном состоянии.
Фазовые и структурные изменения, происходящие на состояния, если в диффузионном взаимодействии участвуют всего два элемента диффузионной стадии процесса, можно предсказать с помощью двойных диаграмм. При этом предполагается, что диффузионный процесс не интенсифицируется и образующаяся диффузионная зона находится в равновесном состоянии.
 Так, при длительном (τ3) диффузионном насыщении элемента А элементом В можно добиться соответствия фазового состава диффузионной зоны равновесной диаграмме состояния (рис. 8.1). Последовательность образования фаз при температуре диффузионного насыщения соответствует последовательности их расположения на диаграмме (γ, ɑ, β, δ на рис. 8.1). Однако фазы, имеющие на диаграмме состояния очень узкие области гомогенности, могут расти медленно, что их слои в диффузионной зоне не обнаруживаются.
Так, при длительном (τ3) диффузионном насыщении элемента А элементом В можно добиться соответствия фазового состава диффузионной зоны равновесной диаграмме состояния (рис. 8.1). Последовательность образования фаз при температуре диффузионного насыщения соответствует последовательности их расположения на диаграмме (γ, ɑ, β, δ на рис. 8.1). Однако фазы, имеющие на диаграмме состояния очень узкие области гомогенности, могут расти медленно, что их слои в диффузионной зоне не обнаруживаются.
 Двухфазные области в диффузионной зоне не образуются, так как через фазу постоянного состава диффузионный процесс невозможен из-за отсутствия градиента концентрации.
Двухфазные области в диффузионной зоне не образуются, так как через фазу постоянного состава диффузионный процесс невозможен из-за отсутствия градиента концентрации.
Двухфазный слой в диффузионной зоне может образоваться при медленном охлаждении от температуры диффузионного насыщения вследствие переменой растворимости и вторичных выделений α- и β-фазы. Кроме того, двухфазная смесь может образоваться в диффузионной зоне в результате фазовой перекристаллизации в процессе охлаждения от температуры диффузионного насыщения (рис. 8.2), в то время как при диффузионном насыщении образуется твердый раствор γ переменной концентрации.
Для однофазных областей диффузионной зоны зависимость роста толщины слоя от продолжительности насыщения при t диф =const подчиняется параболическому закону: 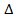 = k1
= k1 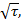 а зависимость толщины слоя от температуры при
а зависимость толщины слоя от температуры при 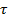 =const – экспоненциальному закону:
=const – экспоненциальному закону: 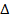 = k2е –Q/(2RT), где k1, k2 – константы; Q – энергия активации диффузионных процессов. Толщина диффузионного слоя при t диф =const и
= k2е –Q/(2RT), где k1, k2 – константы; Q – энергия активации диффузионных процессов. Толщина диффузионного слоя при t диф =const и 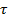 =const тем больше, чем выше концентрация диффундирующего элемента на насыщаемой поверхности.
=const тем больше, чем выше концентрация диффундирующего элемента на насыщаемой поверхности.
Существует множество способов химико-термической обработки, однако наибольшее распространение в промышленности получили процессы диффузионного насыщения из активных жидких и газовых сред. Более рациональной исходной средой является активизированная газовая среда, т.е. среда, лишенная нейтральных (балластных) примесей, где активный диффундирующий элемент образуется в результате диссоциации, диспропорционирования или восстановительных реакций, которые называются ведущими. Выявлять ведущие химические реакции можно экспериментально или расчетным путем. В последнем случае более вероятной считается реакция, имеющая более отрицательный изобарно-изотермический потенциал (энергию Гиббса) или большую константу равновесия. В ряде случаев исходную газовую среду активизируют ионизацией в тлеющем разряде.
Цементация стали
Технологический процесс диффузионного насыщения стали углеродом называется цементацией. Обычно после цементации сталь подвергают закалке и низкому отпуску. После такого комплексного процесса концентрация углерода на поверхности стальной детали составляет 0,8 – 1%, структура низко отпущенного мартенсита с мелкими сфероидальными карбидами хорошо сопротивляется износу, твердость поверхности равна 750 – 950HV. Сердцевина детали, содержащая 0,08 – 0,25%С, остается вязкой. Поверхности, не подлежащие цементации, защищают гальваническим омеднением; толщина медного слоя составляет 0,02 – 0,05 мм. Цементации обычно подвергают такие детали машин, которые должны иметь износостойкую рабочую поверхность и вязкую сердцевину: зубчатые колеса, валы и пальцы, распределительные валики, кулачки, червяки и т.д.
Карбюризаторы
Исходную среду для цементации (науглероживания) принято называть карбюризатором. В основном применяют два способа цементации: в твердом и в газовом карбюризаторе. Несмотря на различные названия, процесс цементации в твердом и газовом карбюризаторе идет через газовую фазу. Наиболее распространенный твердый карбюризатор состоит в основном из древесного угля в добавкой 20 – 25% BaCo3 для интенсификации процесса и 3 – 5% CaCo3 для предотвращения спекания частиц карбюризатора. Детали, подлежащие цементации, и карбюризатор упаковывают в контейнер (стальной ящик) и нагревают в печи до 910 - 930 ºС. При нагреве уголь взаимодействует с кислородом остаточного воздуха по реакции
2C + O2 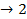 CO
CO
Кроме того, оксид углерода образуется в результате реакции
BaCo3 + С 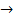 BaO + 2CO
BaO + 2CO
На поверхности деталей протекает ведущая процесс цементации реакция диспропорционирования
2CO  CO2 +C
CO2 +C
в результате которой активный углерод адсорбируется насыщаемой поверхностью, находящейся в аустенитном состоянии, а CO2 взаимодействует с углем, образуя новые порции CO.
Таким образом, в результате обратимой реакции диспропорционирования углерод переносится на насыщаемую поверхность.
При газовой цементации в качестве карбюризатора используют разбавленный природный газ (состоящий почти полностью из метана), контролируемых атмосфер, получаемых в специальных генераторах, а также жидких углеводородов (керосин, бензол и до.), каплями подаваемых в герметичное рабочее пространство печи, где они образуют активную газовую среду. Основная ведущая реакция при наличии метана
CH4  2Н2 + С
2Н2 + С
 В ряде случаев (эндотермическая контролируемая атмосфера) при наличии в газе СО возможна также реакция 2CO
В ряде случаев (эндотермическая контролируемая атмосфера) при наличии в газе СО возможна также реакция 2CO  CO2 +C. В зависимости от состава газовой смеси и содержания углерода в стали атмосфера в рабочем пространстве печи может быть науглероживающей, обезуглероживающей и нейтральной. Нейтральному составу газовой смеси соответствует определенная равновесная концентрация углерода на поверхности стальной детали. Эту концентрацию углерода принято называть углеродным потенциалом контролируемой атмосферы. Следовательно, науглероживание будет происходить в том случае, если концентрация углерода на поверхности стали будет меньше углеродного потенциала газовой смеси при данной температуре.
CO2 +C. В зависимости от состава газовой смеси и содержания углерода в стали атмосфера в рабочем пространстве печи может быть науглероживающей, обезуглероживающей и нейтральной. Нейтральному составу газовой смеси соответствует определенная равновесная концентрация углерода на поверхности стальной детали. Эту концентрацию углерода принято называть углеродным потенциалом контролируемой атмосферы. Следовательно, науглероживание будет происходить в том случае, если концентрация углерода на поверхности стали будет меньше углеродного потенциала газовой смеси при данной температуре.
Азотирование стали
Азотированием называют процесс диффузионного насыщения азотом поверхностной зоны деталей. Азотирование применяют для повышения износостойкости и предела выносливости деталей машин (коленчатые валы, гильзы цилиндров, червяки, валики, шестерни и др.).
До азотирования детали подвергают закалке, высокому отпуску (улучшению) и чистовой обработке. После азотирования детали шлифуют или полируют.
Обычное азотирование проводят при температуре 500 - 600 ºС в муфелях или контейнерах, через которые пропускается диссоциирующий аммиак.
Вероятно, что на стальной поверхности происходит реакция диссоциации аммиака с выделением ионов азота, которые адсорбируются поверхностью детали, а затем диффундируют вглубь.
При нагреве аммиака в изолированном объеме возможна лишь реакция с образованием молекулярного азота
2NH3  N2 + 3H2,
N2 + 3H2,
который не может диффундировать в сталь без ионизации.
Формирование структуры азотированной зоны в углеродистых сталях происходит примерно так же, как при азотировании железа. Поэтому, пользуясь диаграммой состояния Fe – N (рис. 8.7), можно предсказать структуру азотированной зоны низкоуглеродистых сталей. По мере насыщения железа азотом при температуре ниже 590 ºС сначала образуется α-твердый раствор внедрения азота железо, затем слой γ-фазы с ГЦК решеткой и упорядоченным расположением 
 атомов азота в центрах элементарных ячеек. Обычно процесс азотирования завершается образованием на поверхности слоя ε-фазы с ГП решеткой и упорядоченным расположением атомов в широком интервале концентраций азота.
атомов азота в центрах элементарных ячеек. Обычно процесс азотирования завершается образованием на поверхности слоя ε-фазы с ГП решеткой и упорядоченным расположением атомов в широком интервале концентраций азота.
При медленном охлаждении после азотирования вследствие переменной растворимости азота в α и ε-фазах (см. рис. 8.7) происходит выделение вторичной γII-фазы, и структура азотированной зоны от поверхности к сердцевине становится следующей: ε + γ'II  γ'
γ'  α + γ'II
α + γ'II  α.
α.
При азотировании углеродистых сталей с увеличением содержания углерода уменьшается скорость диффузии азота и возможно образование карбонитридных фаз.
Азотированная сталь, имеющая на поверхности слой ε-фазы, коррозионностойка в воде и в атмосферных условиях. В системе Fe – N ε– и γ'–фазы имеют сравнительно невысокую твердость – соответственно 450HV и 550HV. Большая твердость достигается при азотировании специально легированных сталей, которые содержат более активные нитридообразующие элементы: Cr , Mo , Al , V , Ti.
При азотировании структуры диффузионной зоны легированных и углеродистых сталей аналогичны. Однако легирование изменяет состав фаз и температурные границы их образования; при изотермической выдержке в процессе азотирования могут образовываться двухфазные слои в диффузионной зоне.
Высокие твердость и износостойкость получается после азотирования легированной стали 38Х2МЮА, содержащей: 0,35 – 0,42%С; 1,35 – 1,65%С r; 0,7 – 1,1%Al; 0,15 – 0,23%Mo. Комплексное легирование хромом, алюминием и молибденом позволяет повысить твердость азотированного слоя до 1200HV. Молибден также устраняет отпускную хрупкость, которая может возникнуть при медленном охлаждении от температуры азотирования.
Процесс азотирования – весьма длительная операция. Так, при обычном азотировании стали 38Х2МЮА диффузионную зону толщиной около 0,5 мм получают при 500 – 520ºС за 55 ч выдержки. Такую же толщину зоны можно получить за 40 ч, если применить двухступенчатый режим азотирования: 510ºС, 15 и 550ºС, 25ч.
По сравнению с цементованными азотированные слои имеют более высокие твердость и износостойкость. Однако азотирование используют реже, чем цементацию, из-за большей длительности процесса и меньшей толщины упрочненного слоя, что ограничивает контактные нагрузки на поверхность детали.
Магнитомягкие материалы
Магнитомягкие материалы намагничиваются в слабых магнитных полях (Н 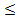 5
5  103 А/м) вследствие большой магнитной проницаемости (
103 А/м) вследствие большой магнитной проницаемости ( 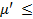 70
70  103 и
103 и 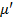 max
max 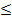 240
240 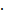 103) и малых потерь на перемагничивание.
103) и малых потерь на перемагничивание.
Такие материалы применяют для изготовления сердечников катушек, электромагнитов, трансформаторов, динамомашин.
При перемагничивании ферромагнетиков в магнитном поле возникает несколько видов энергетических потерь. Потери на гистерезис или перемагничивание для магнитомягких материалов невелики, в отличие от тепловых удельных потерь, связанных с возникновением токов Фуко.
При заданной напряженности магнитного поля Н тепловые потери растут пропорционально квадратам амплитуды магнитной индукции Bm, частоты магнитного поля f, толщины сердечника d и обратно пропорционально удельному электрическому сопротивлению 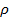 .
.
В переменных полях появляется еще один вид потерь, как результат сдвига по фазе индукции B и напряженности поля Н. в таком поле магнитная проницаемость выражается комплесным числом
 =
= 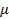 1 +
1 + 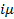 2. (9.2)
2. (9.2)
Потери энергии характеризует tg δ = 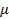 2/
2/ 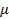 1. С ростом частоты поля
1. С ростом частоты поля 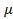 1 снижантся интенсивнее, чем растет
1 снижантся интенсивнее, чем растет 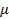 2.
2.
Тепловые потери и значение tg δ определяют допустимые рабочие частоты, поэтому магнитомягкие материалы подразделяют на низко- и высокочастотные.
Припои
Сплавы, используемые при пайке металлов высокой проводимости, - припои должны обеспечивать небольшое переходное электросопротивление (сопротивление контакта).
Различают припои двух типов: для низкотемпературной пайки, имеющие температуру плавления до 400  , и для высокотемпературной пайки с более высокой температурой плавления. Для получения хорошего соединения припой должен иметь более низкую температуру плавления, чем металл, подвергающийся пайке; в расплавленном состоянии припой должен хорошо смачивать поверхности. Температурные коэффициенты линейного расширения металла и припоя должны быть близки.
, и для высокотемпературной пайки с более высокой температурой плавления. Для получения хорошего соединения припой должен иметь более низкую температуру плавления, чем металл, подвергающийся пайке; в расплавленном состоянии припой должен хорошо смачивать поверхности. Температурные коэффициенты линейного расширения металла и припоя должны быть близки.
Для этих целей используют припои на основе олова, свинца, цинка, серебра, имеющих хорошую электрическую проводимость. Сплавы этих металлов образуют эвтектические смеси, электросопротивление которых мало отличается от металлов, образующих сплав.
В приборостроении для низкотемпературной пайки применяют оловянно-свинцовые и оловянно-цинковые (ГОСТ 21931-76) припои.
Сплавы олова и свинца образуют диаграмму состояния эвтектического типа с твердыми растворами ограниченной растворимости. Сплав эвтектического типа (61%Sn и 39%Pb) имеет низкую температуру плавления (183  ) и хорошую жидкотекучесть, что обеспечивает качественное формирование шва и высокие механические свойства. Такой сплав обозначают ПОС-61. Применяют также сплавы доэвтектического ПОС-18, ПОС-30, ПОС-40, ПОС-50 и заэвтектического составов. Цифра в марке указывает на содержание олова. Припои такого типа имеют удельное электросопротивление
) и хорошую жидкотекучесть, что обеспечивает качественное формирование шва и высокие механические свойства. Такой сплав обозначают ПОС-61. Применяют также сплавы доэвтектического ПОС-18, ПОС-30, ПОС-40, ПОС-50 и заэвтектического составов. Цифра в марке указывает на содержание олова. Припои такого типа имеют удельное электросопротивление 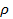 = 0,14…0,21 мкО
= 0,14…0,21 мкО 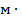 м и применяются для пайки очень тонких проводов из меди и медных сплавов, а также в тех случаях, когда недопустим высокий нагрев в зоне пайки.
м и применяются для пайки очень тонких проводов из меди и медных сплавов, а также в тех случаях, когда недопустим высокий нагрев в зоне пайки.
Сплавы олова и цинка также образуют диаграмму эвтектического типа. Наилучшим припоем является сплав ПОЦ-90, отвечающий эвтектическому составу: 90%Sn и 10%Zn. Сплав имеет самую низкую температуру плавления из всех сплавов этой системы, равную 199  . Сплавы ПОЦ-70, ПОЦ-60, ПОЦ-40, так же как и ПОЦ-90, используют для пайки алюминия и его сплавов.
. Сплавы ПОЦ-70, ПОЦ-60, ПОЦ-40, так же как и ПОЦ-90, используют для пайки алюминия и его сплавов.
В тех случаях, когда требуется очень низкая температура нагрева ( 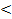 100
100  ), для пайки используют сплавы висмута со свинцом, оловом, кадмием. В процессе сплавления металлы образуют между собой легкоплавкие тройные и более сложные эвтектики, чем объясняется низкая температура плавления сплавов. Следует отметить, что такие припои не обеспечивают высокой прочности соединения. Кроме того, сплавы с висмутом хрупки.
), для пайки используют сплавы висмута со свинцом, оловом, кадмием. В процессе сплавления металлы образуют между собой легкоплавкие тройные и более сложные эвтектики, чем объясняется низкая температура плавления сплавов. Следует отметить, что такие припои не обеспечивают высокой прочности соединения. Кроме того, сплавы с висмутом хрупки.
Припои для высокотемпературной пайки обеспечивают более прочные соединения, чем для низкотемпературной, так как вследствие высокой температуры нагрева происходит взаимная диффузия элементов основного металла и припоя. Переходное электросопротивление таких припоев ниже, чем низкотемпературных припоев.
В качестве высокотемпературных припоев используют медь, медно-цинковые и медно-фосфористые припои, а также припои, содержащие серебро. Медно-цинковые припои ПМЦ-36, ПМЦ-48, ПМЦ54 (цифра указывает содержание меди) имеют удельное электросопротивление в пределах 0,03…0,04 мкО 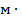 м; температура плавления их при увеличении содержания меди возрастает от 825 до 880
м; температура плавления их при увеличении содержания меди возрастает от 825 до 880  .
.
Применение медно-фосфористых припоев ПМФ7 (цифра указывает процентное содержание фосфора) позволяет вести пайку меди без флюса, что на практике удобнее и проще.
Припои, содержащие серебро, очень технологичны, так как обладают хорошей растворимостью и смачиваемостью; они пригодны для пайки любых металлов и сплавов, обеспечивают соединения с хорошими механическими свойствами и имеют невысокое переходное электросопротивление. Кроме серебра, содержание которого указывает цифра в марке, припой содержит медь или медь с цинком. В припоях ПСр-72, ПСр-61, ПСр-45, ПСр-10 удельное электросопротивление возрастает от 0,022…0,065 мкО 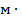 м, температура плавления соответственно изменяется от 779 до 920
м, температура плавления соответственно изменяется от 779 до 920  (см. рис. 18.6).
(см. рис. 18.6).
Сверхпроводники

 Особую группу материалов с высокой электрической проводимостью образуют сверхпроводники. С понижением температуры удельное электросопротивление всех металлов монотонно падает (рис. 11.7). однако есть металлы и сплавы, у которых при критической температуре значение
Особую группу материалов с высокой электрической проводимостью образуют сверхпроводники. С понижением температуры удельное электросопротивление всех металлов монотонно падает (рис. 11.7). однако есть металлы и сплавы, у которых при критической температуре значение 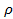 резко падает до нуля – материал становится сверхпроводником. Сверхпроводимость обнаружена у 30 элементов и у около 1000 сплавов.
резко падает до нуля – материал становится сверхпроводником. Сверхпроводимость обнаружена у 30 элементов и у около 1000 сплавов.
Сверхпроводящие свойства имеют многоие сплавы со структурой упорядоченных твердых растворов и промежуточных фаз (σ-фаза, фаза Лавеса и т.д.). при обычных температурах эти вещества не обладают высокой проводимостью. Переход металла в сверх проводящее состояние связывают с фазовым превращение. Новое фазовое состояние характеризуется тем, что свободные электроны перестают взаимодействовать с ионами кристаллической решетки, но вступают во взаимодействие между собой. В результате этого электроны с противоположно направленными спинами спариваются. Результирующий спиновый момент становится равными нулю, и сверхпроводник превращается в диамагнетик. Все электронные пары располагаются на низких энергетических уровнях, где они перестают испытывать тепловые рассеяния, так как энергия, которую пара может получить от взаимодействия с ионами решетки, слишком мала, чтобы вызвать это рассеяние.
Сверхпроводящее состояние разрушается не только в результате нагрева, но также в сильных магнитных полях и при пропускании электрического тока большой силы (критические значения поля и тока).
Из всех элементов, способных переходить в сверх проводящее состояние, ниобий имеет самую высокую критическую температуру перехода 9,17 К (-263,83  ). Практическое использование нашли сверхпроводящие сплавы с высоким содержанием ниобия: 65БТ и 35БТ (ГОСТ 10994-74). Сплав 65БТ содержит 22 – 26% Ti; 63 - 68%Nb; 8,5 – 11,5%Zr и имеет критическую температуру перехода 9,7К (–263,3
). Практическое использование нашли сверхпроводящие сплавы с высоким содержанием ниобия: 65БТ и 35БТ (ГОСТ 10994-74). Сплав 65БТ содержит 22 – 26% Ti; 63 - 68%Nb; 8,5 – 11,5%Zr и имеет критическую температуру перехода 9,7К (–263,3  ). Для T = 4,2К критические значения плотности тока и напряженность магнитного поля составляют 2,8
). Для T = 4,2К критические значения плотности тока и напряженность магнитного поля составляют 2,8 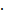 106 А/м2 и (6 – 7)
106 А/м2 и (6 – 7)  106 А/м соответственно. Проволоку из сплава 35БТ состава 60 – 64% Ti; 33,5 – 36,5% Nb; 1,7 – 4,3% Zr из-за повышенной хрупкости заливают в медную матрицу.
106 А/м соответственно. Проволоку из сплава 35БТ состава 60 – 64% Ti; 33,5 – 36,5% Nb; 1,7 – 4,3% Zr из-за повышенной хрупкости заливают в медную матрицу.
Оба сплава сверхпроводников, являющихся диамагнетиками, «выталкивать» магнитное поле, используют в магнитных насосах, позволяющих генерировать магнитные поля колоссальной напряженности, а также в криогенных гироскопах. Якорь гироскопа, изготовленный из сверхпроводника, «плавает» в магнитном поле. Отсутствие опор и подшипников устраняет трение и повышает долговечность гироскопа.
Контактные материалы
Электрические контакты подразделяют на разрывные, скользящие и неподвижные. Основное требование для всех контактов – малое переходное электросопротивление.
Разрывные контакты. Эти контакты предназначены для периодического замыкания и размыкания цепи и работают в наиболее трудных условиях. В процессе работы разрывных контактов возникает искра или электрическая дуга, что вызывает коррозию и электроэрозионный износ.
В результате происходит окисление контакта. Это повышает переходное электросопротивление, вызывает разогрев и сваривание (или прилипание) контакта. Электроэрозионное изнашивание приводит к появлению на контактных поверхностях кратера на одном контакте и иглы – на другом. Это объясняется тем, что металл контакта плавится, испаряется, распыляется на рабочей поверхности и переносится с одного контакта на другой. Сопротивление электроэрозионному изнашиванию в металлах растет с повышением температуры плавления, в сплавах оно дополнительно повышается с ростом твердости и прочности. Из сказанного следует, что материал для разрывных контактов должен иметь не только небольшое переходное электросопротивление, но и хорошее сопротивление химической коррозии и электроэрозионному изнашиванию.
В зависимости от электрической мощности разрывные контакты подразделяют на слабонагруженные и высоконагруженные.
Слабонагруженные контакты изготовляют из благородных металлов: золота, серебра, платины, палладия и их сплавов, которые обладают низким переходным сопротивлением и повышенной стойкостью против окисления. Высоким сопротивлением электроэрозионному изнашиванию эти металлы и сплавы не обладают, поэтому их можно использовать только в слабонагруженных контактах.
Обычно материалами для таких контактов служат серебро и сплавы на его основе. Основным преимуществом серебра является его высокая электрическая проводимость. Однако при воздействии электрической дуги оно окисляется и подвергается электроэрозионному изнашиванию. Окисление не приводит к значительному росту переходного электрического сопротивления, так как оксид серебра электропроводен и при нагреве восстанавливается. Чистое серебро применяют в слабонагруженных контактах при небольшой частоте переключений. Серебро технологично при производстве проката и наиболее дешево из всех благородных металлов.
Широко используют также сплавы серебра с медью (см. рис. 11.6). такие сплавы сохраняют высокую электрическую проводимость и имеют более высокие твердость и сопротивление электрическому изнашиванию, чем чистое серебро. Однако медь ухудшает стойкость сплавов против окисления, поэтому их используют только в слабонагруженных контактах.
Высоконагруженные контакты изготовляют из вольфрама, молибдена, их сплавов и порошковых композиций.
 Вольфрам благодаря своей тугоплавкости хорошо сопротивляется электроэрозионному изнашиванию. Несмотря на окисление, вольфрам имеет невысокое и устойчивое переходное электросопротивление, так как он достаточно электропроводен, а оксидная пленка вольфрама при работе контакта разрушается. Кроме того, такие контакты н свариваются при эксплуатации, поэтому их применяют при частых переключениях.
Вольфрам благодаря своей тугоплавкости хорошо сопротивляется электроэрозионному изнашиванию. Несмотря на окисление, вольфрам имеет невысокое и устойчивое переходное электросопротивление, так как он достаточно электропроводен, а оксидная пленка вольфрама при работе контакта разрушается. Кроме того, такие контакты н свариваются при эксплуатации, поэтому их применяют при частых переключениях.
Такое же назначение имеют сплавы с молибденом (рис. 11.8). содержащие 40 – 50% Mo, эти сплавы обладают высоким сопротивлением электроэрозионному изнашиванию, но вследствие образования непрерывного ряда твердых растворов их переходное и общее электросопротивление велики. Сплавы обладают пониженным сопротивлением газовой коррозии, так как молибден и его сплавы образуют легко испаряющиеся оксидные пленки. Такие сплавы можно использовать для мощных контактов, но в среде инертных газов или в вакууме. Сплавы вольфрама с 45% используют также для нитей накаливания электрических ламп и катодов.
В наиболее мощных контактах используют спеченные композиции вольфрама с серебром или медью, либо спекают пористый вольфрам, который затем в вакууме пропитывают жидкой медью или серебром.
 Разработан способ обработки серебряно-медных контактов – метод внутреннего окисления. Сплав СОМ-10, содержащий 10% Cu, подвергают длительному (50 ч) окислению при 700
Разработан способ обработки серебряно-медных контактов – метод внутреннего окисления. Сплав СОМ-10, содержащий 10% Cu, подвергают длительному (50 ч) окислению при 700  на воздухе. Благодаря большой растворимости и скорости диффузии кислорода в серебре (в α–фазе) он проникает в металл и окисляет менее благородную медь (
на воздухе. Благодаря большой растворимости и скорости диффузии кислорода в серебре (в α–фазе) он проникает в металл и окисляет менее благородную медь ( 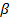 -фазу). В результате такой обработки получается композиционный материал: серебряной матрице равномерно распределены оксиды меди. Наличие оксидов меди повышает сопротивление свариванию и стойкость против электроэрозионного изнашивания. Такие сплавы применяют в тяжелонагруженных контактах. Кроме того, такие материалы можно использовать в скользящих контактах, так как у них высокое сопротивление свариванию.
-фазу). В результате такой обработки получается композиционный материал: серебряной матрице равномерно распределены оксиды меди. Наличие оксидов меди повышает сопротивление свариванию и стойкость против электроэрозионного изнашивания. Такие сплавы применяют в тяжелонагруженных контактах. Кроме того, такие материалы можно использовать в скользящих контактах, так как у них высокое сопротивление свариванию.
Скользящие контакты. К материалам для скользящих контактов предъявляют те же требования, что и для разрывных, но основное требование к ним – высокое сопротивление свариванию. Кроме окисленного серебряно-медного сплава для скользящих контактов применяют композиции из порошков меди или серебра с небольшой добавкой графита, препятствующего свариванию (МГ3, МГ5, СГ3, СГ5). Цифра в марках указывает на содержание графита в процентах.
Неподвижные контакты. Эти контакты должны иметь низкое значение переходного электросопротивления, которое, кроме того, должно быть стабильным при небольших контактных усилиях. Поэтому для зажимных контактов выбирают коррозионностойкий материал, не образующий оксидных пленок с высоким электросопротивлением на контактной поверхности. Всем этим требованиям удовлетворяют медь, латунь, цинк.
Полупроводниковые материалы
Диэлектрики
Диэлектриками называют вещества, у которых валентная зона отделена от зоны проводимости широкой зоной запрещенных энергий. Важнейшими твердыми диэлектриками являются керамика, полимеры и стекло. В них преобладает ионный или ковалентный тип связи, нет свободных носителей зарядов. Их удельное электросопротивление равно 108 – 1016 Ом 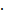 м.
м.
Электрические свойства диэлектрика определяют область его применения; при этом принимаются во внимание механические свойства материала, его химическая стойкость и другие параметры.
Характерной особенностью диэлектрика является способность поляризоваться в электрическом поле. Сущность поляризации заключается в смещении связанных электрических зарядов под действием поля. Смещенные заряды создают собственное внутреннее электрическое поле, которое направлено противоположно внешнему полю. Мерой поляризации является диэлектрическая проницаемость 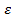 . Она оценивается отношением емкостей Сд/С0 конденсатора. Емкость Сд определяется, когда между пластинами конденсатора находится диэлектрик, а емкость С0 – когда вместо диэлектрика – вакуум. В твердом диэлектрике одновременно проявляется несколько видов поляризации которые в сумме определяют значение
. Она оценивается отношением емкостей Сд/С0 конденсатора. Емкость Сд определяется, когда между пластинами конденсатора находится диэлектрик, а емкость С0 – когда вместо диэлектрика – вакуум. В твердом диэлектрике одновременно проявляется несколько видов поляризации которые в сумме определяют значение 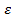 и его зависимость от температуры и частоты поля. Конструкционные диэлектрики общего назначения имеют небольшое значение
и его зависимость от температуры и частоты поля. Конструкционные диэлектрики общего назначения имеют небольшое значение 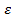 (не более 10 – 12). Диэлектрики, которые используют в конденсаторах, должны иметь высокие значения
(не более 10 – 12). Диэлектрики, которые используют в конденсаторах, должны иметь высокие значения 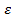 , чтобы увеличить емкость конденсатора. у конденсаторных диэлектриков
, чтобы увеличить емкость конденсатора. у конденсаторных диэлектриков 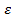 изменяется от 12 – 15 до 100000.
изменяется от 12 – 15 до 100000.
Наиболее важными видами поляризации являются электронная, ионная, дипольно-релаксационная (рис. 11.22) и самопроизвольная (спонтанная).
Электронная поляризация (рис. 11.12, а) вызывается деформацией электронных оболочек атомов. Электроны смещаются почти мгновенно, время установки поляризации ничтожно мало (10-15 с), и поэтому она не зависит от частоты.
Ионная поляризация (рис. 11.12. б) возникает при упругом смещении ионов на расстояния, не превышающие межионные. Отрицательные ионы смещаются в сторону положительного электрода, а положительные ионы – в сторону отрицательного. Время установления ионной поляриации также мало (10-15 с), и 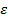 также не зависит от частоты.
также не зависит от частоты.

 Дипольно-релаксационная поляризация (рис. 11.22. в) проявляется в полярных диэлектриках. Повороты диполей существенно меняют
Дипольно-релаксационная поляризация (рис. 11.22. в) проявляется в полярных диэлектриках. Повороты диполей существенно меняют 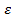 . У неполярных диэлектриков
. У неполярных диэлектриков  немного больше 2, у полярных – в несколько раз больше. Повороты диполей при наложении поля и возвращение их к неупорядоченному состоянию после его снятия требуют преодоления некоторого сопротивления молекулярных сил. Эта поляризация появляется и исчезает значительно медленнее электронной и ионной поляризации.
немного больше 2, у полярных – в несколько раз больше. Повороты диполей при наложении поля и возвращение их к неупорядоченному состоянию после его снятия требуют преодоления некоторого сопротивления молекулярных сил. Эта поляризация появляется и исчезает значительно медленнее электронной и ионной поляризации.
При нагреве диэлектрическая проницаемость 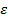 изменяется, температурный коэффициент αε принимает значения от –1300 до 3000 10-6
изменяется, температурный коэффициент αε принимает значения от –1300 до 3000 10-6  -1. Отрицательный αε имеют диэлектрики с электронной поляризацией, при нагреве увеличивается их объем и соответственно уменьшается плотность зарядов. Диэлектрики с ионной поляризацией имеют положительный αε. При нагреве поляризация возрастает вплоть до верхней границы рабочего интервала температур. Это объясняется ослаблением притяжения между ионами и увеличением их смещения.
-1. Отрицательный αε имеют диэлектрики с электронной поляризацией, при нагреве увеличивается их объем и соответственно уменьшается плотность зарядов. Диэлектрики с ионной поляризацией имеют положительный αε. При нагреве поляризация возрастает вплоть до верхней границы рабочего интервала температур. Это объясняется ослаблением притяжения между ионами и увеличением их смещения.
Особенно сильно повышается поляризация, когда ионы начинают смещаться на расстояния больше межионных. В этом случае поляризация зависит от частоты, устанавливается медленно (за 10-5 – 10-3с) и называется ионно-релаксационной.
Изменения дипольно-релаксационной поляризации при нагреве определяются соотношением межмолекулярного притяжения и теплового движения. Ослабление притяжения облегчает ориентацию диполей, а усиление теплового движения ей мешает. В связи с этим поляризация сначала увеличивается до некоторого максимума, а затем уменьшается.
Самопроизвольная поляризация наблюдается только у одного класса диэлектриков – сегнетоэлектриков. При охлаждении сегнетоэлектрика ниже определенной температуры, которую называют точкой Кюри, самопроизвольно, без внешних воздействий, возникает поляризация. Объем сегнетоэлектрика разбивается на домены, в каждом из которых вещество сильно поляризовано. В отсутствие поля домены расположены беспорядочно, и суммарная поляризация Р равна нулю. При наложении поля поляризация увеличивается нелинейно благодаря переориентации доменов. При циклическом изменении поля от +Е до –Е возникает петля гистерезиса (рис.11.23). Когда напряженность поля возрастает, поляризация Р достигает насыщения; при этом 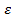 увеличивается до максимального значения и вновь уменьшается. По аналогии с ферромагнетиками напряженность поля Ес, при которой меняется направление поляризации, называется коэрцитивной силой. Когда Ес
увеличивается до максимального значения и вновь уменьшается. По аналогии с ферромагнетиками напряженность поля Ес, при которой меняется направление поляризации, называется коэрцитивной силой. Когда Ес 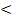 0,1 МВ/м, сегнетоэлектрик является мягким; когда Ес
0,1 МВ/м, сегнетоэлектрик является мягким; когда Ес 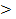 1МВ/м – жестким. Известно около 500 сегнетоэлектриков. Они принадлежат к классу активных диэлектриков, которые используются для генерации и преобразования электрических сигналов. Между
1МВ/м – жестким. Известно около 500 сегнетоэлектриков. Они принадлежат к классу активных диэлектриков, которые используются для генерации и преобразования электрических сигналов. Между  электрическими, механическими, тепловыми и другими свойствами сегнетоэлектриков существуют нелинейные зависимости. Значения свойств вблизи точки Кюри имеют максимумы и минимумы. В частности, максимальное значение
электрическими, механическими, тепловыми и другими свойствами сегнетоэлектриков существуют нелинейные зависимости. Значения свойств вблизи точки Кюри имеют максимумы и минимумы. В частности, максимальное значение 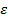 достигается около точки Кюри.
достигается около точки Кюри.
 Электрическая проводимость твердых диэлектриков связана с появлением в них свободных ионов или электронов. Основное значение имеет ионная проводимость, обусловленная примесями.
Электрическая проводимость твердых диэлектриков связана с появлением в них свободных ионов или электронов. Основное значение имеет ионная проводимость, обусловленная примесями.
Электрическую проводимость диэлектрика подразделяют на объемную (сквозную) и поверхностную. Каждая из них характеризуется своим удельным электросопротивлением: объемным 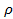 v (Ом м) и поверхностным
v (Ом м) и поверхностным 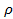 s (Ом).
s (Ом).
Диэлектрики имеют высокое удельное объемное электросопротивление  v
v 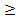 108 Ом м). при нагреве оно понижается в результате роста подвижности ионов.
108 Ом м). при нагреве оно понижается в результате роста подвижности ионов.
Поверхностное электросопротивление 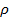 s зависит как от состава и структуры диэлектрика, так и от состояния его поверхности и влажности среды. Загрязнения и влага на шероховатой или пористой поверхности образуют проводящую пленку, диэлектрик может полностью утратить изоляционные свойства, хотя его объемное электрическое сопротивление при этом останется высоким. Для повышения поверхностного электрического сопротивления поверхность изделий стремятся сохранить чистой и гладкой, используя для этого покрытия – лаки, эмали, глазури.
s зависит как от состава и структуры диэлектрика, так и от состояния его поверхности и влажности среды. Загрязнения и влага на шероховатой или пористой поверхности образуют проводящую пленку, диэлектрик может полностью утратить изоляционные свойства, хотя его объемное электрическое сопротивление при этом останется высоким. Для повышения поверхностного электрического сопротивления поверхность изделий стремятся сохранить чистой и гладкой, используя для этого покрытия – лаки, эмали, глазури.

 Диэлектрические потери представляют собой часть энергии электрического поля, которая превращается в диэлектрике в теплоту и нагревает его. При частотах свыше 20 кГц их величина становится одним из самых важных параметров диэлектрика. Для определения потерь диэлектрик удобно рассматривать как конденсатор в цепи переменного тока (рис 18.24). у идеального конденсатора угол сдвига фаз между током I и напряжением U равен 90
Диэлектрические потери представляют собой часть энергии электрического поля, которая превращается в диэлектрике в теплоту и нагревает его. При частотах свыше 20 кГц их величина становится одним из самых важных параметров диэлектрика. Для определения потерь диэлектрик удобно рассматривать как конденсатор в цепи переменного тока (рис 18.24). у идеального конденсатора угол сдвига фаз между током I и напряжением U равен 90 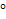 , поэтому активная мощность N а = IU cos
, поэтому активная мощность N а = IU cos 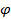 равна нулю. Диэлектрик не является идеальным конденсатором, и угол сдвига фаз у него меньше 90
равна нулю. Диэлектрик не является идеальным конденсатором, и угол сдвига фаз у него меньше 90 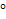 на угол
на угол 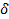 , называемый углом диэлектрических потерь. Тангенс угла
, называемый углом диэлектрических потерь. Тангенс угла 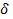 и диэлектрическая постоянная
и диэлектрическая постоянная  характеризуют удельные потери (на единицу объема диэлектрика), Вт/м3:
характеризуют удельные потери (на единицу объема диэлектрика), Вт/м3:
p = k E 2 f  tg
tg 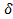 ,
,
где k – коэффициент; Е – напряженность электрического поля, Вт/м; f – частота поля, Гц.
Произведение 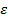 tg
tg  называют коэффициентом диэлектрических потерь. В зависимости от значения tg
называют коэффициентом диэлектрических потерь. В зависимости от значения tg  диэлектрики подразделяют на низкочастотные (tg
диэлектрики подразделяют на низкочастотные (tg  = 0,1 … 0,001) и высокочастотные (tg
= 0,1 … 0,001) и высокочастотные (tg 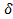
 0,001). К основным источникам потерь диэлектрика относятся его поляризация и электрическая проводимость, ионизация газов в имеющихся порах и неоднородность структуры из-за примесей и включений.
0,001). К основным источникам потерь диэлектрика относятся его поляризация и электрическая проводимость, ионизация газов в имеющихся порах и неоднородность структуры из-за примесей и включений.
Электрическая прочность характеризуется сопротивлением пробою. Пробой – это необратимое разрушение твердого диэлектрика под действием поля и потеря изолирующих свойств. Электрической прочностью или пробивной напряженностью Епр называется отношение пробивного напряжения U пр к толщине диэлектрика в месте пробоя. Различают три вида пробоя: электрический, тепловой и электрохимический.
Электрический пробой возникает вследствие ударной ионизации нарастающей лавиной электронов. Пробой наступает почти мгновенно (за 10-7 – 10-8 с) под действием поля большой напряженности (свыше 1000 МВ/м) независимо от нагрева диэлектрика. Обычно диэлектрик пробивается при включении напряжения или при его резком скачке.
Тепловой пробой наступает при комбинированном воздействии поля и нагрева, причем пробивная напряженность Епр из-за повышения температуры диэлектрика снижается. Чем лучше отвод теплоты в окружающую среду, тем ниже температура диэлектрика и выше Епр. Тепловой пробой ускоряется при повышении частоты (так кк при этом возрастают потери) и замедлении теплоотвода.
Электрохимический пробой наступает при длительном действии поля, сопровождающемся необратимыми изменениями в структуре диэлектрика и понижением его электрической прочности.
По химическому составу диэлектрики подразделяют на органические и неорганические. К первым относятся полимеры, резина, шелк; ко вторым – слюда, керамика, стекло, ситаллы.
По электрическим свойствам диэлектрики подразделяют на низкочастотные (электротехнические) и высокочастотные (радиотехнические). Для электроизоляционных материалов решающее значение имеет их стойкость к нагреву, т.е. способность без ущерба для свойств выдерживать нагрев в течение длительного времени. По этой стойкости диэлектрики разделяют на классы (ГОСТ 8865-93): Y, A, E, B, F, H и др. В классе Y объединены наименее стойкие целлюлозные, шелковые и полимерные материалы, для них рабочая температура не превышает 90  . Самыми стойкими к нагреву являются слюда, керамика, ситаллы, а также полиимиды и фторопласт-4. Они выдерживают длительный нагрев 180
. Самыми стойкими к нагреву являются слюда, керамика, ситаллы, а также полиимиды и фторопласт-4. Они выдерживают длительный нагрев 180  и выше. Большое влияние на свойства диэлектриков оказывают гигроскопичность и влагопроницаемость. Образование токопроводящих пленок на поверхности и в толще изделий понижает изолирующую способность и может закончиться пробоем. Наиболее гигроскопичны материалы с порами и капиллярами на поверхности – бумага, обычная пористая керамика, слоистые пластики. Проницаемость для водяных паров исключительно важна для пропиточных, заливочных и других защитных материалов. Диаметр молекулы воды равен всего 2,5 10-10 м, и водяной пар проходит сквозь мельчайшие поры. Плотные, непористые материалы не пропускают водяные пары и негигроскопичны. К ним относятся ситаллы, малощелочное стекло, вакуумно-плотная керамика, эпоксидные пластмассы и неполярные полимеры. Для изделий из гигроскопичных диэлектриков используют пропитку, их поверхности защищают лаками, глазурью и т.п.Прочность диэлектриков и особенности их механических свойств являются дополнительным критерием выбора материалов. Керамика, стекло и ситаллы – наиболее прочные диэлектрики. Характерной особенностью этих материалов является хрупкость; их прочность на сжатие в несколько раз больше прочности на изгиб. Предел прочности на изгиб равен 30 – 300 МПА, а у ряда ситаллов возрастает до 500 МПа. Для хрупких диэлектриков исключительно важно учитывать тепловое расширение, особенно когда речь идет о работе в условиях быстрых смен температуры или о соединении диэлектриков с металлами. Температурный коэффициент линейного расширения керамики и тугоплавкого стекла не превышает 8 10-6 К-1, а у ситаллов в зависимости от химического состава – (-4 …31,5) 10-6 К-1. Особенно велико тепловое расширение органических диэлектриков ( α t = (60 …100) 10-6 К-1), но у пластмасс с неорганическими наполнителями оно примерно такое же, как у металлических сплавов. Кроме того, органические диэлектрики достаточно пластичны, для них термические напряжения не столь опасны.
и выше. Большое влияние на свойства диэлектриков оказывают гигроскопичность и влагопроницаемость. Образование токопроводящих пленок на поверхности и в толще изделий понижает изолирующую способность и может закончиться пробоем. Наиболее гигроскопичны материалы с порами и капиллярами на поверхности – бумага, обычная пористая керамика, слоистые пластики. Проницаемость для водяных паров исключительно важна для пропиточных, заливочных и других защитных материалов. Диаметр молекулы воды равен всего 2,5 10-10 м, и водяной пар проходит сквозь мельчайшие поры. Плотные, непористые материалы не пропускают водяные пары и негигроскопичны. К ним относятся ситаллы, малощелочное стекло, вакуумно-плотная керамика, эпоксидные пластмассы и неполярные полимеры. Для изделий из гигроскопичных диэлектриков используют пропитку, их поверхности защищают лаками, глазурью и т.п.Прочность диэлектриков и особенности их механических свойств являются дополнительным критерием выбора материалов. Керамика, стекло и ситаллы – наиболее прочные диэлектрики. Характерной особенностью этих материалов является хрупкость; их прочность на сжатие в несколько раз больше прочности на изгиб. Предел прочности на изгиб равен 30 – 300 МПА, а у ряда ситаллов возрастает до 500 МПа. Для хрупких диэлектриков исключительно важно учитывать тепловое расширение, особенно когда речь идет о работе в условиях быстрых смен температуры или о соединении диэлектриков с металлами. Температурный коэффициент линейного расширения керамики и тугоплавкого стекла не превышает 8 10-6 К-1, а у ситаллов в зависимости от химического состава – (-4 …31,5) 10-6 К-1. Особенно велико тепловое расширение органических диэлектриков ( α t = (60 …100) 10-6 К-1), но у пластмасс с неорганическими наполнителями оно примерно такое же, как у металлических сплавов. Кроме того, органические диэлектрики достаточно пластичны, для них термические напряжения не столь опасны.
Стабильность структуры и свойств диэлектриков определяет сроки их эксплуатации. Наибольшую стабильность имеет керамика и ситаллы, в стеклах под влиянием поля мигрируют ионы щелочных металлов и образуются электропроводящие мостики. Добавки PbO и BaO увеличивают стойкость стекла против электрохимического пробоя, связанного с миграцией ионов щелочных металлов. Органические диэлектрики разрушаются при комбинированном действии нагрева, окисления на воздухе и ионизации, поэтому их срок службы меньше, чем у керамики или стекла. Большинство пластмасс под действием разрядов обугливается и теряет изолирующую способность. Этого недостатка лишены полистирол, органическое стекло, фторопласты и кремнийорганические пластики. Среди диэлектриков самыми важными являются керамические материалы и особенно сегнетокерамика. Керамика имеет наиболее разнообразные электрические свойства (табл. 18.6), она почти не подвержена старению и устойчива к нагреву.
Установочная керамика применяется для изготовления изоляторов, колодок, плат, каркасов, катушек и т.п. Она должна иметь низкие потери, хорошие электроизоляционные свойства и прочность.
 |
|
Для работы на низких частотах используют электрофарфор, который дешев и имеет неплохие электрические свойства. Его недостатки – большие потери, резко возрастающие при нагреве выше 200  , и низкая механическая прочность. Объясняются они свойствами стекла, которго в электрофарфоре содержится довольно много.
, и низкая механическая прочность. Объясняются они свойствами стекла, которго в электрофарфоре содержится довольно много.
Основным материалом, используемым для изготовления деталей, предназначенных для работы на высоких частотах, является стеатит, который получают из талька. Стеатиты не содержат вредных примесей, их свойства стабильны до 100  . Они легко прессуются (при обжиге дают усадку всего 1 – 2%) и используются для деталей с плотной и пористой структурой и точными размерами. В отличие от других видов керамики стеатит удовлетворительно режется (после предварительного обжига). Недостатки стеатита – растрескивание при быстрых сменах температуры и трудность обжига.
. Они легко прессуются (при обжиге дают усадку всего 1 – 2%) и используются для деталей с плотной и пористой структурой и точными размерами. В отличие от других видов керамики стеатит удовлетворительно режется (после предварительного обжига). Недостатки стеатита – растрескивание при быстрых сменах температуры и трудность обжига.
Кондесаторная керамика, применяется при высоких частотах, не должна иметь очень большие значения 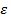 во избежание потерь. Для высокочастотных конденсаторов применяют ультрафарфор, стеатит, станнатную керамику, но лучшие свойства имеет керамика на основе TiO 2. Эту керамику подразделяют на две группы: тиконды – Т-60, Т-80, Т-150 и термоконды – Т-20, Т-40 (цифра указывает значение
во избежание потерь. Для высокочастотных конденсаторов применяют ультрафарфор, стеатит, станнатную керамику, но лучшие свойства имеет керамика на основе TiO 2. Эту керамику подразделяют на две группы: тиконды – Т-60, Т-80, Т-150 и термоконды – Т-20, Т-40 (цифра указывает значение 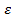 ). В тикондах основным видом кристаллов является рутил – наиболее плотная модификация TiO 2. Чембольше содержание TiO 2 в керамике, тем выше значения
). В тикондах основным видом кристаллов является рутил – наиболее плотная модификация TiO 2. Чембольше содержание TiO 2 в керамике, тем выше значения 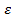 и α
и α 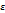 . Основная область применения тикондов термокомпенсирующие конденсаторы. Термоконды наряду с TiO 2 содержат ZrO 2 и другие добавки. Они имеют низкие значения α
. Основная область применения тикондов термокомпенсирующие конденсаторы. Термоконды наряду с TiO 2 содержат ZrO 2 и другие добавки. Они имеют низкие значения α 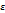 и используются для конденсаторов с высокой стабильностью.
и используются для конденсаторов с высокой стабильностью.
 Лучшая конденсаторная керамика, применяемая при низких частотах, – сегнетокерамика, так как у нее велики значения
Лучшая конденсаторная керамика, применяемая при низких частотах, – сегнетокерамика, так как у нее велики значения 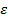 . Недостатками сегнетокерамики являются сравнительно большие потери и невысокая электрическая прочность. Сегнетокерамику подразделяют на материалы с небольшой и большой линейностью. У материалов первой группы
. Недостатками сегнетокерамики являются сравнительно большие потери и невысокая электрическая прочность. Сегнетокерамику подразделяют на материалы с небольшой и большой линейностью. У материалов первой группы 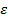 во всем интервале рабочих температур и напряженностей поля изменяется не более чем на 30% (рис. 11.25). различные марки керамики этой группы отличаются значением
во всем интервале рабочих температур и напряженностей поля изменяется не более чем на 30% (рис. 11.25). различные марки керамики этой группы отличаются значением 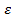 (изменяется от 1000 до 7500) и положением температурного максимума
(изменяется от 1000 до 7500) и положением температурного максимума 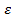 . У материалов второй группы зависимость
. У материалов второй группы зависимость 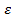 от
от
 Напряженности поля характеризуется коэффициентом нелинейности К, равному отношению
Напряженности поля характеризуется коэффициентом нелинейности К, равному отношению 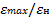 в слабом поле (2 – 5 В/м).
в слабом поле (2 – 5 В/м).
Материалы с большой нелинейностью используют в варикондах – конденсаторах переменной емкости. При одновременном действии постоянного и переменного полей 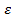 ситановится изменчивой (ее называют реверсивной
ситановится изменчивой (ее называют реверсивной 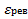 ), а ее значение определяется соотношением напряженностей полей. Выбором постоянного и переменного напряжений, приложенных к конденсатору, изменяют его емкость в несколько раз (в пределах, определяемых коэффициентом нелинейности). Вариконды используют в усилителях, делителях, умножителях частоты и других устройствах.
), а ее значение определяется соотношением напряженностей полей. Выбором постоянного и переменного напряжений, приложенных к конденсатору, изменяют его емкость в несколько раз (в пределах, определяемых коэффициентом нелинейности). Вариконды используют в усилителях, делителях, умножителях частоты и других устройствах.
Пьезоэлектрики – вещества, у которых под действием механических напряжений возникает поляризация (прямой пьезоэффект) или под действием электрического поля изменяются размеры (обратный пьезоэффект). К пьезоэлектрикам относятся поляризованные сегнетоэлектрики с остаточной поляризацией, а также кристаллы не имеющие центра симметрии. В основе пьезоэффекта лежит смещение ионов в кристаллической решетке при упругой деформации. Пьезоэффект анизотропен и характеризуется пьезомодулем – зарядом, который появляется на поверхности пластин пьезоэлектрика под действием единичной силы. Обычно измеряют так называемый продольный пьезомодуль dзз по заряду на поверхности, перпендикулярной направлению поляризации, когда нагрузка приложена перпендикулярно этой же поверхности. От пьезоэлектриков требуются высокие значения пьезомодуля и малые потери. Пьезомодули dзз у сегнетокерамики и пленки поливинидиленфторида [–CH2–CF2–]n равны соответственно 2…4 10-10 и 3,5 10-11 Кл/Н, что на один-два порядка больше пьезомодудей кварца.
В полимерных пленках свойства пьезоэлектрика появляются после создания в материале системы «сидячих» зарядов благодаря ориентации диполей или обработке поверхности высокоэнергетическим потоком электронов. Для практического применения таких материалов требуется стабильность исходных характеристик, чтобы время полураспада было бы не меньше нескольких лет. Утечка зарядов из-за малой, но не равной нулю объемной проводимости или медленная релаксация ориентированных диполей уменьшают исходные значения пьезомодулей.
Применение полимерных пленок со свойствами пьезоэлектриков обходится дешевле и имеет технологические преимущества при изготовлении датчиков с большой рабочей поверхностью. Высокая чувствительность пленок к сжатию стала основой для их применения в датчиках давления, акселерометрах, а также в датчиках, работающих в жидких средах (гидроакустическая аппаратура, медицинские приборы).
Углеродистые стали
На долю углеродистых сталей приходится 80% от общего объема. Это объясняется тем, что углеродистые стали дешевы и сочетают удовлетворительные механические свойства с хорошей обрабатываемостью резанием и давлением. При одинаковом содержании углерода по обрабатываемости резанием и давлением они значительно превосходят легированные стали. Однако углеродистые стали менее технологичны при термической обработке. Из-за высокой критической скорости закалки углеродистые стали охлаждают в воде, что вызывает значительные деформации и коробление деталей. Кроме того, для получения одинаковой прочности с легированными сталями их следует подвергать отпуску при более низкой температуре, поэтому они сохраняют более высокие закалочные напряжения, снижающие конструкционную прочность.
Главный недостаток углеродистых сталей – небольшая прокаливаемость (до 12 мм), что существенно ограничивает размер деталей, упрочняемых термической обработкой. Крупные детали изготавливают из сталей без термического упрочнения – в горячекатаном или нормализованном состояниях, что требует увеличения металлоемкости конструкций.
По статической прочности углеродистые стали относятся преимущественно к сталям нормальной прочности. Углеродистые конструкционные стали выпускают двух видов: обыкновенного качества и качественные.
Легированные стали
Легированные стали производят и поставляют качественными, высококачественными и особовысококачественными. Эта группа сталей многочисленна по числу марок.
Маркировка легированных сталей
Марка легированных сталей состоит из сочетания букв и цифр, обозначающих ее химический состав. По ГОСТ 4543-71 принято обозначать хром – Х, никель – Н, марганец – Г, кремний – С, молибден – М, вольфрам – В, титан – Т, ванадий – Ф, алюминий – Ю, медь – Д, ниобий – Б, бор – Р, кобальт – К. число, стоящее после буквы, указывает на примерное содержание легирующего элемента меньше или около 1%.
Число в начале марки конструкционной легированной стали показывает содержание углерода в сотых долях процента. Например, сталь 20ХН3А в среднем содержит 0,20%C, 1%Cr и 3%Ni. Буква А в конце марки означает, что сталь высококачественная. Особовысококачественные стали (например, после электрошлакового переплава) имеют в конце марки букву Ш, например 30ХГС-Ш.
Некоторые группы сталей содержат дополнительные обозначения: марки подшипниковых сталей начинаются с буквы Ш, автоматных – с буквы А.
Нестандартные легированные стали, выплавляемые заводом «Электросталь», маркируют сочетанием букв ЭИ (электросталь исследовательская) или ЭП (П – пробная) и порядковым номером (например, ЭИ415, ЭП716 и т.д.). После промышленного освоения условное обозначение заменяют на марку, отражающую примерный состав стали.
Медь и ее сплавы
Стекло
Износостойкие материалы
Антифрикционные материалы
Фрикционные материалы
Алюминий и его сплавы.
Алюминий – металл серебристо-белого цвета. Он не имеет полиморфных превращений и кристаллизуется в решетке ГЦК с периодом, а = 0,4041 нм.
Алюминий обладает малой плотностью, хорошими теплопроводностью и электропроводностью, высокой пластичностью и коррозионной стойкостью. Примеси ухудшают все эти свойства алюминия.
Постоянные примеси алюминия – Fe , Si , Cu , Zn , Ti. В зависимости от содержания примесей первичный алюминий подразделяют на три класса: особой чистоты А999 ( 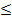 0,001% примесей) высокой чистоты А995, А99, А97, А95 (0,005 – 0,05% примесей) и технической чистоты А85, А8 и др. (0,15 – 1% примесей). Технический алюминий, выпускаемый в виде деформируемого полуфабриката (листы, профили, прутки и др.), маркируют АД0 и АД1. Механические свойства алюминия зависят от его чистоты и состояния. Увеличение содержания примесей и пластическая деформация повышают прочность и твердость алюминия (табл. 13.2).
0,001% примесей) высокой чистоты А995, А99, А97, А95 (0,005 – 0,05% примесей) и технической чистоты А85, А8 и др. (0,15 – 1% примесей). Технический алюминий, выпускаемый в виде деформируемого полуфабриката (листы, профили, прутки и др.), маркируют АД0 и АД1. Механические свойства алюминия зависят от его чистоты и состояния. Увеличение содержания примесей и пластическая деформация повышают прочность и твердость алюминия (табл. 13.2).
Ввиду низкой прочности алюминий применяют для ненагруженных деталей и элементов конструкций, когда от материала требуется легкость, свариваемость и пластичность. Так, из него изготовляют рамы, двери, трубопроводы, фольгу, цистерны для перевозки нефти и нефтепродуктов, посуду и др. благодаря высокой теплопроводности его используют для различных теплообменников, в промышленных и бытовых холодильниках. Высокая электрическая проводимость алюминия способствует его широкому применению для конденсаторов, проводов, кабелей, шин и т.п.
Следует также отметить высокую отражательную способность алюминия, в связи с чес его используют в прожекторах, рефлекторах, экранах телевизоров. Алюминий имеет малое эффективное поперечное сечение захвата нейтронов, он хорошо обрабатывается давлением, сваривается газовой и контактной сваркой, но плохо обрабатывается резанием. Алюминий имеет большую усадку при затвердевании (6%). Высокие теплота плавления и теплоемкость способствуют медленному остыванию алюминия из жидкого состояния, что дает возможность улучшать отливки из алюминия и его сплавов путем модифицирования, рафинирования и других технологических операций.
Литейные алюминиевые сплавы
Химический состав и механические свойства некоторых промышленных литейных сплавов приведены в табл. 13.4. для литейных алюминиевых сплавов наиболее распространена классификация по химическому составу (Al – Si , Al – Cu и Al – Mg).
Лучшими литейными свойствами обладают сплавы Al – Si (силумины). Высокая жидкотекучесть, малая усадка, отсутствие или низкая склонность к образованию горячих трещин и хорошая герметичность силуминов объясняются наличием большого количества эвтектики в структуре этих сплавов. В двойных сплавах Al – Si эвтектика состоит из твердого раствора и кристаллов практически чистого кремния (рис. 13.6, а), в легированных (АК9ч и др.) помимо двойной имеются тройные и более сложные эвтектики.
Плотность большинства силуминов 2650 кг/м3, т.е. меньше плотности чистого алюминия (2700 кг/м3). Они хорошо свариваются.
Механические свойства зависят от химического состава, технологии изготовления (модифицирования, способа литья и т.д.), а также термической обработки (см. табл. 13.4). в двойных силуминах с увеличением содержания кремния до эвтектического состава снижается пластичность и повышается прочность. Появление в структуре сплавов крупных кристаллов первичного кремния вызывает снижение прочности и пластичности (рис. 13.7). несмотря на увеличение растворимости кремния в алюминии от 0,05% при 200  до 1,65% при эвтектической температуре, двойные сплавы на упрочняются термической обработкой. Это объясняется высокой скоростью распада твердого раствора, который частично происходит уже при закалке, а также большой склонностью к коагуляции стабильных выделений кремния. Единственным способом повышения механических свойств этих сплавов является измельчение структуры путем модифицирования.
до 1,65% при эвтектической температуре, двойные сплавы на упрочняются термической обработкой. Это объясняется высокой скоростью распада твердого раствора, который частично происходит уже при закалке, а также большой склонностью к коагуляции стабильных выделений кремния. Единственным способом повышения механических свойств этих сплавов является измельчение структуры путем модифицирования.
Силумины обычно модифицируют натрием, который в виде хлористых и фтористых солей вводят в количестве 2 – 3% от массы сплава. Помимо модифицирующего действия натрий сдвигает эвтектическую точку в системе Al – Si в сторону больших содержаний кремния (рис. 13.8). Благодаря этому эвтектический по составу сплав АК12 становится доэвтектическим. В его структуре помимо мелкокристаллической эвтектики появляются первичные кристаллы мягкой пластичной фазы – твердого раствора (рис.13.6, б). Все это приводит к увеличению пластичности и прочности (см. рис.13.7, табл. 13.4). табл. 13.
Модифицируют как двойные, так и легированные силумины, содержащие более 5 – 6% Si. Для легирования силуминов часто используют Mg , Cu , Mn , Ti ; реже Ni , Zr , Cr и др. растворяясь в алюминии, он повышают прочность и твердость силуминов. Кроме того, медь улучшает обрабатываемость резанием, титан оказывает модифицирующее действие. Медь и магний, обладая переменной растворимостью в алюминии, способствуют упрочнению силуминов при термической обработке, как правило, состоящей из закалки и искусственного старения. Температура закалки различных силуминов находится в пределах 515 – 535  , температура старения – в интервале 150 - 180
, температура старения – в интервале 150 - 180  . Грубокристаллическая структура литейных сплавов требует больших выдержек при нагреве под закалку (5 – 10 ч) и при старении (10 – 20 ч).
. Грубокристаллическая структура литейных сплавов требует больших выдержек при нагреве под закалку (5 – 10 ч) и при старении (10 – 20 ч).
Переходные металлы, например, Mn , Ti , Zr, способствуют получению пересыщенных твердых растворов при кристаллизации в условиях больших скоростей охлаждения, что вызывает некоторое упрочнение сплавов при старении без предварительной закалки.
Из легированных силуминов средней прочности наибольшее применение в промышленности нашли сплавы с добавками магния (АК7ч), и марганца (АК9ч). Наибольшее упрочнение вызывает метастабильная 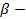 фаза (Mg 2 Si).
фаза (Mg 2 Si).
Легированные силумины применяют для средних и крупных литых деталей ответственного назначения: корпусов компрессора, картеров, головок цилиндров. Высокопрочный сплав АК8М, разработанный в МВТУ им. Н.Э. Баумана, предназначен для литья под давлением. Сплав обладает хорошими литейными свойствами, обрабатываемостью резанием, свариваемостью и коррозионной стойкостью. Марганец и титан, а также большая скорость кристаллизации при литье под давление способствуют получению метастабильной структуры при отливке деталей. Это дает возможность упрочнять отливки путем искусственного старения без предварительной закалки. Упрочнение вызывают 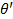 - и β '-фазы (CuAl 2 и Mg 2 Si). Наилучшим является старение при 175
- и β '-фазы (CuAl 2 и Mg 2 Si). Наилучшим является старение при 175  в течение 8 ч, когда выделяются метастабильные
в течение 8 ч, когда выделяются метастабильные 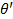 - и β '-фазы; при этом σв увеличивается на 30 – 40 МПа, НВ – на 18.
- и β '-фазы; при этом σв увеличивается на 30 – 40 МПа, НВ – на 18.
При изготовлении деталей другими методами литья сплав АК8М подвергают полной упрочняющей термической обработке – закалке от 515 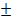 5
5  .
.
Сплав АК8М применяют для литья под давление нагруженных деталей, например, блоков цилиндров, головок блоков и других деталей автомобильных двигателей.
Сплавы системы Al – Cu (АМ4,5; АМ5) характеризуются высокой прочностью при обычных и повышенных температурах; они хорошо обрабатываются резанием и свариваются. Вместе с тем из-за отсутствия эвтектики сплавы обладают плохими литейными свойствами, имеют низкую герметичность. Как и деформируемые сплавы этой системы, они имеют структуру твердого раствора, но отличаются повышенным содержанием меди (см. рис. 13.4, в). Эвтектика в данной системе ( в отличие от силуминов) образуется при высоком содержании меди (33%), поэтому имеет большое количество твердой и хрупкой -фазы (CuAl 2), вызывающей хрупкость эвтектических сплавов.
Литейные и механические свойства сплавов системы Al – Cu улучшаются в результате легирования титаном и марганцем (АМ5). Марганец, образуя пересыщенный твердый раствор при кристаллизации из жидкого состояния, способствует значительному упрочнению сплава. Во время нагрева сплава под закалку наряду с растворением -фазы из твердого раствора выпадают мелкодисперсные частицы фазы Al 12 Mn 2 Cu, увеличивающие прочность при обычных и повышенных температурах. Сплавы системы Al – Cu используют для деталей, работающих при температурах до 300  .
.
Сплавы системы Al – Mg (АМг, АМг10) обладают высокой коррозионной стойкостью, прочностью, вязкостью и хорошей обрабатываемостью резанием. Они не содержат в структуре эвтектики по той же причине, что и сплавы системы Al – Cu, и характеризуются невысокими литейными свойствами, пониженной герметичностью и, кроме того, повышенной чувствительностью к примесям Fe, Si, которые образуют в этих сплавах нерастворимые фазы, снижающие пластичность сплавов.
Для того, чтобы предотвратить окисление, плавку и разливку двойных сплавов алюминия с магнием АМг необходимо вести под защитными флюсами.
Сплавы системы Al – Mg применяют для изготовления деталей, работающих в условиях высокой влажности, в судо-, самолето- и ракетостроении. Их них делают детали приборов, вилки шасси и хвостового оперения, штурвалы и др.
Гранулированные сплавы
Гранулированными называют сплавы, полученные путем компактирования из частиц (гранул), отлитых со сверхвысокой скоростью кристаллизации. Гранулы получают при кристаллизации в условиях скоростей охлаждения 103 – 106  /с. Такие скорости охлаждения достигаются различными методами, например, распылением жидкого металла струей чистого нейтрального газа. В зависимости от давления газа и условий кристаллизации диаметр гранул колеблется от нескольких микрометров до нескольких миллиметров.
/с. Такие скорости охлаждения достигаются различными методами, например, распылением жидкого металла струей чистого нейтрального газа. В зависимости от давления газа и условий кристаллизации диаметр гранул колеблется от нескольких микрометров до нескольких миллиметров.
Гранулы, а следовательно, и готовые полуфабрикаты (изделия) имеют чрезвычайно мелкозернистую структуру и минимальную легкоустранимую ликвацию. Но особенно большим достоинством гранулированных сплавов является метастабильное состояние. При столь высоких скоростях охлаждения при кристаллизации получаются пересыщенные твердые растворы с концентрацией, в 2,5 – 5 раз превосходящей предельную растворимость компонентов в равновесных условиях. Такие твердые растворы называют аномально пересыщенными. Степень пересыщения возрастает в соответствии с расположением металлов в следующем ряду: Cr , V , Mn , Ti , Zr.
В процессе технологических операций горячего компактирования сплавов (400  450
450  ) из пересыщенного твердого раствора выпадают дисперсные частицы интерметаллидных фаз (Al 6 Mn , Al 7 Cr , Al 3 Zr и др.), которые повышают температуру рекристаллизации (рис. 13.9), увеличивают прочность при обычных (рис. 13.10) и повышенных температурах.
) из пересыщенного твердого раствора выпадают дисперсные частицы интерметаллидных фаз (Al 6 Mn , Al 7 Cr , Al 3 Zr и др.), которые повышают температуру рекристаллизации (рис. 13.9), увеличивают прочность при обычных (рис. 13.10) и повышенных температурах.
Большой интерес представляют гранулированные сплавы алюминия с элементами, практически нерастворимыми в нем в равновесных условиях и сильно отличающимися от алюминия по плотности. Такие сплавы имеют гетерогенную структуру, представляющую собой алюминиевую матрицу с равномерно распределенными дисперсными (из-за высокой скорости кристаллизации) включениями второй фазы. В сплавах, легированных сравнительно тугоплавкими металлами (Fe , Ni , Co), такими фазами будут интерметаллиды. Они эффективно упрочняют сплавы. В сплавах с такими легкоплавкими металлами, как олово и свинец, в алюминии будут присутствовать дисперсные включения чистых металлов соответственно олова и свинца. Эти сплавы обладают хорошими антифрикционными свойствами. Стандартные деформируемые сплавы типа дуралюминов (Д16) в гранулированном варианте имеют дополнительный эффект упрочнения из-за наличия дисперсных частиц интерметаллидных фаз переходных металлов и нерастворимых фаз. При повышенном содержании переходных металлов σв достигает 800МПа.
Сплавы на основе магния
Свойства магния
Магний - металл серебристо белого цвета. Он не имеет полиморфных и кристаллизуется в ГП решетке с периодами а = 0,3202 нм, с = 0,5199 нм (с/а = 1,6209).
Магний и его сплавы отличаются низкой плотностью, хорошей обрабатываемостью резанием, способностью воспринимать ударные и гасить вибрационные нагрузки. Удельная вибрационная прочность магниевых сплавов с учетом демпфирующей способности почти в 100 раз больше, чем у дуралюминов, и в 20 раз, чем у легированных сталей. Теплопроводность магния в 1,5, а электрическая проводимость – 2 раза ниже, чем у алюминия. Примерно в 1,5 раза меньше, чем у алюминия, и его большой модуль нормальной упругости. Однако магний и алюминий близки по удельной жесткости.
В зависимости от содержания примесей установлены следующие марки магния (ГОСТ 804-93: Мг96 (99,96% Mg), Мг95 (99,95% Mg), Мг90 (99,90% Mg ). В настоящее время освоено производство магния высокой чистоты (99,9999% Mg). Примеси Fe , Si , Ni, Cu понижают и без того низкие пластичность и коррозионную стойкость магния. При нагреве магний активной окисляется и при температуре выше 623  на воздухе воспламеняется. Это затрудняет плавку и разливку магния и его сплавов. Порошок, тонкая лента, мелкая стружка магния представляет большую опасность, так как они способны самовозгораться на воздухе, горят с выделением большого количества теплоты и излучением ослепительно яркого света.
на воздухе воспламеняется. Это затрудняет плавку и разливку магния и его сплавов. Порошок, тонкая лента, мелкая стружка магния представляет большую опасность, так как они способны самовозгораться на воздухе, горят с выделением большого количества теплоты и излучением ослепительно яркого света.
Литой магний имеет крупнокристаллическую структуру и низкие механические свойства: σв = 110 … 120; МПа; σ0,2 = 20 … 30; МПа; δ =6 … 8%; К1с = 30 МПа м1/2; твердость – 30 HB. Модифицирование цирконием и пластическая деформация, приводящие к измельчению структуры, несколько улучшают его механические свойства: σв = 260 … 120; МПа; МПа; δ = 9% (холоднокатаный лист). Отжиг для снятия наклепа проводят при 330  350
350  , в результате чего магний имеет следующие свойства: σв = 190 МПа; σ0,2 = 98; МПа; δ = 15 … 17%; твердость – 40 HB. Наклеп для упрочнения магния применяют редко, так как он вызывает возникновение развитой текстуры деформации и анизотропии свойств. Магний и его сплавы обрабатывают давлением при 350
, в результате чего магний имеет следующие свойства: σв = 190 МПа; σ0,2 = 98; МПа; δ = 15 … 17%; твердость – 40 HB. Наклеп для упрочнения магния применяют редко, так как он вызывает возникновение развитой текстуры деформации и анизотропии свойств. Магний и его сплавы обрабатывают давлением при 350  450
450  в состоянии наибольшей пластичности.
в состоянии наибольшей пластичности.
Чистый магний из-за низких механических свойств как конструкционный материал практически не применяют. Его используют в пиротехнике, в химической промышленности для синтеза органических соединений, в металлургии различных металлов и сплавов как раскислитель, восстановитель и легирующий элемент.
Литейные магниевые сплавы
По химическому составу многие литейные сплавы магния близки к деформируемым (см. табл. 13.5). Преимуществом литейных сплавов перед деформируемыми является значительная экономия металла при производстве деталей, поскольку высокая точность размеров и хорошая чистота поверхности отливок почти исключает их обработку резанием. Однако из-за грубозернистой структуры они имеют более низкие механические свойства, особенно пластичность. Улучшение механических свойств литейных сплавов достигается различными способами: перегревом, модифицированием, гомогенизацией отливок, а также применением особо чистых шихтовых материалов при приготовлении сплавов. Перегрев дает хорошие результаты в сплавах с алюминием, выплавленных в железных тиглях. В результате взаимодействия алюминия с железом образуются частицы соединения FeAl 3, которые являются дополнительными центрами кристаллизации.
Для модифицирования используют цирконий, магнезит, мел. При гомогенизации происходит растворение грубых интерметаллидных фаз, охрупчивающих сплавы.
Механические свойства литейных магниевых сплавов в основном находятся на уровне свойств литейных алюминиевых сплавов, но, обладают меньшей плотностью, превосходят их по удельной прочности.
Наибольшее применение нашли сплавы системы Mg – Al – Zn, особенно сплавы с повышенным содержанием алюминия. Для сплавов этой системы характерен более широкий, чем у алюминиевых сплавов, интервал кристаллизации. В результате они обладают пониженной жидкотекучестью, усадочной пористостью и низкой герметичностью, склонностью к образованию горячих трещин. С увеличением содержания алюминия литейные свойства сначала ухудшаются, поскольку увеличивается интервал кристаллизации, а затем при появлении неравновесной эвтектики – улучшаются; повышаются прочностные характеристики. Однако из-за большого количества интерметаллидных фаз, в том числе и эвтектических (рис. 13.14), сплавы с большим содержанием алюминия обладают пониженной пластичностью. Наилучшее сочетание литейных и механических свойств имеют сплавы, содержащие 7,5 – 10% Al (МЛ5, МЛ6). Небольшие добавки цинка способствуют улучшению технологических свойств. Гомогенизация при 420  (12 – 24 ч) и закалка с этой температуры способствуют повышению прочности и пластичности. Вследствие малой скорости диффузии алюминия в магнии сплавы закаливаются при охлаждении на воздухе. Старение при 170 – 190
(12 – 24 ч) и закалка с этой температуры способствуют повышению прочности и пластичности. Вследствие малой скорости диффузии алюминия в магнии сплавы закаливаются при охлаждении на воздухе. Старение при 170 – 190  дополнительно повышает временное сопротивление и особенно предел текучести сплавов.
дополнительно повышает временное сопротивление и особенно предел текучести сплавов.
Малая плотность магниевых сплавов, а в отдельных случаях высокая удельная прочность способствует их широкому применению в самолетостроении (корпуса приборов, насосов, коробок передач, фонари и двери кабин и т.д., ракетной технике (корпуса ракет, обтекатели, топливные и кислородные баки, стабилизаторы) конструкциях автомобилей, особенно гоночных (корпуса, колеса, помпы и др.), в приборостроении (корпуса и детали приборов). Вследствие малой способности к поглощению тепловых нейтронов магниевые сплавы используют в атомной технике, а благодаря высокой демпфирующей способности – при производстве кожухов электронной аппаратуры.
Более высокими технологическими и механическими свойствами при 20 – 25  и повышенных температурах обладают сплавы магния с цинком и цирконием (МЛ12), а также сплавы, дополнительно легированные кадмием (МЛ8), редкоземельными металлами (МЛ9, МЛ10). Последние улучшают литейные свойства магниевых сплавов, снижают склонность к образованию горячих трещин и пористости, увеличивают прочность при обычных и повышенных температурах. Цирконий значительно измельчает крупнозернистую структуру отливок, способствует очистке сплавов от вредных примесей, благоприятно влияет на свойства твердого раствора, повышает температуру рекристаллизации. Кадмий улучшает механические и технологические свойства.
и повышенных температурах обладают сплавы магния с цинком и цирконием (МЛ12), а также сплавы, дополнительно легированные кадмием (МЛ8), редкоземельными металлами (МЛ9, МЛ10). Последние улучшают литейные свойства магниевых сплавов, снижают склонность к образованию горячих трещин и пористости, увеличивают прочность при обычных и повышенных температурах. Цирконий значительно измельчает крупнозернистую структуру отливок, способствует очистке сплавов от вредных примесей, благоприятно влияет на свойства твердого раствора, повышает температуру рекристаллизации. Кадмий улучшает механические и технологические свойства.
Высокопрочные литейные сплавы применяют для нагруженных деталей самолетов и авиадвигателей (корпусов компрессоров, картеров, ферм шасси, колонок управления и др.).
Неметаллические материалы
Пластмассы
Общая характеристика
Пластическими массами, или пластмассами, называют материалы, изготовленные на основе полимеров. Состав композиций разнообразен: простые пластмассы – это полимеры без добавок, сложные пластмассы – это смеси полимеров с различными добавками (наполнители, стабилизаторы, пластификаторы и т.д.)
Наполнители – это органические и неорганические вещества в виде порошков (древесная мука, сажа, слюда, SiO 2, тальк, TiO 2, графит), волокон (хлопчатобумажные, стеклянные, асбестовые, полимерные), листов (бумага, ткани из различных волокон, древесный шпон). Их добавляют в количестве 40 – 70% для повышения механических свойств, снижения стоимости, изменения других параметров.
Стабилизаторы – различные органические вещества, которые вводят в количестве нескольких процентов для сохранения структуры молекул и стабилизации свойств. Под влиянием окружающей среды происходит как разрыв макромолекул на части, так и соединение макромолекул между собой поперечными связями. Изменения исходной структуры макромолекул составляют сущность старения пластмасс, которое необратимо снижает прочность и долговечность изделий. Добавки стабилизаторов замедляют старение.
Пластификаторы – вещества, которые уменьшают межмолекулярное взаимодействие и хорошо совмещаются с полимерами. Их добавляют в количестве 10 – 20% для уменьшения хрупкости и улучшения формуемости. Часто пластификаторами служат эфиры, а иногда и полимеры с гибкими молекулами.
Специальные добавки – смазочные материалы, красители, добавки для уменьшения статических зарядов и горючести, для защиты от плесени, ускорители и замедлители отверждения и другие – служат для изменения или усиления какого-либо свойства.
Отвердители в количестве нескольких процентов добавляют к термореактивным пластмассам для отверждения. При этом между макромолекулами возникают поперечные связи, а макромолекулы отвердителя встраиваются в общую молекулярную сетку. В качестве отвердителей используют органические перекиси и другие вещества, серу (в резинах).
Основой классификации пластмасс как конструкционных материалов, экономически целесообразно. По сравнению с металлами переработка пластмасс менее трудоемка, число операций в несколько раз меньше и отходов получается немного. Пластмассовые детали, как правило, не нуждаются в отделочных операциях.
Отличительными особенностями пластмасс являются малая плотность (1 – 2 г/см3, а у пенопластов от 0,015 до 0,8 г/см3); высокая химическая стойкость, хорошие электроизоляционные свойства, невысокая теплопроводность (0,2 – 0,3 Вт/(м  К)) и значительное тепловое расширение в 10 – 30 раз больше, чем у обычных сталей). Преимущества пластмасс в сочетании с удобством переработки обеспечили им применение в машиностроении, несмотря на ограниченную теплостойкость, малую жесткость и небольшую вязкость по сравнению с металлами.
К)) и значительное тепловое расширение в 10 – 30 раз больше, чем у обычных сталей). Преимущества пластмасс в сочетании с удобством переработки обеспечили им применение в машиностроении, несмотря на ограниченную теплостойкость, малую жесткость и небольшую вязкость по сравнению с металлами.
Композиционные материалы
Хладостойкие материалы
МОДУЛЬ 1. СТРУКТУРА И СВОЙСТВА МАТЕРИАЛОВ
Дата: 2019-02-18, просмотров: 325.