Учебное пособие
по междисциплинарному курсу МДК 01.02
МЕТАЛЛУРГИЯ АЛЮМИНИЯ
для студентов специальности 22.02.02. Металлургия цветных металлов
Разработка и оформление преподавателя Минаковой Л.Н.
В учебном пособии рассмотрены: сырьё для производства алюминия электролизом и требования к нему, состав и свойства промышленных электролитов, теория электролиза криолитоглиноземных расплавов, конструкция и монтаж электролизеров, основы управления процессом (АСУТП) и нарушения технологии, обслуживание электролизёров, производство АВЧ, получение товарной продукции из алюминия, вопросы экологии и экономии сырья.
Содержание
1 Сырьё и материалы для производства алюминия. 3
1.1 Фтористые соли. 3
1.1.1 Свойства фторсолей и технические требования к ним.. 3
1.1.2 Кислотный способ получения криолита. 3
1.1.3 Производство других фторсолей. 4
1.1.4 Получение криолита щелочным способом.. 5
1.2 Производство углеродистых изделий. 6
1.2.1 Сырье для производства углеродистых изделий. 6
1.2.2 Общая схема производства углеродистых изделий. 6
1.2.3 Виды углеродистых изделий. 9
1.3 Глинозём.. 10
1.3.1 Месторождения руд алюминия. 10
1.3.2 Получение глинозема из бокситовых руд. 11
1.3.3 Разновидности глинозема и их свойства. 12
1.3.4 Требования к глинозёму как сырью для электролиза. 12
3 Теоретические основы электролиза глинозёма. 15
3.1 Основы электрохимии. 15
Основы теории электролиза криолит-глиноземных расплавов. 15
3.2 Диаграммы плавкости солевых систем.. 17
3.3 Состав и свойства электролита. 18
Физико-химические свойства электролитов. 22
6 Конструкция алюминиевых электролизёров. 32
Монтаж и демонтаж электролизёров. 37
Обжиг, пуск и послепусковой период. 39
Обслуживание алюминиевых электролизёров. 40
Оборудование электролизного производства. 43
Срок службы электролизеров. 44
Магнитное поле в электролизере. 47
1 Распределение тока. 47
2 Электромагнитные силы в металле. 47
3 Массо - и теплоперенос в электролизерах. 47
Автоматизация процесса электролиза. 48
Нарушения технологии электролиза алюминия. 49
Электролизный цех. 51
Сырьё и материалы для производства алюминия
Фтористые соли
1.1.1 Свойства фторсолей и технические требования к ним
Металлургия алюминия – один из крупнейших потребителей чистых фторсолей: криолита, AlF3, NaF. Криолит при получении алюминия служит расплавленной средой – электролитом, в котором осуществляется электролиз глинозёма. Для улучшения свойств и корректировки электролита в состав его вводят: AlF3, MgF2, CaF2, LiF и другие фтористые соли.
Криолит – двойная соль фторида натрия и фторида алюминия 3NaF*AlF3 или Na3AlF6. Чистый криолит содержит 54,4% F, 32,8% Na и 12,8% Al или 60% NaF и 40% AlF3.
Молярное отношение NaF к AlF3 называют криолитовым отношением, которое для чистого криолита равно: КО = 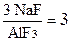
В переводе с греческого криолит значит “ледяной камень”, так как по внешнему виду сходен со льдом. Впервые криолит был найден в 1800 г. Естественный криолит в природе распространён ограниченно. Единственное в мире промышленное месторождение криолита находится в Гренландии. В нашей стране небольшое месторождение есть на Урале. Поэтому весь криолит для электролиза алюминия получают искусственным путём. Искусственный криолит готовят обычно с избытком AlF3 против его теоретической формулы, вплоть до состава 5NaF*3AlF3 (или Na5Al3F14), что соответствует составу природного минерала хиолита с молекулярным отношением NaF/AlF3 = 1,66.
Криолит – серовато-белый порошок, плохо растворим в воде. Плотность его при 20 °С равна 2,95 г/см3. Плавится при t=1008 °С, плотность расплавленного криолита 2,09 г/см3, электропроводность 2,67 Ом-1*см-1 (См/см).
Фтористый алюминий AlF3 – кристаллическая соль, бело-розоватый порошок, плотностью 2,88 г/см3, плохо растворим в воде. Кристаллический AlF3 при нагревании не плавится, а сублимирует. При t = 1260 оС упругость его паров равна атмосферному давлению. Является наиболее летучим компонентом электролита алюминиевой ванны.
Фтористый натрий NaF – кристаллическая соль, ядовитое вещество, плохо растворим в воде. При 20 °С имеет плотность 2,73 г/см3. Плавится при t = 992 оС, кипит при t = 1695оС, плотность при 1000 оС равна 1,942 г/см 3.
Чтобы получаемый алюминий был необходимой чистоты, криолит и другие фтористые соли должны содержать минимальное количество примесей в виде соединений элементов с более электроположительным потенциалом, чем потенциал алюминия. Для лучшего протекания процесса электролиза фторсоли должны содержать минимальное количество влаги и сульфатов, приводящих к разложению криолита в расплавленном состоянии.
Эти требования, предъявляемые алюминиевой промышленностью к искусственному криолиту и фторсолям, регламентируются техническими условиями:
- На криолит искусственный технический ГОСТ 10561-80.
- На алюминий фтористый технический ГОСТ 19181-78.
- На натрий фтористый технический ТУ 113-08-586-86.
- На соду ГОСТ 5100-85.
Исходный криолит может быть получен кислотным, щелочным способом, а также из отходов газов суперфосфатного производства.
Подготовка твёрдых углеродистых материалов
Подготовка твердых углеродистых материалов сводится к их дроблению, прокаливанию и размолу.
Твердые углеродистые материалы поступают на завод в кусках, их дробят в щековых дробилках до 75 мм, тем самым обеспечивая должное качество прокаливания. Более крупные куски, пройдя через печь, не успевают хорошо прокалиться, а более мелкие увеличивают угар при прокаливании. Прокаливанию подвергают все углеродистые материалы (кроме графита) для их усадки и удаления летучих веществ до 0,2%. Прокаливают при 1300— 1400° С в печах двух типов: ретортных без доступа воздуха или в ТВП.
Ретортная печь состоит из вертикальных камер (реторт), сырьё в них загружают сверху, тепло от сжигания газов ≈ 1400 °С передается материалу через стенки реторт. Время прокаливания 24—32 час. Достоинства ретортной печи:
1) использование в качестве горючего летучих веществ, выделяющихся из прокаливаемого материала;
2) получают равномерно прокаленный углеродистый материал;
3) малые потери материала за счет окисления, (угар 1—3 %), так как прокаливают практически без доступа воздуха.
Недостатки ретортных печей: большие капитальные затраты на их сооружение и сложность эксплуатации.
Вращающиеся трубчатые прокалочные печи длиной 20—45 м и диаметром 2—3 м, футерованные внутри огнеупорным материалом (шамотным кирпичом). Ось печи наклонена под углом 3 – 7 градусов к горизонту в сторону выхода материала из печи. Над печью установлен бункер, из которого материал равномерно подается в печь. При вращении печи 2—3 об/мин, прокаливаемый материал медленно движется со скоростью 1 —1,2 м/мин от загрузочного конца печи к разгрузочному, проходя зоны сушки, подогрева и прокаливания. Топливом служит мазут или природный газ, который подается в печь форсункой, установленной в разгрузочной головке печи. В отличие от ретортных печей, здесь горячие газы и пламя непосредственно соприкасаются с углеродистым материалом, причем топливом служат также летучие из углеродистых материалов и частично сам прокаливаемый материал.
Участок печи, где из углеродистого материала выделяются и сгорают летучие, называется зоной прокалки, температура достигает 1200—1300 °С. По выходе из печи материал выгружается в холодильный барабан, расположенный под печью и охлаждается до 60—75 °С пропускаемым через него воздухом, а также путем теплоотдачи через поверхность холодильного барабана, который охлаждается снаружи водой.
Вращающаяся трубчатая печь по сравнению с ретортными печами имеет следующие преимущества:
1) на содержание требуется меньше капитальных затрат;
2) проста в эксплуатации;
3) прост переход с одного вида материала на другой;
4) процесс прокаливания непрерывный,
5) возможна механизация и автоматизация процесса прокаливания.
К недостаткам этих печей следует отнести повышенный угар углеродистых материалов (до 14%) и более низкую температуру прокаливания, чем в ретортных печах.
Из углеродистых материалов полностью удаляется влага, резко снижается количество летучих веществ и повышается плотность за счет усадки (сокращения объема). Усадка кусков сопровождается распадом их на более мелкие, что предотвращает деформацию и появление трещин в готовых электродных изделиях при их обжиге. Поэтому температура прокаливания твердых углеродистых материалов всегда должна быть выше температуры, при которой ведется обжиг готовых электродных изделий. После прокаливания понижается реакционная способность углеродистых материалов к кислороду воздуха, повышается их электропроводность, теплопроводность и механическая прочность.
Прокаленный материал поступает в размольное отделение. Измельчение твердых углеродистых материалов необходимо для получения определенной крупности зерна (фракции), чтобы получать изделия с нужной пористостью и механической прочностью. Прокаленный материал измельчают в несколько приемов:
- дробление на валковых или молотковых дробилках до 25—5 мм;
- мелкий помол — от 20—5 мм до 10—0,5 мм
- тонкий помол — 0,1 мм и мельче.
Мелкий и тонкий помол осуществляют в шаровых мельницах, приэтом углеродистый материал загрязняется железом вследствие износа дробилок, мельниц и шаров, поэтому железные частицы удаляют электромагнитом.
После измельчения углеродистый материал рассеивают (классифицируют) на вибрационных грохотах по фракциям, которые поступают в сортовые бункера, а оттуда на дозировку и смешение в соответствии с принятым гранулометрическим составом (рецептом) для различных электродных изделий.
Подготовка связующего
Пек на завод на склад пека поступает в специальных железнодорожных вагонах-битумовозах с внешней паровой рубашкой. Пек в вагонах может находиться в жидком или твёрдом виде. Если пек в вагоне-бункере оказался застывшим, в паровую рубашку подводят перегретый пар и пек начинает плавиться. Вагон опрокидывают и жидкий пек сливают в обогреваемые паром цистерны- пекоплавители емкостью 50— 60 т. Пек в пекоплавителях выдерживается 2-3 суток при 110 – 120 ºC. При этом из пека удаляется влага и усредняется его состав. Вода содержится в пеке в двух видах: в капельно-жидком и в тонкораспыленном. Капельно-жидкая вода легко отделяется при расплавлении пека, распыленная же выделяется только при нагревании его до 110 °С и вызывает сильное вспенивание пека.
Дозировка и смешение шихты
В зависимости от типа изготовляемых изделий из сортовых бункеров отвешивают порошки углеродистых материалов и связующего. Эту операцию называют дозировкой. Сыпучие материалы и связующие дозируют механическим или автоматическим способом, взвешивая на весах или отмеривая материалы по объему.
Цель дозировки — обеспечить определенный гранулометрический состав, такое соотношение между размерами зерен и связующим, при котором электродное изделие получилось бы с необходимой плотностью и механической прочностью. Этого достигают, смешивая крупные зерна с мелкими. Крупные зерна образуют основу электрода, придавая ему надлежащую прочность, а более мелкие вместе со связующими веществами служат заполнителем пустот между крупными. Избыток связующего в шихте вреден, так как твердые частицы будут отделены друг от друга утолщенным слоемпека. При обжиге такой массы из-за значительной усадки пека в изделии могут образовываться пустоты и трещины.
Подбор гранулометрического состава смеси твердых материалов и соотношения его и связующего — весьма ответственная операция. В заводской практике сначала изготовляют опытные партии углеродистых изделий по той или иной рецептуре, а затем проверяют на эксплуатационную стойкость в производственных условиях.
Таблица 1 - Примерный состав шихтовых материалов, применяемых при изготовлении электродов
Размеры в процентах
| Обожжённые электроды | Кол. | Графитированные электроды | Кол. |
| Кокс | 50 - 60 | Нефтяной кокс | 70-75 |
| Оборотный материал (электродный бой) | 3 - 5 | Связующее | 25-30 |
| Графит | 20 - 30 | ||
| Связующее | 20 - 33 |
В углеродистую массу, предназначенную для прессованных изделий, вводят меньше связующего (20—22 %), чем в анодную массу (28—33 %). Повышенное содержание связующего в анодной массе необходимо для лучшего размягчения, равномерного распределения и схватывания с предыдущей анодной массой в аноде.
Цель смешения сухих порошков со связующим — обеспечить полное соприкосновение зерен твердых углеродистых материалов со связующим и получить однородную массу с равномерным распределением в ней компонентов. Связующее должно покрыть тонкой пленкой каждую частицу твердого материала и заполнить пустоты между ними.
Твердые углеродистые материалы загружают в предварительно нагретый до 100—120 °С смеситель и перемешивают 20-30 мин., пока они не нагреются. Связующее подают в смеситель в расплавленном состоянии и перемешивают ещё 50—60 мин. По окончании смешивания готовую массу выгружают и транспортными устройствами подают на прессование. Если же в смесителях готовили анодную или подовую массу, то её формуют в брикеты, проверяют на качество, а затем транспортируют на склад.
Виды углеродистых изделий
Электроды
Электродами в широком смысле этого слова называют проводники, служащие для подвода электрического тока к среде, на которую он воздействует. Эта среда может быть водным раствором, расплавленным или твердым раскаленным веществом. Электроды изготавливают из различных токоподводящих материалов: железа, меди, угля и др.
Одним из наиболее крупных потребителей электродов является алюминиевая промышленность. Электроды здесь работают в весьма жестких эксплуатационных условиях (высокая температура, агрессивная среда в виде расплавленных солей и т.д.), поэтому они должны удовлетворять следующим основным требованиям:
1. выдерживать высокую температуру;
2. иметь хорошую электропроводность, малую пористость и достаточную механическую прочность;
3. обладать хорошей стойкостью против окисления кислородом воздуха и разъедания различными химическими веществами;
4. содержать минимальное количество примесей, ухудшающих качество получаемой продукции;
5. иметь правильную геометрическую форму;
6. быть достаточно дешевыми.
Наиболее полно этим требованиям отвечают электроды из углеродистых материалов.
В большинстве случаев электрод не только служит средством подвода тока к среде, но и сам участвует в происходящих в ней процессах. Например, при электротермических процессах материал электрода служит восстановителем; при электролитическом получении алюминия энергия, выделяемая при окислении электрода (анода), положительно влияет на энергетический баланс электролизера (деполяризация).
В алюминиевой промышленности применяются следующие виды электродных изделий: прессованные призматические и цилиндрические обожженные и графитированные электроды, подовые и боковые блоки, электродные массы (анодная и подовая).
Анодные материалы
В современных электролизерах используются два вида анодных материалов:
1) самообжигающиеся аноды - формуются из анодной массы непосредственно в процессе электролиза;
2) предварительно обожжённые анодные блоки.
Анодная масса выпускается в России в соответствии с ТУ 48-5-80-86 из пекового или нефтяного коксов. Масса из пекового кокса лучше по прочности, пористости, удельному электросопротивлению, чем на основе нефтяного кокса, но пековый кокс дефицитен и дороже.
Содержание золы в массе влияет на содержание примесей в алюминии, так как на производство 1 т алюминия расходуется более 500 кг анодной массы. В свою очередь, зольность массы определяется качеством коксов, а также износом технологического оборудования и, прежде всего, футеровки прокалочных печей.
Содержание серы в массе зависит от ее содержания в коксах. В нефтяных коксах содержание серы до 4 %, однако для производства анодной массы не рекомендуется использование кокса с содержанием серы более 1,5 %, в основном из-за экологических соображений.
Удельное электросопротивление (УЭС) массы и ее пористость — взаимозависимые величины: с увеличением пористости возрастает УЭС и увеличиваются потери электроэнергии в аноде. Пористость массы зависит от: вида и качества исходного кокса, его гранулометрического состава, содержания и качества связующего, технологии обжига анода и пр. С уменьшением пористости повышается механическая прочность анода, что полезно до определенного предела, так как с увеличением механической прочности растет хрупкость анода, что влечет за собой образование трещин и сколов.
Разрушаемость анода состоит из суммы двух составляющих: окисляемости и осыпаемости. Окисляемость численно равна тому количеству углерода, которое расходуется при окислении анода углекислым газом (по реакции Будуара: С + СО2 = 2СО). Чем меньше эта составляющая, тем меньше расход анода в процессе электролиза. Осыпаемость частиц кокса-наполнителя происходит в результате более высокой реакционной способности вторичного кокса из связующего, и чем он меньше, тем меньше расход анода.
Содержание влаги в массе не является браковочным показателем, а определяется для взаиморасчетов потребителей с поставщиками. Повышенная влажность может повлечь вспучивание анодной массы в процессе ее расплавления в аноде.
Прессованные обожженные аноды применяют при производстве алюминия. Они представляют собой призматические блоки (40 х 40 х 55 см), снабженные двумя ниппельными гнездами (углублениями) для заливки чугуном стальных ниппелей контактов, с помощью которых подводят электрический ток к телу анода.
Глинозём
Месторождения руд алюминия
Алюминий в земной коре содержится в различных соединениях, которые делятся на две равные группы:
- первичные минералы , образованные при кристаллизации магмы, в основном алюмосиликаты: ортоклаз, альбит, лейцит и нефелин. Меньше распространены дистен, силлиманит, андалузит, шпинели MeO*Al2O3 и свободный оксид алюминия – корунд;
- вторичные минералы, образовавшиеся в результате выветривания части элементов из первичных, имеют более высокое содержание оксида алюминия (таблица 1). Широко распространённые гидросиликаты алюминия – каолинит и его разновидности; гидроксиды и оксигидроксиды алюминия – гиббсит (гидраргиллит), бемит и диаспор являются главной составной частью бокситов. Природные бокситы в основном смешанного типа гиббсит-бемитовые или бемит - диаспоровые. К этой же группе относится и алунит.
Таблица 1 – Содержание основных компонентов в минералах алюминия
Размеры в % (масс.)
| Минерал | Оксиды | Химическая формула | ||
| Al2O3 | SiO2 | R2O | ||
| Первичные минералы | ||||
| Корунд | 100 | – | – | Al2O3 |
| Андалузит, дистен, силлиманит | 63 | 37 | – | Al2O3*SiO2 |
| Нефелин | 32,3–36 | 38–42,3 | 19,6–21 | (Na, K)2O*Al2O3*SiO2 |
| Лейцит | 23,5 | 55,1 | 21,5 | K2O*Al2O3*4SiO2 |
| Ортоклаз | 18 | 65 | 17 | K2O*Al2O3*6SiO2 |
| Альбит | 20 | 68 | 12 | Na2O*Al2O3*6SiO2 |
| Вторичные минералы | ||||
| Диаспор, бемит | 85 | - | - | Al2O3*H2O |
| Гиббсит | 65,4 | - | - | Al2O3*3H2O |
| Каолинит | 39,5 | 46,4 | - | Al2O3*2SiO2*2H2O |
| Гидрослюда (мусковит) | 38,5 | 45,2 | 9,7 | K2O*3Al2O3*6SiO2*3H2O |
| Хлориты (шамозит) | 21-27,7 | 16-30 | - | (Mg, Al, Fe+2, Fe+3)*(Si, Al)4*(OH, F)4 |
| Алунит | 37 | - | 11,3 | K2SO4*Al2(SO4)3*4Al(OH)3 |
Боксит (фр. bauxite) получил название по местности Baux на юге Франции. Бокситы очень широко применяются в промышленности: в производстве глинозема, абразивных и огнеупорных материалов; для сушки газов и чистки нефти от серы; в качестве красителя и флюса для выплавки мартеновской стали.
Химический состав бокситов и их физические свойства весьма разнообразны. Содержание Al2O3 в них колеблется от 35 до 60% и выше; SiO2 – от десятых долей до 25%; Fe2O3 – от 2 до 40%; TiO2 – от следов до 11%. Примеси в бокситах составляют сотые и даже тысячные доли процента. Так, содержание ванадия составляет 0,025-0,15%, а галлия – 0,001-0,007%. Бокситы, содержащие до 0,35% S, относят к малосернистым, от 0,3 до 0,8% – к сернистым, и более 0,8% – к высокосернистым. По содержанию оксидов железа различают: маложелезистые (Fe2O3 до 10%), железистые (10 – 18%) и высокожелезистые (более 18%). В зависимости от содержания СО2, бокситы делятся на малокарбонатные (до 0,6%), карбонатные (0,6 – 2%) и высококарбонатные (более 2%).
Первое месторождение алюминиевых руд в России было открыто в 1914 г. под Санкт-Петербургом. Рядом с городом Тихвин на данном месторождении было построено шесть заводов, самый большой - Волховский алюминиевый завод (ВАЗ). На сегодняшний день Тихвинское месторождение истощено, завод работает на привозном сырье.
В 1931 г. было открыто уникальное Северо-Уральское месторождение высококачественных бокситов (СУБР). Оно послужило базой для строительства в 1939 г. Уральского алюминиевого завода (УАЗ). А на основе Южно-Уральского бокситового рудника (ЮУБР) был построен Богословский алюминиевый завод (БАЗ).
Североонежское месторождение находится вблизи Кольского полуострова. Висловское месторождение каолинного типа, для получения глинозема не используется. Тиманское месторождение (Республика Коми, Воркута).
На сегодняшний день главными поставщиками бокситов в мире являются:
- Австралия; также там находятся огромные залежи Fe, Au, U, Ni, Ti, Co, Cu и др.
- Гвинея – у России есть несколько приобретённых месторождений.
- Центральная Америка: Гайана, Ямайка, Суриман. Бразилия.
- Греция, но бокситы низкого качества. В Европе все месторождения истощены.
Качество бокситов определяется кремниевым модулем, который представляет собой массовое отношение содержания Al2O3/SiO2, - чем выше модуль, тем выше качество боксита. Около 95 % всего глинозема для получения из него алюминия в мире получают из бокситовых руд.
Требования к глинозёму как сырью для электролиза
К глинозему, используемому для производства алюминия, предъявляются требования по химическому составу в соответствии с ГОСТ 30558–98. Глинозем представляет собой белый, абразивный, мелкокристаллический порошок, нерастворимый в воде. Для производства алюминия он должен максимально совмещать следующие свойства:
- хорошую текучесть при возможно меньшем пылении;
- повышенную скорость растворения в электролите;
- достаточную адсорбционную (поглощающую) активность поверхностью летучих фтористых соединений;
- удовлетворительные теплофизические свойства.
Типичные производственные требования к глинозёму при электролизе:
- хорошая растворимость в электролите, без образования осадка;
- минимальное содержание вредных примесей, снижающих сорт алюминия;
- низкая степень пыления, т.е. минимальное содержание мелкой фракции;
- хорошая текучесть (глинозём транспортируют в узлы заправки и загружают в бункера АПГ).
- диапазон содержания фракций – 45 мкм 5–30 % (до 50%); + 150 мкм 1–6 % (до 30%).
- угол естественного откоса глинозёмной загрузки на корке электролита должен быть 29-32 градуса.
Глинозем подразделяется на следующие типы:
- мучнистый (пылевидный);
- песчаный (крупнозернистый), основное отличие - в гранулометрическом составе и содержании α-Al2O3;
- фторированный (поступает с сухой газоочистки).
Физико – химические свойства глинозема зависят от исходного сырья и технологии его получения. Свойства глинозема влияют на его расход и на показатели электролиза: расход электроэнергии, анода и фторидов, запыленность атмосферы в рабочей зоне, качество улавливания фтора и другие (табл.2).
Таблица 2 - Физические свойства глинозема
| Свойство | Способ получения глинозема | ||
| Байера | спекания | из алунитов | |
| Удельная поверхность, м2/г | 40 – 100 | 40 – 90 | 46 – 80 |
| Плотность, г/см3 | 3,42 – 3,67 | 3,44 – 3,72 | 3,47 – 3,63 |
| Насыпная плотность, г/см3: без уплотнения с уплотнением | 1,07 – 1,24 1,40 – 1,50 | 0,91 – 1,08 1,30 – 1,43 | 1,10 – 1,17 1,45 – 1,55 |
| Угол естественного откоса, град | 30 – 38 | 35 – 43 | 35 – 39 |
| Содержание фракций, % : +100 мкм -40 мкм -30 мкм | 0 – 14 18 – 56 10 – 30 | 0 – 40 22 – 60 11 – 50 | 1 – 5 22 – 53 20 – 40 |
| Средний размер частиц, мкм | 22 - 44 | 20 – 40 | 23 – 32 |
Скорость растворения в электролите - наиболее значимый показатель качества глинозёма. Промышленный опыт показывает, что частицы песчаного глинозёма +45-100 мкм с содержанием α-Al2O3 не более 10% (остальное γ-Al2O3), хорошо смачиваются электролитом и растворяются. Гамма-Al2O3 имеет развитую ультрапористую структуру, достаточно большую удельную поверхность (более 60-80 м2/г) и большое химическое сродство к фтору, что проявляется в повышенной растворимости в электролите и в эффективном улавливании фтористых соединений.
Не менее важным свойством глинозёма является его способность образовывать устойчивую корку на поверхности электролита. Мягкая, но достаточно плотная корка с хорошим сцеплением частиц образуется при использовании глинозёма с теми же характеристиками, которые указаны выше, но класса менее 45 мкм,. Такая корка хорошо пропитывается электролитом, содержит больше глинозёма, легче поддаётся разрушению при обработке электролизёров и при ударе пробойника АПГ, чем корки, образующиеся при использовании мучнистого глинозёма. Мучнистый глинозём, в отличие от песчаного, смачивается значительно хуже, и корка состоит преимущественно из застывшего электролита, поверх которого находится глинозём. Прочность такой корки очень высока.
Теплопроводность и объёмная плотность глинозема играют большую роль в тепловом балансе электролизёра, в том числе в регулировании тепловых потерь через глинозёмную засыпку или укрытие анодного массива у электролизёров ОА, в поддержании стабильного уровня электролита и защите боковых поверхностей анода от окисления.
Текучесть глинозёма определяется в гранулометрическим составом материала и содержанием в нём α-Al2O3. Высокой текучести удовлетворяет песчаный глинозем, содержащий фракцию < 45 мкм не более 10% и α-Al2O3.в пределах 5%, с углом естественного откоса менее 35. Хорошая текучесть у глинозёма с пониженной степенью прокалки, он имеет крупность зерна более 45 мкм, высокую степень однородности гранулометрического состава и угол естественного откоса 30-40. Глинозёмы со слабой текучестью и углом естественного откоса > 40-45 комкуются при контакте с электролитом, и, имея больший удельный вес, оседают через электролит и металл, образуя осадок на подине. Однако если текучесть глинозема будет слишком велика, то надежное укрытие обожженных анодов будет затруднено.
Потери глинозема за счет уноса с анодными газами в виде пыли зависят от его гранулометрического состава, от технологии обработки электролизёров, настройки АПГ и частоты анодных эффектов. Суммарные потери мучнистого глинозёма составляют 17-25 кг/т алюминия, что на 10-15 кг/т выше, чем для песчаного глинозёма.
Глинозем должен содержать минимальное количество оксидов железа, кремния и других более электроположительных, чем алюминий, элементов, так как, выделяясь на катоде вместе с алюминием, они ухудшают его качество. Нежелательно присутствие в глиноземе оксидов щелочных и щелочноземельных металлов, поскольку взаимодействуют с AlF3, изменяют состав электролита, что вызывает необходимость его корректировки
3 Na2О + 2 АlF3 = 6 NaF + Аl2О3
С увеличением содержания оксида натрия возрастает расход фторида алюминия, что видно из следующих данных:
Содержание Na2O в Al2O3, % 0,25 0,30 0,35 0,40 0,60
Расход AlF3, кг/т Al 10,0 13,8 17,5 24,7 35,3
При содержании Na2O в глиноземе более 0,33 % начинает нарабатываться излишнее количество электролита, который приходится выливать из ванны. Кроме того, оксид калия, проникая в угольную футеровку, снижает срок службы ванны.
Крайне нежелательно присутствие влаги в глиноземе, так как при взаимодействии воды с криолитом и фторидом алюминия образуется фтористый водород HF, что приводит к дополнительному расходу фторидов.
2Na3AlF6 + 3H2O = Al2O3 + 6NaF + 6HF↑
2AlF3 + 3H2O = Al2O3 + 6HF↑
Как следует из этих реакций, из каждых 18 г воды, попавших в электролит, образуется 56 г HF.
В алюминиевом электролизере глинозем выполняет множество функций:
- является основным расходуемым компонентом, который растворяется в электролите и подвергается электролитическому разложению с получением алюминия и анодных газов;
- участвует в образовании корки над электролитом и боковой настыли;
- является тепловой изоляцией и герметизацией ванны, находясь на корке электролита;
- защищает анод от окисления;
- улавливает пары фторидов;
- укрывает обожжённые аноды, предотвращая их окисление
- является адсорбентом газообразных и твёрдых фторидов в сухой газоочистке.
Применяемые в производстве алюминия глиноземы отличаются большим разнообразием свойств, и если их не учитывать, то это может нанести технологии, экономике и экологии серьезный ущерб. Для производства алюминия на КрАЗе применяют глинозём высших марок: Г–000, Г–00, Г–0.
Основы электрохимии
В электрохимии исследуют процессы превращения химической энергии в электрическую (гальванические элементы) и электрической энергии в химическую (электролиз). Электрохимические исследования получили развитие после изобретения в 1799 г. итальянским учёным Луиджи Вольта электрической батареи, называемой вольтовым столбом.
Вещества, проводящие электрический ток, разделяются на проводники первого и второго рода. В связи с этим различают электронную и ионную проводимость.
Все металлы, сплавы металлов и углеродистые электроды относятся к проводникам первого рода. В них часть электронов, слабо связанных с ядрами атомов, образует так называемый «электронный газ», причём электроны неупорядоченно перемещаются от одних атомов к другим. При наложении электрического поля начинается упорядоченное движение электронов. Прохождение электрического тока по проводникам первого рода не связано с переносом вещества.
К проводникам второго рода относятся электролиты: водные растворы солей, кислот, щелочей и расплавленные соли. В проводниках второго рода электричество переносится ионами. Прохождение электрического тока через проводники второго рода сопровождается переносом вещества.
В 1833 г. Фарадей открыл законы электролиза, являющиеся основой количественного изучения электродных процессов. При электролизе на электроды подаётся разность потенциалов от источника постоянного тока. Отрицательно заряженный электрод называется катодом, а положительно заряженный – анодом.
Процесс разложения молекул вещества на ионы при взаимодействии с растворителем называется электролитической диссоциацией, в результате которой образуются ионы, несущие положительный заряд – катионы, или отрицательный заряд – анионы. При этом сумма положительных зарядов образовавшихся катионов равна сумме отрицательных зарядов анионов.
Процесс выделения веществ на электродах в растворах или расплавах называется электролизом.
Среда, в которой осуществляется процесс электролиза, называется электролитом, это смесь ионов, проводящих электрический ток.
Чтобы осуществить разряд катиона, нужно создать на катоде избыток электронов, причём для разных металлов избыток электронов различен. В зависимости от величины электродного потенциала металла и водорода, все металлы располагаются в так называемый электрохимический ряд напряжений:
Требования к электролитам
Электролит для электролиза глинозема должен удовлетворять следующим требованиям:
1. Не содержать более электроположительных элементов, чем алюминий, которые выделяются на катоде - в жидком алюминии – и загрязняют его.
2. В расплавленном состоянии хорошо растворять глинозем.
3. Обладать меньшей плотностью, чем расплавленный алюминий, что благоприятствует процессу электролиза.
4. Обладать достаточной жидкотекучестью, что способствует удалению анодных газов, а также выравниванию состава электролита.
5. Обладать хорошей электропроводностью, что дает возможность иметь меньшее падение напряжения в электролите и, следовательно, меньший расход электроэнергии.
6. Образовывать с глиноземом сплавы, обладающие температурой плавления, близкой к Тпл алюминия.
7. При температуре электролиза химически не разлагаться, а также слабо улетучиваться.
8. Химически не взаимодействовать с углеродистой футеровкой и угольным анодом.
9. Должен быть не гигроскопичным.
Совокупность свойств у криолитоглиноземных расплавов наиболее благоприятна. Были попытки замены состава электролита на смеси хлористых солей, но они не имели успеха.
Основные компоненты электролита - криолит и глинозем, но всегда присутствуют добавки в сумме не более 15-10 % (по массе):
· избыток AlF3 -- для уменьшения криолитового отношения;
· CaF2, MgF2, LiF и др.- для улучшения физико-химических свойств .
Для характеристики состава технического криолита служит криолитовое отношение (КО): молярное отношение NaF/AlF3 в данном электролите. Электролиты с:
КО = 3 называются нейтральными,
КО > 3 называются щелочными (избыток NaF),
КО < 3 называются кислыми (избыток AlF3).
Современные промышленные электролиты имеют КО = 2,1 – 2,4.
Учебное пособие
по междисциплинарному курсу МДК 01.02
МЕТАЛЛУРГИЯ АЛЮМИНИЯ
для студентов специальности 22.02.02. Металлургия цветных металлов
Разработка и оформление преподавателя Минаковой Л.Н.
В учебном пособии рассмотрены: сырьё для производства алюминия электролизом и требования к нему, состав и свойства промышленных электролитов, теория электролиза криолитоглиноземных расплавов, конструкция и монтаж электролизеров, основы управления процессом (АСУТП) и нарушения технологии, обслуживание электролизёров, производство АВЧ, получение товарной продукции из алюминия, вопросы экологии и экономии сырья.
Содержание
1 Сырьё и материалы для производства алюминия. 3
1.1 Фтористые соли. 3
1.1.1 Свойства фторсолей и технические требования к ним.. 3
1.1.2 Кислотный способ получения криолита. 3
1.1.3 Производство других фторсолей. 4
1.1.4 Получение криолита щелочным способом.. 5
1.2 Производство углеродистых изделий. 6
1.2.1 Сырье для производства углеродистых изделий. 6
1.2.2 Общая схема производства углеродистых изделий. 6
1.2.3 Виды углеродистых изделий. 9
1.3 Глинозём.. 10
1.3.1 Месторождения руд алюминия. 10
1.3.2 Получение глинозема из бокситовых руд. 11
1.3.3 Разновидности глинозема и их свойства. 12
1.3.4 Требования к глинозёму как сырью для электролиза. 12
3 Теоретические основы электролиза глинозёма. 15
3.1 Основы электрохимии. 15
Основы теории электролиза криолит-глиноземных расплавов. 15
3.2 Диаграммы плавкости солевых систем.. 17
3.3 Состав и свойства электролита. 18
Физико-химические свойства электролитов. 22
6 Конструкция алюминиевых электролизёров. 32
Монтаж и демонтаж электролизёров. 37
Обжиг, пуск и послепусковой период. 39
Обслуживание алюминиевых электролизёров. 40
Оборудование электролизного производства. 43
Срок службы электролизеров. 44
Магнитное поле в электролизере. 47
1 Распределение тока. 47
2 Электромагнитные силы в металле. 47
3 Массо - и теплоперенос в электролизерах. 47
Автоматизация процесса электролиза. 48
Нарушения технологии электролиза алюминия. 49
Электролизный цех. 51
Сырьё и материалы для производства алюминия
Фтористые соли
1.1.1 Свойства фторсолей и технические требования к ним
Металлургия алюминия – один из крупнейших потребителей чистых фторсолей: криолита, AlF3, NaF. Криолит при получении алюминия служит расплавленной средой – электролитом, в котором осуществляется электролиз глинозёма. Для улучшения свойств и корректировки электролита в состав его вводят: AlF3, MgF2, CaF2, LiF и другие фтористые соли.
Криолит – двойная соль фторида натрия и фторида алюминия 3NaF*AlF3 или Na3AlF6. Чистый криолит содержит 54,4% F, 32,8% Na и 12,8% Al или 60% NaF и 40% AlF3.
Молярное отношение NaF к AlF3 называют криолитовым отношением, которое для чистого криолита равно: КО = 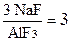
В переводе с греческого криолит значит “ледяной камень”, так как по внешнему виду сходен со льдом. Впервые криолит был найден в 1800 г. Естественный криолит в природе распространён ограниченно. Единственное в мире промышленное месторождение криолита находится в Гренландии. В нашей стране небольшое месторождение есть на Урале. Поэтому весь криолит для электролиза алюминия получают искусственным путём. Искусственный криолит готовят обычно с избытком AlF3 против его теоретической формулы, вплоть до состава 5NaF*3AlF3 (или Na5Al3F14), что соответствует составу природного минерала хиолита с молекулярным отношением NaF/AlF3 = 1,66.
Криолит – серовато-белый порошок, плохо растворим в воде. Плотность его при 20 °С равна 2,95 г/см3. Плавится при t=1008 °С, плотность расплавленного криолита 2,09 г/см3, электропроводность 2,67 Ом-1*см-1 (См/см).
Фтористый алюминий AlF3 – кристаллическая соль, бело-розоватый порошок, плотностью 2,88 г/см3, плохо растворим в воде. Кристаллический AlF3 при нагревании не плавится, а сублимирует. При t = 1260 оС упругость его паров равна атмосферному давлению. Является наиболее летучим компонентом электролита алюминиевой ванны.
Фтористый натрий NaF – кристаллическая соль, ядовитое вещество, плохо растворим в воде. При 20 °С имеет плотность 2,73 г/см3. Плавится при t = 992 оС, кипит при t = 1695оС, плотность при 1000 оС равна 1,942 г/см 3.
Чтобы получаемый алюминий был необходимой чистоты, криолит и другие фтористые соли должны содержать минимальное количество примесей в виде соединений элементов с более электроположительным потенциалом, чем потенциал алюминия. Для лучшего протекания процесса электролиза фторсоли должны содержать минимальное количество влаги и сульфатов, приводящих к разложению криолита в расплавленном состоянии.
Эти требования, предъявляемые алюминиевой промышленностью к искусственному криолиту и фторсолям, регламентируются техническими условиями:
- На криолит искусственный технический ГОСТ 10561-80.
- На алюминий фтористый технический ГОСТ 19181-78.
- На натрий фтористый технический ТУ 113-08-586-86.
- На соду ГОСТ 5100-85.
Исходный криолит может быть получен кислотным, щелочным способом, а также из отходов газов суперфосфатного производства.
Дата: 2019-02-25, просмотров: 665.