Фотоэлектрическим эффектом (фотоэффектом) называется явление взаимодействия света с веществом, в результате которого энергия фотонов передается электронам вещества. Различают внешний, внутренний и вентильный фотоэффект.
Внешним фотоэффектом называется испускание электронов веществом под действием электромагнитного излучения. Наблюдается в твердых телах, а также в газах на отдельных атомах и молекулах (фотоионизация).
Внутренний фотоэффект – это вызванные электромагнитным излучением переходы электронов внутри полупроводника или диэлектрика из связанных состояний в свободные без вылета наружу. В результате концентрация носителей тока внутри тела увеличивается, что приводит к возникновению фотопроводимости(повышению электропроводности полупроводника или диэлектрика при его освещении) или к возникновению э.д.с.
Вентильный фотоэффект - возникновение э.д.с. (фото-э.д.с.) при освещении контакта двух разных полупроводников или полупроводника и металла (при отсутствии внешнего электрического поля).
Исследования Столетова привели к установлению 3-х основных законов фотоэффекта:
1.Сила фототока насыщения Iн прямо пропорциональна падающему световому потоку Ф
Iн = кФ, где к – коэффициент пропорциональности.
2.Скорость фотоэлектронов увеличивается с увеличением частоты (с уменьшением длины волны) падающего света и не зависит от интенсивности светового потока
3.Независимо от интенсивности светового потока фотоэффект начинается при определенной для данного вещества минимальной частоте (максимальной длине) световой волны, называемой красной границей фотоэффекта.
2-й и 3-й законы фотоэффекта противоречат представлениям волновой теории света. Согласно этим представлениям электроны вещества должны совершать колебания с амплитудой, пропорциональной амплитуде падающей световой волны. При достаточной амплитуде связь электрона с веществом может быть нарушена и электроны будут вылетать наружу со скоростью, величина которой будет зависеть от амплитуды, т.е. интенсивности падающего света. В действительности такой зависимости нет, скорость электронов зависит только от частоты падающего света.
Для объяснения этого факта Эйнштейн выдвинул гипотезу, что свет не только испускается, но и распространяется и поглощается дискретными порциями – квантами. По Эйнштейну квант энергии (света) поглощается полностью одним электроном и энергия кванта hν расходуется на работу по вырыванию электрона из вещества Авых и на сообщение электрону кинетической энергии
Формула Эйнштейна для ФЭ: 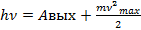
Из неё следует, что энергия падающего фотона расходуется на совершение электроном работы выхода А из металла и на сообщение вылетевшему фотоэлектрону кинетической энергии.
Максимальная скорость фотоэлектронов, так же как и задерживающий потенциал зависят от частоты света и работы выхода электронов из металла, и не зависят от интенсивности светового потока.
Максимальная начальная энергия фотоэлектрона обращается в нуль при значении частоты света, соответствующей красной границе фотоэффекта
При очень больших интенсивностях света, достижимых в настоящее время с помощью лазеров, наблюдается многофотонный фотоэффект, когда электрон может одновременно получить энергию не одного, а N фотонов.
34.Модель строения атома Бора. Постулаты Бора
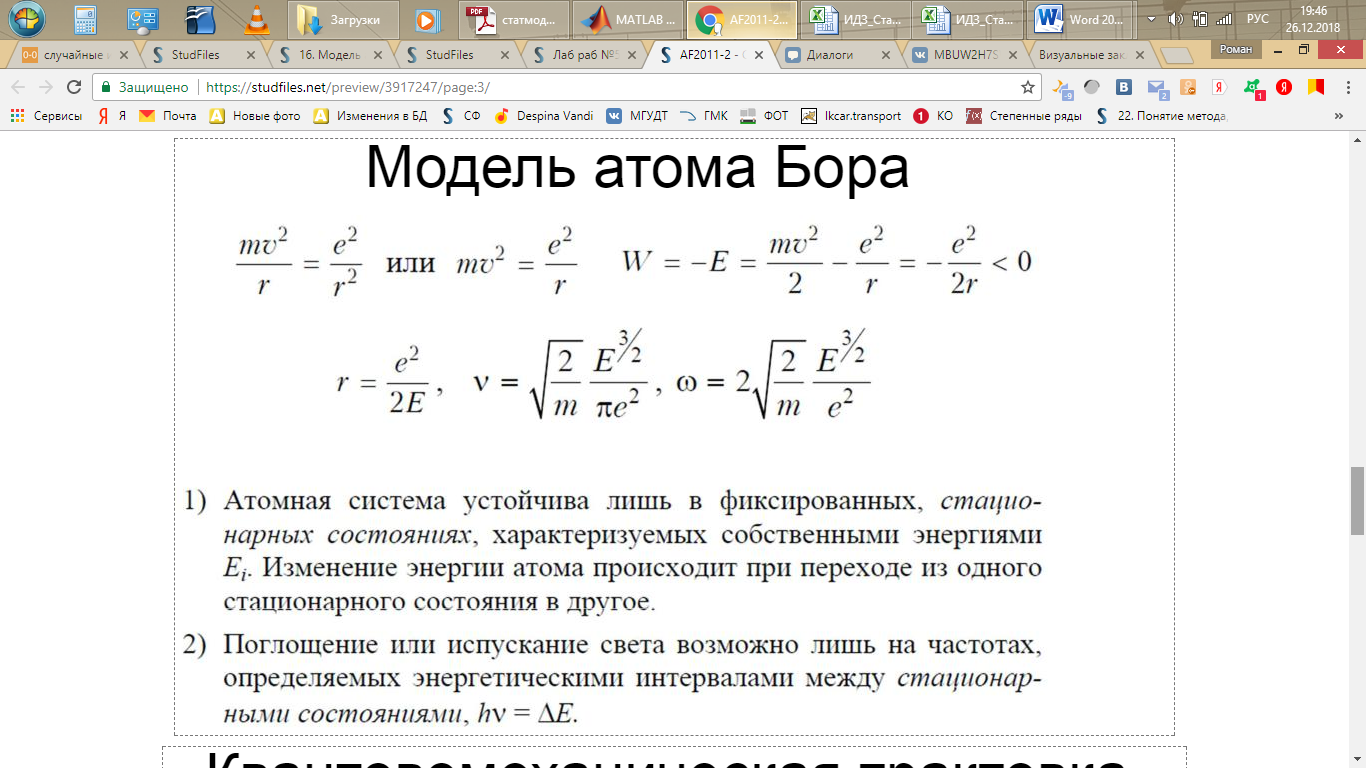
Первый постулат Бора (постулат стационарных состояний). В атоме существуют стационарные (не изменяющиеся со временем) состояния, в которых он не излучает энергии. Стационарным состояниям атома соответствуют стационарные круговые орбиты, по которым движутся электроны. Движение электронов по стационарным орбитам не сопровождается излучением электромагнитных волн.
В стационарном состоянии атома электрон имеет дискретные значения момента импульса, удовлетворяющие условию
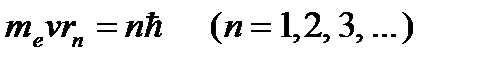 , где
, где 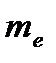 – масса электрона, v – его скорость по n-й орбите радиуса
– масса электрона, v – его скорость по n-й орбите радиуса 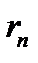 .
.
Второй постулат Бора (правило частот). При переходе электрона с одной стационарной орбиты на другую излучается (поглощается) один фотон с энергией
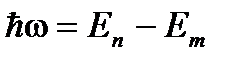 , (2)
, (2)
где 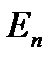 и
и 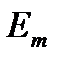 – соответственно энергии стационарных состояний атома до и после излучения (поглощения). Набор возможных дискретных частот
– соответственно энергии стационарных состояний атома до и после излучения (поглощения). Набор возможных дискретных частот 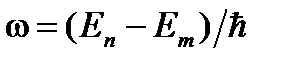 квантовых переходов и определяет линейчатый спектр атома.
квантовых переходов и определяет линейчатый спектр атома.
Теория Бора позволила разрешить очень важный вопрос о расположении электронов в атомах различных элементов и установить зависимость свойств элементов от строения электронных оболочек их атомов. В настоящее время разработаны схемы строения атомов всех химических элементов. Однако, иметь ввиду, что все эти схемы это лишь более или менее достоверная гипотеза, позволяющая объяснить многие физические и химические свойства элементов.
Теория Бора подошла к выяснению структуры отдельных атомов и установлению связи между ними. Однако оставалось еще много явлений в этой области, объяснить которые теория Бора не могла.
Движение электронов в атомах Бор представлял как простое механическое, однако оно является сложным и своеобразным.
И так, электрон в атоме характеризуется:
Главным квантовым числом n, указывающим на энергию электрона;
Орбитальным квантовым числом l, указывающим на характер орбиты;
Магнитным квантовым числом, характеризующим положение облаков в пространстве;
И спиновым квантовым числом, характеризующим веретенообразное движение электрона вокруг своей оси.
Исследование спектров атомов водорода обнаружили излучение водорода в ультрафиолетовой (Лайман) и инфракрасной (Пашен, Брэкет, Пфунд) областях спектра. Причем все эти линии располагаются сериями.
Дата: 2019-02-25, просмотров: 388.