Различают гормоны-белки, пептиды, производные аминокислот и стероидные гормоны. Первые из них могут быть простыми белками (инсулин, соматотропин, липотропин, пролактин и др.) или гликопротеинами (фоллитопин, лютеотропин, тиреотропин и др.). Пептидами являются глюкагон, кортикотропин, кальцитонин, вазопрессин, окситоцин и др., а производными аминокислот – норадреналин, адреналин, тироксин, меланотонин и др. К стероидным относят гормоны коры надпочечников (кортизон, кортизол, альдостерон и др.) гормонам и половых желез (тестостерон, прогестерон, эстрон, эстриол и эстрадиол).
Гормоны передней гипофиза (тропные гормоны) вырабатываются под действием релизинг-гормонов гипоталамуса. Током крови они доставляются к другим железам внутренней секреции и инициирующие выработку в них рабочих гормонов, непосредственно оказывающих влияние на метаболизм в различных органах.
Соматотропин (гормон роста, диабетогенный, диуретический фактор) – белок, обладающий видовой специфичностью. Поступая с током крови в печень и почки, инициирует выработку в них соматомединов (посредников). Последние обладают анаболичным эффектом – усиливает биосинтез ДНК,
иРНК и белка в рибосомах. Особенно активен он в соединительной ткани, где усиливает биосинтез коллагена. При усиленной выработке соматотропина у молодняка развивается гигантизм, а у взрослых животных – акромегалия (увеличение конечностей, хрящей ушей и губ). Может развиться диабетоподобное состояние: гипергликемия, усиленное выведение воды из организма. При сниженной выработке развивается карликовость.
Кортикотропин – пептид, состоящий из 39 аминокислот. Участвует в развитии стрессорной реакции организма. Воздействует по мембранно-цитозольному механизму через цАМФ на клетки коркового слоя надпочечников, где усиливает расщепление эфиров холестерина до свободного холестерола. Последний поступает в митохондрии, где происходит превращение его в глюко- и минералокортикоиды.
Лактотропин (пролактин) – крупный белок, состоящий из 199 аминокислот, собранных в одну полипептидную цепь с тремя дисульфидными связями. Основное действие его – развитие молочных желез и поддержание выработки ими молока. Другие функции - стимулирует рост внутренних органов, секрецию желтого тела, кроветворение, функцию почек, увеличивает концентрацию глюкозы в крови и др. Концентрация пролактина в крови самок резко увеличивается перед родами.
Тиреотропин – гликопротеин, состоящий из двух субъединиц, не обладающих биологической активностью по отдельности. Контролирует развитие, функцию щитовидной железы, захват ее фолликулами иода, выработку и инкрецию тироксина и других тиреоидных гормонов.
Гонадотропные гормоны (гонадотропины) являются гликопротеинами. К ним относят фолликулостимулирующий гормон (фоллитропин), стимулирующий созревание фолликулов у самок и сперматогенез у самцов, и лютеинизирующий гормон (лютропин), стимулирующий интерстициальные клетки. Последний у самок усиливает секрецию эстрогенов и прогестерона, разрыв фолликулов с образованием желтого тела, а у самцов – секрецию тестостерона и развитие интерстициальной ткани.
Липотропины – два белка, β- и γ-липотропин, каждый из которых состоят из 91 аминокислотных остатков. Первый из них усиливает мобилизацию жира из его депо, выработку гормонов коркового слоя надпочечников, средней доли гипофиза, стимулирует, как и инсулин, потребление глюкозы клетками, но снижает концентрацию кальция в крови. Липотропный эффект осуществляется по мембрано-цитозольному механизму: цАМФ активирует протеинкиназу, она – липазу, расщепляющую ацилглицеролы жировых депо до глицерола и жирных кислот. При сниженной выработке липопротеинов развивается ожирение, при повышенной – кахексия (истощение).
Гормоны промежуточной доли гипофиза (эпифиза)- α- и β- меланоцитостимулирующие гормоны. Первый из них у многих животных состоит из 13 аминокислотных остатков, второй – из 18. Физиологическая роль их заключается в регуляции выработки пигмента меланина в пигментных клетках кожных покровов. Они также влияют на число и размер клеток- меланоцитов, окраску меха, кожных покровов, секреторную функцию сальных желез. β- меланоцитостимулирующий гормон влияет также на функцию клеток коркового слоя надпочечников, но в меньшей степени, чем кортикотропин.
Гормоны задней доли гипофиза, окситоцин и вазопрессин, синтезируются в гигипоталамусе. Оттуда они перемещаются в заднюю долю гипофиза, затем инкретируются в кровяное русло и доставляются к клеткам-мишеням. Оба являются пептидами, незначительно отличающимися по аминокислотному составу, состоящими из остатков 8 аминокислот, в которых между первым и шестым остатками цистеина имеется дисульфидная связь.
Окситоцин по мембрано-цитозольному механизму через цАМФ и протеинкиназу усиливает сокращение гладкой мускулатуры матки во время родов. При этом расслабляет гладкие мышцы сосудов, вызывая кратковременное снижение артериального давления. После родов сокращает миоэпителиальные клетки вокруг альвеол молочной железы, способствуя кормлению животного. Используется в ветеринарной практике для стимуляции родовой деятельности, при атонии матки и маточных кровотечениях.
Вазопрессин связывается с рецепторами почечных канальцев. По мембрано-цитозольному механизму через цАМФ и протеинкиназу он запускает каскад реакций, приводящих к усилению обратного всасывания из них воды. Регулирует содержание воды в организме. При недостаточной выработке вазопрессина развивается несахарный диабет. Признаки его: выделение большого количества светлой мочи с низкой плотностью, не содержащей глюкозу.
Гормоны поджелудочной железы. Данная железа – железа со смешанной секрецией: вырабатывает пищеварительные ферменты тонкого кишечника и гормоны, поступающие в кровь под действием импульса, поступающего прямо из центральной нервной системы. α-клетки ее вырабатывают глюкагон, а β-клетки - инсулин.
Глюкагон – пептид, состоящий из 29 аминокислот. При снижении концентрации глюкозы в крови импульс из центральной нервной системы поступает к α-клеткам поджелудочной железы и индуцирует выработку в них проглюкагона, содержащего на С-конце молекулы пептид из восьми аминокислот. После отщепления последнего образуется активный глюкагон. Он доставляется током крови к клеткам печени, на которые действует по мембрано-цитозольному механизму: через цАМФ и протеинкиназу
Последняя активирует гликогенфосфорилазу, присоединяя к ней остаток фосфорной кислоты, и запускается процесс расщепления гликогена и поступление глюкозы в кровь. Глюкагон способен увеличивать концентрацию глюкозы в крови и другим путем. Он увеличивает интенсивность реакции глюконеогененза, индуцируя по мембрано-цитозольному механизму биосинтез ключевых ферментов этого метаболического пути.
Инсулин усиленно вырабатывается в ответ на увеличение концентрации глюкозы в крови в виде проинсулина, состоящего из остатков 84-х аминокислот. Затем от него отщепляется С-пептид, состоящий из остатков 33-х аминокислот и образуется активный инсулин, состоящий из двух полипептидных цепей, связанных между собой двумя дисульфидными (-S-S-)
связями.
Механизм действия инсулина:
1. Оказывает эффект по мембранному механизму. Связываясь с рецептором мембраны, вызывает изменения третичной структуры белков транспортных систем. После этого в клеточную оболочку встраиваются каналы, через которые глюкоза и аминокислоты поступают в цитоплазму.
2. Усиливает откладывание поступившей в печень глюкозы в гликоген, активируя гликогенсинтазу.
3. Стимулирует аэробное окисление глюкозы в клетках, активируя ключевые ферменты гликолиза (гексокиназу, фосфофруктокиназу и пируваткиназу) и цикла Кребса.
4. Усиливает реакции пентозного цикла, активируя глюкозо-6-фосфатдегидрогеназу, выработку в нем НАДФ-Н2.
5. Стимулируя выработку ацетил-КоА и НАДФ-Н, усиливает биосинтез липидов, тормозя при этом их гидролиз в жировых депо.
6. Тормозит реакции глюконеогенеза (превращение аминокислот в углеводы).
Сахарный диабет первого типа развивается при недостаточной выработке поджелудочной железой инсулина, второго типа – при сниженной чувствительности к этому гормону его рецепторов. Нарушается поступление глюкозы в клетки, откладывание в гликоген печени, окисление в клетках и концентрация ее в крови увеличивается (гипергликемия). Если она становится выше 15 ммоль/л, возможно выделение глюкозы с мочой (глюкозурия).
В условиях длительной гипергликемии остатки глюкозы присоединяются к молекуле гемоглобина, образуется гликозилированный гемоглобин. Гипергликемия приводит к повышению осмотического давления крови, ощущению в чувства жажды (полидипсия). Животное потребляет много воды, что сопровождается выделение большого количества мочи (полиурия). Окраска мочи более светлая, чем у здоровых животных. При поступлении в мочу глюкозы увеличивается ее плотность.
В условиях гипергликемии глюкоза повреждает стенки кровеносных сосудов, развивается атеросклероз. Из-за этого в крови увеличивается концентрация триглицеридов, преβ- и β-липопротеинов, холестерина β-липопротеинов на фоне снижения уровня α-липопротеинов и фосфоглицеридов.
Несмотря на развившуюся гипергликемию, клетки обеспечены глюкозой в недостаточной степени, развивается энергодефицит. Он восполняется за счет усиленного окисления аминокислот, что приводит к отщеплению аммиака и повышенному обезвреживанию его в орнитиновом цикле в мочевину. Содержание последней увеличивается в крови (продукционная гиперазотемия) и моче (гиперазотурия).
Развившийся дефицит глюкозы в клетках компенсируется и за счет усиления в печени β-окисления жирных кислот с последующим увеличением в крови концентрации ацетоуксусной кислоты (гиперкетонемия), что приводит к закислению ее (кетоацидоз). Этому способствует также недостаточно эффективное окисление ацетоуксусной кислоты в цикле Кребса вследствие снижения в клетках уровня первого метаболита его – щавелево-уксусной кислоты.
Эта кислота генерируется из пировиноградной кислоты, образующейся при окислении глюкозы. Клетки обеспечены последней в недостаточной степени. В этих условиях ацетоуксусная кислота превращается в другие разновидности кетоновых тел – β-гидроксимасляную кислоту и ацетон. Все вместе они поступаю в мочу (кетонуря). Прогрессирование этих явлений может привести к потери сознания (диабетическая кома), гибели животного.
Лекция №15.
ЭНДОКРИННАЯ СИСТЕМА (продолжение).
План.
1. Гормоны надпочечников.
2. Гормоны половых желез.
3. Гормоны щитовидной и паращитовиных желез
Гормоны мозгового слоя надпочечников, норадреналин и адреналин, вырабатываются из аминокислоты тирозин, подвергающейся реакциям гидроксилирования, декарбоксилирования и метилирования. Этот процесс усиливается при стрессовых ситуациях. Выброс в кровь этих гормонов приводит не только к сужению периферических сосудов, расширению их в жизненно важных органах, но и к изменению метаболизма.
Адреналин, как и глюкагон, действуя по мембранно-цитозольному механизму, активирует гликогенфосфорилазу печени, усиливая расщепление гликогена и поступление глюкозы в кровь. Действие первого из них более кратковременное, но сильнее, приводящее к «залповому» увеличению концентрации глюкозы в крови. Гипергликемический эффект норадреналина ниже. Он больше функционирует как нейромедиатор в нервной ткани.
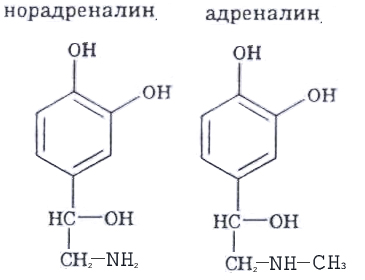
В мышцах адреналин стимулирует анаэробное окисление гликогена до молочной кислоты, способствуя усилению их сокращения. В жировых депо адреналин, активируя липазу, усиливает липолиз ацилглицеролов до глицерола и жирных кислот. Последние являются основным источником энергии для клеток миокарда.
Гормоны коркового слоя надпочечников. Выработка их запускается нервным импульсом, инициирующим высвобождение в гипоталамусе релизинггормона кортиколиберина. Последний поступает в переднюю долю гипофиза, где по мембрано-цитозольному механизму через цАМФ запускает выработку кортикотропина. Он током крови доставляется к клеткам коркового слоя надпочечников, где также по мембрано-цитозольному механизму через цАМФ запускает биосинтез из холестерола около 50 кортикостероидов. Главными из них являются регуляторы углеводного обмена (глюкокортикоиды) кортизол, кортикостерон и регуляторы минерального обмена (минералокортикоиды) альдостерон и дезоксикортикостерон. Они током крови доставляются к клеткам-мишеням и и по цитозольному механизму запускают биосинтез ряда биологически активных веществ.
Кортизол и другие глюкокортикоиды усиленно вырабатываются при хроническом стрессе. В мышечной, лимфатической, соединительной и жировой тканях снижают проницаемость клеточных мембран и тормозят поступление в клетки глюкозы и аминокислот. В печени они не только оказывают противоположный эффект, но интенсифицируют реакции глюконеогенеза, усиливая биосинтез четырех ключевых ферментов этого процесса.
Глюкокортикоиды также тормозят окисление глюкозы в клетках и синтез из нее гликогена в мышцах. При этом они усиливают липолиз ацилглицеролов и окисление жирных кислот, способствуя таким образом лучшей сохранности фонда углеводов в организме. В конечном итоге все это приводит к развитию гипергликемии, благоприятствуя таким образом лучшей обеспеченности в условиях стресса жизненно важных органов энергетическими субстратами.
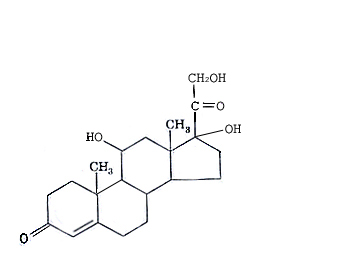
Глюкортикоиды также обладают противоаллергическим и противовоспалительным эффектом и широко применяются для лечения больных бронхиальной астмой, системной красной волчанкой, ревматоидным артритом, дерматозами и другими хроническими заболеваниями.
Альдостерон и другие минералокортикоиды регулируют главным образом водно-солевой обмен в организме. Они способствуют удержанию в тканях ионов натрия, хлора, вместе с ними воды и выведению с мочой ионов калия. Это связывают с влиянием на обратное всасывание ионов натрия, хлора в канальцах почек в обмен на выведение этими органами других продуктов обмена веществ, в частности мочевины.
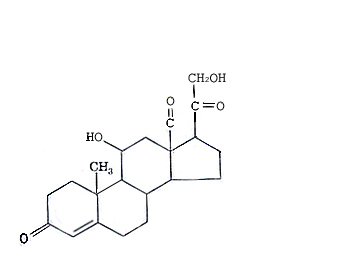
Половые гормоны синтезируются из холестерола в основном в яичниках у самок и семенниках у самцов. Некоторое количество их может синтезироваться и в плаценте и корковом слое надпочнчников.
Половые гормоны у самок. В фолликулах яичников в первую фазу полового цикла продуцируются в основном эстрогены: эстрадиол, эстрон (фолликулин) и эстриол. Во вторую фазу полового цикла в желтом теле беременности вырабатываются преимущественно прогестины, в частности прогестерон. Биосинтез этих гормонов запускают гонадотропные гормоны гипофиза (фоллитропин и лютропин), действующие по мембрано-цитозольному механизму через цАМФ и протеинкиназу. Синтезированные эстрогены током крови доставляются к различным органам, где оказывают анаболическое действие, стимулируя биосинтез белка.
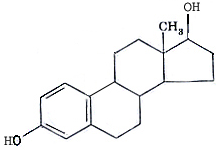

Эстрадиол
Прогестерон
Основная биологическая функция эстрогенов и прогестинов, синтез которых усиливается после наступления половой зрелости, заключается в обеспечении репродуктивной функции организма самки. Они регулируют развитие вторичных половых признаков, создают оптимальные условия для оплодотворения яйцеклетки после овуляции.
Специфической функцией прогестерона является подготовка слизистой оболочки матки к имплантации яйцеклетки после оплодотворения, а при наступлении беременности – сохранение ее. При этом прогестерон тормозит овуляцию и стимулирует развитие тканей молочной железы.
Гормоны плаценты вырабатываются во время беременности. В этом органе, начиная с первых дней беременности, синтезируется хорионический гонадотропин, который регулирует развитие у плода половой системы, синтез гормонов фетоплацентарного комплекса, прогестерона в желтом теле, гестагенов и эстрогенов. Плацента не может синтезировать стероидные гормоны одна, а вырабатывает их совместно с организмом плода. Они образуют фетоплацентарный комплекс. Исходный материал – холестерин - поставляется организмом матери, в плаценте происходит последовательное превращение холестерола в прегнолон и прогестерон. Дальнейшее превращение последнего происходит только в тканях плода. Плацента также вырабатывает хорионические лактотропин, тиреотропин и релаксин.
Половые гормоны самцов вырабатываются в семенниках, а также в небольших количествах в надпочечниках и яичниках. Главным из них является прогестерон. Биосинтез этих гормонов также запускают гонадотропные гормоны гипофиза (фоллитропин и лютропин), действующие по мембрано-цитозольному механизму через цАМФ и протеинкиназу. Продуцируются половые гормоны уже у эмбриона, влияя на дифференцировку тканей, развитие половых органов, скелета и других структур, определяют характер секреции их после рождения.
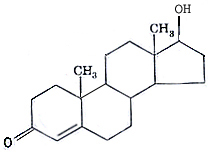
Тестостерон
Во взрослых животных регулируют развитие вторичных половых признаков, половое поведение, сперматогенез в семенниках и т.д. Обладают значительным анаболическим эффектом, выражающимся в стимуляции биосинтеза белков в различных тканях, особенно в скелетных мышцах. Для реализации этого эффекта необходима параллельная выработка соматотропина.
Гормоны щитовидной железы вырабатываются после поступления в гипоталамус импульса от коры головного мозга. Там вырабатывается релизинггормон тиреолиберин, поступающий в дальнейшем в переднюю долю гипофиза и инициирующий выработку в ней тиреотропина. Последний током крови доставляется в щитовидную железу. В фолликулах ее содержится аминокислота тирозин, которая имеется в составе особого иодсодержащего гликопротеина иодтиреоглобулина. Тиреотропин инициирует выработку из тирозина гормонов трииодтронина, обладающего наибольшей активностью, тетраиодтиронина (тироксина) и дииодтиронина.
Эти гормоны током крови переносятся в желудок, кишечник, печень, сердце, почки, скелетные мышцы и другие органы. Воздействуя на их клетки цитозольному механизму, они усиливают процессы транскрипции и, как следствие, биосинтез ферментов энергетического обмена и других белков. Они влияют на обмен веществ, стимулируя потребление тканями энергетических ресурсов, кислорода, повышают эффективность Na+/K+-АТФазного насоса, регулируют размножение, рост и дифференцировку клеток.
Усиленная выработка тиреоидных гормонов отмечается при Базедовой болезни, что проявляется в интенсификации основного обмена, учащенном сердцебиении и повышении артериального давления. Снижается их инкреция при эндемическом зобе, микседеме, при которых интенсивность метаболизма снижена, а скорость сердцебиения и артериальное давление уменьшены.
Гормоны паращитовидных желез – полипептиды паратгормон и кальцитонин. Второй из них синтезируется также клетками щитовидной железы.
Паратгормон синтезируется под воздействием импульса из коры головного мозга в виде предшественника, состоящего из 115 аминокислотных остатков. После отщепления с N-конца молекулы его 31 аминокислотного остатка образуется активный паратгормон. Током крови он доставляется в клетки костной ткани и почек, на которые воздействует по мембрано-цитозольному механизму через выработку фосфолипазой С фосфоинозитолтрифосфата и диацилглицерола. Эти вторичные посредники усиливают поступление в кровь ионов кальция за счет стимулирования рассасывания костей и обратного всасывания этого иона из почечных канальцев. При этом он усиливает выведение почками с мочой ионов фосфата. После оказания эффекта паратгормон инактивируется ферментами крови.
Кальцитонин синтезируется под воздействием импульса из коры головного мозга также в виде предшественника, состоящего из 136 аминокислотных остатков. В результате пострансляционного процессинга образуется активный кальцитонин, состоящий из 32 аминокислотных остатков. Данный гормон является антагонистом паратгормона. Доставляясь током крови в клеткам костной ткани и воздействуя на них по мембрано-цитозольному механизму через выработку цАМФ. Он тормозит рассасывание матрикса кости, снижая тем самым высвобождение ионов кальция и фосфата и поступление их в кровь.
Кальцитонин также влияет на метаболизм фосфата, способствуя поступлению его в клетки кости и периостальную жидкость. При этом вместе с фосфатом в костную ткань поступают и ионы кальция. Тем самым тормозится поступление последних из костной ткани в кровь. Кальцитонин тормозит в остеокластах биосинтез белка остеопорина, ответственного за использование кальция для образования костей, т.е. он фактически способствует формированию остеопороза.
Снижение выработки гормонов паращитовидных желез, особенно паратгормона, наблюдается при вторичной остеодистрофии у жвачных животных, являющейся осложнением кетоацидоза. Клетки этих желез весьма
чувствительны к закислению кетоновыми телами, приводящему к усилению катаболизма пуриновых мононуклеотидв с последующей интенсификацией липипероксидации в них мембранных структур
Лекция №16
Витамины
План
1. Классификация витаминов.
2. Гиповитаминозы
3. Жирорастворимые витамины.
4. Водорастворимые витамины.
5. Витаминоподобные вещества.
Витамины – низкомолекулярные органические соединения, необходимые для жизнедеятельности организма, но не синтезирующиеся в нем или синтезирующиеся в недостаточных количествах и поэтому поступающие в малых количествах с пищей или от микроорганизмов, базирующихся в органах пищеварительной системы.
Еще в 1880 г. Н.И. Лунин доказал, что, кроме белков, углеводов, липидов, воды и минеральных веществ, организму необходимы дополнительные вещества. К. Функ выделил из рисовых отрубей одно из таких веществ, витамин В1, содержащий аминогруппу. Поэтому он предложил называть эти вещества витаминами (vita – жизнь). Потом оказалось, что не все витамины содержат аминогруппу.
Классификация витаминов. Из делят на 2 группы: жиро- и водорастворимые. У каждого витамина имеется 3 названия: буквенное, клиническое и химическое. Существуют еще ряд витаминоподобных веществ, не подходящих по какому-то из признаков к понятию «витамины». При отсутствии поступления витаминов развиваются авитаминозы, при сниженном поступлении – гиповитаминозы. При чрезмерном поступлении некоторых витамино (А, Д и др.) возможны гипервитаминозы.
Причины гиповитаминозов.
А. Экзогенныегиповитаминозы развиваются при:
1) отсутствии определенных продуктов питания: свежих овощей, мяса, жиров и т.д.;
2) потери витаминов при хранении, обработке продуктов, приготовлении пищи и т.д.
Б. Эндогенныегиповитаминозы развиваются при:
1) недостаточно эффективном поступлении витаминов из кишечника при воспалении его, а также из-за нарушения поступление в него желчных кислот при патологии печени и перекрытии желчевыводящих путей, приводящего к снижению гидролиза и всасывания липидов с растворенными в них витаминами;
2) гибели микроорганизмов пищеварительного тракта при кормлении высоко концентратными кормами, лечении антибиотиками и от других причин;
3) нарушении транспорта витаминов кровью при снижении содержания в ней некоторых белков;
4) нарушении превращения провитаминов в витамины при недостаточном ультрафиолетовом облучении, отсутствии ферментов, осуществляющих это превращение;
5) поступлении в организм антивитаминов.
Жирорастворимые витамины.
Витамин А (антиксерофтальмический); ретинол.
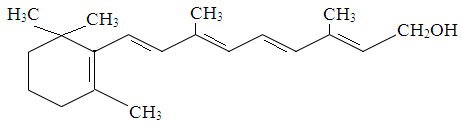
Биологическая роль витамина А:
1. Является компонентом биологических мембран, способствует биосинтезу их углевод-белковых комплексов, стабилизирует структуру клеток, особенно эпителиальных, поддерживает барьерную функцию их.
2. Обладает антиоксидантными свойствами.
3. Регулирует рост, дифференциацию тканей, развитие организма в целом, особенно организма молодняка.
4. Поддерживает функцию иммунной системы.
5. Входит в состав родопсина (зрительного пурпура) колбочек и палочек сетчатки глаза. Под действием света родопсин расщепляется на белок опсин и ретинальдегид (производное витамина А), что приводит к генерации светового импульса.
Суточная потребность (для человека) – 2,3 мг.
Продукты, богатые витамином А: рыбий жир, печень, молочные продукты, яичный желток и др. Каротин (предшественник витамина А, состоящий из двух остатков его) содержится в моркови и других коренеплодах, зеленых листьях, сочных кормах и т.д. В организме животного каротин расщепляется до витамина А каротиназой.
Проявления гиповитаминоза А:
Первые проявления его – ухудшение зрения в темноте (куриная слепота). Замедляется рост и развитие организма. Снижается иммунитет. Из-за нарушения барьерной функции эпителия поражаются слезные протоки, слеза не проходит к роговице глаза и она размягчается (ксерофтальмия). Поражается также эпителий дыхательных, мочеполовых путей, кожи и других структур, что приводит к их воспалению.
Витамины группы Д (антирахитические); кальциферолы (эргокальциферол и холекальциферол) Предшественником первого из них является эргостерин, который после облучения ультрафиолетовыми лучами превращается в эргокальциферол (витамин Д2). В коже содержится второй провитамин Д, который также после облучения ультрафиолетовыми лучами превращается в холекальциферол (витамин Д3). Обо витамина поступают в печень, где у них 25-й атом углерода подвергается гидроксилированию под действием 25-гидроксилазы, а затем – в почки. В последней под действием 1-гидроксилазы гидроксилируется еще и первый атом углерода и образуются 1,25-дигидрокальциферолы, обладающие биологической активностью. При недостаточной активности 25- и 1- гидроксилазы развивается Д-резистентный рахит.
Суточная потребность (у человека)- 10-25 мкг.
Дата: 2019-02-02, просмотров: 409.