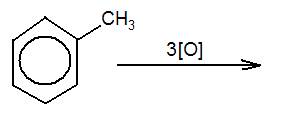
В пробирку с 5 каплями воды (I) поместите 1 каплю 0,1 Н КМпО4 (101) и 1каплю 2 Н H2SO4 (27). Добавьте 1 каплю толуола С6Н5СН3 (93) и энергично встряхивая, нагревайте над пламенем горелки. Какие изменения наблюдаются при нагревании?

В результате окисления каждая боковая цепь в кольце бензола, независимо от её длины образует карбоксильную группу. Поэтому, пользуясь реакцией окисления боковых цепей, можно установить наличие боковых цепей в ароматических углеводородах.
Допишите уравнение реакции окисления толуола:
Выполнение работы проверил(а)
 |
Дата:
 |
Лабораторная работа №2
Тема: Химические свойства спиртов и фенолов.
Опыт №1. Окисление этилового спирта хромовой кислотой.
В пробирку внесите 2 капли этилового спирта (на общем столе). Добавьте 1 каплю 2Н H2SO4 (27) и 2 капли 0,5Н К2Сг2О7 (18). Полученный оранжевый раствор нагрейте над пламенем горелки до начала изменения его окраски. Обычно, уже через несколько секунд, цвет раствора становится синевато-зелёным. При этом осуществляются следующие химические превращения:
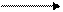 K2Cr2O7 + H2SO4 H2Cr2O7 + K2SO4
K2Cr2O7 + H2SO4 H2Cr2O7 + K2SO4
 H2Cr2O7 2CrO3 + H2O
H2Cr2O7 2CrO3 + H2O
 2CrO3 Cr2O3 + 3O (идет на окисление спирта)
2CrO3 Cr2O3 + 3O (идет на окисление спирта)
Одновременно происходит образование сульфата хрома (III) сине-зеленого цвета:
 Cr2O3 + H2SO4 Cr2(SO4)3 + H2O
Cr2O3 + H2SO4 Cr2(SO4)3 + H2O
1 .Напишите уравнение реакции окисления этилового спирта кислородом до уксусного альдегида.
2.Объясните, почему раствор в процессе реакции приобрёл сине-зелёную
окраску?

Опыт№2. Реакция глицерина с гидроксидом меди ( II ) в щелочной среде.
Поместите в пробирку 3 капли 0,2 Н CuSO4 (19), 3 капли 2 Н NaOH (2) и взболтайте. Появляется голубой студенистый осадок гидроксида меди (II):
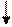
 CuSO4 + 2NaOH Cu(OH)2 + Na2SO4
CuSO4 + 2NaOH Cu(OH)2 + Na2SO4
Нагрейте пробирку над пламенем горелки. При нагревании в щелочной среде до кипения полученный гидроксид меди (II) разлагается. Это видно по выделению чёрного осадка оксида меди (II):

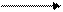 Cu(OH)2 CuO + H2O
Cu(OH)2 CuO + H2O
Вновь получите осадок гидроксида меди(II),как было описано выше. Но перед кипячением полученного Сu(ОН)2 добавьте в пробирку 1 каплю глицерина (22) и взболтайте.
Что происходит с осадком при взбалтывании? Как меняется цвет раствора?

Нагрейте полученный раствор до кипения и убедитесь в том, что при этом гидроксид меди (II) не разлагается и чёрный осадок оксида меди(II) не выделяется. В этом случае образуется хелатное соединение - глицерат меди, которое при нагревании не разрушается.
Напишите уравнение реакции взаимодействия глицерина с гидроксидом меди (II) в щелочной среде с образованием хелатного комплекса.
Щелочной раствор глицерата меди под названием реактива Гайнеса применяется в клинических лабораториях для открытия глюкозы в моче.
Дата: 2019-02-02, просмотров: 664.