Задача № 73. Исходный расплав содержит 20 % А, 10 % В; 70 % С. Определить: 1) фазовое равновесие системы при температуре 1200 оС; 2) температуру окончания затвердевания расплава и состав эвтектических кристаллов.
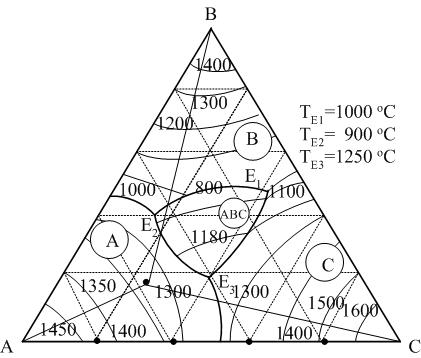
Рис. 14. Диаграмма состояния трехкомпонентной системы с тройным
химическим соединением ABC, плавящимся инконгруэнтно
Задача № 74. Расплав какого состава необходимо взять, чтобы при его закалке от температуры 1050 °С получить систему, состоящую из 26 % кристаллов В, 52 % кристаллов ABC и 22 % стекла.
Задача № 75. Дана твердая смесь, содержащая 33,5 % кр. А и 66,5 % кр. ABC. Определить: 1) температуру начала и конца плавления этой смеси;
2) фазовый состав системы при температуре 1350 °С.
Задача № 76. Расплав какого состава необходимо взять, чтобы выполнялись следующие требования: 1) первично выпадающими в системе кристаллами были бы кристаллы компонента А; 2) при 1180 °С из расплава должны выделяться кристаллы ABC, a кристаллы А исчезать в результате химической реакции с расплавом; 3) в тот момент, когда в системе начнут выделяться кристаллы С, система станет трехфазной, причем соотношение двух выделившихся твердых фаз С и ABC будет 1:2.
Задача № 77. Дана твердая смесь, содержащая 19 % кристаллов В, 26 % кристаллов С и 55 % кристаллов ABC. Определить, во сколько раз увеличится количество расплава в этой смеси при ее нагревании от 1100 до 1200 °С. Каким будет состав жидкой фазы при температуре начала плавления этой смеси?
Задача № 78. Необходимо получить кристаллический продукт, состоящий из 65 % крупных, хорошо оформленных кристаллов компонента С и 35 % мелкокристаллической смеси кристаллов В, С и АВС. Какой исходный состав расплава необходимо для этого взять, при какой температуре начнется и закончится его кристаллизация?
Задача № 79. Исходный состав содержит 45 % А, 20 % В, 35 % С. От какой температуры необходимо закалить смесь указанного состава, чтобы получить продукт, состоящий из 9 % кристаллов С, 75 % кристаллов ABC и стекла? При какой температуре начнется кристаллизация указанного расплава и какие фазы будут в равновесии при 1250 °С?
Задача № 80. Твердая смесь содержит 32,5 % А, 17,5 % С и 50 % ABC. Определить температуру начала и конца плавления этой смеси и количественное соотношение фаз в тот момент, когда система становится двухфазной.
Задача № 81. Исходный расплав содержит 30 % А, 40 % В и 30 % С. Определить фазовое равновесие при температуре 1100 °С и состав жидкой фазы в момент кристаллизации расплава эвтектического состава.
Задача № 82. Какой исходный состав твердой смеси, состоящей из кристаллов С и ABC, необходимо взять, чтобы после того, как система станет трехфазной, она содержала бы 10 % кристаллов А и 40 % кристаллов С? При какой температуре начнется и закончится плавление этой смеси ?
4.7. Система СаО – А l 2 O 3 – SiO 2
Задача № 83. Оценить, какой из двух огнеупоров, имеющих состав 53,4 % Аl2O3, 46,6 % SiO2 и 42,2 % Аl2O3, 57,8 % SiO2, будет иметь большее количество твердой фазы при нагревании до температуры 1600 °С по отношению к флюсующему действию шлака, имеющего в своем составе 50 % СаО, 20 % Аl2О3 и 30 % SiO2, если во взаимодействие вступает 10 % шлака и 90 % огнеупора.
Задача № 84. Алюмосиликат кальция имеет состав 80 % Аl2О3, 20 % SiО2. Определить количество расплава, образующегося при температуре 1710 °С при его взаимодействии со шлаком состава: 25 % CaO, 28 % Al2O3 и 47 % SiO2, если во взаимодействие вступает 20 % шлака и 80 % огнеупора.
Задача № 85. Динасовый огнеупор содержит 3 % СаО, 2 % Аl2О3 и остальное SiO2 остальное. Определить, при какой температуре в огнеупоре появится жидкая фаза и каков состав жидкой фазы будет при температуре 1400 °С.
Задача № 86. Шихта белого цемента содержит 67,5 % СаО, 2,5% Аl2О3 и остальное SiO2. Определить минералогический состав продукта обжига сырьевой смеси при температуре 1700 и 1800 оС.
Задача № 87. Химический состав гидравлической извести: 80 % СаО, 10 % Аl2О3, 10 % SiO2. Определите максимальную температуру нагрева камня этого материала, чтобы содержание расплава в нем не превышало 80 %. Содержание какого компонента: Аl2О3 или SiO2, в расплаве будет больше?
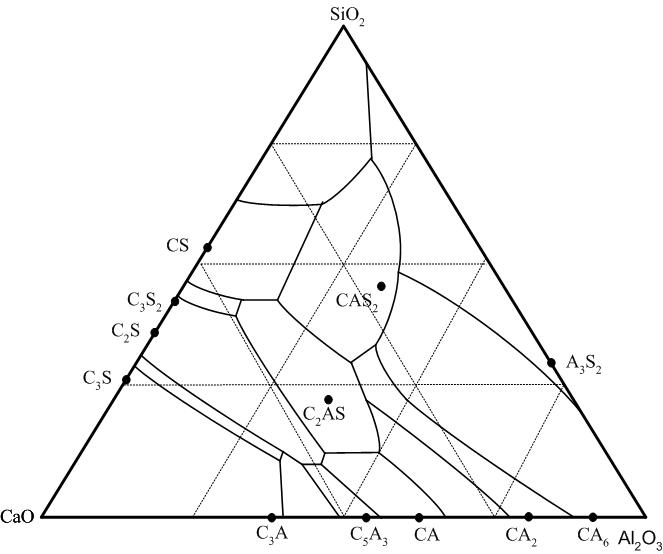
Рис. 15. Диаграмма состояния системы СаО – Аl2O3 – SiO2.
Температуры, соответствующие некоторым тройным точкам: S – CAS2 – A3S2 – 1345 °C; CAS2 – C2AS – CA6 – 1380 °С; CS – CAS2 – C2AC – 1265 °С; С3S – С2S – С3A – 1455 °С; C3S – C2S – C3A – 1310 °С
Задача № 88. Исходная смесь содержит 28, 5 % анортита и 71,5 % геленита. Определить, при какой температуре закончится плавление этой смеси и каков будет фазовый состав системы при температуре 1500 °С.
Задача № 89. Какой исходный состав системы необходимо взять, чтобы в продукте его кристаллизации подучить 34 % крупных кристаллов анортита и 66 % смеси мелкозернистых кристаллов анортита и кремнезема?
Задача № 90. Расплав при 2200°С имеет состав 80 % СаО, 14 % Аl2О3, 6 % SiO2. Как необходимо охладить расплав, чтобы получить продукт, содержащий 25 % стекла, и равные количества кристаллических фаз? Определить химический состав полученного стекла.
Задача № 91. При какой температуре из твердой смеси воллостанита, геленита и анортита, имеющий химический состав 40 % СаО, 30 % Аl2О3, можно получить продукт, имеющий в своем составе 40 % кристаллов геленита и 60 % расплава? Каков химический состав расплава?
4.8. Система MgO – А l 2 О3 – Si О2
Задача № 92. Температуру начала плавления исходной смеси, содержащей 20 % MgO, 50 % Аl2О3, 30 % SiО2, а также фазовое равновесие системы при температуре 1600 °С.
Задача № 93. В исходную массу, предназначенную для изготовления алюмомагнезиальной керамики, дополнительно ввели 60 % корунда и 40 % магнезиально-кремнеземистой фритты, содержащей 37,5 % MgO. При какой температуре обжига в системе образуется 22 % расплава и каков его химический состав?
Задача № 94. Как изменится температура начала плавления муллито-корундового огнеупора в процессе его эксплуатации, содержащего 19 % Аl2О3 за счет загрязнения массы добавкой оксида магния в количестве 9,5 %? Определить содержание расплава в этом огнеупоре при температуре 1680 °С.
Задача № 95. Определить температуру начала плавления твердой смеси, содержащей равное количество кордиерита и муллита.
Задача № 96. Состав расплава задан точкой на пограничной кривой, разделяющей поля кристаллизации муллита и кордиерита. Содержание кремнезема в расплаве при этом составляет 60 %. Определить фазовый состав системы при температуре 1400 °С.
Задача № 97. Как изменится температура начала плавления твердой смеси из равных количеств кристаллов форстерита и шпинели при введении в нее 10 процентов SiO2?
Задача № 98. Как изменится температура начала плавления в подвергаемой обжигу смеси из равных долей кристаллов форстерита и кордиерита при введении в нее добавки 20 % кристаллов клиноэнстатита.
Задача № 99. Определить температуры начала и окончания кристаллизации расплава, содержащего 25 % MgO, 65 % Аl2О3, 10 % SiO2. Каким будет соотношение количеств твердой фазы и расплава в системе в тот момент, когда кристаллы корунда, первоначально выпавшие в процессе кристаллизации расплава, полностью растворятся?
Задача № 100. Как повлияет примесь 10 % Аl2О3 на температуру появления жидкой фазы в форстеритовом огнеупоре?
Задача № 101. Из какого по составу расплава в результате его полной кристаллизации может быть получен материал, содержащий 42,6 % муллита, 31,5 %, сапфирина и 25,9 % кордиерита? Определить температуру начала и конца кристаллизации этого расплава.
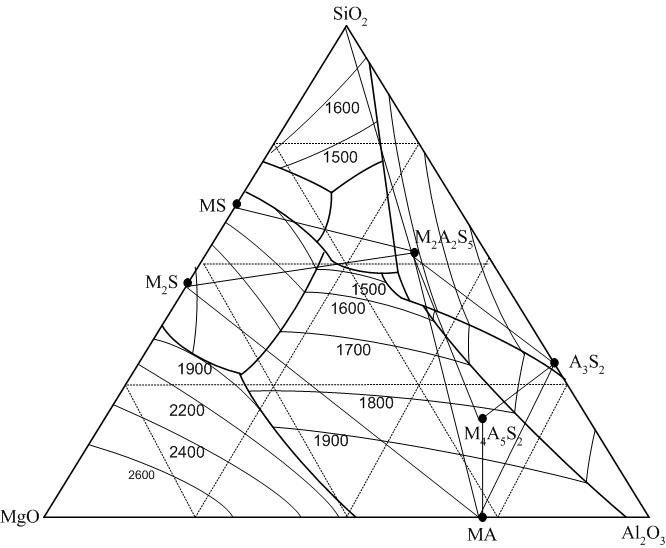
Рис. 16. Диаграмма состояния системы MgO – Аl2О3 – SiО2.
Температуры, соответствующие некоторым тройным точкам: MA – A3S2 – M4A5S2 – 1482 oC; A3S2 – M4A5S2 – M2A2S5 – 1460 oC; M2A2S5 – S – MS – 1355 oC; M2A2S5 – MA – MS – 1370 oC; M2S – MS – M2A2S5 – 1365 oC; MA – M4A5S2 – M2A2S5 – 1453 oC
БИБЛИОГРАФИЧЕСКИЙ СПИСОК
1. Физическая химия силикатов: Учебник для студентов вузов/ А.А. Пащенко, А.А. Мясников, Е.А. Мясникова и др. ; Под ред. А.А. Пащенко. – М.: Высшая школа, 1986. – 368 с.
2. Горбунов С.П. Физическая химия силикатов: Текст лекций. – Челябинск: ЧГТУ, 1996. –95 с.
З. Куколев Г.В.Химия кремния и физическая химия силикатов. –М.: Высшая школа, 1966. – 455 с.
4. Сборник вопросов и задач по физической химии для самостоятельного контроля: Учебное пособие для вузов/ А. Г. Атанасянц, С.Ф. Блевский, Г.С. Каретников и др.; Под ред. С.Ф. Блевского. – М.: Высшая школа, 1979. – 119 с.
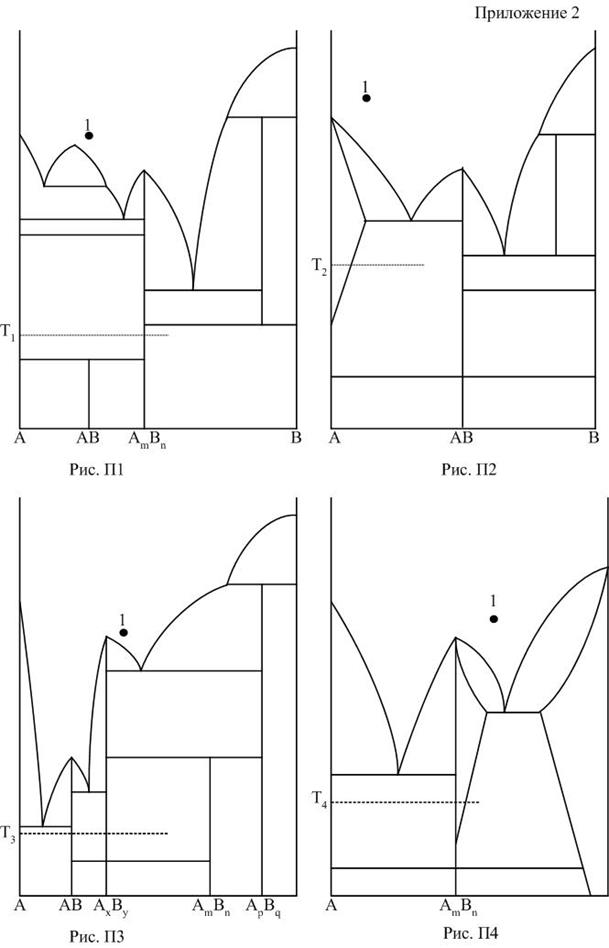
ПРИЛОЖЕНИЯ

Дата: 2018-11-18, просмотров: 910.