Основные положения теории, объясняющей механизм возбуждения и распространения взрыва, разработаны в конце XIX века профессором Московской сельскохозяйственной академии В.А. Михельсоном. В трудах ученых Л.Д. Ландау, Я.Б. Зельдовича, К.П. Станюковича и других теория взрыва нашла свое дальнейшее развитие.
В настоящее время физическая сущность механизма возбуждения взрыва при различных воздействиях сводится к следующему [3]. В результате диссипации энергии от механических воздействий во ВВ возникают местные разогревы («горячие точки»), в которых начинается горение ВВ вначале с небольшой скоростью. Затем, в зависимости от природы ВВ и внешних условий, это горение ускоряется и переходит во взрыв или затухает. Факторами, способствующими развитию взрыва, являются повышенная склонность ВВ к воспламеняемости, резкая зависимость скорости горения от давления, высокая детонационная способность. Такая схема процесса возбуждения взрыва при механических воздействиях экспериментально подтверждена работами Ф. Боудена, Д. Иоффе [4] и других исследователей.
Сущность механизма возникновения местных разогревов состоит в следующем:
1) очаги возбуждения реакции («горячие точки») при ударе или другом механическом воздействии возникают в результате адиабатического сжатия газовых пузырьков, находящихся во взрывчатом веществе;
2) в результате воздействия происходит неравномерное течение ВВ, при котором возникают силы трения между отдельными слоями ВВ, между ВВ и соударяющимися поверхностями, между частицами ВВ и находящимися в нем твердыми инородными частицами. Это трение и является причиной появления местных разогревов;
3) очаги возбуждения возникают также за счет вязкостного разогрева ВВ в результате быстрого выдавливания его из зазора соударяющимися поверхностями.
Дальнейшее развитие процесса распространения взрыва заключается в следующем. При быстром и сильном сжатии ВВ нагреваются, в результате происходит химическая реакция, сопровождающаяся выделением большого количества энергии и образованием газообразных продуктов. Образующиеся газообразные продукты производят резкий удар по соседним слоям ВВ. Эти слои, в свою очередь, сжимаются, в них также образуется ударная волна и происходит интенсивная химическая реакция.
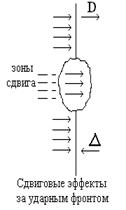
Ударная волна распространяется по всей массе ВВ со скоростью, равной нескольким километрам в секунду. Ударная волна имеет впереди резко очерченный фронт, на котором происходит сильное повышение давления и температуры. Непосредственно за фронтом волны происходит превращение ВВ в газообразные продукты и выделение энергии. Продукты взрыва не удаляются из зоны реакции, а движутся в направлении распространения процесса вслед за ударной волной.
Благодаря выделению энергии в процессе химической реакции и постоянному ее восполнению скорость распространения ударной волны во взрывчатом веществе может остаться постоянной. Такое распространение взрыва является детонацией ВВ. Скорость детонации определяется как скорость распространения ударной волны по заряду ВВ, т.е. детонация представляет собой наиболее совершенную форму взрыва, когда процесс протекает с постоянной и максимально возможной для данного ВВ скоростью.
Скорость детонации является одной из наиболее важных характеристик ВВ, которая определяется экспериментально разными методами (оптическим, осциллографическим, хронографическим). Наиболее простым методом определения скорости детонации является метод Дитриша, основанный на сравнении известной скорости детонации детонирующего шнура со скоростью детонации используемого заряда [5]. В таблице 2.3 приведены скорости детонации некоторых ВВ.
Таблица 2.3 - Скорость детонации некоторых ВВ
| Взрывчатое вещество | Плотность, г/см3 | Скорость детонации, м/с |
| Гремучая ртуть | 3,30 | 4500 |
| Азид свинца | 4,00 | 5100 |
| Тротил | 1,61 | 7000 |
| Тетрил | 1,67 | 7420 |
| ТЭН | 1,60 | 8380 |
| Гексоген | 1,60 | 7900 |
С увеличением плотности заряда скорость детонации бризантных ВВ возрастает, достигая максимума при предельной для данного ВВ плотности. Зависимости скорости детонации от плотности заряда представлены в таблице 2.4.
Таблица 2.4 – Скорость детонации ВВ от плотности заряда
| Плотность, г/см3 | 1,3 | 1,4 | 1,5 | 1,6 | 1,6 | 1,7 |
| Взрывчатое вещество | Скорости детонации, м/с | |||||
| Тротил | 6025 | 6320 | 6650 | 6980 | 7000 | - |
| Тетрил | - | 6780 | 7075 | 7400 | - | 7650 |
| Гексоген | - | 7380 | 7180 | 8200 | - | 8600 |
| ТЭН | - | 7280 | 7550 | 7880 | - | 8240 |
Взрывчатые вещества различны по своей способности детонировать. Для каждого из них имеется некоторое наименьшее количество ВВ, необходимое для того, чтобы произошла детонация. Как было установлено академиком Ю.Б. Харитоном, мерой способности ВВ к взрыву может служить критический диаметр заряда, т.е. такой предельный диаметр, при котором детонация может распространиться по заряду. Чем меньше критический диаметр, тем больше способность ВВ к детонации. Величина критического диаметра зависит от физического состояния взрывчатого вещества. Так, критический диаметр прессованного тротила около 10 мм, а литого – 32 мм. Поэтому в заряде из прессованного тротила возбудить детонацию легче, чем в заряде из литого тротила.
2.5 Горение взрывчатых веществ
Взрыв представляет собой одну из форм химического превращения взрывчатых веществ. Другой его формой является горение. Для горения также характерны большое количество выделяемого тепла, газообразных продуктов и большая скорость процесса. И тем не менее горение принципиально отлично от взрыва. Это отличие заключается в первую очередь в механизме распространения процесса.
Как было показано выше, распространение взрыва обусловлено прохождением по заряду ВВ ударной волны, возбуждающей в каждом последующем слое интенсивную химическую реакцию, сопровождающуюся выделением тепла. Распространение же процесса горения по взрывчатому веществу обусловлено передачей тепла от одного слоя к другому за счет теплопроводности, диффузии и излучения газообразных продуктов горения.
Принципиальное отличие в механизме распространения взрыва и горения предопределяет различные скорости этих процессов: скорость горения всегда меньше скорости распространения звука в данном веществе, скорость взрыва превосходит скорость звука в заряде ВВ. Отличием механизмов распространения взрыва и горения объясняется и различное их воздействие на внешнюю среду: продукты горения осуществляют метание тел в сторону наименьшего сопротивления, взрыв вызывает дробление преград, соприкасающихся с зарядом или находящихся на некотором расстоянии от места взрыва.
Процесс горения ВВ довольно сложен и изучен еще далеко не полностью. Большой вклад в изучение процесса горения внесли: академик Н.Н. Семенов, профессора К.К. Андреев, А.Ф. Беляев, Я.Б. Зельдович и другие [3]. Сущность процесса горения представляется следующим образом.
При нагревании ВВ происходит плавление и испарение тонкого слоя вещества. Образующиеся пары нагреваются до температуры, при которой начинается процесс самовоспламенения с последующей интенсивной химической реакцией, которая сопровождается выделением тепла и газообразных продуктов. Продукты горения нагревают следующий слой ВВ, в котором повторяются также физические процессы и химические реакции. За счет образования газообразных продуктов горения давление у горящей поверхности ВВ повышается. Газы расширяются и оттекают от поверхности вещества. Давление над поверхностью зависит от соотношения между скоростью газопритока и скоростью газооттока. Скорость газопритока зависит от скорости горения ВВ, которая для различных веществ разная и по-разному зависит от давления. Если с увеличением давления скорость горения растет быстрее, чем скорость газооттока, то давление будет возрастать и горение перейдет во взрыв.
Инициирующие ВВ имеют большую скорость горения, существенным образом возрастающую с увеличением давления. Поэтому их горение, как правило, является неустойчивым и переходит во взрыв.
Если же при повышении давления скорость горения растет медленнее скорости газооттока, то образующиеся газы успевают расшириться и горение будет носить устойчивый характер. Именно этим объясняется устойчивое горение тротила и других бризантных ВВ, у которых скорость горения мала и в малой степени зависит от давления.
Однако горение бризантных ВВ в некоторых случаях также может перейти во взрыв. Это случается, когда ВВ жидкие или имеют рыхлую пористую структуру. При горении пористого ВВ горячие газообразные продукты проникают через поры в глубь вещества и зажигают его. В результате возрастают поверхность горения и соответствующим образом увеличивается скорость газопритока. Давление растет, и горение переходит во взрыв.
Пироксилин, имеющий пористую структуру, не представлялось возможным использовать для метательных целей до тех пор, пока не нашли способ устранить его пористость. Получение пироксилиновых порохов в принципе и заключается в придании пироксилину плотной структуры.
Благодаря плотной структуре пороха горят устойчиво. Горение является наиболее характерным видом их взрывного превращения.
2.6 Возбуждение взрывных превращений и начальный
импульс
Наличие взрывчатых свойств у того или иного вещества определяет его потенциальную способность к взрывным превращениям в форме горения или детонации. Чтобы вызвать взрывное превращение, необходимо на взрывчатое вещество оказать определенное внешнее воздействие. Это внешнее воздействие называют начальным или инициирующим импульсом. Возможность возникновения взрывного превращения под действием начального импульса зависит от количества энергии, сообщаемой при этом ВВ.
В зависимости от природы ВВ его взрывное превращение можно вызвать различными начальными импульсами: тепловым (нагревом, лучом огня), механическим (ударом, трением, прострелом пулей), взрывным (взрывом другого ВВ).
Вид начального импульса влияет на характер взрывного превращения, что учитывается для тех или иных условий применения ВВ.
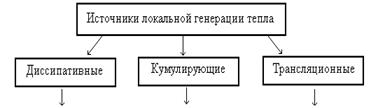
В настоящее время достигнут определенный уровень исследований проблемы ударно-волнового инициирования ВВ. В работе [6] показаны механизм возникновения источников локальной генерации тепла при инициировании ВВ и сравнение эффективности элементарных процессов в веществе.
При инициировании жидких и твердых (литых, прессованных) ВВ существуют принципиальные отличия, которые являются следствием того, что жидкие ВВ гомогенны, а твердые, изготовленные каким-либо из известных технологических способов, гетерогенны. Поэтому критические параметры ударно-волнового инициирования для однородных бездефектных систем существенно выше, чем для структурно-неоднородных с пористостью от 1 до 3 %. Это связано с тем, что для гомогенных ВВ необходимо в течение определенного времени прогреть объём за фронтом инициирующей ударной волны.
Модель формирования детонационных волн в гомогенных ВВ (например, нитрометан и его смеси) была предложена Чепменом и уточнена А.Н. Дреминым и сотрудниками [3]. Определение критических условий инициирования детонации для гомогенных ВВ сводится к задаче адиабатического теплового взрыва в условиях изменяющейся во времени температуры с заданным начальным давлением инициирующей ударной волны (УВ).
Гетерогенные же ВВ являются химически однородными, но структурно они неоднородны. Для данной группы ВВ существенны процессы, протекающие на неоднородностях структуры непосредственно за фронтом УВ. При этом для гетерогенных ВВ влияние температурного фона из-за объёмного разогрева значительно, особенно на стадии резкого ускорения инициирующей УВ и установления стационарной детонации. Критические параметры инициирования и пространственно-временная картина течения за фронтом инициирующей УВ для данной группы зависят от баланса между энергией, вводимой в ВВ ударной волной, и энерговыделением от разложения. При этом к локализации выделения энергии приводят следующие структурные дефекты в материале заряда:
· макроуровневые срезы и разрушения на неоднородностях структуры заряда;
· разрыв сплошности течения вблизи пустот, на границах кристаллов и включений;
· дробление и впрыск вещества в полости материала;
· макрокумулятивные эффекты в порах;
· внутрикристаллические дефекты.
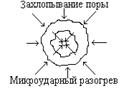
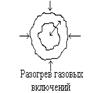
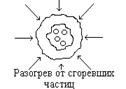
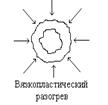
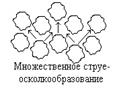
Совокупность структурных неоднородностей в веществе – источников локальной генерации тепла – представлена схемой на рисун-
ке 2.4.
|
| ||

| 
| 
|

| 
| 
|
|  
|
|
| ||
| Рисунок 2.4 - Механизм локальной генерации тепла [6] | ||
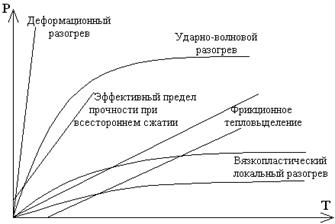
Превалирующая роль того или иного механизма локальной генерации тепла до настоящего времени не выяснена. Условия начала разложения в очаге могут быть достигнуты при любом механизме генерации тепла в зависимости от физико-механической структуры и свойств ВВ, его пористости, совокупности термокинетических характеристик и характера действующей нагрузки. Однако эффективность этих механизмов не равнозначна и по проведенным оценкам может быть в порядке возрастания представлена следующим образом (рисунок 2.5): деформационный разогрев – ударно-волновой разогрев – фрикционное тепловыделение – вязкопластический локальный разогрев.
|
| Рисунок 2.5 - Сравнение эффективности элементарных процессов инициирования [6] |
Необходимо отметить, что достаточный для начала химической реакции разогрев в очаге еще не гарантирует распространения процесса в объёме и, следовательно, создания предпосылок формирования самоподдерживающейся инициирующей ударной волны и ее перехода в детонационную. Последнее возможно только в тех случаях, когда создаются необходимые условия для суммирования энергии элементарных процессов, когда развитие процесса в очагах приобретает коллективный характер и роль газодинамики становится преобладающей. В результате возрастает влияние фронтальных процессов и формируется локальная зона максимума давления и массовой скорости, а именно ударно-волновой комплекс с энерговыделением в непосредственной близости от фронта, способный при определенных условиях перестроиться в стационарный, детонационный.
3 Физические основы термодинамики взрывчатых веществ
3.1 Энергетические характеристики
Критериями действия взрыва являются количество тепла, выделяемое при взрыве, объём образующихся газообразных продуктов и температура взрыва.
Для взрывчатых веществ количество тепла, выделяющееся при взрыве, является очень важной характеристикой, определяющей возможность использования того или иного ВВ в соответствующих условиях. Чем больше выделилось тепла, тем выше температура продуктов взрыва, выше давление, а следовательно, и существеннее воздействие продуктов взрыва на окружающую среду. В реальных условиях применения ВВ не вся теплота, выделяющаяся при взрыве, переходит в механическую работу. Часть ее расходуется на нагревание оболочки, в которую заключено ВВ, и окружающей среды.
Количество тепла, выделяющееся при взрыве 1 кг ВВ, называется теплотой взрыва. Теплота взрыва является важной энергетической характеристикой, определяющей работоспособность ВВ. Количество тепла, выделяемое в результате процесса, протекающего с участием газов, зависит от того, происходит процесс в постоянном или переменном объёме. Полагают, что при детонации ВВ химическая реакция успевает закончиться раньше, чем начнется расширение газообразных продуктов взрыва, и выделение тепла происходит при постоянном
объёме.
Для сравнения энергетических возможностей различных ВВ пользуются величиной QV, то есть теплотой взрыва, определяемой при постоянном объёме. Теплота взрыва некоторых взрывчатых веществ QV приведена в таблице 3.1.
Таблица 3.1 – Теплота взрыва некоторых ВВ
| Взрывчатое вещество | Теплота взрыва QV, ккал/кг |
| Азид свинца | 367 |
| Гремучая ртуть | 414 |
| Тротил | 1000 |
| Пикриновая кислота | 1030 |
| Тетрил | 1090 |
| Гексоген | 1300 |
| ТЭН | 1400 |
| Нитроглицерин | 1490 |
Теплота взрыва определяется экспериментально или расчетным путем. Экспериментальное определение теплоты взрыва производится в калориметрической установке по количеству тепла, поглощенного массой установки при взрыве внутри нее определенного количества ВВ [5].
В основе вычисления теплоты взрыва лежит открытый в 1840 году русским химиком Г.И. Гессом основной закон термохимии, который представляет собой частный случай закона сохранения энергии. В соответствии с этим законом тепловой эффект химической реакции не зависит от того, какие были промежуточные вещества при протекании реакции, а зависит только от состава исходных веществ и конечных продуктов реакции.
Согласно закону Гесса теплота взрыва QV равна алгебраической разности между теплотой образования продуктов взрыва и теплотой образования взрывчатого вещества:
QV = Q1 - Q2,
где Q1 - теплота образования всех продуктов взрыва, равная сумме теплот отдельных продуктов взрыва;
Q2 - теплота образования взрывчатого вещества.
Теплота образования различных веществ приведена в специальных таблицах [22]. Продукты взрывного превращения могут быть определены методом газового анализа или рассчитаны теоретически.
Точно определить состав продуктов взрыва методом газового анализа довольно трудно, так как газовому анализу подвергаются уже охлажденные продукты взрыва, а состав охлажденных продуктов в силу ряда обстоятельств может отличаться от первоначального состава, соответствующего максимальной температуре и давлению взрыва. Поэтому чаще всего состав продуктов взрыва определяют расчетным путем [9].
При этом исходят из следующих соображений. Подавляющее большинство ВВ представляет собой органические вещества, состоящие из атомов углерода, водорода, кислорода и азота. Состав продуктов взрыва определяется главным образом соотношением горючих составляющих (углерода, водорода) и кислорода.
Приведем некоторые особенности расчета теплоты взрыва. Все ВВ условно делят на 3 группы:
· к первой группе относят ВВ с количеством кислорода, достаточным для полного сгорания горючих элементов (например, нитроглицерин);
· ко второй группе - ВВ с количеством кислорода, недостаточным для полного сгорания, но достаточным для полного газообразования (например, гексоген);
· к третьей группе - ВВ с количеством кислорода, недостаточным для полного газообразования (например, тротил).
Руководствуясь общими закономерностями физической химии и термодинамики, можно достаточно точно подсчитать состав продуктов взрыва. Для этого необходимо составить уравнение реакции взрывного превращения. Приближенные реакции взрывного превращения для ВВ первой и второй групп могут быть составлены достаточно просто. Считают, что в результате взрыва ВВ, относящихся к первой группе, образуются лишь продукты полного сгорания CO2 и H2O. С учётом этого реакцию взрывного превращения, например, нитроглицерина можно представить следующим образом:
2C3H5(ONO2)3=6CO2+5H2O+0,5O2+3N2. (3.1)
Для взрывчатых веществ второй группы пользуются правилом, согласно которому кислород, входящий в молекулу взрывчатого вещества, сначала окисляет весь углерод до окиси углерода, а затем оставшаяся часть кислорода распределяется поровну между водородом и образовавшейся окисью углерода, в результате чего образуются вода и углекислый газ. Руководствуясь этим положением, можно написать уравнение взрывного превращения, например, гексогена:
C3H6O6N6=3CO+1,5O2+3H2+3N2=1,5CO+1,5CO2+1,5H2O+1,5H2+3N2. (3.2)
Для третьей группы ВВ составить уравнение реакции несколько труднее. Зная реакцию взрывного превращения и состав продуктов взрыва, нетрудно подсчитать их объём V0, приведенный к нормальным условиям (при 0 оС и давлении 760 мм.рт.ст.) и отнесенный к килограмму ВВ:
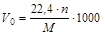 , (3.3)
, (3.3)
где 22,4 – объём 1 грамм-моля газа при нормальных условиях, л;
n – количество молей газообразных продуктов, образующихся при взрыве 1 моля ВВ;
М – молекулярная масса ВВ, г.
Зная теплоту взрыва и состав продуктов взрыва, легко вычислить температуру взрыва:
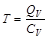 ,
,
где CV – теплоёмкость продуктов взрыва в зависимости от изменения температуры.
3.2 Стойкость взрывчатых веществ
Немаловажным критерием безопасности ВВ при хранении является стойкость взрывчатых веществ. ВВ способны не только взрываться от действия начальных импульсов, но и самопроизвольно разлагаться и претерпевать различные физико-химические превращения в процессе длительного хранения. Поэтому при определении срока служебной пригодности ВВ обязательно нужно учитывать такое их свойство, как стойкость (стабильность). С учётом этого свойства определяются условия применения и безопасного обращения с ВВ после истечения определенных сроков хранения. Различают химическую и физическую стойкость ВВ.
Химической стойкостью называют способность ВВ сохранять в процессе длительного хранения неизменными химический состав и химические свойства. Она зависит от природы ВВ, наличия в них примесей других веществ, условий хранения. Применяемые в настоящее время для снаряжения ВВ разлагаются крайне медленно. Они обладают большой химической стойкостью. Это значит, что ВВ могут храниться десятилетиями, практически не изменяя своего химического состава и химических свойств.
Физическая стойкость характеризует склонность ВВ к физическим изменениям (физическое состояние, структура, механическая прочность, форма и размеры) самопроизвольно или под влиянием внешних причин.
Природа и механизм этих изменений для разных ВВ могут быть различными. Так, например, при длительном хранении в условиях жаркого климата (t > +40 оС) недостаточно очищенного тротила, получаемого по ускоренной технологии, из него выделяется оливково-желтоватая маслянистая жидкость, получившая название тротилового масла. Тротиловое масло представляет собой легкоплавкую эвтектическую смесь динитротолуолов и тротила. Выделение тротилового масла приводит к разрыхлению ВВ и потере зарядом монолитности, что влечет изменение его взрывчатых характеристик.
Ограниченной физической стойкостью обладают аммонийно-селитренные ВВ, отличающиеся высокой гигроскопичностью и сильной увлажняемостью. Склонность к увлажнению является крупным недостатком аммонийно-селитренных ВВ, ограничивающим их применение и затрудняющим изготовление и снаряжение изделий.
Основной причиной усадки аммотоловых изделий является самопроизвольное слипание и укрупнение кристаллов аммиачной селитры, сопровождающееся уменьшением объёма изделия. Укрупнению кристаллов способствует повышенная влажность аммотола и переход аммиачной селитры из одной модификации в другую. Аммиачная селитра, обладая свойством полиморфизма (модификация форм кристаллов), существует в пяти кристаллических модификациях, каждая из которых стабильна в определенных температурных условиях. Переход из одной модификации в другую (рекристаллизация) происходит при температуре ниже 18, 32, 85 и 125 оС. Этот переход сопровождается изменением плотности и соответственно объёма вещества. Если при хранении изделий или боеприпасов температура окружающего воздуха поднимается выше 32 оС, то наблюдается «рост» зарядов, так как переход через указанную температуру приводит к модификационным превращениям аммиачной селитры, связанным с увеличением объёма. Поэтому хранение изделий, снаряженных аммотолами, в различных климатических условиях сопровождается многократными полиморфными превращениями, которые могут привести к разрушению изделий. Повышенная влажность аммотоловых зарядов снижает их восприимчивость к детонации, уменьшает скорость детонации и может привести к неполным, а также к затухающим взрывам, переходящим в выгорание.
Изменение объёма, или так называемый «рост» ВВ, происходит у некоторых прессованных зарядов за счет остаточной деформации.
В результате такого «роста» невозможно без предварительной обработки ввернуть взрыватель в боеприпасы, что приводит к дополнительным мероприятиям по безопасности. Поэтому очень важно своевременно обнаружить «рост» ВВ.
Химическая стабильность (стойкость) ВВ характеризует скорость разложения ВВ при хранении и определяет способность его сохранять химический состав и связанные с ним физико-химические и взрывчатые свойства в течение гарантийного срока хранения. Она зависит от химической природы ВВ, наличия или отсутствия в нем нестойких примесей или компонентов, несовместимых друг с другом, а также от условий хранения. При низкой стойкости ВВ хранение больших количеств может привести к самоускоряющемуся разложению и взрыву.
Для отдельных ВВ в основе процесса медленного термического распада разложения лежит, как правило, реакция мономолекулярного распада, протекающая в соответствии с уравнением Аррениуса. Константа скорости реакции К находится в экспоненциальной зависимости от температуры Т:
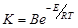 , (3.4)
, (3.4)
где В – предэкспонента (константа уравнения Аррениуса);
Е – энергия активации реакции распада;
R – универсальная газовая постоянная.
Особенностью распада взрывчатых веществ по сравнению с обычными химическими реакциями является необычайно высокое значение как предэкспоненты, так и энергии активации.
В обычных условиях, т.е. при невысоких температурах, химически чистые ВВ достаточно стойкие. Так, если принять для константы скорости первичной мономолекулярной реакции распада, например нитроглицерина, значения В=10-18,64 и Е=183540 Дж/моль, то период полураспада, рассчитанный по формуле Z1,2=ln2/К, в зависимости
от температуры можно представить в виде следующей таблицы (таблица 3.2).
Таблица 3.2 - Период полураспада в зависимости от температуры
| Температура, оС | 0 | 20 | 40 | 60 |
| Предэкспонента скорости | 10-64,34 | 10-13,95 | 10-10,93 | 10-9,2 |
| Период полураспада, лет | 4,8×108 | 2×106 | 1870 | 35 |
Катализировать процесс разложения могут не только продукты собственного распада, но и некоторые примеси. Такими свойствами, в частности, обладают примеси азотной кислоты. Вот почему в технологическом процессе получения нитроэфиров и других мощных ВВ предусмотрена их тщательная отмывка от примесей азотной кислоты и других нестойких продуктов.
В таблице 3.3 приведены энергии активации и кинетические коэффициенты медленного химического разложения ряда индивидуальных взрывчатых веществ [7].
Таблица 3.3 - Энергии активации и кинетические коэффициенты
разложения ряда индивидуальных ВВ
| Вещество | Е, кДж/моль | lgB | Вещество | Е, кДж/моль | lgB |
| Нитроглицерин | 179 | 18 | Нитрат аммония | 170 | 13,8 |
| Диэтиленгликольдинитрат | 178 | 16,5 | Тротил | 225 | 19,0 |
| ТЭН | 197 | 19,8 | Гексоген | 199 | 18,5 |
Методы определения химической стойкости ВВ
Для оценки стойкости ВВ обычно определяют скорость их разложения при повышенных температурах, в пределе – при температуре вспышки. Для сокращения времени испытания ограничиваются определением скорости только начальной стадии разложения.
Стойкость нитроглицерина и нитроэфиросодержащих ВВ определяют йодокрахмальной пробой, по которой продукты разложения (окислы азота) улавливаются чувствительной йодокрахмальной бумажкой. Окислы азота, воздействуя на бесцветный ион йода в йодистом калии, переводят его в элементарный йод, который с крахмалом окрашивается в бурый цвет. Для более четкого обнаружения реакции йодокрахмальную бумажку перед испытанием смачивают до половины водным раствором глицерина. Тогда на границе раздела сухой и влажной бумажки видна ясно различимая цветная полоса. Нитроглицерин, предназначенный для приготовления нитроэфиросодержащих ВВ, не окрашивает бумажку в течение 30 минут, нитроэфиросодержащие ВВ – в течение 10 минут [5].
Реологические свойства
К реологическим свойствам относятся пластичность и текучесть ВВ.
Пластичность – способность ВВ легко деформироваться под воздействием небольших нагрузок и сохранять придаваемую им форму. Пластичные промышленные ВВ характеризуются высоковязкой структурой, обусловленной наличием в них пластификаторов и связующих, в динамитах в виде динамитного желатина (раствор нитроклетчатки в нитроглицерине или нитрогликоле), в водосодержащих ВВ – в виде водного геля. Пластичные свойства ВВ зависят от вязкости динамитного желатина и его содержания в ВВ.
К пластичным промышленным ВВ относятся динамиты, содержащие взрывчатую желатину, и высоковязкие водосодержащие ВВ (акваниты, акваналы, гелеобразные акватолы). При очень высокой вязкости желатина и значительном содержании его в составе ВВ приобретают резиноподобную структуру, деформация становится упругой, ВВ теряет свойство пластичности. К таким ВВ, в частности, относятся динамиты, содержащие более 60 % желатины.
Текучесть – способность ВВ вытекать из емкостей под действием силы тяжести. Этим свойством помимо собственно жидких ВВ обладают низковязкие суспензии – смеси жидкостей и порошкообразных наполнителей. Как и жидкости, такие системы могут перекачиваться по трубам и шлангам с помощью насосов различной конструкции.
Некоторые пластичные ВВ при хранении приобретают структуру твердого тела и вновь становятся пластичными при разминании. Такое явление называется тиксотропией. Для стабилизации пластичности в состав ВВ вводят добавки поверхностно-активных веществ, таких как алкиламины.
Исследования структурно-механических (реологических) свойств показали, что водосодержащие ВВ как с алюминием, так и сенсибилизированные тротилом, по характеру аномалии вязкости относятся к неньютоновским жидкостям с ярко выраженными вязкопластичными и тиксотропными свойствами. При снижении вязкости увеличивается текучесть водосодержащих ВВ, которая обратно пропорциональна вязкости. Вязкость и пластичность ВВ определяется с помощью консистометра Геплера, которым измеряют скорость проникновения иглы с шариком на конце в массу вещества или деформацию цилиндриков из ВВ при действии на них в течение определенного времени заданной нагрузки. В таблице 3.4 приведены данные об изменении пластичности динамита и водосодержащего ВВ, определенные на консистометре
Геплера.
Таблица 3.4 – Пластичность динамита и водосодержащего ВВ
| ВВ | Усадка (мм) столбиков диаметром 10 мм высотой | |||
| -10 | -15 | -20 | -25 | |
| Динамит | 4,14 | 1,50 | 0,81 | 0 |
| Водосодержащее ВВ | 4,8 | 0,37 | 0,27 | 0 |
Для определения пластичности ВВ чаще пользуются более простым прибором – пенетрометром (от лат. penetro - проникаю). Пластичность оценивается в этом случае скоростью проникновения иглы пенетрометра. Ниже приведены результаты испытания водосодержащего ВВ (ВВВ) пенетрометром (таблица 3.5).
Таблица 3.5 – Результаты определения пластичности пенетрометром
| Содержание воды в ВВ, % | 4 | 6 | 8 | 10 |
| Время проникновения иглы до основания столбика из ВВ высотой 40 мм, с | 180 | 50 | 30 | 10 |
В полевых условиях пластичность ВВ качественно можно оценить по способности изделий разминаться в руке и сплющиваться в шпуре или скважине при нажатии забойником.
3.3 Разрушающие факторы взрывчатых веществ
Детонация ВВ
Детонация представляет собой самоподдерживающийся процесс перемещения по ВВ со сверхзвуковой скоростью ударного фронта (скачка давления), сопровождающийся химическим превращением вещества. Химическая реакция возникает в результате адиабатического сжатия и разогрева вещества в ударном фронте. Комплекс из ударного фронта и зоны химической реакции называется детонационной волной. Давление на ударном фронте имеет порядок от десятков атмосфер (газы) до сотен тысяч атмосфер (мощные бризантные вещества). Установившаяся (стационарная) детонационная волна распространяется по ВВ с постоянной скоростью (от 1 до 10 км/с). Постоянство параметров детонационной волны объясняется тем, что потери энергии, связанные со сжатием и вовлечением в движение вещества, компенсируются теплом, выделяющимся в ударно-сжатом ВВ при его химическом превращении.
Первую математическую модель детонационной волны в газах, опирающуюся на теорию ударных волн, в виде гидродинамической теории детонации разработали в конце прошлого века одновременно несколько ученых – В.А. Михельсон в России, Д.Л. Чепмен в Англии, Е. Жуге во Франции. Эта модель не рассматривает кинетики (пространственно-временных характеристик) химической реакции в детонационной волне, а представляет ударный фронт в ней формально в виде поверхности разрыва, отделяющей исходное вещество от продуктов его химического превращения. В подвижной системе координат процесс представляется таким образом, что в ударный фронт втекает вещество в исходном состоянии и вытекает из него в виде продуктов своего химического превращения. В этом случае, как и в теории ударных волн, но с учётом энерговыделения при детонации, основные соотношения между начальными и конечными параметрами состояния вещества, а также кинематическими параметрами детонации – скоростью перемещения фронта (скоростью детонации) D и массовой скоростью движения продуктов превращения за фронтом U находят из законов сохранения массы, количества движения (импульса) и энергии в волне.
Развитие эта теория получила в работах Я.Б. Зельдовича [10],
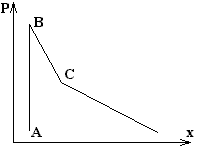
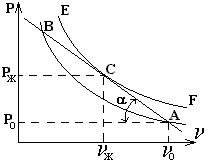
Д. Неймана, В. Деринга, независимо предложивших модель детонационной волны, учитывающую физическую зону превращения исходного ВВ в конечные продукты (зону «химпика»). Основные представления об этой модели дают рисунки 3.1 и 3.2. На рисунке 3.1 схематически показан профиль детонационной волны в координатах «давление-расстояние», а на рисунке 3.2 - PV‑диаграмма волны.
| 
|
| Рисунок 3.1 - Профиль детонационной волны | Рисунок 3.2 - PV-диаграмма детонационной волны |
Согласно данной модели исходное вещество с начальными параметрами P0, V0 (точка А на рисунке 3.2) сжимается в ударном фронте до состояния, отвечающего точке В. В этом состоянии в результате адиабатического сжатия и разогрева в веществе возникает экзотермическая реакция взрывного превращения, заканчивающаяся в точке С, называемой точкой Жуге или Чепмена-Жуге и лежащей на адиабате продуктов детонации (адиабате Гюгонио). Процесс превращения сопровождается расширением нагретых газообразных продуктов детонации (ПД), поэтому давление ПД в точке Жуге Рж примерно в два раза ниже, чем в точке В. За точкой Жуге (плоскостью Чепмена-Жуге) происходит дальнейший спад давления в ПД вследствие их расширения (волна разгрузки). Прямую АВ, являющуюся касательной к адиабате Гюгонио в точке Жуге, называют прямой Михельсона.
На рисунке 3.1 адиабатическому сжатию вещества отвечает прямая АВ с очень малым наклоном относительно оси абсцисс, что свидетельствует о крайне малом времени сжатия и малой толщине сжатого слоя. Зоне химического пика отвечает участок ВС на кривой спада давления, точка излома С отвечает точке Жуге, участок за этой точкой характеризует спад давления в расширяющихся продуктах детонации.
Исходя из гидродинамической модели, основными соотношениями для детонационной волны являются, согласно законам сохранения:
| массы | 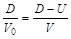 , ,
| (3.5) |
| импульса | 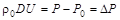 , ,
| (3.6) |
| энергии | 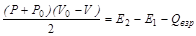 , ,
| (3.7) |
где U – массовая скорость движения продуктов взрыва за фронтом;
D - скорость детонации ВВ;
Е1, Е2 – внутренняя энергия продуктов взрыва соответственно в начальном и конечном состоянии;
Qвзр – теплота взрыва;
V0 и P0 – соответственно удельный объём и давление исходного вещества;
P и V – соответственно давление и удельный объём продуктов детонации.
Совместное решение уравнений (3.5) и (3.6) дает формулы для расчета кинетических параметров детонации:
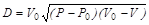 , (3.8)
, (3.8)
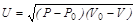 . (3.9)
. (3.9)
Данные выражения являются одной из форм записи уравнения ударной адиабаты Гюгонио для продуктов детонации.
Большинство исследователей пришли к выводу, что при
r0³1 г/см3 скорость детонации (D) может быть описана линейной зависимостью вида
D= A+ B(r0) (3.10)
или, как это предложил М.А. Кук:
D2= D1+ M(r2-r1), (3.11)
где D2 и D1 – скорость детонации при плотности ВВ соответственно r2 и r1;
М – размерный коэффициент.
М.А. Кук в качестве усредненного коэффициента М рекомендует величину 3500. Значения коэффициентов А, В и величин D1,0 (плотность 1,0 г/см3) и D1,6 (плотность 1,6 г/см3) для некоторых веществ приведены в таблице 3.6 [7].
Таблица 3.6 – Значения коэффициентов А, В и величин D1,0 и D1,6 для некоторых ВВ
| Вещество | А, км/с | В | D1,0 , км/с | D1,6 , км/с |
| Тротил | 1,84 | 3,20 | 5,10 | 6,97 |
| Гексоген | 2,40 | 3,59 | 6,08 | 8,03 |
| Гексоген флегматизированный | 2,12 | 3,80 | – | – |
| Октоген | 2,56 | 3,48 | 6,09 | 8,08 |
| Октоген флегматизированный | 1,09 | 4,31 | – | – |
| ТЭН | 2,25 | 3,41 | 5,90 | 7,85 |
Приведенные основные соотношения в детонационной волне приемлемы для случая плоской волны, когда вся потенциальная химическая энергия реализуется в детонационной волне и определяет параметры детонации – её скорость, давление и другие. В случае неодномерного течения за ударным фронтом параметры детонации в определенных границах становятся зависимыми от поперечных размеров заряда, как это впервые показал Ю.Б. Харитон. Так как зона химического превращения в детонационной волне имеет конечные размеры, то за время химической реакции (участок ВС на рисунке 3.2) образующиеся сжатые газообразные продукты стремятся к расширению в радиальном направлении. В результате этого в зону реакции с боковой поверхности входит волна разрежения, а охваченная ею масса вещества теряется как поставщик энергии относительного ударного фронта. Так как глубина проникновения волны разрежения обратно пропорциональна радиусу заряда, то относительные потери энергии в детонационной волне должны уменьшаться с увеличением радиуса заряда, т.е. детонация может устойчиво распространяться по заряду, если продолжительность реакции t в волне меньше времени разброса вещества q в радиальном направлении. Исходя из этого, существует такой минимальный диаметр заряда d кр, при котором еще возможно устойчивое распространение детонации. Этот диаметр называется критическим диаметром детонации. Его величина находится из условий устойчивости:
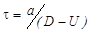 , ,
| 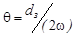 , ,
| 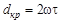 , ,
| (3.12) |
где а - ширина зоны реакции;
d з – диметр заряда взрывчатого вещества;
w - скорость волны разрежения, равная скорости звука в расширяющихся продуктах детонации;
U – массовая скорость.
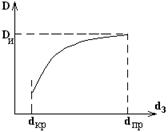
При d з >d кр потери энергии в детонационной волне должны уменьшаться, а параметры волны соответственно возрастать, асимптотически приближаясь к своему максимуму. Диаметр заряда, при котором параметры детонации близки к максимальным (рисунок 3.3), называют предельным диаметром детонации d пр. Детонацию, протекающую в заряде с d кр < d з < d пр, называют детонацией в неидеальном
режиме.
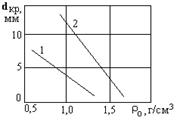
Критический диаметр зависит от многих физико-химических факторов и уменьшается с увеличением реакционной способности ВВ, которая зависит от природы вещества, его физического состояния – размеров частиц, пористости (плотности) заряда, для смесевых ВВ – от равномерности смешивания. На рисунке 3.4 приведена зависимость критического диаметра заряда тротила от плотности при различных размерах частиц.
| 
|
| Рисунок 3.3 - Зависимость скорости детонации от диаметра заряда (D И - идеальная скорость детонации) | Рисунок 3.4 - Зависимость критического диаметра заряда тротила от плотности при различных размерах частиц: 1 – от 0,01 до 0,05 мм; 2 – от 0,07 до 0,20 мм |
Критические диаметры детонации в стеклянных трубках для некоторых веществ при их плотности около 1,0 г/см3 и размере частиц от 0,05 до 0,20 мм приведены в таблице 3.7.
Таблица 3.7 – Критические диаметры детонации некоторых ВВ
в стеклянных трубах при плотности 1,0 г/см3 и размере частиц
от 0,05 до 0,20 мм
| Вещество | d кр, мм |
| Азид свинца | 0,01-0,02 |
| ТЭН | 1,0-1,5 |
| Гексоген | 1,0-1,5 |
| Тротил | 8-10 |
| Нитроглицерин | 1-2 |
| Аммонит 6Ж В | 10-12 |
Для жидких и газообразных ВВ имеются другие объяснения критических условий распространения детонации. Они основываются на механизме срыва реакции на стенке. Соответственно значение dкр определяется не временем собственно реакции в детонационной волне, а временем индукции этой реакции, развивающейся по законам теплового взрыва. При диаметре меньше критического теплового взрыва не происходит. Такой механизм [11] позволяет объяснить очень малый диапазон между значениями dкр и dпр для жидких ВВ.
Для твердых промышленных ВВ характерен большой разрыв между величинами dкр и dпр, их отношение может достигать 10. Так, например, значение dкр тонкодисперсных аммонитов в открытых зарядах диаметром 40 мм составляет 150 мм, а максимальная скорость детонации фиксируется в зарядах диаметром более 200…300 мм (рисунок 3.5). В прочных оболочках этот разрыв сужается.
Дата: 2019-12-10, просмотров: 1142.